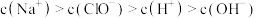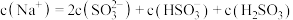298 K 时,0.1 mol/L H2R溶液中H2R、HR‾、R2‾ 三种微粒的分布系数δ随 pH 变化的关系如图所示。已知:298 K时,HF的Ka=1.0×10‾3.4。下列表述正确的是
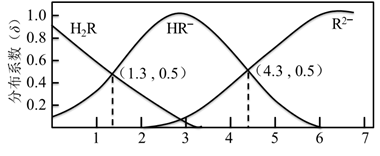

| A.H2R的Ka1 = 1.0×10‾1.3 |
| B.Na2R 溶液中离子存在关系:c(Na+) = c(HR‾ ) +2c(R2‾ ) |
| C.等物质的量的NaHR 和Na2R溶于水,所得溶液的pH 恰好为4.3 |
| D.在足量的NaF 溶液中加入少量 H2R 溶液:H2R + 2F‾ = 2HF + R2‾ |
更新时间:2018-02-06 15:19:14
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】常温下,下列关于溶液的说法错误的是
A.某盐溶液pH<7,则此溶液中水电离的 浓度大于 浓度大于 |
B.pH均为3的 和HCl溶液的导电能力基本相同 和HCl溶液的导电能力基本相同 |
C.0.1mol/L的氨水pH约为11,则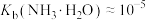 |
D.将 溶液稀释,pH减小 溶液稀释,pH减小 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】下列说法正确的是
| A.常温下某醋酸溶液的pH=a,将溶液稀释到原体积的103倍,则溶液的pH=(a+3) |
| B.常温下pH=3盐酸溶液和pH=11的氨水等体积混合,溶液的pH>7 |
| C.滴有酚酞溶液的氨水里,加入NH4Cl至溶液恰好无色,则此时溶液的pH<7 |
| D.等浓度等体积的CH3COONa和NaClO溶液中离子总数,前者小于后者 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】室温下,通过下列实验探究NaHCO3、NaHSO3溶液的性质:
下列说法正确的是
| 实验 | 实验操作和现象 |
| 1 | 用pH试纸测定浓度为0.1mol·L-1NaHSO3溶液的pH,pH≈5 |
| 2 | 用pH试纸测定浓度为0.1mol·L-1NaHCO3溶液的pH,pH≈8 |
| 3 | 将浓度均为0.1mol·L-1的NaHSO3和Ba(OH)2溶液等体积混合,产生白色沉淀 |
| A.实验1可得0.1mol·L-1NaHSO3溶液中:Ka1(H2SO3)·Ka2(H2SO3)<10-10 |
B.实验2可得0.1mol·L-1NaHCO3溶液中:c(HCO )>c(CO )>c(CO )>c(H2CO3) )>c(H2CO3) |
C.实验3所得溶液中:c(Ba2+)·c(SO )=2.5×10−3 )=2.5×10−3 |
D.浓度均为0.1mol·L-1的NaHSO3和NaHCO3两份溶液中:c(HCO )+2c(CO )+2c(CO )<c(HSO )<c(HSO )+2c(SO )+2c(SO ) ) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】类比pH的定义,对于稀溶液可以定义pC=-lgC,pKa=-lgKa。常温下,某浓度H2A溶液中滴加NaOH溶液,测得pC(H2A)、pC(HA-)、pC(A2-)变化如图所示。下列说法正确的是


| A.pH=3.50时,c(H2A)>c(HA-)>c(A2-) |
| B.从a点开始滴入NaOH溶液,溶液中c(H+)/c(H2A)先减小后增大 |
| C.将等浓度等体积的Na2A与H2A溶液混合后,溶液显碱性 |
| D.pH从3.00到5.30时,c(H2A)+c(HA-)+c(A2-)先增大后减小 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】高铁酸盐在水溶液中有四种含铁型体,25 ℃时,它们的物质的量分数随pH 的变化如图所示,下列叙述错误的是


| A.向pH=5 的高铁酸盐溶液中加入KOH溶液,离子方程式为HFeO4-+OH-=FeO42-+H2O |
| B.为获得尽可能纯净的高铁酸盐,应控制pH≥9 |
| C.已知H3FeO4+的电离平衡常数分别为:K1=2.5×10-2,K2=4.8×10-4,K3=5.0×10-8,当pH= 4时,溶液中c(HFeO4-)/ c(H2FeO4)= 1.2 |
| D.pH=2 时,溶液中主要含铁型体浓度的大小关系为 c(H2FeO4)> c(H3FeO4+)> c(HFeO4-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】已知:25℃下,H2C2O4的Ka1=5.6×10-2,Ka2=5.4×10-5。25℃时,向20mL 0.1000mol/L H2C2O4溶液中滴加0.1000mol/L NaOH溶液,混合溶液pH随加入NaOH溶液体积的变化如图所示(不考虑反应过程中温度变化)。下列有关叙述不正确的是( )


| A.点②所示溶液中:2c(H+)+c(HC2O4-)+3c(H2C2O4)=2c(OH-)+c(C2O42-) |
| B.点③所示溶液中:c(HC2O4-)+2c(C2O42-)=c(Na+) |
| C.滴定过程中c(Na+)+c(HC2O4-)+c(C2O42-)+ c(H2C2O4)=0.1000mol/L |
| D.滴定过程中可能出现:c(Na+)>c(HC2O4-)=c(C2O42-)>c(OH-)>c(H+) |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
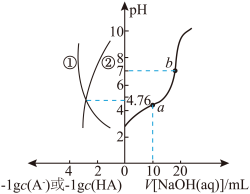
【推荐1】甲酸铵常用于电解、电容器行业。25℃时,用HCl或NaOH固体改变0.1 mol/L的HCOONH4溶液的pH,1gc(HCOOH)、1gc(NH3·H2O)、1gc(H+)和1gc(OH-)随pH变化的关系如图所示。下列说法错误的是
[已知:Ka(HCOOH)=1.8×10-4,Kb(NH3·H2O)=1.8×10-5]

[已知:Ka(HCOOH)=1.8×10-4,Kb(NH3·H2O)=1.8×10-5]

| A.Q点对应溶液pH=7 |
| B.曲线①代表lgc(H+),曲线③代表1gc(NH3·H2O) |
| C.0.1 mol/LHCOONH4溶液中,c(H+)+c(HCOOH)=c(OH-)+c(NH3·H2O) |
| D.P点存在c(NH3·H2O)>c(OH-)=c(HCOOH)>c(H+) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】已知室温下,
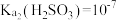
 ,用氨水吸收
,用氨水吸收 并探究吸收后溶液的性质,吸收过程中所引起的溶液体积变化和挥发可忽略。下列说法正确的是
并探究吸收后溶液的性质,吸收过程中所引起的溶液体积变化和挥发可忽略。下列说法正确的是

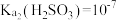
 ,用氨水吸收
,用氨水吸收 并探究吸收后溶液的性质,吸收过程中所引起的溶液体积变化和挥发可忽略。下列说法正确的是
并探究吸收后溶液的性质,吸收过程中所引起的溶液体积变化和挥发可忽略。下列说法正确的是| 序号 | 实验操作和现象 |
| 实验1 | 向10 mL 0.1 mol·L 氨水中通入0.0005 mol 氨水中通入0.0005 mol  ,测得反应后溶液 ,测得反应后溶液 |
| 实验2 | 向“实验1”所得溶液中继续通入0.0005 mol  ,测得反应后溶液 ,测得反应后溶液 |
| 实验3 | 取“实验2”所得溶液,向其中加入过量 溶液,产生白色沉淀 溶液,产生白色沉淀 |
| 实验4 | 取“实验2”所得溶液,向其中加入 至溶液 至溶液 |
A.“实验1”得到的溶液中: |
B.实验2”得到的溶液中: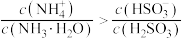 |
C.“实验3”发生反应的离子方程式: |
D.“实验4”得到的溶液中: |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】常温下,向10.00mL浓度均为0.100mol•L-1的NaOH和二甲胺[(CH3)2NH•H2O]的混合溶液中逐滴加入盐酸。利用传感器测得该过程溶液中的阳离子总浓度变化曲线如图;已知二甲胺在水中的电离与NH3·H2O相似,常温下Kb[(CH3)2NH•H2O]=1.60×10-4。下列说法正确的是


A.a点溶液中,c[(CH3)2NH ]约为l.60×l0-4mol/L ]约为l.60×l0-4mol/L |
| B.从a到c的过程中,水的电离程度最大的是b点 |
C.c点溶液中:3c(Na+)+c[(CH3)2NH ]=2c(Cl-) ]=2c(Cl-) |
D.V(盐酸)=15.00mL时,c[(CH3)2NH ]<c[(CH3)2NH•H2O] ]<c[(CH3)2NH•H2O] |
您最近一年使用:0次

 ]=-lg[
]=-lg[
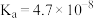 ,在
,在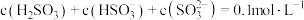 的
的 和NaOH混合溶液中含硫微粒的物质的量分数
和NaOH混合溶液中含硫微粒的物质的量分数 随pH的变化曲线如图所示。对于浓度均为
随pH的变化曲线如图所示。对于浓度均为 的NaClO和
的NaClO和 溶液,下列叙述正确的是
溶液,下列叙述正确的是