常温下,下列关于溶液的说法错误的是
A.某盐溶液pH<7,则此溶液中水电离的 浓度大于 浓度大于 |
B.pH均为3的 和HCl溶液的导电能力基本相同 和HCl溶液的导电能力基本相同 |
C.0.1mol/L的氨水pH约为11,则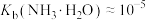 |
D.将 溶液稀释,pH减小 溶液稀释,pH减小 |
更新时间:2022-06-24 18:59:26
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】电位滴定法是根据滴定过程中指示电极电位的变化来确定滴定终点的一种滴定分析方法。在一定条件下,用0.1000mol/L的高氯酸溶液滴定10.0mL某弱酸酸式盐KHP溶液,测得电压变化与滴入HClO4溶液的体积关系如图所示。做空白对照实验,消耗HClO4溶液的体积为0.25mL。已知N为滴定终点。下列说法正确的是

| A.初始时该酸式盐KHP的浓度为0.1725mol/L |
B.M点时溶液中存在: |
C.水的电离程度: |
D.已知 的 的 ,若M点处为中性,则有 ,若M点处为中性,则有 约为1 约为1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】现有25℃下的四份溶液:①0.01mol/L 溶液、②0.01mol/L HCl溶液、③pH=12的氨水、④pH=12的NaOH溶液。下列说法不正确的是
溶液、②0.01mol/L HCl溶液、③pH=12的氨水、④pH=12的NaOH溶液。下列说法不正确的是
 溶液、②0.01mol/L HCl溶液、③pH=12的氨水、④pH=12的NaOH溶液。下列说法不正确的是
溶液、②0.01mol/L HCl溶液、③pH=12的氨水、④pH=12的NaOH溶液。下列说法不正确的是| A.①中水的电离程度最大,②③④中水的电离程度相等 |
| B.将②、③混合,若pH=7,则消耗溶液的体积:②=③ |
| C.将四份溶液稀释相同倍数后,溶液的pH:③>④,①>② |
D.将①、④混合,若有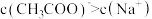 ,则混合液一定呈酸性 ,则混合液一定呈酸性 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】常温下,NH3·H2O的Kb约为10-5。在下列装置中存在不同pH的两种溶液,溶液中离子不能穿过隔膜,分子可以自由穿过隔膜(如图所示)。已知 。当达到平衡时,下列叙述正确的是
。当达到平衡时,下列叙述正确的是
 。当达到平衡时,下列叙述正确的是
。当达到平衡时,下列叙述正确的是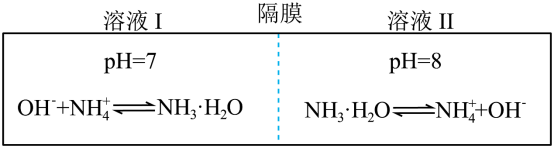
A.溶液I中c(OH-)=c(H+)+c(NH ) ) |
| B.溶液I和Ⅱ中的c平衡(NH3·H2O)不相等 |
C.溶液Ⅱ中 为0.1 为0.1 |
| D.溶液I和Ⅱ中c起始I(NH3·H2O):c起始Ⅱ(NH3·H2O)=101:110 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】下列叙述正确 的是
A.用水稀释0.1 mol/L的氨水,则溶液中 增大 增大 |
| B.pH=3的盐酸和醋酸分别升高相同的温度,pH均不变 |
| C.在等体积等pH 的盐酸和醋酸两溶液中分别加入等质量的相同锌粒,若只有一种溶液中的锌粒有剩余,则该溶液一定是盐酸; |
| D.两种氨水溶液的物质的量浓度分别为c1和c2,pH分别为a和a+1,则c2=10 c1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】25℃,向
 的
的 溶液中滴加
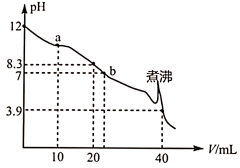
溶液中滴加 的盐酸,溶液pH随盐酸体积(V)的变化如图所示。下列说法
的盐酸,溶液pH随盐酸体积(V)的变化如图所示。下列说法不正确 的是

 的
的 溶液中滴加
溶液中滴加 的盐酸,溶液pH随盐酸体积(V)的变化如图所示。下列说法
的盐酸,溶液pH随盐酸体积(V)的变化如图所示。下列说法
A.在a点的溶液中,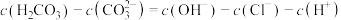 |
B.在b点的溶液中,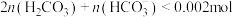 |
C.煮沸可能造成溶液中的 分解,但不影响滴定结果 分解,但不影响滴定结果 |
D.若将盐酸换成同浓度 ,当滴至 ,当滴至 时, 时,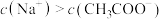 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】含硫各微粒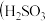 、
、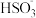 和
和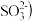 存在于
存在于 与NaOH溶液反应后的溶液中,它们的物质的量分数
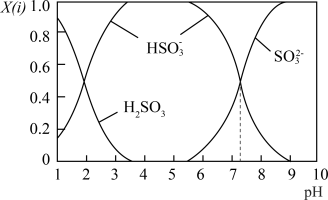
与NaOH溶液反应后的溶液中,它们的物质的量分数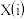 与溶液pH的关系如下图所示.下列说法正确的是
与溶液pH的关系如下图所示.下列说法正确的是
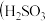 、
、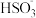 和
和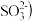 存在于
存在于 与NaOH溶液反应后的溶液中,它们的物质的量分数
与NaOH溶液反应后的溶液中,它们的物质的量分数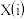 与溶液pH的关系如下图所示.下列说法正确的是
与溶液pH的关系如下图所示.下列说法正确的是 
A. 时,溶液中 时,溶液中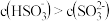 |
B. 时,溶液中 时,溶液中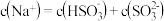 |
C.为获得尽可能纯的 ,可将溶液的pH控制在 ,可将溶液的pH控制在 左右 左右 |
D.由图中数据可估算出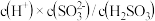 为 为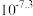 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】常温下,往某浓度的氯水中滴入Na2S03溶液的pH变化如图所示,下列离子浓度的关系错误的是

| A.a点:c(H+)>c(Cl-)>c(ClO-) |
| B.b点:l/2 c(Cl-)=c(SO42-)=0.005mol·L-1 |
| C.点:c(Na+)=2c(HSO3-)+2c(SO32-) |
| D.d 点:c(Na+)=c(Cl-)+c(HSO3-)+2c(SO32-)+2c(SO42-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】在常温下,在一组c(H2A)+ c(HA–)+ c(A2–)=0.10 mol·L–1的H2A和NaOH混合溶液中,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示。下列说法正确的是
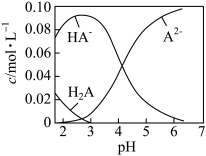

| A.c(Na+)=0.10 mol·L–1的溶液中:c(H+)- c(A2–)=c(OH–)- c(H2A) |
| B.NaHA溶液中,水的电离程度比纯水大 |
| C.c(HA–)=c(A2–)的溶液是由等物质的量的NaHA和Na2A混合而成 |
| D.pH=2.5的溶液中:c(H2A)+c(A2–)>c(HA–) |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐3】常温下下列关于粒子浓度大小比较正确的是:
| A.pH=4的CH3COOH溶液和pH=10的KOH溶液等体积混合:3c(K+) + c(H+) = c(OH-) + c(CH3COOH) + 2c(CH3COO-) |
B.向0.10mol/LNaHSO3溶液中通入NH3至溶液pH=7(体积变化可忽略):c(Na+) > c(NH ) > c(SO ) > c(SO ) ) |
C.0.3mol的SO2通入1L0.4mol/L的NaOH溶液中:4c(Na+) = 3c(HSO ) + 3c(SO ) + 3c(SO ) + 3c(H2SO3) ) + 3c(H2SO3) |
| D.0.1mol/L的HF溶液和0.1mol/L的NaOH溶液等体积混合:c(Na+) + c(OH-) > c(H+) + c(F-) |
您最近一年使用:0次

 的
的 溶液中滴加
溶液中滴加 溶液,产生白色沉淀
溶液,产生白色沉淀 具有强氧化性
具有强氧化性 溶液中加入95%乙醇,析出蓝色晶体
溶液中加入95%乙醇,析出蓝色晶体 转化为
转化为 是放热反应
是放热反应 的酸性强
的酸性强 时,分别用
时,分别用 计测定
计测定 溶液和
溶液和 溶液的
溶液的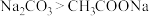
 相比,
相比, 能加速破坏铝片表面的氧化膜
能加速破坏铝片表面的氧化膜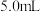 等浓度的
等浓度的 溶液和
溶液和 溶液中
溶液中
 浓度均为
浓度均为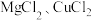 混合溶液中加入
混合溶液中加入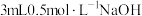 溶液
溶液

