元素A、B、C、D、E、F原子序数依次增大,且都为短周期元素。A与C可形成A2C2和A2C两种化合物;B的最高价氧化物对应的水化物甲与气体BA3化合生成离子化合物乙;D与A位于同一主族;E与C形成的化合物是大气污染物,容易形成酸雨;F元素最高化合价与最低化合价的代数和为6。
(1)由A、C、F三种元素按原子个数比1∶1∶1组成的化合物的电子为_________ ,
该化合物与BA3反应生成B的单质,写出该反应的化学反应方程式______________ 。
(2)将化合物EC2通入只含有 n mol 化合物D2E的溶液中,充分反应后,溶液出现浑浊,则该化合物D2E的溶液最多能吸收化合物EC2的物质的量为______ (不考虑水中溶解的化合物EC2)
(3)常温下,若甲、乙两溶液的pH均等于5,则由水电离出的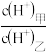 =
=________ ;乙溶液中所含离子的物质的量浓度由大到小的顺序是________________ 。
(4)电解由A与F形成化合物的溶液时,若阴、阳极都用石墨作电极,则阴极发生_______ 反应(填“氧化”、“还原”),阳极的电极反应式为____________________ 。
(1)由A、C、F三种元素按原子个数比1∶1∶1组成的化合物的电子为
该化合物与BA3反应生成B的单质,写出该反应的化学反应方程式
(2)将化合物EC2通入只含有 n mol 化合物D2E的溶液中,充分反应后,溶液出现浑浊,则该化合物D2E的溶液最多能吸收化合物EC2的物质的量为
(3)常温下,若甲、乙两溶液的pH均等于5,则由水电离出的
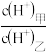 =
=(4)电解由A与F形成化合物的溶液时,若阴、阳极都用石墨作电极,则阴极发生
更新时间:2016-12-09 07:54:13
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】有关物质间有下图所示的转化关系。其中:A的浓溶液与单质B在加热时才发生反应①;A的稀溶液与足量B发生反应②。据此填写下列空白:
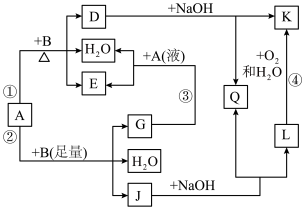
(1)反应④的现象是________________________________________________ 。
(2)写出反应②的离子方程式________________________________________ 。
(3)根据题示信息判断,A的浓溶液和单质B加热时能否产生G,说明理由(写出化学方程式回答):_____________________________________

(1)反应④的现象是
(2)写出反应②的离子方程式
(3)根据题示信息判断,A的浓溶液和单质B加热时能否产生G,说明理由(写出化学方程式回答):
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下图是中学化学中常见物质的转化关系,部分物质和反应条件略去。

(1)写出单质B与强碱溶液反应的离子方程式___________________________ ,写出由沉淀J生成H溶液的离子方程式_______________________________ 。
(2)溶液E中加入氨水时,先生成白色沉淀L,白色沉淀L最终变为红褐色沉淀G,写出L变为G的化学反应方程式______________________________ 。
(3) K是一种集消毒与净水为一体的新型净水剂,试写出G→K的化学方程式:_______________
(4)溶液I中所含金属离子是__________________ 。

(1)写出单质B与强碱溶液反应的离子方程式
(2)溶液E中加入氨水时,先生成白色沉淀L,白色沉淀L最终变为红褐色沉淀G,写出L变为G的化学反应方程式
(3) K是一种集消毒与净水为一体的新型净水剂,试写出G→K的化学方程式:
(4)溶液I中所含金属离子是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】用NaOH标准液滴定未知浓度的H2A溶液,其操作步骤如下:
①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上;
②固定好滴定管并使滴定管尖嘴处充满溶液;
③调节液面至“0”或“0”刻度线以下,并记下读数;
④移取20.00 mL待测液注入洁净的未干燥的锥形瓶中,加入2滴指示剂溶液;
⑤用标准液滴定至终点,记下滴定管液面读数。
请回答下列问题:
(1)以上操作步骤有错误的是___________ (填数字序号)。下列操作中,能造成中和滴定的测定结果偏高的有___________ (填字母序号)。
a.配制标准溶液的固体NaOH中混有KOH杂质
b.中和滴定到达终点时俯视滴定管内液面读数
c.振荡时锥形瓶中溶液飞溅出来
d.滴定到终点读数时,发现滴定管尖嘴处悬挂一滴溶液
(2)某同学在滴定实验中,碱式滴定管中的液面如图所示。侧消耗的NaOH溶液的体积为___________ mL。

(3)常温下向0.2000 mol/L二元酸H2A溶液中滴加0.2000 mol/L NaOH溶液。溶液中H2A、HA-、A2-的物质的量分数( )随溶液pH的变化关系如图所示。
)随溶液pH的变化关系如图所示。
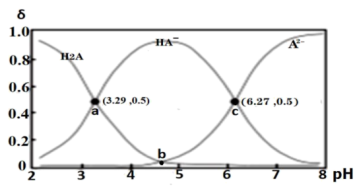
①列说法正确的是___________ (填字母序号)。
A.该滴定过程若选择单一指示剂最好选择甲基橙
B.当V(NaOH)=V(H2A)时,溶液中存在:
C.pH=6.27时,c(HA-)=c(A2-)>c(H+)>c(OH-)
D.V(NaOH):V(H2A)=3:2时,
②常温下H2A的电离平衡常数Ka1=___________ 。
③当pH=6时
___________ mol/L。
④滴加至a、b、c三个交点处,溶液中水的电离程度由大到小依次为___________ (用字母排序)。
①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上;
②固定好滴定管并使滴定管尖嘴处充满溶液;
③调节液面至“0”或“0”刻度线以下,并记下读数;
④移取20.00 mL待测液注入洁净的未干燥的锥形瓶中,加入2滴指示剂溶液;
⑤用标准液滴定至终点,记下滴定管液面读数。
请回答下列问题:
(1)以上操作步骤有错误的是
a.配制标准溶液的固体NaOH中混有KOH杂质
b.中和滴定到达终点时俯视滴定管内液面读数
c.振荡时锥形瓶中溶液飞溅出来
d.滴定到终点读数时,发现滴定管尖嘴处悬挂一滴溶液
(2)某同学在滴定实验中,碱式滴定管中的液面如图所示。侧消耗的NaOH溶液的体积为

(3)常温下向0.2000 mol/L二元酸H2A溶液中滴加0.2000 mol/L NaOH溶液。溶液中H2A、HA-、A2-的物质的量分数(
 )随溶液pH的变化关系如图所示。
)随溶液pH的变化关系如图所示。
①列说法正确的是
A.该滴定过程若选择单一指示剂最好选择甲基橙
B.当V(NaOH)=V(H2A)时,溶液中存在:

C.pH=6.27时,c(HA-)=c(A2-)>c(H+)>c(OH-)
D.V(NaOH):V(H2A)=3:2时,

②常温下H2A的电离平衡常数Ka1=
③当pH=6时

④滴加至a、b、c三个交点处,溶液中水的电离程度由大到小依次为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】盐酸和醋酸是生活中常用的酸。某实验小组进行了以下实验。
(1)对比盐酸和醋酸与NaOH的反应。常温下,用0.1000mol·L−1NaOH溶液分别滴定20mL0.1000mol·L−1的盐酸和醋酸,滴定过程中溶液pH的变化曲线如下图所示。
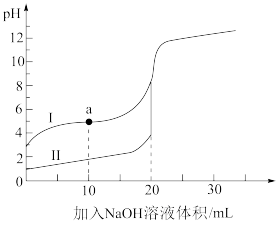
①表示滴定盐酸的曲线是_______ (填“I”或“II”)。
②a点溶液中,离子浓度由大到小的顺序为_______ 。
③V[NaOH(aq)]=20mL时,c(Cl−)_______ c(CH3COO−)(填“>”“<”或“=”)。
(2)对比盐酸和醋酸与NaClO的反应。资料:25℃时CH3COOH和HClO的电离平衡常数Ka分别为1.75×10−5和4.0×10−8。
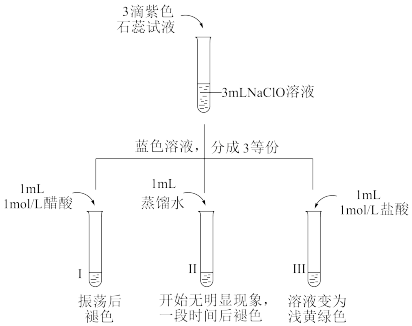
①NaClO溶液中加入石蕊溶液变蓝,用化学用语解释原因_______ 。
②实验II的目的是_______ 。
③结合资料和化学用语解释I的实验现象_______ 。
④III中溶液变为浅黄绿色,用离子方程式解释原因_______ 。
(1)对比盐酸和醋酸与NaOH的反应。常温下,用0.1000mol·L−1NaOH溶液分别滴定20mL0.1000mol·L−1的盐酸和醋酸,滴定过程中溶液pH的变化曲线如下图所示。

①表示滴定盐酸的曲线是
②a点溶液中,离子浓度由大到小的顺序为
③V[NaOH(aq)]=20mL时,c(Cl−)
(2)对比盐酸和醋酸与NaClO的反应。资料:25℃时CH3COOH和HClO的电离平衡常数Ka分别为1.75×10−5和4.0×10−8。

①NaClO溶液中加入石蕊溶液变蓝,用化学用语解释原因
②实验II的目的是
③结合资料和化学用语解释I的实验现象
④III中溶液变为浅黄绿色,用离子方程式解释原因
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】滴定是一种定量分析的方法,在科学研究中具有广泛的应用。
(1)对比盐酸和醋酸分别与 的反应
的反应
室温下,用0.1mol/LNaOH溶液分别滴定20mL0.1mol/L的醋酸和盐酸溶液,滴定过程中溶液pH的变化曲线如下图所示。
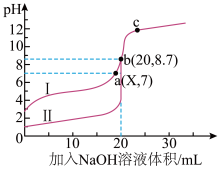
①曲线Ⅱ表示滴定盐酸的过程,判断的理由是_______ 。
②a点溶液中,离子浓度大小关系为_______ 。
③b点溶液中,由水电离的
_______  。
。
④ 时,
时,
_______  (填“>”“<”或“=”,下题同)。
(填“>”“<”或“=”,下题同)。
⑤c点溶液中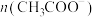
_______ b点的。
(2)测定某些物质的含量。 由
如测定血液中钙的含量时,进行如下实验:
ⅰ可将amL血液用蒸馏水稀释后,向其中加入足量草酸铵 晶体,反应生成
晶体,反应生成 沉淀,过滤、洗涤,将沉淀用稀硫酸处理得
沉淀,过滤、洗涤,将沉淀用稀硫酸处理得 溶液。
溶液。
ⅱ将ⅰ得到的 溶液,再用
溶液,再用 酸性溶液滴定,氧化产物为
酸性溶液滴定,氧化产物为 ,还原产物为
,还原产物为 。
。
ⅲ终点时用去 的
的 溶液。
溶液。
①写出用 酸性溶液滴定
酸性溶液滴定 的离子方程式
的离子方程式_______ 。
②如何判定滴定终点_______ 。
③计算:血液中含钙离子的浓度为_______  (用字母表示)。
(用字母表示)。
(1)对比盐酸和醋酸分别与
 的反应
的反应室温下,用0.1mol/LNaOH溶液分别滴定20mL0.1mol/L的醋酸和盐酸溶液,滴定过程中溶液pH的变化曲线如下图所示。

①曲线Ⅱ表示滴定盐酸的过程,判断的理由是
②a点溶液中,离子浓度大小关系为
③b点溶液中,由水电离的

 。
。④
 时,
时,
 (填“>”“<”或“=”,下题同)。
(填“>”“<”或“=”,下题同)。⑤c点溶液中
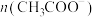
(2)测定某些物质的含量。 由
如测定血液中钙的含量时,进行如下实验:
ⅰ可将amL血液用蒸馏水稀释后,向其中加入足量草酸铵
 晶体,反应生成
晶体,反应生成 沉淀,过滤、洗涤,将沉淀用稀硫酸处理得
沉淀,过滤、洗涤,将沉淀用稀硫酸处理得 溶液。
溶液。ⅱ将ⅰ得到的
 溶液,再用
溶液,再用 酸性溶液滴定,氧化产物为
酸性溶液滴定,氧化产物为 ,还原产物为
,还原产物为 。
。ⅲ终点时用去
 的
的 溶液。
溶液。①写出用
 酸性溶液滴定
酸性溶液滴定 的离子方程式
的离子方程式②如何判定滴定终点
③计算:血液中含钙离子的浓度为
 (用字母表示)。
(用字母表示)。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D、E五种短周期元素,已知:
①原子半径递增顺序为:A、D、C、B、E
②短周期(除稀有气体元素外)所有元素中A的原子半径与E的原子半径之比为最小
③B、C、D三种元素电子层相同,三者原子序数之和为21,且D原子次外层电子数为最外层电子数的,
请回答下列问题:
(1)写出E单质在D单质中燃烧产物的电子式:_________ 。(2)C2A4·H2O与NH3·H2O相似,水溶液也呈弱碱性,用电离方程式表示其水溶液呈弱碱性的原因:___________ 。(3)B、D、E三种元素可组成常见化合物X,A、B、D、E可组成常见化合物Y,X、Y均是生活中常见的化学试剂,它们在一定条件下可互相转化。当a mol Y转化成amol X时:(溶液中进行)
①若加入a mol纯净物Z就可实现转化,则加入Z为___ (填一种Z物质化学式)。②若加入0.5a mol纯净物Z就可实现转化,则加入Z为___ (填一种Z物质化学式)。(4)C2A4可用作高能燃料电池的燃料,生成物之一为C的单质,惰性材料作电极,KOH作电解质溶液构成原电池,写出负极的电极反应:__________ ;用该电池电解过量CuSO4溶液,共收集到3.36 L(标准状况)的气体,电池消耗6.4 g C2A4,则该燃料的利用率为_____ 。
①原子半径递增顺序为:A、D、C、B、E
②短周期(除稀有气体元素外)所有元素中A的原子半径与E的原子半径之比为最小
③B、C、D三种元素电子层相同,三者原子序数之和为21,且D原子次外层电子数为最外层电子数的,
请回答下列问题:
(1)写出E单质在D单质中燃烧产物的电子式:
①若加入a mol纯净物Z就可实现转化,则加入Z为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】锑(Sb)及其化合物广泛用于化工生产。以粗锑氧为原料制备Sb和 的工艺流程如图所示。
的工艺流程如图所示。
Ⅰ.粗锑氧主要成分为 ,含有PbO、
,含有PbO、 、
、 、ZnO、FeO等杂质;
、ZnO、FeO等杂质;
Ⅱ.浸出液主要含 、
、 和
和 ,还含有
,还含有 、
、 、
、 和
和 等杂质;
等杂质;
Ⅲ. 为两性氧化物;
为两性氧化物;
Ⅳ.25℃时, 、
、
回答下列问题:
(1)已知 在熔融状态下不导电,则
在熔融状态下不导电,则 是
是________ 化合物(填“共价”或“离子”)。
(2)“还原”是用锑粉还原高价金属离子。其中Sb将 转化为
转化为 ,该转化有利于“水解”时锑与铁的分离,避免在滤渣Ⅱ中混入杂质
,该转化有利于“水解”时锑与铁的分离,避免在滤渣Ⅱ中混入杂质_________ (填化学式)。
(3)“过滤”得到滤渣成分SbOCl,加过量氨水对其“除氯”的化学反应方程式为___________ ,“除氯”步骤能否用NaOH溶液代替氨水,原因是:____________________ 。
(4)“除砷”时有 生成,该反应的离子方程式为
生成,该反应的离子方程式为_____________________ 。
(5)“电解”过程中单位时间内锑的产率与电压大小关系如图所示。当电压在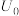 V之前时,阴极主要的电极反应式
V之前时,阴极主要的电极反应式__________ ,当电压超过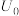 V时,单位时间内产率降低的原因可能是
V时,单位时间内产率降低的原因可能是______________ 。 的纯度,操作方法为:称取0.30g样品溶于稀硫酸中,用0.2000mol/L的硫酸铈
的纯度,操作方法为:称取0.30g样品溶于稀硫酸中,用0.2000mol/L的硫酸铈 滴定,使用邻二氮菲-亚铁指示剂,发生反应:
滴定,使用邻二氮菲-亚铁指示剂,发生反应: ,重复3次实验平均消耗标准溶液15.60mL,则产物的纯度为
,重复3次实验平均消耗标准溶液15.60mL,则产物的纯度为________ %。
 的工艺流程如图所示。
的工艺流程如图所示。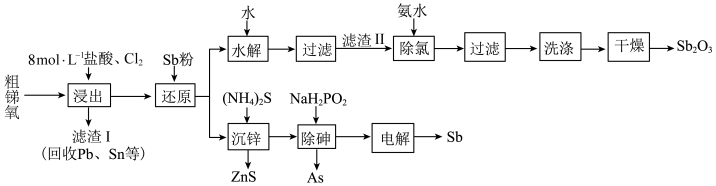
Ⅰ.粗锑氧主要成分为
 ,含有PbO、
,含有PbO、 、
、 、ZnO、FeO等杂质;
、ZnO、FeO等杂质;Ⅱ.浸出液主要含
 、
、 和
和 ,还含有
,还含有 、
、 、
、 和
和 等杂质;
等杂质;Ⅲ.
 为两性氧化物;
为两性氧化物;Ⅳ.25℃时,
 、
、
回答下列问题:
(1)已知
 在熔融状态下不导电,则
在熔融状态下不导电,则 是
是(2)“还原”是用锑粉还原高价金属离子。其中Sb将
 转化为
转化为 ,该转化有利于“水解”时锑与铁的分离,避免在滤渣Ⅱ中混入杂质
,该转化有利于“水解”时锑与铁的分离,避免在滤渣Ⅱ中混入杂质(3)“过滤”得到滤渣成分SbOCl,加过量氨水对其“除氯”的化学反应方程式为
(4)“除砷”时有
 生成,该反应的离子方程式为
生成,该反应的离子方程式为(5)“电解”过程中单位时间内锑的产率与电压大小关系如图所示。当电压在
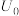 V之前时,阴极主要的电极反应式
V之前时,阴极主要的电极反应式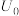 V时,单位时间内产率降低的原因可能是
V时,单位时间内产率降低的原因可能是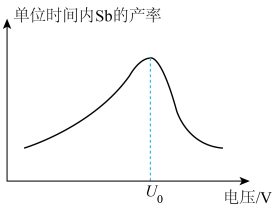
 的纯度,操作方法为:称取0.30g样品溶于稀硫酸中,用0.2000mol/L的硫酸铈
的纯度,操作方法为:称取0.30g样品溶于稀硫酸中,用0.2000mol/L的硫酸铈 滴定,使用邻二氮菲-亚铁指示剂,发生反应:
滴定,使用邻二氮菲-亚铁指示剂,发生反应: ,重复3次实验平均消耗标准溶液15.60mL,则产物的纯度为
,重复3次实验平均消耗标准溶液15.60mL,则产物的纯度为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】一氯甲烷主要用于生产甲基氯硅烷,一氯乙烯主要用于生产聚氯乙烯等高聚物,1,2-二氯乙烷常用作有机溶剂和化工原料。回答下列问题:
I.在加热或光照条件下,“甲烷—氯气”法得到一氯甲烷是按自由基机理进行的,即
 。该反应涉及两个基元步骤①、②,其相对能量—反应历程图如下:
。该反应涉及两个基元步骤①、②,其相对能量—反应历程图如下: 键能为4.56eV,
键能为4.56eV, 键能为4.46eV,1eV相当于
键能为4.46eV,1eV相当于 。则步骤①的焓变
。则步骤①的焓变 =
=___________  ;一氯取代反应的总焓变
;一氯取代反应的总焓变 =
=___________ (用 、
、 表示)。
表示)。
Ⅱ.一氯乙烯(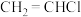 )的工业生产方法之一是乙烯氯化裂解法,该方法分以下两个过程进行:
)的工业生产方法之一是乙烯氯化裂解法,该方法分以下两个过程进行:
乙烯氯化加成:

1,2-二氯乙烷裂解:ClCH2CH2Cl(g)⇌CH2=CHCl(g)+HCl(g) =+73.4
=+73.4
(2)乙烯氯化加成反应进行的热力学趋势很大,原因是___________ 。1,2-二氯乙烷裂解反应 ,则该裂解反应能自发进行的最低温度约为
,则该裂解反应能自发进行的最低温度约为___________ K(保留整数)。
(3)在某恒压密闭容器中通入一定量的 ,仅发生1,2-二氯乙烷裂解生成氯乙烯和氯化氢的反应,实验测得
,仅发生1,2-二氯乙烷裂解生成氯乙烯和氯化氢的反应,实验测得 的转化率随温度和反应时间的关系如图所示。
的转化率随温度和反应时间的关系如图所示。 、
、 、
、 的大小关系为
的大小关系为___________ ,原因是___________ 。
②若 点刚好达到平衡状态,则
点刚好达到平衡状态,则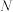 点的
点的
___________  (填“大于”“小于”或“等于”)。
(填“大于”“小于”或“等于”)。
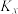 是以物质的量分数表示的平衡常数,则
是以物质的量分数表示的平衡常数,则 温度下1,2-二氯乙烷裂解生成氯乙烯和氯化氢的反应的
温度下1,2-二氯乙烷裂解生成氯乙烯和氯化氢的反应的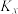 =
=___________ (写成分数形式)。
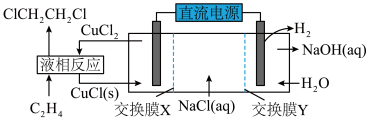
Ⅲ.一种电化学合成1,2-二氯乙烷的实验装置如图所示。___________ 。
I.在加热或光照条件下,“甲烷—氯气”法得到一氯甲烷是按自由基机理进行的,即

 。该反应涉及两个基元步骤①、②,其相对能量—反应历程图如下:
。该反应涉及两个基元步骤①、②,其相对能量—反应历程图如下: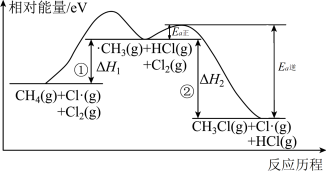
 键能为4.56eV,
键能为4.56eV, 键能为4.46eV,1eV相当于
键能为4.46eV,1eV相当于 。则步骤①的焓变
。则步骤①的焓变 =
= ;一氯取代反应的总焓变
;一氯取代反应的总焓变 =
= 、
、 表示)。
表示)。Ⅱ.一氯乙烯(
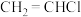 )的工业生产方法之一是乙烯氯化裂解法,该方法分以下两个过程进行:
)的工业生产方法之一是乙烯氯化裂解法,该方法分以下两个过程进行:乙烯氯化加成:


1,2-二氯乙烷裂解:ClCH2CH2Cl(g)⇌CH2=CHCl(g)+HCl(g)
 =+73.4
=+73.4
(2)乙烯氯化加成反应进行的热力学趋势很大,原因是
 ,则该裂解反应能自发进行的最低温度约为
,则该裂解反应能自发进行的最低温度约为(3)在某恒压密闭容器中通入一定量的
 ,仅发生1,2-二氯乙烷裂解生成氯乙烯和氯化氢的反应,实验测得
,仅发生1,2-二氯乙烷裂解生成氯乙烯和氯化氢的反应,实验测得 的转化率随温度和反应时间的关系如图所示。
的转化率随温度和反应时间的关系如图所示。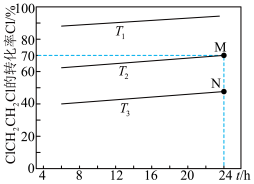
 、
、 、
、 的大小关系为
的大小关系为②若
 点刚好达到平衡状态,则
点刚好达到平衡状态,则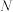 点的
点的
 (填“大于”“小于”或“等于”)。
(填“大于”“小于”或“等于”)。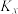 是以物质的量分数表示的平衡常数,则
是以物质的量分数表示的平衡常数,则 温度下1,2-二氯乙烷裂解生成氯乙烯和氯化氢的反应的
温度下1,2-二氯乙烷裂解生成氯乙烯和氯化氢的反应的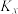 =
=Ⅲ.一种电化学合成1,2-二氯乙烷的实验装置如图所示。
您最近一年使用:0次




