已知2NO2(g) N2O4(g)ΔH(298K)=-52.7kJ·mol-1,某课外活动小组为了探究温度和压强对化学平衡的影响,做了如下两组实验:
N2O4(g)ΔH(298K)=-52.7kJ·mol-1,某课外活动小组为了探究温度和压强对化学平衡的影响,做了如下两组实验:
Ⅰ.该小组的同学取了两个烧瓶A和B,分别加入相同浓度的NO2与N2O4的混合气体,中间用夹子夹紧,并将A和B浸入到已盛有水的两个烧杯中(如图所示),然后分别向两个烧杯中加入浓硫酸和NH4NO3固体。
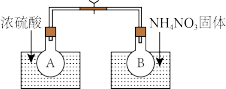
请回答:
(1)A中的现象_____________ ,B中的现象_______________________ ;
(2)由此可知,降低温度,该化学平衡向_____ (填“正”或“逆”)反应方向移动;
(3)该化学反应的浓度平衡常数表达式为___________ ,升高温度,该反应中NO2的转化率将________ (填“增大”、“减小”或“不变”)。
Ⅱ.在三支容积均为30cm3针筒中分别抽入10cm3NO2气体,将针筒前端封闭。
(4)将第二支针筒活塞迅速推至5cm3处,此时气体的颜色变深,一段时间后气体颜色又变浅了,但仍比第一支针筒气体的颜色深。
①推进针筒后颜色变深的原因是_________________________ ;
②一段时间后气体颜色又变浅的原因是__________________________ ;
③由此实验得出的结论是___________________ 。
(5)将第三支针筒活塞拉至20cm3处,该同学观察到的现象是________________ ;在此过程中,该反应的化学平衡常数将________ (填“增大”、“减小”或“不变”,下同),NO2的转化率将____ 。
 N2O4(g)ΔH(298K)=-52.7kJ·mol-1,某课外活动小组为了探究温度和压强对化学平衡的影响,做了如下两组实验:
N2O4(g)ΔH(298K)=-52.7kJ·mol-1,某课外活动小组为了探究温度和压强对化学平衡的影响,做了如下两组实验:Ⅰ.该小组的同学取了两个烧瓶A和B,分别加入相同浓度的NO2与N2O4的混合气体,中间用夹子夹紧,并将A和B浸入到已盛有水的两个烧杯中(如图所示),然后分别向两个烧杯中加入浓硫酸和NH4NO3固体。

请回答:
(1)A中的现象
(2)由此可知,降低温度,该化学平衡向
(3)该化学反应的浓度平衡常数表达式为
Ⅱ.在三支容积均为30cm3针筒中分别抽入10cm3NO2气体,将针筒前端封闭。
(4)将第二支针筒活塞迅速推至5cm3处,此时气体的颜色变深,一段时间后气体颜色又变浅了,但仍比第一支针筒气体的颜色深。
①推进针筒后颜色变深的原因是
②一段时间后气体颜色又变浅的原因是
③由此实验得出的结论是
(5)将第三支针筒活塞拉至20cm3处,该同学观察到的现象是
13-14高二上·吉林·期末 查看更多[2]
更新时间:2016-12-09 08:25:49
|
相似题推荐
【推荐1】近些年,全球变暖明显,尽快实现碳达峰、碳中和成为紧迫目标。为实现该目标,一方面要减少 的排放量,另一方面可以利用
的排放量,另一方面可以利用 参与反应,实现能源再生。
参与反应,实现能源再生。
(1) 催化加氢制甲醇能有效利用
催化加氢制甲醇能有效利用 资源,涉及的反应如下:
资源,涉及的反应如下:
反应Ⅰ:

反应Ⅱ:
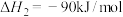
①写出 催化加氢直接合成甲醇反应的热化学方程式
催化加氢直接合成甲醇反应的热化学方程式___________ ,写出该反应能自发进行的条件___________ 。
②其他条件相同时, 催化加氢制甲醇,
催化加氢制甲醇, 的平衡总转化率随着反应温度的升高先减小后增大,说明原因
的平衡总转化率随着反应温度的升高先减小后增大,说明原因___________ 。
(2) 与烷烃的耦合反应有利于减少空气中
与烷烃的耦合反应有利于减少空气中 含量,已知
含量,已知 与
与 发生耦合反应时涉及的反应如下:
发生耦合反应时涉及的反应如下:
反应Ⅰ:
反应Ⅱ: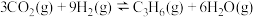
反应Ⅲ:
①在恒温恒容密闭容器中充入一定量的 ,若只发生反应Ⅰ,达到平衡时压强增大
,若只发生反应Ⅰ,达到平衡时压强增大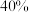 ,计算平衡时
,计算平衡时 的转化率
的转化率___________ (不要求计算过程)。
②在某恒温恒压的容器中充入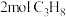 和
和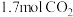 ,达平衡后,容器中
,达平衡后,容器中 、
、 、
、 分别为
分别为 、
、 、
、 ,反应III的压力平衡常数
,反应III的压力平衡常数 ,计算平衡时容器中
,计算平衡时容器中 的物质的量
的物质的量___________ (不要求计算过程)。
③为提高丙烷与 耦合过程中
耦合过程中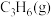 的产率,写出采取的措施
的产率,写出采取的措施___________ (请举一例)。
(3)一种二甲醚和 直接制备碳酸二甲酯(
直接制备碳酸二甲酯( )的电化学方法如下图所示。
)的电化学方法如下图所示。 电极连接的直流电源的电极名称
电极连接的直流电源的电极名称___________ ,写出 电极的电极反应式
电极的电极反应式___________ 。
 的排放量,另一方面可以利用
的排放量,另一方面可以利用 参与反应,实现能源再生。
参与反应,实现能源再生。(1)
 催化加氢制甲醇能有效利用
催化加氢制甲醇能有效利用 资源,涉及的反应如下:
资源,涉及的反应如下:反应Ⅰ:


反应Ⅱ:

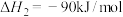
①写出
 催化加氢直接合成甲醇反应的热化学方程式
催化加氢直接合成甲醇反应的热化学方程式②其他条件相同时,
 催化加氢制甲醇,
催化加氢制甲醇, 的平衡总转化率随着反应温度的升高先减小后增大,说明原因
的平衡总转化率随着反应温度的升高先减小后增大,说明原因(2)
 与烷烃的耦合反应有利于减少空气中
与烷烃的耦合反应有利于减少空气中 含量,已知
含量,已知 与
与 发生耦合反应时涉及的反应如下:
发生耦合反应时涉及的反应如下:反应Ⅰ:

反应Ⅱ:
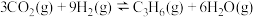
反应Ⅲ:

①在恒温恒容密闭容器中充入一定量的
 ,若只发生反应Ⅰ,达到平衡时压强增大
,若只发生反应Ⅰ,达到平衡时压强增大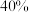 ,计算平衡时
,计算平衡时 的转化率
的转化率②在某恒温恒压的容器中充入
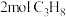 和
和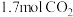 ,达平衡后,容器中
,达平衡后,容器中 、
、 、
、 分别为
分别为 、
、 、
、 ,反应III的压力平衡常数
,反应III的压力平衡常数 ,计算平衡时容器中
,计算平衡时容器中 的物质的量
的物质的量③为提高丙烷与
 耦合过程中
耦合过程中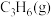 的产率,写出采取的措施
的产率,写出采取的措施(3)一种二甲醚和
 直接制备碳酸二甲酯(
直接制备碳酸二甲酯( )的电化学方法如下图所示。
)的电化学方法如下图所示。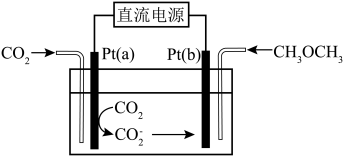
 电极连接的直流电源的电极名称
电极连接的直流电源的电极名称 电极的电极反应式
电极的电极反应式
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐2】尿素/H2O2溶液可用于烟气的脱硫脱硝。
(1)已知T℃时,2SO2(g)+O2(g) 2SO3(g) △H1
2SO3(g) △H1
2H2O2(I)=2H2O(I)+O2(g) △H2
SO3(g)+H2O(I))=H2SO4(I) △H3
则SO2(g)+H2O2(I))=H2SO4(I) △H4=__________ (用含△H1、△H2、△H3的代数式表示)
(2)尿素[CO(NH2)2]溶液对NOx及SO2有一定的脱除率。将SO2和NOx (N〇约占90%)通入氧气的体积分数为7%、尿素浓度为5%的反应器中进行反应。
①烟气中SO2最终转化为一种正盐,其化学式为______________ ;NO和NO2以物质的量之比1:1与CO(NH2)2反应生成无毒气体的化学方程式为_______________ 。
②氨基甲酸铵(H2NCOONH4)是尿素的水解产物,将一定量的氨基甲酸铵置于恒容密闭容器中,发生反应:NH2COONH4(s) 2NH3(g)+CO2(g) △H,实验测得不同温度下平衡时气体的总浓度如下表:
2NH3(g)+CO2(g) △H,实验测得不同温度下平衡时气体的总浓度如下表:
该反应的△H__________ (填“>”或“<”)0;348K时,该反应的平衡常数K__________________ 。
(3)其他条件不变,向尿素溶液中添加H2O2溶液,测得不同 pH下氮氧化物的脱除率与时间的关系如图所示。
①NO与H2O2发生反应生成亚硝酸时,氧化剂与还原剂的物质的量之比为____________ 。
(2)脱硝时,最佳pH为_________ ;在碱性较强时,NOx脱除率降低,其原因是___________ (任写一点)。
(1)已知T℃时,2SO2(g)+O2(g)
 2SO3(g) △H1
2SO3(g) △H12H2O2(I)=2H2O(I)+O2(g) △H2
SO3(g)+H2O(I))=H2SO4(I) △H3
则SO2(g)+H2O2(I))=H2SO4(I) △H4=
(2)尿素[CO(NH2)2]溶液对NOx及SO2有一定的脱除率。将SO2和NOx (N〇约占90%)通入氧气的体积分数为7%、尿素浓度为5%的反应器中进行反应。
①烟气中SO2最终转化为一种正盐,其化学式为
②氨基甲酸铵(H2NCOONH4)是尿素的水解产物,将一定量的氨基甲酸铵置于恒容密闭容器中,发生反应:NH2COONH4(s)
 2NH3(g)+CO2(g) △H,实验测得不同温度下平衡时气体的总浓度如下表:
2NH3(g)+CO2(g) △H,实验测得不同温度下平衡时气体的总浓度如下表:温度/K | 338 | 343 | 348 | 353 |
平衡时气体的总浓度/mol • L-1 | 0.36 | 0.48 | 0.60 | 0.72 |
该反应的△H
(3)其他条件不变,向尿素溶液中添加H2O2溶液,测得不同 pH下氮氧化物的脱除率与时间的关系如图所示。
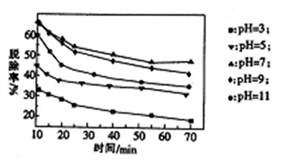
①NO与H2O2发生反应生成亚硝酸时,氧化剂与还原剂的物质的量之比为
(2)脱硝时,最佳pH为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】甲烷是重要的气体燃料和化工原料,由CH4制取合成气(CO、H2)的反应原理为CH4(g)+H2O(g) CO(g)+3H2(g) ΔH>0。回答下列问题:
CO(g)+3H2(g) ΔH>0。回答下列问题:
(1)若生成7g CO,吸收热量a kJ,相关化学键的键能(断裂1mol化学键所吸收的能量),如表所示。
①C≡O(CO)的键能为_______ (用含a的式子表示) kJ/mol。
②当体系温度等于T K时ΔH−TΔS=0,温度大于T时ΔH−TΔS_______ (填“>”“<”或“=”)0。
(2)在体积为1L的恒容密闭容器中通入1mol CH4和1mol H2O(g),在不同条件下发生反应CH4(g)+H2O(g) CO(g)+3H2(g),测得平衡时H2O(g)的体积分数与温度、压强的关系如图所示。
CO(g)+3H2(g),测得平衡时H2O(g)的体积分数与温度、压强的关系如图所示。
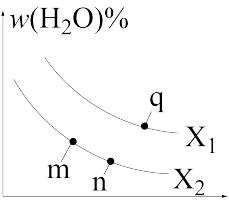
①X表示_______ (填“温度”或“压强”),该反应的平衡常数表达式Kc=_______ 。
②m、n、q点的平衡常数由大到小的顺序为_______ 。
③若q点对应的纵坐标为30,此时甲烷的转化率为_______ ,该条件下平衡常数Kc=_______ (保留两位有效数字)。
 CO(g)+3H2(g) ΔH>0。回答下列问题:
CO(g)+3H2(g) ΔH>0。回答下列问题:(1)若生成7g CO,吸收热量a kJ,相关化学键的键能(断裂1mol化学键所吸收的能量),如表所示。
| 化学键 | C-H | H-H | H-O |
| 键能/ kJ/mol | 414 | 436 | 467 |
①C≡O(CO)的键能为
②当体系温度等于T K时ΔH−TΔS=0,温度大于T时ΔH−TΔS
(2)在体积为1L的恒容密闭容器中通入1mol CH4和1mol H2O(g),在不同条件下发生反应CH4(g)+H2O(g)
 CO(g)+3H2(g),测得平衡时H2O(g)的体积分数与温度、压强的关系如图所示。
CO(g)+3H2(g),测得平衡时H2O(g)的体积分数与温度、压强的关系如图所示。
①X表示
②m、n、q点的平衡常数由大到小的顺序为
③若q点对应的纵坐标为30,此时甲烷的转化率为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】消除城市中汽车尾气的污染是一个很重要的课题.回答下列问题:
(1)汽车排气管装有三元催化剂装置,在催化剂表面通过发生吸附、解吸消除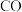 、
、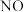 等污染物.反应机理如下[
等污染物.反应机理如下[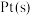 表示催化剂,右上角带“*”表示吸附状态]:
表示催化剂,右上角带“*”表示吸附状态]:
①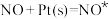 ②
②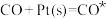 ③
③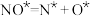
④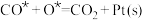 ⑤
⑤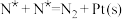 ⑥
⑥
经测定汽车尾气中生成物浓度随温度T变化关系如图所示.
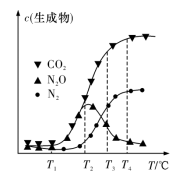
图中温度为 时反应⑤的活化能
时反应⑤的活化能__________ 反应④的活化能(填“<”“>”或“=”);温度为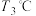 时发生的主要反应为
时发生的主要反应为_________ (填“④”“⑤”或“⑥”).
(2)已知: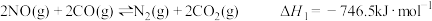 ,据此可在一定条件下反应消除
,据此可在一定条件下反应消除 和
和 的污染;某研究小组在三个容积均为
的污染;某研究小组在三个容积均为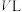 的恒容密闭容器中,分别充入
的恒容密闭容器中,分别充入 和
和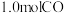 ,在三种不同实验条件(见下表)下进行上述反应,反应体系的总压强
,在三种不同实验条件(见下表)下进行上述反应,反应体系的总压强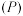 随时间变化情况如图所示:
随时间变化情况如图所示:
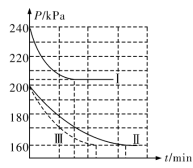
①曲线Ⅲ对应的实验编号是_______________ ,曲线Ⅰ中压强降低的原因是_____________________________ .
②由曲线Ⅱ数据计算出对应条件下的压强平衡常数
____________ ;若在曲线Ⅲ对应条件下, 、
、 、
、 、
、 的分压依次是
的分压依次是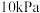 、
、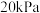 、
、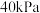 、
、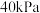 ,则此时反应的速率
,则此时反应的速率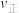
_______ 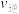 (填“<”“=”或“>”).
(填“<”“=”或“>”).
(3)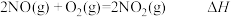 的反应机理和各基元反应(基元反应是指在反应中一步直接转化为产物的反应,又称为简单反应)的活化能及速率方程如下:
的反应机理和各基元反应(基元反应是指在反应中一步直接转化为产物的反应,又称为简单反应)的活化能及速率方程如下:
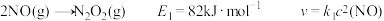

(提示:为第一步正反应的活化能)
___________ ,平衡常数K与上述反应速率常数、、、的关系式为__________ .
(1)汽车排气管装有三元催化剂装置,在催化剂表面通过发生吸附、解吸消除
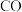 、
、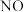 等污染物.反应机理如下[
等污染物.反应机理如下[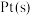 表示催化剂,右上角带“*”表示吸附状态]:
表示催化剂,右上角带“*”表示吸附状态]:①
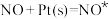 ②
②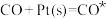 ③
③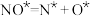
④
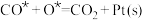 ⑤
⑤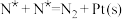 ⑥
⑥
经测定汽车尾气中生成物浓度随温度T变化关系如图所示.

图中温度为
 时反应⑤的活化能
时反应⑤的活化能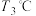 时发生的主要反应为
时发生的主要反应为(2)已知:
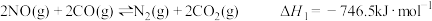 ,据此可在一定条件下反应消除
,据此可在一定条件下反应消除 和
和 的污染;某研究小组在三个容积均为
的污染;某研究小组在三个容积均为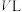 的恒容密闭容器中,分别充入
的恒容密闭容器中,分别充入 和
和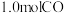 ,在三种不同实验条件(见下表)下进行上述反应,反应体系的总压强
,在三种不同实验条件(见下表)下进行上述反应,反应体系的总压强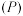 随时间变化情况如图所示:
随时间变化情况如图所示:
| 实验编号 | a | b | c |
| 温度/K | 500 | 500 | 600 |
催化剂的比表面积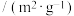 | 82 | 124 | 124 |
②由曲线Ⅱ数据计算出对应条件下的压强平衡常数

 、
、 、
、 、
、 的分压依次是
的分压依次是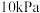 、
、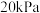 、
、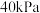 、
、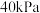 ,则此时反应的速率
,则此时反应的速率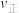
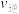 (填“<”“=”或“>”).
(填“<”“=”或“>”).(3)
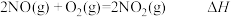 的反应机理和各基元反应(基元反应是指在反应中一步直接转化为产物的反应,又称为简单反应)的活化能及速率方程如下:
的反应机理和各基元反应(基元反应是指在反应中一步直接转化为产物的反应,又称为简单反应)的活化能及速率方程如下: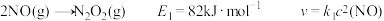

(提示:为第一步正反应的活化能)
您最近一年使用:0次
【推荐2】为了实现“碳达峰、碳中和”的目标,可以用 为碳源制取多种化学物质。
为碳源制取多种化学物质。
(1) 与
与 在固载金属催化剂上发生反应:
在固载金属催化剂上发生反应: ,下列叙述正确的是___________(填字母)。
,下列叙述正确的是___________(填字母)。
(2) 与
与 合成尿素的反应为
合成尿素的反应为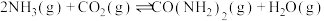 ,下图是合成尿素的历程及能量变化,TS表示过渡态。
,下图是合成尿素的历程及能量变化,TS表示过渡态。___________ 个基元反应,其中决速步骤的方程式是___________ 。
(3)以 、
、 为原料合成
为原料合成 的主要反应如下:
的主要反应如下:
Ⅰ.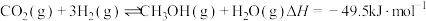
Ⅱ.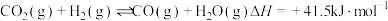
①不同条件下,按照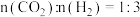 投料,同时发生反应Ⅰ和反应Ⅱ,
投料,同时发生反应Ⅰ和反应Ⅱ, 的平衡转化率如图甲所示。
的平衡转化率如图甲所示。___________ (填“正向”、“逆向”或“不”)移动;压强为 时,温度高于300℃后,
时,温度高于300℃后, 的平衡转化率随温度升高而增大的主要原因是
的平衡转化率随温度升高而增大的主要原因是___________ 。
②在温度为T℃下,将amol 和bmol
和bmol 充入容积为VL的恒容密闭容器中,同时发生反应Ⅰ和反应Ⅱ,体系中各组分分压(各组分分压=总压×各组分物质的量分数)随时间的变化情况如图乙所示。图中缺少一种组分(CO)的分压变化,T℃时,反应Ⅰ的平衡常数
充入容积为VL的恒容密闭容器中,同时发生反应Ⅰ和反应Ⅱ,体系中各组分分压(各组分分压=总压×各组分物质的量分数)随时间的变化情况如图乙所示。图中缺少一种组分(CO)的分压变化,T℃时,反应Ⅰ的平衡常数
___________ 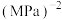 (用分压代替浓度,计算结果保留两位有效数字)。
(用分压代替浓度,计算结果保留两位有效数字)。 电催化还原为乙烯,如下图所示,写出阴极的电极反应式:
电催化还原为乙烯,如下图所示,写出阴极的电极反应式:___________ ;若电解前两极区溶液的质量相等,电解一段时间后,阴阳两极共收集气体(标准状况下)8.96L(假设气体全部逸出),两极区溶液的质量差为___________ g。
 为碳源制取多种化学物质。
为碳源制取多种化学物质。(1)
 与
与 在固载金属催化剂上发生反应:
在固载金属催化剂上发生反应: ,下列叙述正确的是___________(填字母)。
,下列叙述正确的是___________(填字母)。| A.恒温、恒容条件下,加入惰性气体,压强增大,反应速率加快 |
| B.恒温、恒容条件下,加入氢气,活化分子百分数增大,反应速率加快 |
| C.升高温度,活化分子百分数增大,有效碰撞频率增大,反应速率加快 |
| D.加入合适的催化剂,能实现单位时间内转化率增大 |
(2)
 与
与 合成尿素的反应为
合成尿素的反应为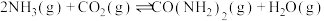 ,下图是合成尿素的历程及能量变化,TS表示过渡态。
,下图是合成尿素的历程及能量变化,TS表示过渡态。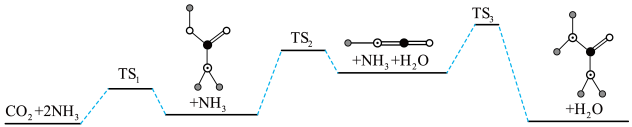
(3)以
 、
、 为原料合成
为原料合成 的主要反应如下:
的主要反应如下:Ⅰ.
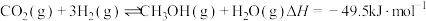
Ⅱ.
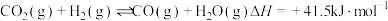
①不同条件下,按照
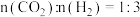 投料,同时发生反应Ⅰ和反应Ⅱ,
投料,同时发生反应Ⅰ和反应Ⅱ, 的平衡转化率如图甲所示。
的平衡转化率如图甲所示。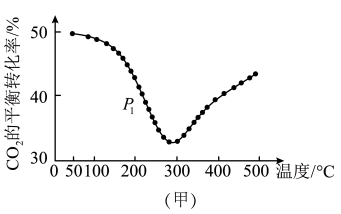
 时,温度高于300℃后,
时,温度高于300℃后, 的平衡转化率随温度升高而增大的主要原因是
的平衡转化率随温度升高而增大的主要原因是②在温度为T℃下,将amol
 和bmol
和bmol 充入容积为VL的恒容密闭容器中,同时发生反应Ⅰ和反应Ⅱ,体系中各组分分压(各组分分压=总压×各组分物质的量分数)随时间的变化情况如图乙所示。图中缺少一种组分(CO)的分压变化,T℃时,反应Ⅰ的平衡常数
充入容积为VL的恒容密闭容器中,同时发生反应Ⅰ和反应Ⅱ,体系中各组分分压(各组分分压=总压×各组分物质的量分数)随时间的变化情况如图乙所示。图中缺少一种组分(CO)的分压变化,T℃时,反应Ⅰ的平衡常数
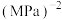 (用分压代替浓度,计算结果保留两位有效数字)。
(用分压代替浓度,计算结果保留两位有效数字)。
 电催化还原为乙烯,如下图所示,写出阴极的电极反应式:
电催化还原为乙烯,如下图所示,写出阴极的电极反应式: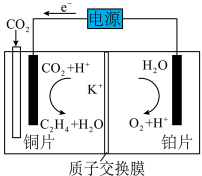
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐3】工业废气、汽车尾气排放出的 、
、 等是形成酸雨的主要物质,其综合治理是当前重要的研究课题。回答下列问题:
等是形成酸雨的主要物质,其综合治理是当前重要的研究课题。回答下列问题:
(1)汽车尾气中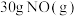 与足量
与足量 在一定温度和催化剂下反应生成
在一定温度和催化剂下反应生成 和
和 ,放出373.25kJ热量,写出该可逆反应的热化学方程式
,放出373.25kJ热量,写出该可逆反应的热化学方程式___________ 。
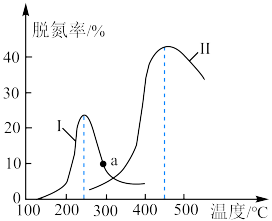
(2)某研究小组探究催化剂对CO、NO转化率的影响。将NO和CO以一定的流速通过两种不同的催化剂进行反应,相同时间内测量逸出气体中NO含量,从而确定尾气脱氮率(脱氮率即NO的转化率),结果如图所示。下列说法正确的是___________(填字母)。
(3)某研究小组对反应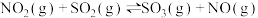
 进行相关实验探究。
进行相关实验探究。
在固定体积的密闭容器中,使用某种催化剂,改变原料气配比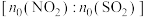 进行多组实验(各组实验的温度可能相同,也可能不同),测定
进行多组实验(各组实验的温度可能相同,也可能不同),测定 的平衡转化率
的平衡转化率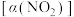 。部分实验结果如图所示。
。部分实验结果如图所示。
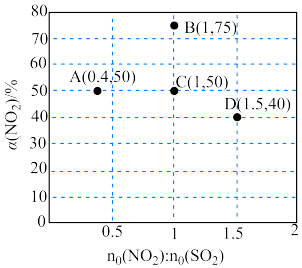
①图中A点对应温度下,该反应的化学平衡常数
___________ 。
②如果将图中C点的平衡状态改变为B点的平衡状态,应采取的措施是___________ 。
③图中C、D两点对应的实验温度分别为 和
和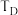 ,通过计算判断
,通过计算判断
___ 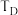 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
 、
、 等是形成酸雨的主要物质,其综合治理是当前重要的研究课题。回答下列问题:
等是形成酸雨的主要物质,其综合治理是当前重要的研究课题。回答下列问题:(1)汽车尾气中
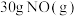 与足量
与足量 在一定温度和催化剂下反应生成
在一定温度和催化剂下反应生成 和
和 ,放出373.25kJ热量,写出该可逆反应的热化学方程式
,放出373.25kJ热量,写出该可逆反应的热化学方程式(2)某研究小组探究催化剂对CO、NO转化率的影响。将NO和CO以一定的流速通过两种不同的催化剂进行反应,相同时间内测量逸出气体中NO含量,从而确定尾气脱氮率(脱氮率即NO的转化率),结果如图所示。下列说法正确的是___________(填字母)。

| A.a点是对应温度下的平衡脱氮率 |
| B.相同条件下,改变压强对脱氮率没有影响 |
| C.曲线Ⅱ中的催化剂适用于450℃左右脱氮 |
D.两种催化剂均能降低活化能,但 不变 不变 |
(3)某研究小组对反应
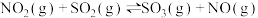
 进行相关实验探究。
进行相关实验探究。在固定体积的密闭容器中,使用某种催化剂,改变原料气配比
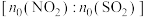 进行多组实验(各组实验的温度可能相同,也可能不同),测定
进行多组实验(各组实验的温度可能相同,也可能不同),测定 的平衡转化率
的平衡转化率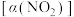 。部分实验结果如图所示。
。部分实验结果如图所示。
①图中A点对应温度下,该反应的化学平衡常数

②如果将图中C点的平衡状态改变为B点的平衡状态,应采取的措施是
③图中C、D两点对应的实验温度分别为
 和
和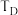 ,通过计算判断
,通过计算判断
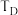 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】乙酸是重要的有机化工原料之一,目前世界上一半以上的乙酸都都采用甲醇与CO反应来制备.某实验小组在一个恒压密闭容器中加入0.20molCH3OH和0.22molCO气体,发生反应CH3OH(g)+CO(g) CH3COOH(I),测得甲醇的转化率随温度的变化关系如图所示,其中曲线Ⅰ表示在5个不同温度下,均经过5min时测得的甲醇的转化率变化曲线,曲线Ⅱ表示不同温度下甲醇的平衡转化率变化曲线,已知在T2温度下,达到平衡时容器的体积刚好为2L.
CH3COOH(I),测得甲醇的转化率随温度的变化关系如图所示,其中曲线Ⅰ表示在5个不同温度下,均经过5min时测得的甲醇的转化率变化曲线,曲线Ⅱ表示不同温度下甲醇的平衡转化率变化曲线,已知在T2温度下,达到平衡时容器的体积刚好为2L.
已知:2CO(g)+O2(g)═2CO2(g) △H=﹣566kJ·mol-1
2CH3OH(g)+3O2(g)═2CO2(g)+4H2O(I) △H=﹣1529kJ·mol-1
CH3COOH(I)+2O2(g)═2CO2(g)+2H2O(I) △H=﹣874kJ·mol-1
按要求回答下列问题:
(1)求工业制乙酸反应:CH3OH(g)+CO(g) CH3COOH(I) △H=
CH3COOH(I) △H= ______ kJ·mol-1
(2)在温度为T2时,从反应开始至5min时,用单位时间内物质的量变化表示的乙酸的平均反应速率为_________ mol·min-1.
(3)在温度为T2时,该反应的平衡常数K=_________ ;在T3温度下,C点时,ν(正) ____ ν(逆)(填“>”、“<”或“=” )。
(4)在温度为T2时,往上述已达到平衡的恒压容器中,再在瞬间通入0.12molCH3OH和0.06molCO混合气体,平衡的移动方向为__________ (填“向左”或“向右”或“不移动” )
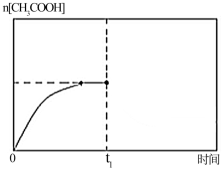
(5)在温度为T1时,乙酸的物质的量随时间变化的趋势曲线如下图所示.当时间到达t1时,将该反应体系温度迅速上升到T3,并维持该温度。请在图中画出t1时刻后乙酸物质的量的变化总趋势曲线.
__________
 CH3COOH(I),测得甲醇的转化率随温度的变化关系如图所示,其中曲线Ⅰ表示在5个不同温度下,均经过5min时测得的甲醇的转化率变化曲线,曲线Ⅱ表示不同温度下甲醇的平衡转化率变化曲线,已知在T2温度下,达到平衡时容器的体积刚好为2L.
CH3COOH(I),测得甲醇的转化率随温度的变化关系如图所示,其中曲线Ⅰ表示在5个不同温度下,均经过5min时测得的甲醇的转化率变化曲线,曲线Ⅱ表示不同温度下甲醇的平衡转化率变化曲线,已知在T2温度下,达到平衡时容器的体积刚好为2L.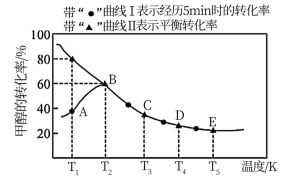
已知:2CO(g)+O2(g)═2CO2(g) △H=﹣566kJ·mol-1
2CH3OH(g)+3O2(g)═2CO2(g)+4H2O(I) △H=﹣1529kJ·mol-1
CH3COOH(I)+2O2(g)═2CO2(g)+2H2O(I) △H=﹣874kJ·mol-1
按要求回答下列问题:
(1)求工业制乙酸反应:CH3OH(g)+CO(g)
 CH3COOH(I) △H=
CH3COOH(I) △H= (2)在温度为T2时,从反应开始至5min时,用单位时间内物质的量变化表示的乙酸的平均反应速率为
(3)在温度为T2时,该反应的平衡常数K=
(4)在温度为T2时,往上述已达到平衡的恒压容器中,再在瞬间通入0.12molCH3OH和0.06molCO混合气体,平衡的移动方向为
(5)在温度为T1时,乙酸的物质的量随时间变化的趋势曲线如下图所示.当时间到达t1时,将该反应体系温度迅速上升到T3,并维持该温度。请在图中画出t1时刻后乙酸物质的量的变化总趋势曲线.
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】CH4—CO2催化重整不仅可以得到合成气(CO和H2),还对温室气体的减排具有重要意义。
(1)在标准状态下,由元素最稳定的单质生成1mol纯化合物时的反应热称为该化合物的标准摩尔生成焓。各物质的标准摩尔生成焓如表:
则制备合成气的反应CH4(g)+CO2(g)⇌2CO(g)+2H2(g)在标准状态下的反应热ΔH=_______ kJ/mol。
(2)在刚性容器中,当投料比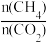 =1.0时,CO2的平衡转化率(α)与温度(T)、初始压强(p)的关系如图所示。
=1.0时,CO2的平衡转化率(α)与温度(T)、初始压强(p)的关系如图所示。

①由图可知:压强P1_______ 2MPa(填“>”、“<”或“=”),理由是_______ 。
②当温度为T3、压强为p1时,a点的v正_______ v逆(填“>”、“<”或“=”)。
③若起始时提高投料比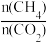 ,则CO2的平衡转化率将
,则CO2的平衡转化率将_______ (填“升高”或“降低”)。
④起始时向容器中加入1molCH4和1molCO2,在温度为T6、初始压强为2MPa时反应,该反应的Kp=_______ (MPa)2。
(3)该催化重整过程中有副产物碳生成,碳的积累会严重影响催化剂的活性。某研究小组计算和模拟实验表明积碳量(催化剂表面碳的质量与催化剂的质量之比)与投料比、温度的关系如图。

当投料比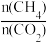 =2.0时,要使积碳量最小,应调节温度为
=2.0时,要使积碳量最小,应调节温度为_______ ℃。
(1)在标准状态下,由元素最稳定的单质生成1mol纯化合物时的反应热称为该化合物的标准摩尔生成焓。各物质的标准摩尔生成焓如表:
| 物质 | CH4 | CO2 | CO | H2 |
| 标准摩尔生成焓/(kJ∙mol-1) | -75 | -394 | -111 | 0 |
则制备合成气的反应CH4(g)+CO2(g)⇌2CO(g)+2H2(g)在标准状态下的反应热ΔH=
(2)在刚性容器中,当投料比
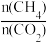 =1.0时,CO2的平衡转化率(α)与温度(T)、初始压强(p)的关系如图所示。
=1.0时,CO2的平衡转化率(α)与温度(T)、初始压强(p)的关系如图所示。
①由图可知:压强P1
②当温度为T3、压强为p1时,a点的v正
③若起始时提高投料比
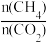 ,则CO2的平衡转化率将
,则CO2的平衡转化率将④起始时向容器中加入1molCH4和1molCO2,在温度为T6、初始压强为2MPa时反应,该反应的Kp=
(3)该催化重整过程中有副产物碳生成,碳的积累会严重影响催化剂的活性。某研究小组计算和模拟实验表明积碳量(催化剂表面碳的质量与催化剂的质量之比)与投料比、温度的关系如图。

当投料比
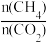 =2.0时,要使积碳量最小,应调节温度为
=2.0时,要使积碳量最小,应调节温度为
您最近一年使用:0次
【推荐3】t℃时,将 和
和 气体通入体积为
气体通入体积为 的密闭容器中(容积不变),发生如下反应:
的密闭容器中(容积不变),发生如下反应: 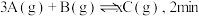 时反应达到平衡状态(温度不变),剩余
时反应达到平衡状态(温度不变),剩余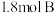 ,并测得C的浓度为
,并测得C的浓度为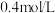 ,请填写下列空白:
,请填写下列空白:
(1)x=_______ 。
(2)比较达到平衡时,A、B两反应物的转化率: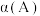
_______ 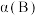 (填>、=或<)
(填>、=或<)
(3)若继续向原平衡混合物的容器中通入少量氨气(氨气和A、B、C都不反应)后,下列说法中正确的是_______(填写字母序号)
(4)若向原平衡混合物的容器中再充入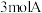 和
和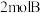 ,在
,在 时达到新的平衡,此时B的物质的量为
时达到新的平衡,此时B的物质的量为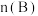
_______ 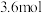 。(填“>”、“<”、或“=”)
。(填“>”、“<”、或“=”)
(5)如果将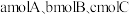 在相同温度和容器中进行反应。欲使反应达到平衡时C的物质的量分数与原平衡相等,起始加入的三种物质的物质的量
在相同温度和容器中进行反应。欲使反应达到平衡时C的物质的量分数与原平衡相等,起始加入的三种物质的物质的量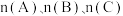 间应该满足的等量关系式:
间应该满足的等量关系式:_______ (a,b及c的关系式)
 和
和 气体通入体积为
气体通入体积为 的密闭容器中(容积不变),发生如下反应:
的密闭容器中(容积不变),发生如下反应: 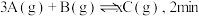 时反应达到平衡状态(温度不变),剩余
时反应达到平衡状态(温度不变),剩余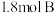 ,并测得C的浓度为
,并测得C的浓度为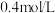 ,请填写下列空白:
,请填写下列空白:(1)x=
(2)比较达到平衡时,A、B两反应物的转化率:
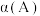
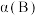 (填>、=或<)
(填>、=或<)(3)若继续向原平衡混合物的容器中通入少量氨气(氨气和A、B、C都不反应)后,下列说法中正确的是_______(填写字母序号)
| A.化学平衡向正反应方向移动 |
| B.化学平衡向逆反应方向移动 |
| C.化学平衡不会发生移动 |
| D.正、逆反应的化学反应速率将发生同等程度的改变 |
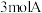 和
和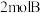 ,在
,在 时达到新的平衡,此时B的物质的量为
时达到新的平衡,此时B的物质的量为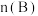
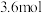 。(填“>”、“<”、或“=”)
。(填“>”、“<”、或“=”)(5)如果将
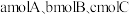 在相同温度和容器中进行反应。欲使反应达到平衡时C的物质的量分数与原平衡相等,起始加入的三种物质的物质的量
在相同温度和容器中进行反应。欲使反应达到平衡时C的物质的量分数与原平衡相等,起始加入的三种物质的物质的量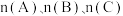 间应该满足的等量关系式:
间应该满足的等量关系式:
您最近一年使用:0次



