下列措施中,一定能使化学平衡移动的是( )
| A.改变温度 | B.改变压强 | C.使用催化剂 | D.改变容器体积 |
15-16高二上·河南安阳·期中 查看更多[8]
更新时间:2016-12-09 10:01:29
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】在密闭容器中发生如下反应:mA(g)+nB(g)⇌pC(g),达到平衡后,保持温度不变,将气体体积缩小到原来的一半,当达到新平衡时,C的浓度为原来1.9倍,下列说法错误的是
| A.m+n>p |
| B.平衡向逆反应方向移动 |
| C.A的转化率降低 |
| D.C的体积分数减小 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】如图是关于可逆反应(正反应为放热反应)的平衡移动图象,影响平衡移动的原因可能是


| A.升高温度 |
| B.降低压强 |
| C.增大反应物浓度,同时使用正催化剂 |
| D.增大反应物浓度,同时减小生成物浓度 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】下列事实不能用平衡移动原理解释的是
A.工业上通常采用压强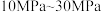 的条件下合成氨 的条件下合成氨 |
| B.生活中可用热的纯碱溶液除去油污 |
| C.唾液可以使淀粉水解的速度加快 |
| D.实验室用排饱和氯化钠溶液的方法收集氯气 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】将CO2和NH3混合通入水中生成碳酸氢铵(NH4HCO3),并放出热量。在一密闭容器中将等物质的量的CO2和NH3混合气体通入水中发生上述反应,并达到平衡。若改变某一条件(其他条件不变),下列相应反应特征和结果都正确的是
选项 | 改变条件 | 反应特征 | 结果 |
A | 升高温度 | 正反应速率减小 | 碳酸氢铵产率减小 |
B | 加入适量的水 | 平衡正向移动 | NH |
C | 增大压强 | 平衡正向移动 | 平衡常数增大 |
D | 通入适量 NH3 | 平衡正向移动 | NH3的转化率增大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】对可逆反应4NH3(g)+5O2(g) 4NO(g) +6H2O (g),下列叙述正确的是( )
4NO(g) +6H2O (g),下列叙述正确的是( )
 4NO(g) +6H2O (g),下列叙述正确的是( )
4NO(g) +6H2O (g),下列叙述正确的是( )| A.反应达到平衡时,若两种反应物的转化率相等,则起始投入的n(NH3):n(O2)=4:5 |
| B.反应达到平衡后,对体系一直进行加压,平衡总是逆向移动 |
| C.反应达到平衡时,若向压强固定的密闭容器中充入稀有气体,平衡不移动 |
| D.当v正(NH3):v正(NO) =1:1时,说明该化学反应已经达到平衡 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列事实中,不能用勒夏特列原理解释的是
| A.氨水应放置低温处密闭保存 | B.由H2、I2(g)、HI组成的平衡体系,加压后颜色加深 |
| C.光照新制氯水,黄绿色逐渐变浅 | D.开启可乐瓶后,瓶中马上泛起大量泡沫 |
您最近一年使用:0次

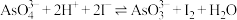 设计如图所示的原电池装置,探究pH对
设计如图所示的原电池装置,探究pH对 氧化性的影响。测得电压与pH的关系如图。下列有关叙述错误的是
氧化性的影响。测得电压与pH的关系如图。下列有关叙述错误的是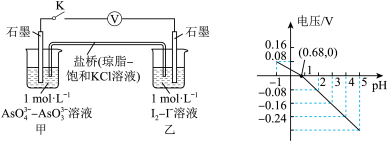
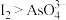
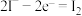
 浓度比原平衡中的小
浓度比原平衡中的小 C(g)+D,达到平衡时,下列说法不正确的是
C(g)+D,达到平衡时,下列说法不正确的是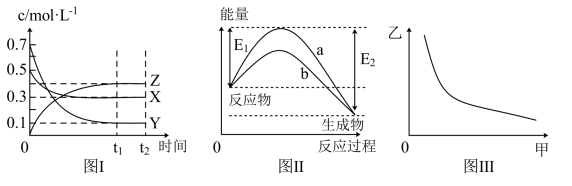
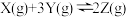
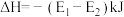
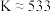 ,且若升高温度,K值减小
,且若升高温度,K值减小

