盐酸、醋酸和碳酸氢钠是生活中常见的物质。下列表述正确的是
A.在NaHCO3溶液中加入与其等物质的量的NaOH,溶液中的阴离子只有CO 和OH- 和OH- |
| B.NaHCO3溶液中:c (H+)+ c (H2CO3)=c(OH-) |
| C.10 mL0.10 mol·L-1CH3COOH溶液加入等物质的量的NaOH后,溶液中离子的浓度由大到小的顺序是:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| D.中和体积与pH都相同的HCl溶液和CH3COOH溶液所消耗的NaOH物质的量相同 |
2008·广东·高考真题 查看更多[4]
2008年普通高等学校招生统一考试化学试题(广东卷)(已下线)2013-2014学年安微省池州市一中高二上学期期中考试化学试题试卷黑龙江省海林市朝鲜族中学2019-2020学年高二上学期期中考试化学试题苏教版选修四化学反应原理专题3第三单元 盐类的水解 同步检测试卷
更新时间:2019-01-30 18:14:09
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】用 0.1000 mol·L−1 NaOH 溶液分别滴定 20.00 mL 0.1000 mol·L−1的盐酸和醋酸,滴定曲线如图所示,下列说法正确的是


| A.Ⅰ、Ⅱ分别表示盐酸和醋酸的滴定曲线 |
| B.V(NaOH) = 10.00 mL 时,醋酸溶液中c(CH3COOH)<c(CH3COO−) |
| C.pH = 7 时,滴定盐酸消耗的 NaOH 溶液体积小于滴定醋酸消耗的 NaOH 溶液体积 |
| D.V(NaOH) = 20.00 mL 时,两溶液中 c(CH3COO−)=c(Cl−) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列事实能说明某一元酸以是弱电解质的是
①HA溶液能导电 ②HA与水能以任意比互溶
③HA的稀溶液中存在HA分子 ④HA能和碳酸钙反应放出CO2
⑤常温下,0.1mol/L HA的pH比0.1mol/L盐酸的pH大
⑥大小相同的铁片与同物质的量浓度的盐酸和HA反应,HA产生H2的速率慢
①HA溶液能导电 ②HA与水能以任意比互溶
③HA的稀溶液中存在HA分子 ④HA能和碳酸钙反应放出CO2
⑤常温下,0.1mol/L HA的pH比0.1mol/L盐酸的pH大
⑥大小相同的铁片与同物质的量浓度的盐酸和HA反应,HA产生H2的速率慢
| A.②④⑥ | B.③⑤⑥ | C.③④⑥ | D.①②⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】改变0.1mol•L—1二元弱酸H2A溶液的pH,溶液中的H2A、HA—、A2—的物质的量分数δ(x)随pH的变化如图所示[已知δ(x)=c(x)/(c(H2A)+c(HA—)+c(A2—)])。下列叙述正确的是
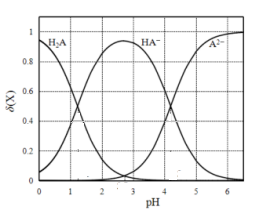

| A.Ka2(H2A)的数量级为10-4 |
| B.NaHA溶液中,HA-的水解能力小于HA-的电离能力 |
| C.在含H2A、HA-和A2-的溶液中,加入少量NaOH固体,δ(HA-)一定增大 |
| D.将等物质的量的NaHA和Na2A混合物溶于水,所得的溶液中δ(HA-)=δ(A2-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】常温下,将少量MSO4粉末缓慢加入20 mL0. 1mol·L-1H2A溶液中(已知MA难溶,忽略溶液体积变化),溶液中c(H+ )与c(M2+ )变化如图所示,已知:Ka1(H2A)=1.0×10-9,Ka2(H2A)=1.0×10-13,下列有关说法不正确的是
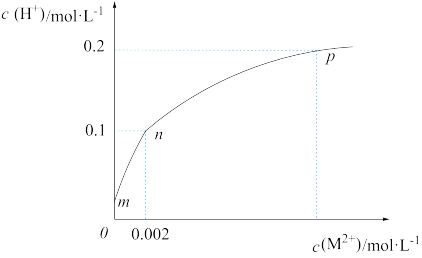

| A.m点溶液的pH约为5.0 |
| B.p点溶液中c(H2A)+c(HA-)+c(A2-)=0.lmol·L-1 |
| C.m、n、p三点中由水电离的c(H+)最大的是m点 |
| D.Ksp(MA)数量级为10-24 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】常温下,向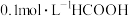 溶液中通入氨气,各微粒的pM(p表示-lg,M表示
溶液中通入氨气,各微粒的pM(p表示-lg,M表示 、
、 、HCOOH、
、HCOOH、 的浓度)与pH的关系如图所示。下列说法正确的是
的浓度)与pH的关系如图所示。下列说法正确的是
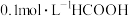 溶液中通入氨气,各微粒的pM(p表示-lg,M表示
溶液中通入氨气,各微粒的pM(p表示-lg,M表示 、
、 、HCOOH、
、HCOOH、 的浓度)与pH的关系如图所示。下列说法正确的是
的浓度)与pH的关系如图所示。下列说法正确的是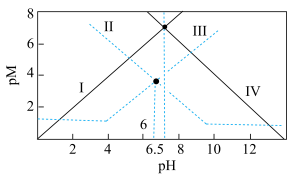
A.Ⅱ、Ⅲ分别为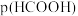 、 、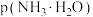 与pH的关系 与pH的关系 |
B.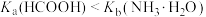 |
C. 时, 时,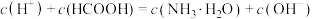 |
D. 时, 时,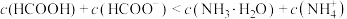 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】室温下,测定农产品中的氮的含量步骤:①用浓硫酸处理样品,得到铵盐;②加入浓NaOH溶液,加热,用水吸收逸出的氨气;③用标准硫酸溶液测定氨的含量,下列说法正确的是
| A.滴定实验选酚酞作指示剂 |
| B.硫酸与氨水恰好中和时溶液pH=7 |
C.氨水与(NH4)2SO4混合溶液中可能存在:c(SO )>c(H+)>c(NH )>c(H+)>c(NH )>c(OH-) )>c(OH-) |
D.(NH4)2SO4溶液中:c(NH )<2c(SO )<2c(SO )+c(OH-) )+c(OH-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】氯气可以用于制取漂白剂和自来水杀菌消毒。常温下,溶液中Cl2(aq)、HClO和ClO-物质的量分数(α)随pH变化的关系如图所示。
已知,Cl2(g) Cl2(aq)K1=10-1.2
Cl2(aq)K1=10-1.2
Cl2(aq)+H2O HClO+H++Cl-K2=10-3.4
HClO+H++Cl-K2=10-3.4
下列说法正确的是
已知,Cl2(g)
 Cl2(aq)K1=10-1.2
Cl2(aq)K1=10-1.2Cl2(aq)+H2O
 HClO+H++Cl-K2=10-3.4
HClO+H++Cl-K2=10-3.4下列说法正确的是

A.Cl2(g)+H2O 2H++ClO-+Cl-K3=10-10.9 2H++ClO-+Cl-K3=10-10.9 |
| B.氯气通入水中,c(HClO)+c(ClO-)<c(H+)-c(OH-) |
| C.pH=7.0时漂白能力要比pH=6.0时要强 |
| D.氯气处理自来水时,在夏天的杀菌消毒效果要比在冬天好 |
您最近一年使用:0次

 、体积均为
、体积均为 的
的 和
和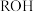 溶液,分别加水稀释至体积
溶液,分别加水稀释至体积 ,
, 随
随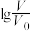 的变化如图所示。下列叙述错误的是
的变化如图所示。下列叙述错误的是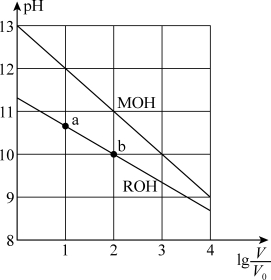
 相等
相等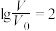 时,若两溶液同时升高温度,则
时,若两溶液同时升高温度,则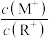 增大
增大

