消除氮氧化物、二氧化硫等物质造成的污染是目前研究的重要课题。
(1)燃煤烟气脱硫常用如下方法。
①用生物质热解气(主要成分CO、CH4、H2)将SO2在高温下还原成单质硫。涉及的部分反应如下:2CO(g)+SO2(g)=S(g)+2CO2(g) △H1= + 8.0 kJ·mol-1
2CO(g)+O2(g)=2CO2(g) △H2=-566.0kJ·mol-1
2H2(g)+O2(g)=2H2O(g) △H3=-483.6 kJ·mol-1
则H2(g)还原SO2(g)生成S(g)和H2O(g)的热化学方程式为______________________ 。
②一氧化碳还原法:在绝热恒容的密闭容器中,反应2CO(g)+SO2(g) S(s)+2CO2(g)达到平衡时,下列说法正确的是
S(s)+2CO2(g)达到平衡时,下列说法正确的是____ (填序号)。
a.容器内气体的压强保持不变 b.分离出S,正反应速率减小
若再充入一定量的CO2,反应的平衡常数不变
③用氨水将SO2转化为NH4HSO3,再氧化成(NH4)2SO4。实验测得NH4HSO3溶液中 =15,则溶液的pH为
=15,则溶液的pH为________ 。 (已知:H2SO3的Ka1=1.5×10-2,Ka2=1.0×10-7)
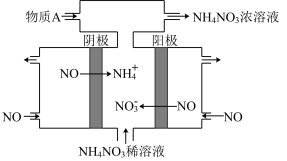
(2)电解NO可以制备NH4NO3,其工作原理如下图所示,阳极的电极反应式为:____________ ,为使电解产物全部转化为NH4NO3,需补充物质A,A是___________ 。
(3)Na2S是常用的沉淀剂。某工业污水中含有等浓度的Cu2+、Fe2+、Pb2+,滴加Na2S溶液后首先析出的沉淀是________ 。当最后一种离子沉淀完全时(该离子浓度为10-5 mol·L-1),此时S2-的浓度为_________________________
(已知: Ksp(FeS)=6.3×10-18 ;Ksp(CuS)=6×10-36 ;Ksp(PbS)=2.4×10-28)
(1)燃煤烟气脱硫常用如下方法。
①用生物质热解气(主要成分CO、CH4、H2)将SO2在高温下还原成单质硫。涉及的部分反应如下:2CO(g)+SO2(g)=S(g)+2CO2(g) △H1= + 8.0 kJ·mol-1
2CO(g)+O2(g)=2CO2(g) △H2=-566.0kJ·mol-1
2H2(g)+O2(g)=2H2O(g) △H3=-483.6 kJ·mol-1
则H2(g)还原SO2(g)生成S(g)和H2O(g)的热化学方程式为
②一氧化碳还原法:在绝热恒容的密闭容器中,反应2CO(g)+SO2(g)
 S(s)+2CO2(g)达到平衡时,下列说法正确的是
S(s)+2CO2(g)达到平衡时,下列说法正确的是a.容器内气体的压强保持不变 b.分离出S,正反应速率减小
若再充入一定量的CO2,反应的平衡常数不变
③用氨水将SO2转化为NH4HSO3,再氧化成(NH4)2SO4。实验测得NH4HSO3溶液中
 =15,则溶液的pH为
=15,则溶液的pH为(2)电解NO可以制备NH4NO3,其工作原理如下图所示,阳极的电极反应式为:

(3)Na2S是常用的沉淀剂。某工业污水中含有等浓度的Cu2+、Fe2+、Pb2+,滴加Na2S溶液后首先析出的沉淀是
(已知: Ksp(FeS)=6.3×10-18 ;Ksp(CuS)=6×10-36 ;Ksp(PbS)=2.4×10-28)
更新时间:2017-07-12 20:15:52
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】利用CO2可合成烷烃、烯怪、醇、甲酸等系列重要化工原料。回答下列有关问题:
I.制备甲烷:
已知:CH4、H2的燃烧热分别为 、
、 ,1molH2O(l)变成水蒸气需吸收44kJ的热量。
,1molH2O(l)变成水蒸气需吸收44kJ的热量。
(1)
___________  。
。
(2)在恒温、恒容容器中进行该反应,下列叙述一定能说明该反应达到平衡状态的是___________。
II.制备甲醇:
主反应:
副反应:
(3)向某一恒容容器中充入1molCO2和3molH2,在催化剂存在的条件下进行反应,测得温度与平衡转化率、产物选择性的关系如下图所示。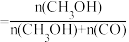
①240℃该反应达到平衡时,产生的CH3OH的物质的量为___________ mol(填标号)。
②有利于提高CH3OH选择性的反应条件是___________ (填标号)。
A.高温高压 B.高温低压 C.低温高压 D.低温低压
III.电解法转化CO2可实现CO2资源化利用,电解CO2制HCOOH的原理示意图如图。___________ (填“a”或“b”)管是不需要的。
(5)写出阴极的电极反应式:___________ 。
(6)电解一段时间后,若两侧电极液中K+的物质的量相差0.02mol,则阳极产生的气体在标准状况下的总体积为___________ mL(假设产生的气体全部逸出)。
I.制备甲烷:

已知:CH4、H2的燃烧热分别为
 、
、 ,1molH2O(l)变成水蒸气需吸收44kJ的热量。
,1molH2O(l)变成水蒸气需吸收44kJ的热量。(1)

 。
。(2)在恒温、恒容容器中进行该反应,下列叙述一定能说明该反应达到平衡状态的是___________。
A. | B.容器内的压强不再变化 |
| C.混合气体的平均摩尔质量不再变化 | D.CO2和H2的转化率之比不再变化 |
II.制备甲醇:
主反应:

副反应:

(3)向某一恒容容器中充入1molCO2和3molH2,在催化剂存在的条件下进行反应,测得温度与平衡转化率、产物选择性的关系如下图所示。
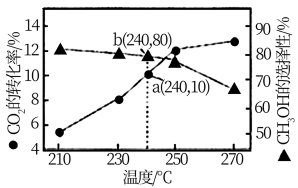
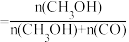
①240℃该反应达到平衡时,产生的CH3OH的物质的量为
②有利于提高CH3OH选择性的反应条件是
A.高温高压 B.高温低压 C.低温高压 D.低温低压
III.电解法转化CO2可实现CO2资源化利用,电解CO2制HCOOH的原理示意图如图。

(5)写出阴极的电极反应式:
(6)电解一段时间后,若两侧电极液中K+的物质的量相差0.02mol,则阳极产生的气体在标准状况下的总体积为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】甲醇是一种新型燃料,工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:CO(g)+2H2(g) CH3OH(g) △H1=-116kJ/mol
CH3OH(g) △H1=-116kJ/mol
(1)已知:CO(g)+ O2(g)=CO2 (g) △H2=-283kJ/mol
O2(g)=CO2 (g) △H2=-283kJ/mol
H2(g) + O2(g)=H2O (g) △H1=-242kJ/mol
O2(g)=H2O (g) △H1=-242kJ/mol
则表示1mol气态甲醇完全燃烧生成CO2和水蒸气时的热化学方程式:________________
(2)在容积为1L的恒容容器中,分别研究在230℃、250℃、270℃三种温度下合成甲醇的规律。如图是上述三种温度下不同的H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系。
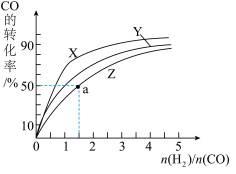
请回答:
①在上述三种温度中,曲线Z对应的温度是_________
②利用图中a点对应的数据,计算出曲线Z在对应温度下CO(g)+2H2(g)=CH3OH(g)的平衡常数 K=_________ 。
③下列既能提高上述反应中 CO 的平衡转化率,又能增大反应速率的是____ (填标号)。
a.增大压强 b.降低温度 c.增大H2浓度 d.加高效催化剂
④若上述反应在某恒温恒容容器中发生,能说明该反应达到平衡的是____ (填标号)。
a.气体平均相对分子质量保持不变 b.△H1保持不变
c.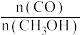 保持不变 d.气体密度保持不变
保持不变 d.气体密度保持不变
(3)在某温度下,将一定量的CO和H2投入10L的密闭容器中,5min时达到平衡,各物质的物质的浓度(mol/L)变化如下表所示:
若5min~10min只改变了某一条件,所改变的条件是______________ 。
 CH3OH(g) △H1=-116kJ/mol
CH3OH(g) △H1=-116kJ/mol(1)已知:CO(g)+
 O2(g)=CO2 (g) △H2=-283kJ/mol
O2(g)=CO2 (g) △H2=-283kJ/mol H2(g) +
 O2(g)=H2O (g) △H1=-242kJ/mol
O2(g)=H2O (g) △H1=-242kJ/mol则表示1mol气态甲醇完全燃烧生成CO2和水蒸气时的热化学方程式:
(2)在容积为1L的恒容容器中,分别研究在230℃、250℃、270℃三种温度下合成甲醇的规律。如图是上述三种温度下不同的H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系。

请回答:
①在上述三种温度中,曲线Z对应的温度是
②利用图中a点对应的数据,计算出曲线Z在对应温度下CO(g)+2H2(g)=CH3OH(g)的平衡常数 K=
③下列既能提高上述反应中 CO 的平衡转化率,又能增大反应速率的是
a.增大压强 b.降低温度 c.增大H2浓度 d.加高效催化剂
④若上述反应在某恒温恒容容器中发生,能说明该反应达到平衡的是
a.气体平均相对分子质量保持不变 b.△H1保持不变
c.
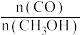 保持不变 d.气体密度保持不变
保持不变 d.气体密度保持不变(3)在某温度下,将一定量的CO和H2投入10L的密闭容器中,5min时达到平衡,各物质的物质的浓度(mol/L)变化如下表所示:
| 0min | 5min | 10min | |
| CO | 0.1 | 0.05 | |
| H2 | 0.2 | 0.2 | |
| CH3OH | 0 | 0.04 | 0.05 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】利用N2和H2可以实现NH3的工业合成,而氨又可以进一步制备硝酸,在工业上一般可进行连续生产。请回答下列问题:
(1)已知:N2(g) + O2(g) === 2NO(g) △H= +180.5kJ/mol
N2(g) + 3H2(g) 2NH3(g) △H=-92.4kJ/mol
2NH3(g) △H=-92.4kJ/mol
2H2(g) + O2(g) ===2H2O(g) △H=-483.6kJ/mol
若有17 g氨气经催化氧化完全生成一氧化氮气体和水蒸气所放出的热量为______ 。
(2)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对N2(g)+3H2(g)⇌2NH3(g)反应的影响。
实验结果如图所示:(图中T表示温度,n表示物质的量)

①图象中T2和T1的关系是:T2______ T1(填“高于”、“低于”、“等于”或“无法确定”)。
②比较在a、b、c三点所处的平衡状态中,反应物N2 的转化率最高的是______ (填字母)。
③在起始体系中加入N2的物质的量为________ mol时,反应后氨的百分含量最大;若容器容积为1L,n=3mol反应达到平衡时H2的转化率为60%,则此条件下(T2),反应的平衡常数K=________________________ 。
(3)N2O5是一种新型硝化剂,其性质和制备受到人们的关注。
①一定温度下,在恒容密闭容器中N2O5可发生下列反应:
2N2O5(g)⇌4NO2(g)+O2(g) ΔH>0下表为反应在T1温度下的部分实验数据
则500s内NO2的平均生成速率为____________________________________ 。
②现以H2、O2、熔融盐Na2CO3组成的燃料电池,采用电解法制备N2O5,
装置如图所示,其中Y为CO2。
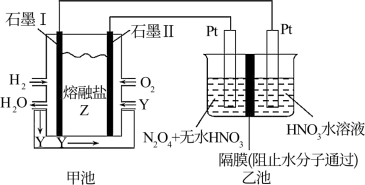
写出石墨I电极上发生反应的电极反应式______________________________ 。
在电解池中生成N2O5的电极反应式为_________________________________ 。
(1)已知:N2(g) + O2(g) === 2NO(g) △H= +180.5kJ/mol
N2(g) + 3H2(g)
 2NH3(g) △H=-92.4kJ/mol
2NH3(g) △H=-92.4kJ/mol2H2(g) + O2(g) ===2H2O(g) △H=-483.6kJ/mol
若有17 g氨气经催化氧化完全生成一氧化氮气体和水蒸气所放出的热量为
(2)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对N2(g)+3H2(g)⇌2NH3(g)反应的影响。
实验结果如图所示:(图中T表示温度,n表示物质的量)

①图象中T2和T1的关系是:T2
②比较在a、b、c三点所处的平衡状态中,反应物N2 的转化率最高的是
③在起始体系中加入N2的物质的量为
(3)N2O5是一种新型硝化剂,其性质和制备受到人们的关注。
①一定温度下,在恒容密闭容器中N2O5可发生下列反应:
2N2O5(g)⇌4NO2(g)+O2(g) ΔH>0下表为反应在T1温度下的部分实验数据
| t/s | 0 | 500 | 1000 |
c(N2O5)/mol L-1 L-1 | 5.00 | 3.52 | 2.48 |
②现以H2、O2、熔融盐Na2CO3组成的燃料电池,采用电解法制备N2O5,
装置如图所示,其中Y为CO2。

写出石墨I电极上发生反应的电极反应式
在电解池中生成N2O5的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】碳及其化合物广泛存在于自然界。请回答下列问题:
(1)反应Ⅰ:Fe(s)+CO2(g) FeO(s)+CO(g) ΔH1平衡常数为K1
FeO(s)+CO(g) ΔH1平衡常数为K1
反应Ⅱ:Fe(s)+H2O(g) FeO(s)+H2(g) ΔH1平衡常数为K2
FeO(s)+H2(g) ΔH1平衡常数为K2
不同温度下,K1、K2的值如下表:
现有反应Ⅲ:H2(g)+CO2(g) CO(g)+H2O(g),结合上表数据,反应Ⅲ是
CO(g)+H2O(g),结合上表数据,反应Ⅲ是___ (填“放热”或“吸热”)反应,为提高CO2的转化率可采用措施有___ (写出任意两条)。
(2)已知CO2催化加氢合成乙醇的反应原理为:2CO2(g)+6H2(g) C2H5OH(g)+3H2O(g) ∆H<0。设m为起始时的投料比,即m= n(H2)/ n(CO2)。
C2H5OH(g)+3H2O(g) ∆H<0。设m为起始时的投料比,即m= n(H2)/ n(CO2)。

①图1中投料比相同,温度从高到低的顺序为______ 。
②图2中m1、m2、m3从大到小的顺序为____ 。
③图3表示在总压为5MPa的恒压条件下,且m=3时,平衡状态时各物质的物质的量分数与温度的关系。则曲线d代表的物质化学名称为____ ,T4温度时,该反应平衡常数KP的计算式为____ 。
(3)工业上常用高浓度的 K2CO3溶液吸收CO2,得溶液X,再利用电解法使K2CO3溶液再生,其装置示意图如图:
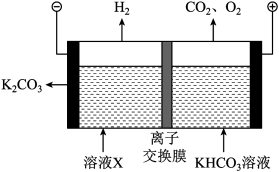
①在阳极区发生的反应包括____ 和H++HCO3- ==CO2↑+H2O
②简述CO32-在阴极区再生的原理:____ 。
(1)反应Ⅰ:Fe(s)+CO2(g)
 FeO(s)+CO(g) ΔH1平衡常数为K1
FeO(s)+CO(g) ΔH1平衡常数为K1反应Ⅱ:Fe(s)+H2O(g)
 FeO(s)+H2(g) ΔH1平衡常数为K2
FeO(s)+H2(g) ΔH1平衡常数为K2不同温度下,K1、K2的值如下表:
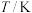 | 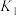 | 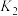 |
| 973 | 1.47 | 2.38 |
| 1173 | 2.15 | 1.67 |
现有反应Ⅲ:H2(g)+CO2(g)
 CO(g)+H2O(g),结合上表数据,反应Ⅲ是
CO(g)+H2O(g),结合上表数据,反应Ⅲ是(2)已知CO2催化加氢合成乙醇的反应原理为:2CO2(g)+6H2(g)
 C2H5OH(g)+3H2O(g) ∆H<0。设m为起始时的投料比,即m= n(H2)/ n(CO2)。
C2H5OH(g)+3H2O(g) ∆H<0。设m为起始时的投料比,即m= n(H2)/ n(CO2)。
①图1中投料比相同,温度从高到低的顺序为
②图2中m1、m2、m3从大到小的顺序为
③图3表示在总压为5MPa的恒压条件下,且m=3时,平衡状态时各物质的物质的量分数与温度的关系。则曲线d代表的物质化学名称为
(3)工业上常用高浓度的 K2CO3溶液吸收CO2,得溶液X,再利用电解法使K2CO3溶液再生,其装置示意图如图:

①在阳极区发生的反应包括
②简述CO32-在阴极区再生的原理:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】以CO2和H2为原料制造更高价值的化学产品是用来缓解温室效应的研究方向。
(1)工业上常用CO2和H2为原料合成甲醇(CH3OH),过程中发生如下两个反应:
反应I:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH=-51 kJ·mol-1
反应II:CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH=+41 kJ·mol-1
①已知几种化学键的键能如下表所示,则a=_______ kJ·mol-1。
②若反应II逆反应活化能Ea′=124 kJ·mol-1,则该反应的正反应的活化能Ea=_______ kJ·mol-1。
(2)向2L容器中充入1 mol CO2和2 mol H2,若只发生反应I,测得反应在不同压强平衡混合物中甲醇体积分数φ(CH3OH)随温度变化如图1所示,逆反应速率与容器中c(CH3OH)关系如图2所示:
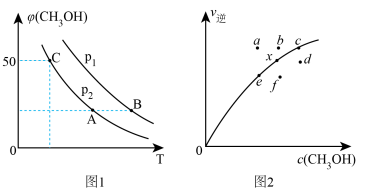
①图1中P1_______ P2(填“>”、“<”或“=”);
②图2中x点平衡体系时升温,反应重新达平衡状态时新平衡点可能是_______ (填字母序号)。
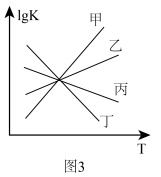
(3)若反应II的正、逆反应速率分别可表示为v正=k正c(CO2)·c(H2)、v逆=k逆c(CO)·c(H2O),k正、k逆分别表示正、逆反应速率常数,只与温度有关。则图3中所示的甲、乙、丙、丁四条直线中,表示lgk正随温度T变化关系的直线是_______ ,表示lgk逆随温度T变化关系的直线是_______ 。
(1)工业上常用CO2和H2为原料合成甲醇(CH3OH),过程中发生如下两个反应:
反应I:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH=-51 kJ·mol-1
反应II:CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH=+41 kJ·mol-1
①已知几种化学键的键能如下表所示,则a=
| 化学键 | C-H | C-O | H-O | H-H | C≡O |
| 键能/kJ·mol-1 | 406 | 351 | 465 | 436 | a |
(2)向2L容器中充入1 mol CO2和2 mol H2,若只发生反应I,测得反应在不同压强平衡混合物中甲醇体积分数φ(CH3OH)随温度变化如图1所示,逆反应速率与容器中c(CH3OH)关系如图2所示:

①图1中P1
②图2中x点平衡体系时升温,反应重新达平衡状态时新平衡点可能是
(3)若反应II的正、逆反应速率分别可表示为v正=k正c(CO2)·c(H2)、v逆=k逆c(CO)·c(H2O),k正、k逆分别表示正、逆反应速率常数,只与温度有关。则图3中所示的甲、乙、丙、丁四条直线中,表示lgk正随温度T变化关系的直线是

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】甲醇既是重要的化工原料,又可作为燃料。利用CO2、CO与H2在一定条件下可反应生成甲醇。研究表明,在某催化剂作用下,发生的主要反应如下:
反应I:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) △H1=-59kJ·mol-1
反应II:CO2(g)+H2(g)⇌CO(g)+H2O(g) △H2
反应III:CO(g)+2H2(g)⇌CH3OH(g) △H3
其中,有关物质化学键的键能如表所示:
请回答下列问题:
(1)仅考虑反应I,有利于提高该反应平衡转化率的条件是___________。
(2)反应II的△H2=___________ 。
(3)当CO2、CO与H2以n(H2)/n(CO+CO2)=2.60的组成比通入时,体系中CO平衡转化率(a)与压强的关系如图1所示。请指出图1中压强由大到小顺序是___________ ,判断理由是___________ 。
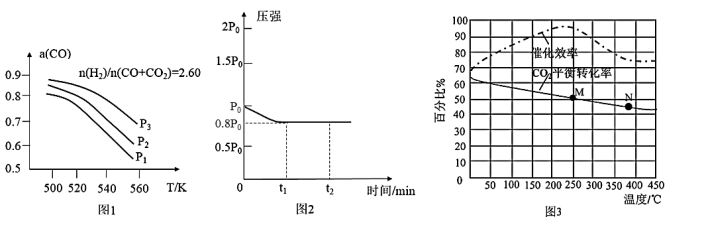
(4)某温度下,向1L固定容积的密闭容器中加入2.5molCO2(g)和2.5molH2(g),仅发生反应I,达到平衡,测得容器内气体的压强随着时间的变化如图2所示。
①请计算该温度下,反应I的平衡常数K=___________ (用具体数值表示);
②若保持其他条件不变,继续向容器中投入2.5molCO2(g)和2.5molH2(g),再次达到平衡,此时,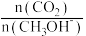 的值与原平衡相比,将
的值与原平衡相比,将___________ (填“增大”、“减小”或“不变”)。
③若采用0.5L固定容积的密闭容器,投料量(仍为2.5molCO2和2.5molH2)、催化剂和反应温度均保持不变,请在图2中画出0~t2时刻,体系内的压强随时间变化的曲线___________ 。
(5)在一定压强下,按n(CO2):n(H2)=1:3(总物质的量为4amol)的投料比充入密闭容器中仅发生反应I。测定温度对的CO2的平衡转化率和催化剂催化效率影响情况如图3所示。下列说法不正确的是___________ 。
A.生成CH3OH的速率:ʋ(M)可能大于ʋ(N)
B.平衡常数:KM>KN
C.其他条件相同时,适当增大催化剂的表面积,可提高CO2的平衡转化率
D.若投料比不变,温度越低,反应一定时间后CO2的转化率一定较高
E.若其他条件不变,投料比改为n(CO2)∶n(H2)=1∶4,可以提高CO2的平衡转化率
反应I:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) △H1=-59kJ·mol-1
反应II:CO2(g)+H2(g)⇌CO(g)+H2O(g) △H2
反应III:CO(g)+2H2(g)⇌CH3OH(g) △H3
其中,有关物质化学键的键能如表所示:
| 化学键 | C=O | H-H | C-O | C≡O | H-O | C-H |
| 键能/(kJ∙mol-1) | 805 | 436 | 343 | 1076 | 465 | 413 |
请回答下列问题:
(1)仅考虑反应I,有利于提高该反应平衡转化率的条件是___________。
| A.高温高压 | B.低温低压 | C.高温低压 | D.低温高压 |
(3)当CO2、CO与H2以n(H2)/n(CO+CO2)=2.60的组成比通入时,体系中CO平衡转化率(a)与压强的关系如图1所示。请指出图1中压强由大到小顺序是

(4)某温度下,向1L固定容积的密闭容器中加入2.5molCO2(g)和2.5molH2(g),仅发生反应I,达到平衡,测得容器内气体的压强随着时间的变化如图2所示。
①请计算该温度下,反应I的平衡常数K=
②若保持其他条件不变,继续向容器中投入2.5molCO2(g)和2.5molH2(g),再次达到平衡,此时,
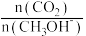 的值与原平衡相比,将
的值与原平衡相比,将③若采用0.5L固定容积的密闭容器,投料量(仍为2.5molCO2和2.5molH2)、催化剂和反应温度均保持不变,请在图2中画出0~t2时刻,体系内的压强随时间变化的曲线
(5)在一定压强下,按n(CO2):n(H2)=1:3(总物质的量为4amol)的投料比充入密闭容器中仅发生反应I。测定温度对的CO2的平衡转化率和催化剂催化效率影响情况如图3所示。下列说法不正确的是
A.生成CH3OH的速率:ʋ(M)可能大于ʋ(N)
B.平衡常数:KM>KN
C.其他条件相同时,适当增大催化剂的表面积,可提高CO2的平衡转化率
D.若投料比不变,温度越低,反应一定时间后CO2的转化率一定较高
E.若其他条件不变,投料比改为n(CO2)∶n(H2)=1∶4,可以提高CO2的平衡转化率
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】综合利用炼锌矿渣(主要含铁酸镓Ga2(Fe2O4)3、铁酸锌ZnFe2O4)获得3种金属盐,并进一步利用镓盐制备具有优异光电性能的氮化镓(GaN),部分工艺流程如图。
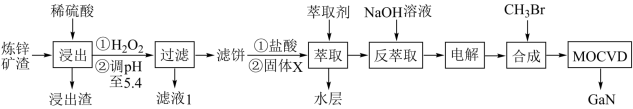
已知:①常温下,浸出液中各离子的浓度及其开始形成氢氧化物沉淀的pH如表1。
②金属离子在工艺条件下的萃取率(进入有机层中金属离子的百分数)如表2。
表1金属离子浓度及开始沉淀的pH
表2金属离子的萃取率
(1)Ga2(Fe2O4)3中Ga的化合价为_____ ,“浸出”后的①中加入H2O2时发生的离子方程式为_____ 。
(2)滤液1中可回收利用的物质是_____ ,滤饼的主要成分是_____ ;萃取前加入的固体X为_____ 。
(3)Ga与Al同主族,化学性质相似。反萃取后,镓的存在形式为_____ 。(填化学式)
(4)电解过程包括电解反萃取液制粗镓和粗镓精炼两个步骤。精炼时,以粗镓为阳极,以NaOH溶液为电解液,阴极的电极反应为_____ 。
(5)GaN可采用MOCVD(金属有机物化学气相淀积)技术制得:以合成的三甲基镓为原料,使其与NH3发生系列反应得到GaN和另一种产物,该过程的化学方程式为______ 。
(6)滤液1中残余的Ga3+的浓度为_____ mol•L-1。

已知:①常温下,浸出液中各离子的浓度及其开始形成氢氧化物沉淀的pH如表1。
②金属离子在工艺条件下的萃取率(进入有机层中金属离子的百分数)如表2。
表1金属离子浓度及开始沉淀的pH
| 金属离子 | 浓度(mol•L-1) | 开始沉淀pH |
| Fe2+ | 1.0×10-3 | 8.0 |
| Fe3+ | 4.0×10-2 | 1.7 |
| Zn2+ | 1.5 | 5.5 |
| Ga3+ | 3.0×10-3 | 3.0 |
| 金属离子 | 萃取率(%) |
| Fe2+ | 0 |
| Fe3+ | 99 |
| Zn2+ | 0 |
| Ga3+ | 97~98.5 |
(2)滤液1中可回收利用的物质是
(3)Ga与Al同主族,化学性质相似。反萃取后,镓的存在形式为
(4)电解过程包括电解反萃取液制粗镓和粗镓精炼两个步骤。精炼时,以粗镓为阳极,以NaOH溶液为电解液,阴极的电极反应为
(5)GaN可采用MOCVD(金属有机物化学气相淀积)技术制得:以合成的三甲基镓为原料,使其与NH3发生系列反应得到GaN和另一种产物,该过程的化学方程式为
(6)滤液1中残余的Ga3+的浓度为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】硒(Se)是动物和人体所必需的微量元素之一,也是一种重要的工业原料。Na2SeO3可用于治疗克山病,H2Se是制备新型光伏太阳能电池、半导体材料和金属硒化物的重要原料。回答下列问题:
(1)硒在元素周期表的位置是:_______ 。
(2)工业上获得硒的方法很多。
方法一:从含硒废料中提取硒:用硫酸和硝酸钠的混合溶液处理含硒废料后获得亚硒酸和少量硒酸;硒酸再与盐酸共热转化为亚硒酸;最后通入SO2析出硒单质。请写出硒酸与盐酸反应的化学方程式为_______ 。
(3)方法二:某科研小组以硫铁矿生产硫酸过程中产生的含硒物料(主要含S、Se、Fe2O3、CuO、ZnO、SiO2等)提取硒,设计流程如图:

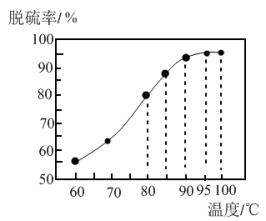
①“脱硫”时,测得脱硫率随温度的变化如图。随着温度的升高,脱硫率呈上升趋势,其原因是_______ 。 “脱硫”时最佳温度是_______ 。
②采用硫脲[ (NH2)2CS]联合亚硫酸钠进行“控电位还原”,将电位高的物质先还原,电位低的物质保留在溶液中,以达到硒与杂质金属的分离。表为“氧化酸浸’液中主要粒子的电位。
a.控制电位在0.740~1.511V范围内,在氧化酸浸液中添加硫脲,可选择性还原ClO2,该过程的还原反应(半反应)式为_______ 。
b.为使硒和杂质金属分离,用亚硫酸钠还原时的最低电位应不低于_______ V。
c.粗硒的精制过程:Na2SO3浸出[Se转化成硒代硫酸钠(Na2SeSO3)]→Na2S净化→H2SO4酸化等步骤。
净化后的溶液中c( Na2S)达到0. 026 mol•L-1,此时溶液中的c(Cu2+ )的最大值为_______ mol. L-1,精硒中基本不含铜。[Ksp(CuS) =1.3×10-36]
(4)某小组同学在实验室利用Na2SeO3溶液与SOCl2也成功制备出Se,请写出相应的离子方程式_______ 。
(1)硒在元素周期表的位置是:
(2)工业上获得硒的方法很多。
方法一:从含硒废料中提取硒:用硫酸和硝酸钠的混合溶液处理含硒废料后获得亚硒酸和少量硒酸;硒酸再与盐酸共热转化为亚硒酸;最后通入SO2析出硒单质。请写出硒酸与盐酸反应的化学方程式为
(3)方法二:某科研小组以硫铁矿生产硫酸过程中产生的含硒物料(主要含S、Se、Fe2O3、CuO、ZnO、SiO2等)提取硒,设计流程如图:

①“脱硫”时,测得脱硫率随温度的变化如图。随着温度的升高,脱硫率呈上升趋势,其原因是

②采用硫脲[ (NH2)2CS]联合亚硫酸钠进行“控电位还原”,将电位高的物质先还原,电位低的物质保留在溶液中,以达到硒与杂质金属的分离。表为“氧化酸浸’液中主要粒子的电位。
| 名称 | Cu2+/Cu | Zn2+/Zn | Fe2+/Fe | Fe3+/Fe | ClO2/Cl- | H2SeO3/Se |
| 电位/V | 0.345 | -0.760 | -0.440 | 0.770 | 1.511 | 0.740 |
b.为使硒和杂质金属分离,用亚硫酸钠还原时的最低电位应不低于
c.粗硒的精制过程:Na2SO3浸出[Se转化成硒代硫酸钠(Na2SeSO3)]→Na2S净化→H2SO4酸化等步骤。
净化后的溶液中c( Na2S)达到0. 026 mol•L-1,此时溶液中的c(Cu2+ )的最大值为
(4)某小组同学在实验室利用Na2SeO3溶液与SOCl2也成功制备出Se,请写出相应的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】金属钼在工业和国防建设中有重要的作用。钼(Mo)的常见化合价为+6、+5、+4。由钼精矿(主要成分是MoS2)可制备单质钼和钼酸钠晶体(Na2MoO4·2H2O),部分流程如图1所示:

已知:钼酸微溶于水,可溶于液碱和氨水。
回答下列问题:
(1)焙烧钼精矿时发生的化学方程式为_____________________________ 。
(2)钼精矿焙烧时排放的尾气对环境的主要危害是___________________ ,请提出一种实验室除去该尾气的方法____________________________________ 。
(3)操作2的名称为________ 。由钼酸得到MoO3所用到的硅酸盐材料仪器的名称是________ 。
(4)焙烧钼精矿所用的装置是多层焙烧炉,图2为各炉层固体物料的物质的量的百分数(φ)。

①x=________ 。
②焙烧炉中也会发生MoS2与MoO3反应生成MoO2和SO2的反应,若该反应转移6mol电子,则消耗的氧化剂的化学式及物质的量分别为________ 、________ 。
(5)操作1中,加入碳酸钠溶液充分反应后,碱浸液中c(MoO42-)=0.80mol·L−1,c(SO42-)=0.04 mol·L−1,在结晶前需加入Ba(OH)2固体以除去溶液中的SO42-。当BaMoO4开始沉淀时,SO42-的去除率是________ 。[Ksp(BaSO4)=1.1×10−10、Ksp(BaMoO4)=4.0×10−8,溶液体积变化可忽略不计]

已知:钼酸微溶于水,可溶于液碱和氨水。
回答下列问题:
(1)焙烧钼精矿时发生的化学方程式为
(2)钼精矿焙烧时排放的尾气对环境的主要危害是
(3)操作2的名称为
(4)焙烧钼精矿所用的装置是多层焙烧炉,图2为各炉层固体物料的物质的量的百分数(φ)。

①x=
②焙烧炉中也会发生MoS2与MoO3反应生成MoO2和SO2的反应,若该反应转移6mol电子,则消耗的氧化剂的化学式及物质的量分别为
(5)操作1中,加入碳酸钠溶液充分反应后,碱浸液中c(MoO42-)=0.80mol·L−1,c(SO42-)=0.04 mol·L−1,在结晶前需加入Ba(OH)2固体以除去溶液中的SO42-。当BaMoO4开始沉淀时,SO42-的去除率是
您最近一年使用:0次
【推荐1】回答下列问题
(1)将SiCl4氢化为SiHCl3有三种方法,对应的反应依次为:
①SiCl4(g)+H2(g) SiHCl3(g)+HCl(g) ΔH1>0
SiHCl3(g)+HCl(g) ΔH1>0
②3SiCl4(g)+2H2(g)+Si(s) 4SiHCl3(g) ΔH2<0
4SiHCl3(g) ΔH2<0
③2SiCl4(g)+H2(g)+Si(s)+HCl(g) 3SiHCl3(g) ΔH3
3SiHCl3(g) ΔH3
反应③的ΔH3=___________ (用ΔH1,ΔH2表示)。
(2)用惰性电极电解一定浓度的硫酸铜溶液一段时间后,若要恢复到电解前的浓度,须向所得的溶液中加入0.3molCu(OH)2。此电解过程中两个电极共放出气体为___________ mol,若要恢复到电解前的浓度,还可加入0.3mol___________ 和0.3molH2O。
(3)用Na2CO3熔融盐作电解质,CO、O2为原料组成的新型电池示意图如图:
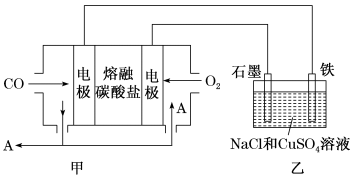
为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时必须有部分A物质参加循环。该电池负极电极反应为___________ 。
(4)用该电池电解200mL一定浓度的NaCl与CuSO4的混合溶液,其装置如乙图。理论上乙中两极所得气体的体积随时间变化的关系如丙图所示(体积为标准状况下的体积)。
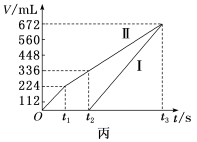
①写出在t1后,石墨电极上的电极反应:___________ ;原NaCl溶液物质的量浓度为___________ mol·L-1(假设溶液体积不变)。
②当向上述甲装置中通入标准状况下的氧气336mL时,理论上在铁电极上可析出铜的质量为___________ g。
(1)将SiCl4氢化为SiHCl3有三种方法,对应的反应依次为:
①SiCl4(g)+H2(g)
 SiHCl3(g)+HCl(g) ΔH1>0
SiHCl3(g)+HCl(g) ΔH1>0②3SiCl4(g)+2H2(g)+Si(s)
 4SiHCl3(g) ΔH2<0
4SiHCl3(g) ΔH2<0③2SiCl4(g)+H2(g)+Si(s)+HCl(g)
 3SiHCl3(g) ΔH3
3SiHCl3(g) ΔH3反应③的ΔH3=
(2)用惰性电极电解一定浓度的硫酸铜溶液一段时间后,若要恢复到电解前的浓度,须向所得的溶液中加入0.3molCu(OH)2。此电解过程中两个电极共放出气体为
(3)用Na2CO3熔融盐作电解质,CO、O2为原料组成的新型电池示意图如图:

为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时必须有部分A物质参加循环。该电池负极电极反应为
(4)用该电池电解200mL一定浓度的NaCl与CuSO4的混合溶液,其装置如乙图。理论上乙中两极所得气体的体积随时间变化的关系如丙图所示(体积为标准状况下的体积)。

①写出在t1后,石墨电极上的电极反应:
②当向上述甲装置中通入标准状况下的氧气336mL时,理论上在铁电极上可析出铜的质量为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】Cl2是重要的化工原料,可以由不同方法制备。
(1)下图是电解饱和食盐水制备Cl2的示意图。

①生成的Cl2从_____ (填“A”或“B”)口收集。
②电解饱和食盐水的总反应方程式为___________ 。
③反应前在阴极区域中加入少量NaOH的作用是___________ (填字母)。
a.增加溶液导电性 b.参与电极反应
④该方法在制备Cl2的同时,在阴极区域可以得到浓NaOH溶液,请结合化学用语解释产生浓NaOH的原因是___________ 。
(2)以HCl为原料,用O2氧化法制取Cl2可提高效益,减少污染。总反应为:4HCl(g)+O2(g) 2Cl2(g)+2H2O(g) ∆H=-115.4kJ/mol。该反应在同一反应器中,通过控制合适条件分两步循环进行,可使HCl转化率接近100%。其基本原理如下图所示。
2Cl2(g)+2H2O(g) ∆H=-115.4kJ/mol。该反应在同一反应器中,通过控制合适条件分两步循环进行,可使HCl转化率接近100%。其基本原理如下图所示。
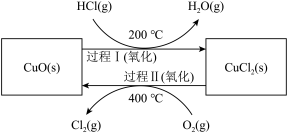
过程I的反应是2HCl(g)+CuO(s) CuCl2(s)+H2O(g) ∆H=-120.4kJ/mol,过程Ⅱ反应的热化学方程式是
CuCl2(s)+H2O(g) ∆H=-120.4kJ/mol,过程Ⅱ反应的热化学方程式是___________ 。
(1)下图是电解饱和食盐水制备Cl2的示意图。

①生成的Cl2从
②电解饱和食盐水的总反应方程式为
③反应前在阴极区域中加入少量NaOH的作用是
a.增加溶液导电性 b.参与电极反应
④该方法在制备Cl2的同时,在阴极区域可以得到浓NaOH溶液,请结合化学用语解释产生浓NaOH的原因是
(2)以HCl为原料,用O2氧化法制取Cl2可提高效益,减少污染。总反应为:4HCl(g)+O2(g)
 2Cl2(g)+2H2O(g) ∆H=-115.4kJ/mol。该反应在同一反应器中,通过控制合适条件分两步循环进行,可使HCl转化率接近100%。其基本原理如下图所示。
2Cl2(g)+2H2O(g) ∆H=-115.4kJ/mol。该反应在同一反应器中,通过控制合适条件分两步循环进行,可使HCl转化率接近100%。其基本原理如下图所示。
过程I的反应是2HCl(g)+CuO(s)
 CuCl2(s)+H2O(g) ∆H=-120.4kJ/mol,过程Ⅱ反应的热化学方程式是
CuCl2(s)+H2O(g) ∆H=-120.4kJ/mol,过程Ⅱ反应的热化学方程式是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】某高能锂离子电池的总反应为2Li+FeS═Fe+Li2S【LiPF6•SO(CH3)2为电解质,Li+可自由移动】,用该锂离子电池作电源电解含镍酸性废水回收Ni的装置如图所示。

(1)锂离子电池中电极Y为_______ 极;中间隔室b可以得到的主要物质Z是_____ (填化学式)。
(2)电解时,通过阴离子交换膜的主要离子是______ ,其迁移方向是_____
(3)电解总反应的离子方程式为__________
(4)若锂离子电池工作t min,维持电流强度为I A,理论回收Ni______ g(写出计算表达式即可,已知F=96500C/mol)
(5)电极的得失电子能力可由电极电势(E)来定量衡量,电势越高,得电子能力越强,则X、Y两极电势的关系为EX_____ EY(填“大于”或“小于”)
(6)104Pa、105Pa时由一定量丙烷脱氢制丙烯,C3H8(g)⇌C3H6(g)+H2(g) △H>0 反应在不同温度下达到平衡,测得丙烷、丙烯的物质的量分数变化关系如图示。

①104Pa时丙烷及丙烯的物质的量分数随温度变化关系的曲线分别是_____ 、_______ 。
②起始时充入一定量的丙烷发生反应,计算Q点对应温度下该反应的平衡常数KP=___________ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。

(1)锂离子电池中电极Y为
(2)电解时,通过阴离子交换膜的主要离子是
(3)电解总反应的离子方程式为
(4)若锂离子电池工作t min,维持电流强度为I A,理论回收Ni
(5)电极的得失电子能力可由电极电势(E)来定量衡量,电势越高,得电子能力越强,则X、Y两极电势的关系为EX
(6)104Pa、105Pa时由一定量丙烷脱氢制丙烯,C3H8(g)⇌C3H6(g)+H2(g) △H>0 反应在不同温度下达到平衡,测得丙烷、丙烯的物质的量分数变化关系如图示。

①104Pa时丙烷及丙烯的物质的量分数随温度变化关系的曲线分别是
②起始时充入一定量的丙烷发生反应,计算Q点对应温度下该反应的平衡常数KP=
您最近一年使用:0次



