一定条件下,工业合成氨的反应达到平衡。下列措施,既能加快该反应的速率,又能增大反应物转化率的是
| A.使用催化剂 | B.移走 NH3 | C.提高反应温度 | D.缩小容器体积 |
更新时间:2018-04-12 18:17:37
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】热催化合成氨面临的两难问题是:采用高温增大反应速率的同时会因平衡限制导致NH3产率降低。我国科研人员研制了Ti-H-Fe双温区催化剂(Ti-H区域和Fe区域的温度差可超过100℃)。Ti-H-Fe双温区催化合成氨的反应历程如图所示,其中吸附在催化剂表面上的物种用*标注。下列说法正确的是
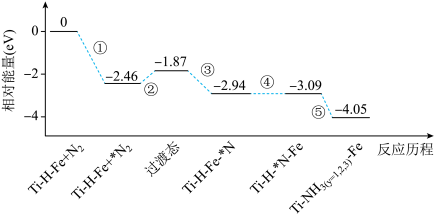

| A.①为氮氮三键的断裂过程 |
| B.①②在高温区发生,③④⑤在低温区发生 |
| C.④为N原子由Fe区域向Ti-H区域的传递过程 |
| D.使用Ti-H-Fe双温区催化剂使合成氨反应转变为吸热反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
| A.向3mL95%乙醇溶液中加入几颗CoCl2·6H2O晶体,充分溶解后再滴加蒸馏水至溶液恰好呈粉红色,用酒精灯加热该试管,溶液呈蓝色 |
| B.金属汞一旦洒落在实验室地面或桌面时,必须尽可能收集,并深埋处理 |
| C.实验室从海带中提取碘单质的方法是:取干海带→浸泡→ 过滤→氧化→结晶→ 过滤 |
| D.制备KNO3晶体实验中,为得到较大颗粒晶体,可将热KNO3溶液快速冷却 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】甲醇是重要的化工原料,应用前景广阔。研究表明,二氧化碳和氢气反应可以合成甲醇,反应如下:
 。下列措施中能提高平衡时
。下列措施中能提高平衡时 转化率的是
转化率的是

 。下列措施中能提高平衡时
。下列措施中能提高平衡时 转化率的是
转化率的是| A.升温 | B.等容下通入 |
| C.加压 | D.增大 和 和 的初始投料比 的初始投料比 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在一密闭容器中通入A、B两种气体,在一定条件下发生反应2A(g)+B(g) 2C(g) ΔH<0,当反应达到平衡后,改变一个条件(x),下表中量(y)一定符合下图中曲线的是( )
2C(g) ΔH<0,当反应达到平衡后,改变一个条件(x),下表中量(y)一定符合下图中曲线的是( )
 2C(g) ΔH<0,当反应达到平衡后,改变一个条件(x),下表中量(y)一定符合下图中曲线的是( )
2C(g) ΔH<0,当反应达到平衡后,改变一个条件(x),下表中量(y)一定符合下图中曲线的是( )| x | y | 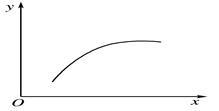 | |
| A | 温度 | 混合气体的平均相对分子质量 | |
| B | 压强 | A的百分含量 | |
| C | 再通入A | B的转化率 | |
| D | 加入催化剂 | A的质量分数 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】NO2和N2O4存在平衡:2NO2(g) N2O4(g) ΔH<0。下列分析正确的是
N2O4(g) ΔH<0。下列分析正确的是
 N2O4(g) ΔH<0。下列分析正确的是
N2O4(g) ΔH<0。下列分析正确的是| A.常温下,11.2LNO2和N2O4混合气体的物质的量为0.5mol |
| B.断裂2molNO2中的共价键所需能量小于断裂1molN2O4中的共价键所需能量 |
| C.恒温时,缩小容积,平衡正向移动,气体颜色变浅 |
| D.恒容时,水浴加热,气体颜色变浅 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】反应2NO(g) + 2CO(g) N2(g) + 2CO2(g)+Q(Q>0)可用于消除汽车尾气中的有害气体。在密闭容器中充入4 mol NO和5 mol CO,平衡时NO的体积分数随温度、压强的变化关系如图。下列说法错误的是
N2(g) + 2CO2(g)+Q(Q>0)可用于消除汽车尾气中的有害气体。在密闭容器中充入4 mol NO和5 mol CO,平衡时NO的体积分数随温度、压强的变化关系如图。下列说法错误的是
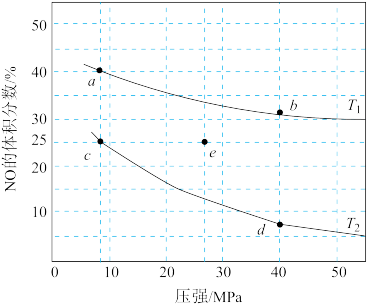
 N2(g) + 2CO2(g)+Q(Q>0)可用于消除汽车尾气中的有害气体。在密闭容器中充入4 mol NO和5 mol CO,平衡时NO的体积分数随温度、压强的变化关系如图。下列说法错误的是
N2(g) + 2CO2(g)+Q(Q>0)可用于消除汽车尾气中的有害气体。在密闭容器中充入4 mol NO和5 mol CO,平衡时NO的体积分数随温度、压强的变化关系如图。下列说法错误的是
| A.温度:T1>T2 |
| B.a点达到平衡所需时间比c点短 |
| C.c点NO的平衡转化率:50% |
| D.若在e点对反应容器升温的同时扩大体积使体系压强减小,重新达到的平衡状态可能是图中的c点 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列说法正确的是
A.恒温恒容下,NH2COONH4(s)  2NH3(g)+CO2(g),当气体的平均相对分子质量不变时,可以判断该反应已经达到平衡 2NH3(g)+CO2(g),当气体的平均相对分子质量不变时,可以判断该反应已经达到平衡 |
B.恒温恒容下,X(g)+Y(g)  2Z(g)+N(s),当混合气体的密度不再发生变化时,能表明该反应达到平衡状态 2Z(g)+N(s),当混合气体的密度不再发生变化时,能表明该反应达到平衡状态 |
C.恒温恒容下,X(g)+Y(g)  2Z(g)+N(s)达到平衡,移走部分N,平衡向正反应方向移动 2Z(g)+N(s)达到平衡,移走部分N,平衡向正反应方向移动 |
D.N2(g)+3H2(g)  2NH3(g) ΔH<0,反应达到平衡后升温,则H2反应速率和平衡转化率均增大 2NH3(g) ΔH<0,反应达到平衡后升温,则H2反应速率和平衡转化率均增大 |
您最近一年使用:0次
【推荐1】一定温度下,在三个恒容体积均为2.0L的容器中发生反应:PCl5(g) PCl3(g)+Cl2(g),下列说法不正确的个数有
PCl3(g)+Cl2(g),下列说法不正确的个数有
①平衡常数K:容器Ⅱ>容器Ⅲ
②反应到达平衡时,PCl5的转化率:容器Ⅱ>容器Ⅰ
③反应从开始到平衡时,容器I中的平均速率为v(PCl5)=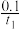 mol·L-1·s-1
mol·L-1·s-1
④起始时向容器Ⅲ中充入PCl50.30mol、PCl30.45mol和Cl20.10mol,则反应正向进行
 PCl3(g)+Cl2(g),下列说法不正确的个数有
PCl3(g)+Cl2(g),下列说法不正确的个数有| 编号 | 温度(℃) | 起始/mol | 平衡/mol | 达到平衡所需时间/s | |
| PCl5(g) | PCl3(g) | Cl2(g) | |||
| Ⅰ | 320 | 0.40 | 0.10 | 0.10 | t1 |
| Ⅱ | 320 | 0.80 | t2 | ||
| Ⅲ | 410 | 0.40 | 0.15 | 0.15 | t3 |
②反应到达平衡时,PCl5的转化率:容器Ⅱ>容器Ⅰ
③反应从开始到平衡时,容器I中的平均速率为v(PCl5)=
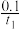 mol·L-1·s-1
mol·L-1·s-1④起始时向容器Ⅲ中充入PCl50.30mol、PCl30.45mol和Cl20.10mol,则反应正向进行
| A.1个 | B.2个 | C.3个 | D.4个 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】在容积为2L的密闭容器中,保持体系内温度800°C不变,将一定量的NO和O2混合发生反应:2NO(g)+O2(g)⇌2NO2(g),其中NO的物质的量(n)随时间(t)的变化关系如下图所示。下列说法错误的是


| A.若30s时反应达到平衡,v(O2)表示达到平衡过程的平均反应速率,则v(O2)=1.1×10-3mol·L-1·s-1 |
| B.图象中曲线II表示NO的变化 |
| C.由图象中曲线和数据,可以计算该温度下的K>1 |
| D.800°C时,反应达平衡时放出akJ热量,写出此条件下的热化学方程式为2NO(g)+O2(g)⇌2NO2(g) △H=-200a/13kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】固定容积为2 L的密闭容器中发生反应xA(g)+yB(g)  zC(g),图I表示200℃时容器中各物质的量随时间的变化关系,图II表示平衡时平衡常数K随温度变化的关系。结合图象判断,下列结论正确的是
zC(g),图I表示200℃时容器中各物质的量随时间的变化关系,图II表示平衡时平衡常数K随温度变化的关系。结合图象判断,下列结论正确的是

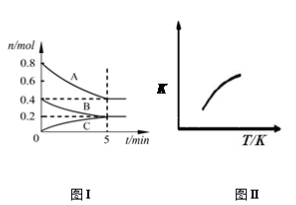
 zC(g),图I表示200℃时容器中各物质的量随时间的变化关系,图II表示平衡时平衡常数K随温度变化的关系。结合图象判断,下列结论正确的是
zC(g),图I表示200℃时容器中各物质的量随时间的变化关系,图II表示平衡时平衡常数K随温度变化的关系。结合图象判断,下列结论正确的是

| A.200℃时,反应从开始到平衡的平均反应速率v(A)=0.08 mol·L-1·min-1 |
B.若0~5 min时容器与外界的热交换总量为m kJ,则该反应的热化学方程式可表示为:2A + B  C ΔH = +5m kJ/mol C ΔH = +5m kJ/mol |
| C.200℃时,若在第6 min再向体系中加入1molAr,A的转化率不变 |
| D.200℃时,平衡后再充入2 mol B和2 mol C时,v正>v逆 |
您最近一年使用:0次

 2NO(g)+Cl2(g)。tmin后,三个容器中NOCl的转化率如图中A、B、C三点。下列叙述正确的是
2NO(g)+Cl2(g)。tmin后,三个容器中NOCl的转化率如图中A、B、C三点。下列叙述正确的是
 中不再变化后,加热能产生大量红棕色气体
中不再变化后,加热能产生大量红棕色气体 的产生
的产生 反应过程中,加入少量
反应过程中,加入少量 固体,促进
固体,促进

