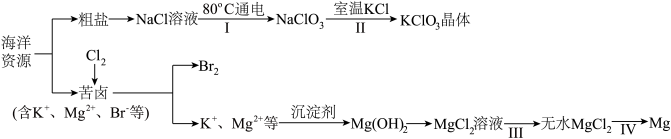
海洋资源丰富,海水水资源的利用和海水化学资源(主要为NaCl 和MgSO4及K、Br 等元素)的利用具有非常广阔的前景。
回答下列问题:
(1)NaCl 溶液由粗盐水精制而成,为除去Ca2+和Mg2+,要加入的试剂分别为__________________ 、__________________ 。
(2)写出步骤Ⅰ 中反应的总化学方程式为NaCl+ ═NaClO3+ 。_____
(3)已知MgCl2溶液受热时易水解(和水反应)生成Mg(OH)Cl,写出该过程的化学方程式__________________________________ 。
(4)步骤Ⅳ中,电解熔融MgCl2 得到的镁需要在保护气中冷却,下列气体可以作为保护气的是_______________。

回答下列问题:
(1)NaCl 溶液由粗盐水精制而成,为除去Ca2+和Mg2+,要加入的试剂分别为
(2)写出步骤Ⅰ 中反应的总化学方程式为NaCl+ ═NaClO3+ 。
(3)已知MgCl2溶液受热时易水解(和水反应)生成Mg(OH)Cl,写出该过程的化学方程式
(4)步骤Ⅳ中,电解熔融MgCl2 得到的镁需要在保护气中冷却,下列气体可以作为保护气的是_______________。
| A.N2 | B.H2 | C.CO2 | D.空气 |
更新时间:2018-10-23 18:50:07
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】I.在恒温、体积为1.0L的密闭容器中通入1.0 mol N2和x mol H2发生如下反应N2(g)+3H2(g) 2NH3(g) ,20 min后达到平衡,测得反应放出的热量为18.4 kJ,混合气体的物质的量为1.6 mol,容器内的压强变为原来的80%。请回答下列问题:
2NH3(g) ,20 min后达到平衡,测得反应放出的热量为18.4 kJ,混合气体的物质的量为1.6 mol,容器内的压强变为原来的80%。请回答下列问题:
(1)20 min内,V(N2)=______ 。
(2)该反应的热化学方程式为____________ 。
(3)下列叙述中能表示该反应达到平衡状态的是_______ (填序号)。
①N2体积分数保持不变②单位时间断裂03tmol H- H键,同时生成0.6 molN-H键
③混合气体的密度不再改变④2v正(H2)=3v逆(NH3)⑤混合气体的平均摩尔质量不再改变
II.1883年,瑞典化学家阿伦尼乌斯创立了电离学说,在水溶液范围内对酸、碱作出了严密的概括。请回答下列有关水溶液的问题:
(4) ①用电离方程式表示氨水溶液是碱性的原因________ ;
②用离子方程式表示碳酸钠溶液显碱性的原因__________ 。
 2NH3(g) ,20 min后达到平衡,测得反应放出的热量为18.4 kJ,混合气体的物质的量为1.6 mol,容器内的压强变为原来的80%。请回答下列问题:
2NH3(g) ,20 min后达到平衡,测得反应放出的热量为18.4 kJ,混合气体的物质的量为1.6 mol,容器内的压强变为原来的80%。请回答下列问题:(1)20 min内,V(N2)=
(2)该反应的热化学方程式为
(3)下列叙述中能表示该反应达到平衡状态的是
①N2体积分数保持不变②单位时间断裂03tmol H- H键,同时生成0.6 molN-H键
③混合气体的密度不再改变④2v正(H2)=3v逆(NH3)⑤混合气体的平均摩尔质量不再改变
II.1883年,瑞典化学家阿伦尼乌斯创立了电离学说,在水溶液范围内对酸、碱作出了严密的概括。请回答下列有关水溶液的问题:
(4) ①用电离方程式表示氨水溶液是碱性的原因
②用离子方程式表示碳酸钠溶液显碱性的原因
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某小组同学设计如下实验,研究亚铁盐与H2O2溶液的反应。
【实验I】试剂:酸化的0.5mol·L-1 FeSO4溶液(pH =0.2),5%H2O2溶液(pH=5)。
(1)上述实验中H2O2溶液与FeSO4溶液反应的离子方程式是________________________ 。
(2)产生气泡的原因是______________________ 。
【实验Ⅱ】试剂:未酸化的0.5mol·L-1FeSO4溶液(pH=3),5% H2O2溶液(pH=5)
(3)将上述混合物分离,得到棕黄色沉淀和红褐色胶体。取部分棕黄色沉淀洗净,加4 mol·L-1盐酸,沉淀溶解得到黄色溶液。初步判断该沉淀中含有Fe2O3,经检验还含有SO42-。检验棕黄色沉淀中SO42-的方法是_______________ 。
(4)对于生成红褐色胶体的原因,提出两种假设:
ⅰ.H2O2溶液氧化Fe2+消耗H+
ii.Fe2+氧化的产物发生了水解
①根据实验Ⅱ记录否定假设ⅰ,理由是____________________ 。
②实验验证假设ⅱ: 取__________ 溶液,加热,溶液变为红褐色,pH下降,证明假设ii成立。
(5)将FeSO4溶液加入H2O2溶液后,产生红褐色胶体,反应的离子方程式是_________________ 。
【实验Ⅲ】若用FeCl2溶液替代FeSO4溶液,其余操作与实验Ⅱ相同,除了产生与Ⅱ相同的现象外,还生成刺激性气味气体,该气体能使湿润的蓝色石蕊试纸变红但不褪色。
(6)产生刺激性气味气体的原因是___________________ 。
(7)由实验I、Ⅱ、Ⅲ可知,亚铁盐与H2O2反应的现象与______________ (至少写两点)有关。
【实验I】试剂:酸化的0.5mol·L-1 FeSO4溶液(pH =0.2),5%H2O2溶液(pH=5)。
| 操作 | 现象 |
| 取2mL上述FeSO4溶液于试管中,加入5滴5%H2O2溶液 | 溶液立即变为棕黄色,稍后,产生气泡。测得反应后溶液pH = 0.9 |
| 向反应后的溶液中加入KSCN溶液 | 溶液变红 |
(2)产生气泡的原因是
【实验Ⅱ】试剂:未酸化的0.5mol·L-1FeSO4溶液(pH=3),5% H2O2溶液(pH=5)
| 操作 | 现象 |
| 取2mL5%H2O2溶液于试管中, 加入5滴上述FeSO4溶液, | 溶液立即变为棕黄色,产生大量气泡,并放热,反应混合物颜色加深且有浑浊。测得反应后溶液pH =1.4 |
(4)对于生成红褐色胶体的原因,提出两种假设:
ⅰ.H2O2溶液氧化Fe2+消耗H+
ii.Fe2+氧化的产物发生了水解
①根据实验Ⅱ记录否定假设ⅰ,理由是
②实验验证假设ⅱ: 取
(5)将FeSO4溶液加入H2O2溶液后,产生红褐色胶体,反应的离子方程式是
【实验Ⅲ】若用FeCl2溶液替代FeSO4溶液,其余操作与实验Ⅱ相同,除了产生与Ⅱ相同的现象外,还生成刺激性气味气体,该气体能使湿润的蓝色石蕊试纸变红但不褪色。
(6)产生刺激性气味气体的原因是
(7)由实验I、Ⅱ、Ⅲ可知,亚铁盐与H2O2反应的现象与
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】二氧化钛广泛应用于各类结构表面涂料、纸张涂层等,二氧化钛还可作为制备钛单质的原料。
Ⅰ.二氧化钛可由以下两种方法制备:
方法1:TiCl4水解生成TiO2·xH2O,过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到粉体TiO2,此方法制备得到的是纳米二氧化钛。
(1)①TiCl4水解生成TiO2·x H2O的化学方程式为_______ ;
②检验TiO2·x H2O中Cl-是否被除净的方法是_______ 。
方法2:可用含有Fe2O3的钛铁矿(主要成分为FeTiO3,其中Ti元素化合价为+4价)制取,其主要流程如图:
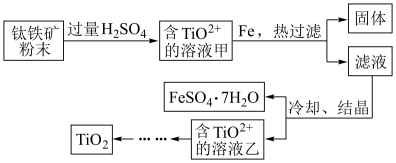
(2)Fe2O3与H2SO4反应的离子方程式是_______ 。
(3)甲溶液中除含TiO2+之外还含有的金属阳离子有_______ 。
(4)加Fe的作用是_______ 。
Ⅱ.二氧化钛可用于制取钛单质
(5)TiO2制取单质Ti,涉及到的步骤如下:
TiO2 TiCl4
TiCl4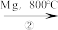 Ti
Ti
反应②的方程式是_______ ,该反应需要在Ar气氛中进行,请解释原因:_______ 。
Ⅰ.二氧化钛可由以下两种方法制备:
方法1:TiCl4水解生成TiO2·xH2O,过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到粉体TiO2,此方法制备得到的是纳米二氧化钛。
(1)①TiCl4水解生成TiO2·x H2O的化学方程式为
②检验TiO2·x H2O中Cl-是否被除净的方法是
方法2:可用含有Fe2O3的钛铁矿(主要成分为FeTiO3,其中Ti元素化合价为+4价)制取,其主要流程如图:

(2)Fe2O3与H2SO4反应的离子方程式是
(3)甲溶液中除含TiO2+之外还含有的金属阳离子有
(4)加Fe的作用是
Ⅱ.二氧化钛可用于制取钛单质
(5)TiO2制取单质Ti,涉及到的步骤如下:
TiO2
 TiCl4
TiCl4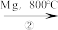 Ti
Ti反应②的方程式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】稀土元素铈及其化合物在生产生活中有重要用途,如汽车尾气用稀土/钯三效催化剂处理,不仅可以降低催化剂的成本,还可以提高催化效能。以氟碳铈矿(主要成分为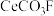 )为原料制备
)为原料制备 的一种工艺流程如图:
的一种工艺流程如图: ,滤渣2的主要成分是
,滤渣2的主要成分是 ;
; 、
、 (a、b均大于0)。
(a、b均大于0)。
②当前工艺条件下,部分金属阳离子开始沉淀和完全沉淀(离子浓度小于 )时的pH如下表:
)时的pH如下表:
回答下列问题:
(1)写出一条提高焙烧效率的方法:_______ 。
(2)加入盐酸和 进行浸取时有污染环境的气体产生,该气体为
进行浸取时有污染环境的气体产生,该气体为_______ (填化学式);操作1和操作2的名称为_______ 。
(3)调节滤液1的pH的范围为_______ ;滤渣3的主要成分为_______ (填化学式)。
(4) 有强氧化性,含
有强氧化性,含 的溶液可吸收雾霾中的NO,生成
的溶液可吸收雾霾中的NO,生成 、
、 (二者物质的量之比为1:1),该反应的离子方程式为
(二者物质的量之比为1:1),该反应的离子方程式为_______ 。
(5)滤渣1经KCl溶液充分浸取后,测得反应体系中 的物质的量浓度为
的物质的量浓度为 ,则
,则 的物质的量浓度为
的物质的量浓度为_______  (用含a、b的式子表示)。
(用含a、b的式子表示)。
(6)在空气中焙烧 的反应方程式为
的反应方程式为_______ 。
(7)某研究小组利用硫化锌锂电池,在酸性环境下电解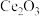 制
制 的装置如图所示。阴极的电极反应式为
的装置如图所示。阴极的电极反应式为_______ ,随着电解反应的进行,为使电解液成分稳定,应不断补充_______ (填化学式)。
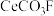 )为原料制备
)为原料制备 的一种工艺流程如图:
的一种工艺流程如图:
 ,滤渣2的主要成分是
,滤渣2的主要成分是 ;
; 、
、 (a、b均大于0)。
(a、b均大于0)。②当前工艺条件下,部分金属阳离子开始沉淀和完全沉淀(离子浓度小于
 )时的pH如下表:
)时的pH如下表:| 金属阳离子 |  |  |
| 开始沉淀时的pH | 1.3 | 7.7 |
| 完全沉淀时的pH | 3.1 | 9.2 |
(1)写出一条提高焙烧效率的方法:
(2)加入盐酸和
 进行浸取时有污染环境的气体产生,该气体为
进行浸取时有污染环境的气体产生,该气体为(3)调节滤液1的pH的范围为
(4)
 有强氧化性,含
有强氧化性,含 的溶液可吸收雾霾中的NO,生成
的溶液可吸收雾霾中的NO,生成 、
、 (二者物质的量之比为1:1),该反应的离子方程式为
(二者物质的量之比为1:1),该反应的离子方程式为(5)滤渣1经KCl溶液充分浸取后,测得反应体系中
 的物质的量浓度为
的物质的量浓度为 ,则
,则 的物质的量浓度为
的物质的量浓度为 (用含a、b的式子表示)。
(用含a、b的式子表示)。(6)在空气中焙烧
 的反应方程式为
的反应方程式为(7)某研究小组利用硫化锌锂电池,在酸性环境下电解
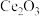 制
制 的装置如图所示。阴极的电极反应式为
的装置如图所示。阴极的电极反应式为
您最近一年使用:0次
【推荐2】氰化钠(NaCN)是一种基本化工原料,同时也是一种剧毒物质。一旦泄漏需要及时处理,一般可以通过喷洒双氧水或过硫酸钠(Na2S2O8)溶液来处理,以减轻环境污染。
I.(1)NaCN用双氧水处理后,产生一种酸式盐和一种能使湿润的红色石蕊试纸变蓝的气体,该反应的化学方程式是____________________ 。
Ⅱ.工业制备过硫酸钠的反应原理如下:
主反应
副反应: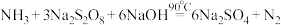
某化学小组利用上述原理在实验室制备过硫酸钠,并用过硫酸钠溶液处理含氰化钠的废水。
实验一:实验室通过如下图所示装置制备Na2S2O8。
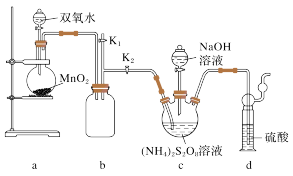
(2)装置中盛放双氧水的仪器名称是_________ 。
(3)装置a中反应产生的气体需要持续通入装置c的原因是______________________ 。
(4)上述装置中还需补充的实验仪器或装置有__________ (填字母)。
A.温度计 B.洗气瓶 C.水浴加热装置 D.环形玻璃搅拌棒
实验二:测定用过硫酸钠溶液处理后的废水中氰化钠的含量。
已知:①废水中氰化钠的最高排放标准为0.50mg/L。
②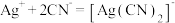 ,
,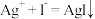 ,AgI呈黄色,
,AgI呈黄色, 优先与
优先与 反应。实验如下:取1L处理后的NaCN废水,浓缩为10.00mL置于锥形瓶中,并滴加几滴KI溶液作指示剂,用
反应。实验如下:取1L处理后的NaCN废水,浓缩为10.00mL置于锥形瓶中,并滴加几滴KI溶液作指示剂,用 mol/L的标准
mol/L的标准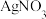 溶液滴定,消耗
溶液滴定,消耗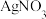 溶液的体积为5.00mL。
溶液的体积为5.00mL。
(5)滴定终点的现象是__________________________________ 。
(6)处理后的废水中氰化钠的浓度为_________ mg/L;处理后的废水是否达到排放标准?___________ (填“是”或“否”)。
Ⅲ.(7)常温下,含硫微粒主要存在形式,受pH影响。利用电化学原理,用惰性电极电解饱和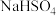 溶液也可以制备过硫酸钠。已知在阳极放电的离子主要为
溶液也可以制备过硫酸钠。已知在阳极放电的离子主要为 ,则阳极反应方程式为
,则阳极反应方程式为_____________________ 。
I.(1)NaCN用双氧水处理后,产生一种酸式盐和一种能使湿润的红色石蕊试纸变蓝的气体,该反应的化学方程式是
Ⅱ.工业制备过硫酸钠的反应原理如下:
主反应

副反应:
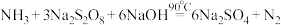
某化学小组利用上述原理在实验室制备过硫酸钠,并用过硫酸钠溶液处理含氰化钠的废水。
实验一:实验室通过如下图所示装置制备Na2S2O8。

(2)装置中盛放双氧水的仪器名称是
(3)装置a中反应产生的气体需要持续通入装置c的原因是
(4)上述装置中还需补充的实验仪器或装置有
A.温度计 B.洗气瓶 C.水浴加热装置 D.环形玻璃搅拌棒
实验二:测定用过硫酸钠溶液处理后的废水中氰化钠的含量。
已知:①废水中氰化钠的最高排放标准为0.50mg/L。
②
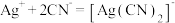 ,
,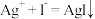 ,AgI呈黄色,
,AgI呈黄色, 优先与
优先与 反应。实验如下:取1L处理后的NaCN废水,浓缩为10.00mL置于锥形瓶中,并滴加几滴KI溶液作指示剂,用
反应。实验如下:取1L处理后的NaCN废水,浓缩为10.00mL置于锥形瓶中,并滴加几滴KI溶液作指示剂,用 mol/L的标准
mol/L的标准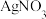 溶液滴定,消耗
溶液滴定,消耗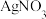 溶液的体积为5.00mL。
溶液的体积为5.00mL。(5)滴定终点的现象是
(6)处理后的废水中氰化钠的浓度为
Ⅲ.(7)常温下,含硫微粒主要存在形式,受pH影响。利用电化学原理,用惰性电极电解饱和
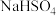 溶液也可以制备过硫酸钠。已知在阳极放电的离子主要为
溶液也可以制备过硫酸钠。已知在阳极放电的离子主要为 ,则阳极反应方程式为
,则阳极反应方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】汽车尾气中含有氮氧化合物和CO,减少它们在大气中的排放是环境保护的重要内容之一。
(1)已知: ① N2(g)+O2(g) 2NO(g) ΔH1=+180kJ•mol﹣1
2NO(g) ΔH1=+180kJ•mol﹣1
②C(s)+O2(g)═CO2(g) ΔH2=﹣393kJ•mol﹣1
③2C(s)+O2(g)═2CO(g) ΔH3=﹣221kJ•mol﹣1
若某反应的平衡常数表达式为K ,请写出此反应的热化学方程式:
,请写出此反应的热化学方程式:_____ 。
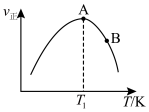
(2)欲研究在某催化剂作用下2CO(g)+2NO(g) N2(g)+2CO2(g)的反应速率与温度的关系,在其他条件相同时,改变反应温度,测得经过相同时间时该反应的正反应速率如图所示,A、B两点对应温度下正反应速率变化的原因可能是
N2(g)+2CO2(g)的反应速率与温度的关系,在其他条件相同时,改变反应温度,测得经过相同时间时该反应的正反应速率如图所示,A、B两点对应温度下正反应速率变化的原因可能是_____ ,A、B两点对应温度下该反应的活化能Ea(A) _____ Ea(B)(填“>”或“<”)。
(3)设K 为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为kPa)除以p0(p0=100kPa)。在某温度下,原料组成n(CO):n(NO)=1:1,初始总压为100kPa的恒容密闭容器中进行上述反应,体系达到平衡时N2的分压为20kPa,则该反应的相对压力平衡常数K
为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为kPa)除以p0(p0=100kPa)。在某温度下,原料组成n(CO):n(NO)=1:1,初始总压为100kPa的恒容密闭容器中进行上述反应,体系达到平衡时N2的分压为20kPa,则该反应的相对压力平衡常数K =
=___________ 。
(4)用NH3可以消除NO污染:4NH3(g)+6NO(g) 5N2(g)+6H2O(l),该反应速率v正=k正•C4(NH3)•c6(NO),v逆=k逆•C5(N2),若将9molNH3和11molNO投入真空容器中恒温恒容(温度298K、体积为10L)进行反应,已知该条件下k正=6.4×102(mol/L)﹣9•s﹣1,当平衡时NH3转化率为
5N2(g)+6H2O(l),该反应速率v正=k正•C4(NH3)•c6(NO),v逆=k逆•C5(N2),若将9molNH3和11molNO投入真空容器中恒温恒容(温度298K、体积为10L)进行反应,已知该条件下k正=6.4×102(mol/L)﹣9•s﹣1,当平衡时NH3转化率为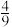 ,v逆=
,v逆=___________ mol•L﹣1•s﹣1。
(5)Na2FeO4是制造高铁电池的重要原料,同时也是一种新型的高效净水剂。在工业上通常利用如图所示装置制备Na2FeO4。
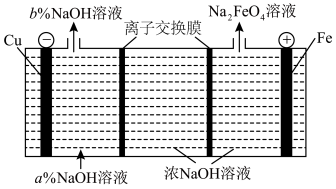
①电解时,阳极电极反应式为___________ 。
②若b>a,图中右侧的离子交换膜为___________ (填“阴”或“阳”)离子交换膜。
(1)已知: ① N2(g)+O2(g)
 2NO(g) ΔH1=+180kJ•mol﹣1
2NO(g) ΔH1=+180kJ•mol﹣1②C(s)+O2(g)═CO2(g) ΔH2=﹣393kJ•mol﹣1
③2C(s)+O2(g)═2CO(g) ΔH3=﹣221kJ•mol﹣1
若某反应的平衡常数表达式为K
 ,请写出此反应的热化学方程式:
,请写出此反应的热化学方程式:(2)欲研究在某催化剂作用下2CO(g)+2NO(g)
 N2(g)+2CO2(g)的反应速率与温度的关系,在其他条件相同时,改变反应温度,测得经过相同时间时该反应的正反应速率如图所示,A、B两点对应温度下正反应速率变化的原因可能是
N2(g)+2CO2(g)的反应速率与温度的关系,在其他条件相同时,改变反应温度,测得经过相同时间时该反应的正反应速率如图所示,A、B两点对应温度下正反应速率变化的原因可能是
(3)设K
 为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为kPa)除以p0(p0=100kPa)。在某温度下,原料组成n(CO):n(NO)=1:1,初始总压为100kPa的恒容密闭容器中进行上述反应,体系达到平衡时N2的分压为20kPa,则该反应的相对压力平衡常数K
为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为kPa)除以p0(p0=100kPa)。在某温度下,原料组成n(CO):n(NO)=1:1,初始总压为100kPa的恒容密闭容器中进行上述反应,体系达到平衡时N2的分压为20kPa,则该反应的相对压力平衡常数K =
=(4)用NH3可以消除NO污染:4NH3(g)+6NO(g)
 5N2(g)+6H2O(l),该反应速率v正=k正•C4(NH3)•c6(NO),v逆=k逆•C5(N2),若将9molNH3和11molNO投入真空容器中恒温恒容(温度298K、体积为10L)进行反应,已知该条件下k正=6.4×102(mol/L)﹣9•s﹣1,当平衡时NH3转化率为
5N2(g)+6H2O(l),该反应速率v正=k正•C4(NH3)•c6(NO),v逆=k逆•C5(N2),若将9molNH3和11molNO投入真空容器中恒温恒容(温度298K、体积为10L)进行反应,已知该条件下k正=6.4×102(mol/L)﹣9•s﹣1,当平衡时NH3转化率为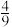 ,v逆=
,v逆=(5)Na2FeO4是制造高铁电池的重要原料,同时也是一种新型的高效净水剂。在工业上通常利用如图所示装置制备Na2FeO4。

①电解时,阳极电极反应式为
②若b>a,图中右侧的离子交换膜为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】硼及其化合物在工业上有许多用途.以铁硼矿(主要成分为 和
和 ,还有少量
,还有少量 、
、 、
、 、
、 和
和 等)为原料制备硼酸
等)为原料制备硼酸 的工艺流程如下:
的工艺流程如下: :7.6~9.6
:7.6~9.6  :2.7~3.7
:2.7~3.7  :3.4~4.7
:3.4~4.7  :9.6~11.1
:9.6~11.1
请回答下列问题:
(1)写出 与硫酸反应的化学方程式:
与硫酸反应的化学方程式:_______ 。
(2)为提高浸出速率,除适当增加硫酸浓度外,还可采取的措施有_______ (写出两条)。
(3)“浸渣”中的物质是_______ (化学式)。
(4)“净化除杂”需先加 溶液,其作用用离子方程式表示为
溶液,其作用用离子方程式表示为_______ ,然后再调节溶液的pH约为5,其目的是_______ 。
(5)硼的重要化合物 与水反应生成硼酸和氢气,在某温度下
与水反应生成硼酸和氢气,在某温度下 与水反应后得
与水反应后得 溶液,其pH值为
溶液,其pH值为_______ (已知该温度下硼酸的电离常数 )。
)。
 和
和 ,还有少量
,还有少量 、
、 、
、 、
、 和
和 等)为原料制备硼酸
等)为原料制备硼酸 的工艺流程如下:
的工艺流程如下:
 :7.6~9.6
:7.6~9.6  :2.7~3.7
:2.7~3.7  :3.4~4.7
:3.4~4.7  :9.6~11.1
:9.6~11.1请回答下列问题:
(1)写出
 与硫酸反应的化学方程式:
与硫酸反应的化学方程式:(2)为提高浸出速率,除适当增加硫酸浓度外,还可采取的措施有
(3)“浸渣”中的物质是
(4)“净化除杂”需先加
 溶液,其作用用离子方程式表示为
溶液,其作用用离子方程式表示为(5)硼的重要化合物
 与水反应生成硼酸和氢气,在某温度下
与水反应生成硼酸和氢气,在某温度下 与水反应后得
与水反应后得 溶液,其pH值为
溶液,其pH值为 )。
)。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】如下图所示(B中冷却装置未画出),将氯气和空气(不参与反应)以体积比约1:3混合通入含水8%的碳酸钠中制备Cl2O,并用水吸收Cl2O制备次氯酸溶液。

已知:Cl2O极易溶于水并与水反应生成HClO;Cl2O的沸点为3.8℃,42℃以上分解为Cl2和O2。
(1)①实验中控制氯气与空气体积比的方法是______ 。
②为使反应充分进行,实验中采取的措施有______ 。
(2)①写出装置B中产生Cl2O的化学方程式并用单线桥法标出电子转移的方向和数目:______ 。
②若B无冷却装置,则进入C中的Cl2O会大量减少。其原因是______ 。
(3)装置C中采用棕色圆底烧瓶是因为______ 。
(4)已知次氯酸可被H2O2、FeCl2等物质还原成Cl-。测定C中次氯酸溶液的物质的量浓度的实验方案为:用酸式滴定管准确量取20.00 mL次氯酸溶液,______ 。(可选用的试剂:H2O2溶液、FeCl2溶液、AgNO3溶液。除常用仪器外须使用的仪器有:电子天平,真空干燥箱)

已知:Cl2O极易溶于水并与水反应生成HClO;Cl2O的沸点为3.8℃,42℃以上分解为Cl2和O2。
(1)①实验中控制氯气与空气体积比的方法是
②为使反应充分进行,实验中采取的措施有
(2)①写出装置B中产生Cl2O的化学方程式并用单线桥法标出电子转移的方向和数目:
②若B无冷却装置,则进入C中的Cl2O会大量减少。其原因是
(3)装置C中采用棕色圆底烧瓶是因为
(4)已知次氯酸可被H2O2、FeCl2等物质还原成Cl-。测定C中次氯酸溶液的物质的量浓度的实验方案为:用酸式滴定管准确量取20.00 mL次氯酸溶液,
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
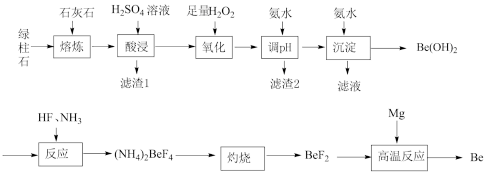
【推荐3】铍作为一种新兴材料日益被重视,有“超级金属”之称。工业上常用绿柱石(主要成分为3BeO·Al2O3·6SiO2,还含有铁等杂质)冶炼铍,工艺流程如图所示:
已知:①按元素周期表的对角线规则Be和Al性质相似;
②几种物质沉淀时的pH如下表:
回答下列问题:
(1)“酸浸”时将熔炼后的熔块粉碎的目的是___________ 。
(2)“调pH”得到沉淀的合理pH范围是___________ 。
(3)“沉淀" 反应不宜使用NaOH溶液的原因是(用离子方程式表示)___________ 。
(4)从“反应”后的溶液中得到(NH4)2BeF4固体的实验操作是___________ 、___________ 、过滤、洗涤、干燥。
(5)“ 高温反应”需要在隔绝空气的环境中进行,其原因是___________ 。
(6)3BeO·Al2O3·6SiO2中O、Si、Al元素第一电离能由大到小的顺序为___________ 。绿柱石中Be元素的质量分数为a%,上述过程中 Be的产率为b%。则1 t该绿柱石理论上能生产含铍量1%的镀铜合金___________ t。

已知:①按元素周期表的对角线规则Be和Al性质相似;
②几种物质沉淀时的pH如下表:
| Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Be(OH)2 | |
| 开始沉淀时 | 1.5 | 3.3 | 6.5 | 5.2 |
| 沉淀完全时 | 3.7 | 5.0 | 9.7 | 8.8 |
(1)“酸浸”时将熔炼后的熔块粉碎的目的是
(2)“调pH”得到沉淀的合理pH范围是
(3)“沉淀" 反应不宜使用NaOH溶液的原因是(用离子方程式表示)
(4)从“反应”后的溶液中得到(NH4)2BeF4固体的实验操作是
(5)“ 高温反应”需要在隔绝空气的环境中进行,其原因是
(6)3BeO·Al2O3·6SiO2中O、Si、Al元素第一电离能由大到小的顺序为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】广西北部湾拥有丰富的海洋资源。关注海洋健康,守护蔚蓝星球,是每个公民义不容辞的责任。基于海水资源开发的氯碱工业、海水提镁等工业蓬勃发展。下图是海水综合利用的部分流程图,据图回答问题:

(1)步骤Ⅰ、Ⅱ、Ⅲ、Ⅳ中不涉及氧化还原反应的是:___________ 。
(2)粗盐中含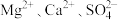 等杂质,为除去以上杂质离子,可加入足量的①
等杂质,为除去以上杂质离子,可加入足量的① 溶液 ②
溶液 ② 溶液 ③
溶液 ③ 溶液过滤后加入稀盐酸,以上操作顺序错误的是
溶液过滤后加入稀盐酸,以上操作顺序错误的是___________ (填字母)。
A.①②③ B.②①③ C.②③① D.③②①
检验提纯后的溶液中是否还存在 的操作是
的操作是___________ 。
(3)步骤Ⅱ是侯氏制碱法的重要步骤,即将二氧化碳通入氨化的饱和食盐水中,使溶解度小的碳酸氢钠从溶液中析出,写出该反应的化学方程式___________ 。
(4)图中制漂白粉的反应中,消耗标准状况下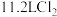 ,转移的电子数是
,转移的电子数是___________  。
。
(5)图中虚框提镁的过程中,没有涉及的化学反应类型是___________(填字母)。
(6)空气吹出的 可以采用纯碱溶液吸收,吸收后得到
可以采用纯碱溶液吸收,吸收后得到 和
和 溶液,同时有
溶液,同时有 放出,该反应的离子方程式是
放出,该反应的离子方程式是___________ 。
(7)如图是实验室蒸馏装置图,可利用此装置将海水淡化,该装置中有一处错误,该错误之处是___________ 。


(1)步骤Ⅰ、Ⅱ、Ⅲ、Ⅳ中不涉及氧化还原反应的是:
(2)粗盐中含
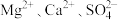 等杂质,为除去以上杂质离子,可加入足量的①
等杂质,为除去以上杂质离子,可加入足量的① 溶液 ②
溶液 ② 溶液 ③
溶液 ③ 溶液过滤后加入稀盐酸,以上操作顺序错误的是
溶液过滤后加入稀盐酸,以上操作顺序错误的是A.①②③ B.②①③ C.②③① D.③②①
检验提纯后的溶液中是否还存在
 的操作是
的操作是(3)步骤Ⅱ是侯氏制碱法的重要步骤,即将二氧化碳通入氨化的饱和食盐水中,使溶解度小的碳酸氢钠从溶液中析出,写出该反应的化学方程式
(4)图中制漂白粉的反应中,消耗标准状况下
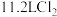 ,转移的电子数是
,转移的电子数是 。
。(5)图中虚框提镁的过程中,没有涉及的化学反应类型是___________(填字母)。
| A.化合反应 | B.分解反应 | C.复分解反应 | D.置换反应 |
 可以采用纯碱溶液吸收,吸收后得到
可以采用纯碱溶液吸收,吸收后得到 和
和 溶液,同时有
溶液,同时有 放出,该反应的离子方程式是
放出,该反应的离子方程式是(7)如图是实验室蒸馏装置图,可利用此装置将海水淡化,该装置中有一处错误,该错误之处是

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】空气吹出法是目前从海水中提取溴的常用方法,流程如下(苦卤:海水蒸发结晶分离出食盐后的母液):

(1)反应①的离子方程式为________ 。
(2)反应②中的还原剂是________ 。
(3)实验室从反应③后的溶液中分离出单质溴的方法是______ 、______ 、蒸馏。
(4)苦卤还可以用来制取金属镁,用化学方程式表示从苦卤制取金属镁的反应原理_______ 。

(1)反应①的离子方程式为
(2)反应②中的还原剂是
(3)实验室从反应③后的溶液中分离出单质溴的方法是
(4)苦卤还可以用来制取金属镁,用化学方程式表示从苦卤制取金属镁的反应原理
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】海水资源的综合利用具有非常广阔的前景,从海水晒盐分离后所得苦卤(含Mg2+、K+、Br-)中提取镁、溴的工艺流程如图:

回答下列问题:
(1)从海水中获得淡水的主要方法有电渗析法、离子交换法和____ 。
(2)为了使海水中的Mg2+沉淀下来,充分利用当地的贝壳资源获得试剂A,试剂A的化学式是____ ,这样做的优点是____ 。
(3)操作I是____ ;操作II是在一定条件下蒸发浓缩,____ ,过滤,洗涤,干燥;操作III涉及的化学方程式是____ 。
(4)吸收塔中会生成NaBr、NaBrO3,同时产生一种气体,化学方程式是____ 。
(5)酸化浓缩时已产生Br2,工业生产中还需经过吹出、吸收、酸化等过程,目的是____ 。
(6)已知海水中Br-含量为65mg•L-1,若主业上制得含65% Br2的产品1t,至少需要海水____ m3。

回答下列问题:
(1)从海水中获得淡水的主要方法有电渗析法、离子交换法和
(2)为了使海水中的Mg2+沉淀下来,充分利用当地的贝壳资源获得试剂A,试剂A的化学式是
(3)操作I是
(4)吸收塔中会生成NaBr、NaBrO3,同时产生一种气体,化学方程式是
(5)酸化浓缩时已产生Br2,工业生产中还需经过吹出、吸收、酸化等过程,目的是
(6)已知海水中Br-含量为65mg•L-1,若主业上制得含65% Br2的产品1t,至少需要海水
您最近一年使用:0次



