回答下列问题:
(1)有一种溶液除H+、OH-外,还有Na+、SO 和Cl-,测得三种离子的浓度分别是0.01 mol·L-1、0.0035 mol·L-1和0.004 mol·L-1,该溶液的pH为
和Cl-,测得三种离子的浓度分别是0.01 mol·L-1、0.0035 mol·L-1和0.004 mol·L-1,该溶液的pH为________ 。
(2)NH4Cl溶液显酸性,试用离子方程式表示这一原理______________________ 。
(3)液氨的电离类似于水,试写出液氨的电离方程式________________________________ ;在液氨中加入NH4Cl,平衡将向________ 移动。
(1)有一种溶液除H+、OH-外,还有Na+、SO
 和Cl-,测得三种离子的浓度分别是0.01 mol·L-1、0.0035 mol·L-1和0.004 mol·L-1,该溶液的pH为
和Cl-,测得三种离子的浓度分别是0.01 mol·L-1、0.0035 mol·L-1和0.004 mol·L-1,该溶液的pH为(2)NH4Cl溶液显酸性,试用离子方程式表示这一原理
(3)液氨的电离类似于水,试写出液氨的电离方程式
更新时间:2018/12/09 14:23:36
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】下表是铬酸(H2CrO4)溶液中离子的组成(单位均为mol/L)与pH的关系,请回答后面的问题:
写出铬酸电离反应方程式_______ 。
| pH | c(CrO ) ) | c(HCrO ) ) | c(Cr2O ) ) | c(H2CrO4) |
| 4 | 0.0003 | 0.104 | 0.448 | 0 |
| 5 | 0.0033 | 0.103 | 0.447 | 0 |
| 6 | 0.0319 | 0.0999 | 0.437 | 0 |
| 7 | 0.2745 | 0.086 | 0.3195 | 0 |
| 8 | 0.902 | 0.0282 | 0.0347 | 0 |
| 9 | 0.996 | 0.0031 | 0.0004 | 0 |
写出铬酸电离反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】连二次硝酸(H2N2O2)是一种二元酸,可用于制N2O气体。
(1)连二次硝酸中氮元素的化合价为_________________ 。
(2)常温下,用0.01mol • L-1的NaOH溶液滴定10mL 0.01mol·L-1的H2N2O2溶液,测得溶液的pH与NaOH溶液体积的关系如图所示。

①写出H2N2O2在水溶液中的电离方程式:____________________ 。
②b点时溶液中c(H2N2O2)_________ c(N2O22-) 。(填“>”“ <”或“=”下同)
③a点时溶液中c(Na+)_________ c(HN2O2-)+c(N2O22-)。
(3)向10mL 0.1mol/L的硝酸银溶液中滴加等浓度的连二次硝酸钠溶液,要使Ag完全沉淀[c(Ag+)小于10-5 mol/L],至少需要连二次硝酸钠溶液___________ mL。[已知Ksp(Ag2N2O2)=4.0×10-12]
(1)连二次硝酸中氮元素的化合价为
(2)常温下,用0.01mol • L-1的NaOH溶液滴定10mL 0.01mol·L-1的H2N2O2溶液,测得溶液的pH与NaOH溶液体积的关系如图所示。

①写出H2N2O2在水溶液中的电离方程式:
②b点时溶液中c(H2N2O2)
③a点时溶液中c(Na+)
(3)向10mL 0.1mol/L的硝酸银溶液中滴加等浓度的连二次硝酸钠溶液,要使Ag完全沉淀[c(Ag+)小于10-5 mol/L],至少需要连二次硝酸钠溶液
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列各小题
(1)H2S溶于水的电离方程式为__________________ 。
(2)向H2S溶液中加入CuSO4(aq)时,电离平衡向_____ 移动(填“左”或“右”),c(H+)___ ,c(S2-)_____ (填“增大”、“减小”或“不变”);
(3)向H2S溶液中加入NaOH(s)时,电离平衡向______ 移动(填“左”或“右”),c(H+)____ ,c(S2-)_____ (填“增大”、“减小”或“不变”);
(4)若将H2S溶液加热至沸腾,c(H2S)_________ 填“增大”、“减小”或“不变”);若要增大H2S溶液中c(S2-),最好加入____________ 。
(1)H2S溶于水的电离方程式为
(2)向H2S溶液中加入CuSO4(aq)时,电离平衡向
(3)向H2S溶液中加入NaOH(s)时,电离平衡向
(4)若将H2S溶液加热至沸腾,c(H2S)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】过氧化氢(H2O2)是淡蓝色的黏稠液体,水溶液为无色透明液体,俗称双氧水,可以看作二元弱酸。
(1)H2O2在水中的电离方程式是__________________。
(2)H2O2常被称为“绿色”氧化剂的原因是____________________。
(3)向1 mol/L FeCl2溶液中滴加30%双氧水,除观察到双氧水分解产生的大量无色气泡外,还观察到浅绿色溶液逐渐变为红褐色,并测得其pH由反应前的3.69变为1.84。实验证明所得液体属于胶体,其方法是;_______,上述Fe2+被氧化成红褐色胶体的离子方程式是___________________。
(4)如图是一种用电解原理来制备H2O2,并用产生的H2O2处理废氨水的装置。
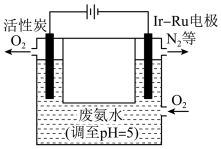
① 为了不影响H2O2的产量,需要向废氨水中加入适量HNO3调节溶液的pH约为5,则所得溶液中c(NH4+)__________c(NO3-)(填“>”、“<”或“=”)。
② Ir-Ru惰性电极吸附O2生成H2O2,其电极反应式是___________________。
③ 理论上电路中每转移3 mol e-,最多可以处理废氨水中溶质(以NH3计)的质量是_________g。
(1)H2O2在水中的电离方程式是__________________。
(2)H2O2常被称为“绿色”氧化剂的原因是____________________。
(3)向1 mol/L FeCl2溶液中滴加30%双氧水,除观察到双氧水分解产生的大量无色气泡外,还观察到浅绿色溶液逐渐变为红褐色,并测得其pH由反应前的3.69变为1.84。实验证明所得液体属于胶体,其方法是;_______,上述Fe2+被氧化成红褐色胶体的离子方程式是___________________。
(4)如图是一种用电解原理来制备H2O2,并用产生的H2O2处理废氨水的装置。

① 为了不影响H2O2的产量,需要向废氨水中加入适量HNO3调节溶液的pH约为5,则所得溶液中c(NH4+)__________c(NO3-)(填“>”、“<”或“=”)。
② Ir-Ru惰性电极吸附O2生成H2O2,其电极反应式是___________________。
③ 理论上电路中每转移3 mol e-,最多可以处理废氨水中溶质(以NH3计)的质量是_________g。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】按要求填空。
(1) 已知H3PO2是一元弱酸,写出H3PO2电离方程式:_________________________________ ,NaH2PO2是___ 盐(填“正盐、酸式盐或碱式盐”)。
(2)熔融NaHSO4的电离方程式:_______________________________________ ;
(3) 中国自古有“信口雌黄”“雄黄入药”之说。雌黄As2S3和雄黄As4S4都是自然界中常见的砷化物,早期都曾用作绘画颜料,因都有抗病毒疗效也用来入药。砷元素有+2、+3两种常见价态。一定条件下,雌黄和雄黄的转化关系如图所示。
①以上转换关系图中发生的Ⅰ、Ⅱ、Ⅲ、Ⅳ反应,属于氧化还原反应的是___________ .
②用双线桥法表示反应Ⅰ中的电子转移方向和数目:_________________________ .
③假设物质转化率为100%,若Ⅱ中有0.1 mol As4S4反应,转移2.8 mol 电子,则标准状况下消耗O2的体积为_________________ 。
(1) 已知H3PO2是一元弱酸,写出H3PO2电离方程式:
(2)熔融NaHSO4的电离方程式:
(3) 中国自古有“信口雌黄”“雄黄入药”之说。雌黄As2S3和雄黄As4S4都是自然界中常见的砷化物,早期都曾用作绘画颜料,因都有抗病毒疗效也用来入药。砷元素有+2、+3两种常见价态。一定条件下,雌黄和雄黄的转化关系如图所示。
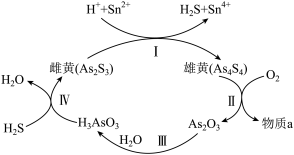
①以上转换关系图中发生的Ⅰ、Ⅱ、Ⅲ、Ⅳ反应,属于氧化还原反应的是
②用双线桥法表示反应Ⅰ中的电子转移方向和数目:
③假设物质转化率为100%,若Ⅱ中有0.1 mol As4S4反应,转移2.8 mol 电子,则标准状况下消耗O2的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题
(1)写出下列离子方程式:
①Ba(OH)2 在水溶液中电离:_______
②H2S 在水溶液中电离:_______
③NaHCO3 在水溶液中电离:_______
④NaHSO4 在水溶液中电离:_______
⑤少量 CO2 通入 NaClO 溶液中_______
⑥泡沫灭火器的原理:_______
(2)已知 NH3·H2O 的 Kb=1.8 ×10-5
①计算 0.10 mol/L 的 NH3·H2O 的 c(OH-)=_______ (可以不化简)。
②若向其中加入固体 NH4Cl,使 c(NH )的浓度达到 0.20 mol/L,计算c(OH-)=
)的浓度达到 0.20 mol/L,计算c(OH-)=_______ 。
(1)写出下列离子方程式:
①Ba(OH)2 在水溶液中电离:
②H2S 在水溶液中电离:
③NaHCO3 在水溶液中电离:
④NaHSO4 在水溶液中电离:
⑤少量 CO2 通入 NaClO 溶液中
⑥泡沫灭火器的原理:
(2)已知 NH3·H2O 的 Kb=1.8 ×10-5
①计算 0.10 mol/L 的 NH3·H2O 的 c(OH-)=
②若向其中加入固体 NH4Cl,使 c(NH
 )的浓度达到 0.20 mol/L,计算c(OH-)=
)的浓度达到 0.20 mol/L,计算c(OH-)=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
(1)写出Na2SO3溶于水发生电离和水解的所有方程式_______ 。
(2)写出BaSO4的沉淀溶解平衡方程式_______ 。
(3)用离子方程式表示下列金属离子和酸根不能在水中大量共存的原因
①
_______ 。
②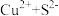
_______ 。
③
_______ 。
(1)写出Na2SO3溶于水发生电离和水解的所有方程式
(2)写出BaSO4的沉淀溶解平衡方程式
(3)用离子方程式表示下列金属离子和酸根不能在水中大量共存的原因
①

②
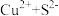
③

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】按要求写出相应的方程式:
电离方程式:
(1) H2S:________________________________________
(2) NH4HSO4:___________________________________
水解反应的离子方程式:
(3)CuSO4:_________________________________________
(4)Na2CO3:________________________________________
(5)AlCl3+NaHCO3:_________________________________
电离方程式:
(1) H2S:
(2) NH4HSO4:
水解反应的离子方程式:
(3)CuSO4:
(4)Na2CO3:
(5)AlCl3+NaHCO3:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】有下列盐溶液:① 、②
、② 、③
、③ 、④
、④ 、⑤
、⑤ .
.
(1)将上述盐溶液根据酸碱性进行分类,概括盐的酸碱性与生成盐对应的酸碱强弱的关系。________
(2)用化学用语表示③ 、④
、④ 溶液表现不同酸碱性的原因。
溶液表现不同酸碱性的原因。______________
(3)常温下, 的
的 溶液中,
溶液中,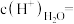
___________ 。
 、②
、② 、③
、③ 、④
、④ 、⑤
、⑤ .
.(1)将上述盐溶液根据酸碱性进行分类,概括盐的酸碱性与生成盐对应的酸碱强弱的关系。
(2)用化学用语表示③
 、④
、④ 溶液表现不同酸碱性的原因。
溶液表现不同酸碱性的原因。(3)常温下,
 的
的 溶液中,
溶液中,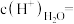
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】请按要求作答。
(1)写出下列物质在水溶液中的电离方程式。
①NH3·H2O:_______ 。
②NaHSO4:_______ 。
(2)下列盐溶液中能发生水解的用离子方程式 表示,不能发生水解的请写上“不发生水解”字样,并说明溶液的酸碱性:
①CuCl2_______ ,溶液呈_______ 性;
②K2SO4_______ ,溶液呈_______ 性;
(3)明矾可用于净水,原因是(用离子方程式表示):_______
(4)纯碱可代替洗涤剂洗涤餐具,原因是(用离子方程式表示)_______
(5)已知下列热化学方程式:
 ①
①
 ②
②
 ③
③
写出FeO(s)被CO(g)还原成Fe(s)和CO2(g)的热化学方程式:_______ 。
(1)写出下列物质在水溶液中的电离方程式。
①NH3·H2O:
②NaHSO4:
(2)下列盐溶液中能发生水解的
①CuCl2
②K2SO4
(3)明矾可用于净水,原因是(用离子方程式表示):
(4)纯碱可代替洗涤剂洗涤餐具,原因是(用离子方程式表示)
(5)已知下列热化学方程式:
 ①
① ②
② ③
③写出FeO(s)被CO(g)还原成Fe(s)和CO2(g)的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】“新冠”疫情期间,包头市第一中学响应迅速,及时制定了预防措施,在校园内建设大量便于师生清洗和消毒的设施,并在正式复课以前采用高效安全的含氯消毒剂“84”对学校教室及公共设施进行了大范围的消毒作业。已知“84”消毒液的主要成分为NaClO,该校无机化学兴趣小组通过pH试纸测定一份“84”消毒液的pH,观察到pH试纸先变蓝,与比色卡对照后判定pH为10,一段时间后试纸褪色。回答以下问题:
(1)请用离子方程式表示pH试纸变蓝的原因___________ ,pH试纸褪色的原因是___________ 。
(2)室温下,该消毒液中由水电离的氢氧根离子浓度为___________ 。
(3)该兴趣小组通过查阅资料得知:次氯酸为一元弱酸,其电离平衡体系中各成分的组成分数 [
[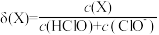 ,X为HClO或ClO-]与pH的关系如下图所示。则HClO的电离常数值为
,X为HClO或ClO-]与pH的关系如下图所示。则HClO的电离常数值为___________ 。

(4)在测量“84”消毒液值时,某同学发现久置于空气中的溶液,其pH会降低。请用化学方程式解释其原因___________ 。(已知:H2CO3的电离平衡常数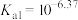 ,
,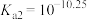 )
)
(1)请用离子方程式表示pH试纸变蓝的原因
(2)室温下,该消毒液中由水电离的氢氧根离子浓度为
(3)该兴趣小组通过查阅资料得知:次氯酸为一元弱酸,其电离平衡体系中各成分的组成分数
 [
[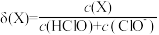 ,X为HClO或ClO-]与pH的关系如下图所示。则HClO的电离常数值为
,X为HClO或ClO-]与pH的关系如下图所示。则HClO的电离常数值为
(4)在测量“84”消毒液值时,某同学发现久置于空气中的溶液,其pH会降低。请用化学方程式解释其原因
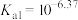 ,
,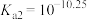 )
)
您最近一年使用:0次



