在25℃时,向50.00mL未知浓度的氨水中逐滴加入0.5mol·L-1的HCl溶液。滴定过程中,溶液的pOH[pOH=-lgc(OH-)]与滴入HCl溶液体积的关系如图所示,则下列说法中正确的是
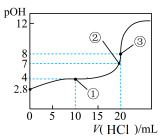
| A.图中②点所示溶液的导电能力弱于①点 |
| B.③点处水电离出的c(H+)=1×10-8mol·L-1 |
| C.图中点①所示溶液中,c(C1-)>c(NH4+)>c(OH-)>c(H+) |
| D.25℃时氨水的Kb约为5×10-5.6mol·L-1 |
2019·山东烟台·一模 查看更多[13]
四川省达州外国语学校2023-2024学年高二下学期3月月考化学试题2024年江西省宜春市第一中学高三下学期第三次模拟考试化学试卷四川省绵阳中学2023-2024学年高二下学期开学化学试题黑龙江省双鸭山市第一中学2023-2024学年高二下学期开学化学试题江西省宜春市上高中学2023-2024学年高二上学期第二次月考化学试卷 黑龙江省齐齐哈尔市2023-2024学年高二上学期1月期末化学试题山西省实验中学2023-2024学年高二上学期期中考试化学试题 湖南师范大学附属中学2022-2023学年高二上学期期末考试化学试题湖南省长沙市湖南师范大学附属中学2022-2023学年高二上学期期末考试化学试题安徽省定远县重点中学2020届高三下学期3月线上模拟考试理科综合化学试题备考突破2020高三化学专题强化集训——盐类水解中三大守恒的应用四川省泸县第五中学2020届高三上学期开学考试理综化学试题【市级联考】山东省烟台市、菏泽市2019届高三下学期5月高考适应性练习(一)理科综合化学试题
更新时间:2019-05-24 12:53:37
|
相似题推荐
单选题
|
困难
(0.15)
名校
【推荐1】25℃时,向 的二元酸
的二元酸 溶液中逐滴滴入
溶液中逐滴滴入 溶液,测得溶液的pH与lgY[Y代表
溶液,测得溶液的pH与lgY[Y代表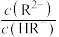 或
或 ]关系如图。下列相关结论错误的是
]关系如图。下列相关结论错误的是
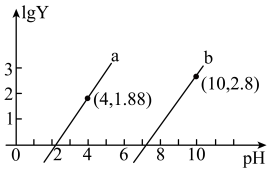
 的二元酸
的二元酸 溶液中逐滴滴入
溶液中逐滴滴入 溶液,测得溶液的pH与lgY[Y代表
溶液,测得溶液的pH与lgY[Y代表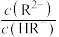 或
或 ]关系如图。下列相关结论错误的是
]关系如图。下列相关结论错误的是
A.曲线b表示pH与 的变化关系 的变化关系 |
B.25℃时, 的 的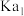 数量级为 数量级为 |
C.溶液的pH=7.2时, |
D.滴入20.00mLNaOH溶液时: |
您最近一年使用:0次
单选题
|
困难
(0.15)
名校
【推荐2】以0.10mol/L的氢氧化钠溶液滴定同浓度某一元酸HA的滴定曲线如图所示(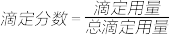 )。下列表述错误的是
)。下列表述错误的是
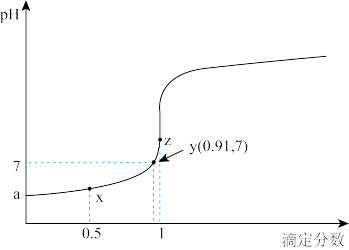
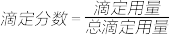 )。下列表述错误的是
)。下列表述错误的是
| A.z点后存在某点,溶液中的水的电离程度和y点的相同 |
| B.a约为3.5 |
C.z点处,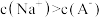 |
D.x点处的溶液中离子满足: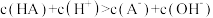 |
您最近一年使用:0次
单选题
|
困难
(0.15)
名校
【推荐3】25℃时,用浓度均为0.1mol·L-1的NaOH 溶液和盐酸分别滴定体积均为20mL,浓度均为0.1mol·L-1的HA溶液与BOH溶液。滴定过程中溶液的pH随滴加溶液的体积变化关系如图所示。下列说法中正确的是
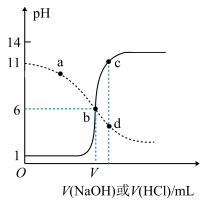

| A.HA为弱酸,BOH为强碱 |
| B.a点时,溶液中粒子浓度存在关系:c(B+)>c(Cl-)>c(OH-)>c(BOH) |
| C.b点时两种溶液中水的电离程度相同,且V=20 |
| D.c、d两点溶液混合后微粒之间存在关系:c(H+)= c(OH-)+c(BOH) |
您最近一年使用:0次
单选题
|
困难
(0.15)
名校
【推荐1】常温下,向某浓度的H2C2O4溶液中逐滴加入已知浓度的NaOH溶液,若pC表示溶液中溶质微粒的物质的量浓度的负对数,则所得溶液中pC(H2C2O4),pC(HC2O4-)、pC(C2O42-)与溶液pH的变化关系如图所示。已知:H2C2O4 HC2O4-+H+ Ka1;HC2O4-
HC2O4-+H+ Ka1;HC2O4- C2O42-+H+ Ka2。则下列说法正确的是
C2O42-+H+ Ka2。则下列说法正确的是

 HC2O4-+H+ Ka1;HC2O4-
HC2O4-+H+ Ka1;HC2O4- C2O42-+H+ Ka2。则下列说法正确的是
C2O42-+H+ Ka2。则下列说法正确的是
| A.当pH=3时,溶液中c(HC2O4-)<c(C2O42-)=c(H2C2O4) |
| B.pH由3增大到5.3的过程中,水的电离程度逐渐减小 |
| C.常温下,Ka2=10-5.3 |
| D.常下随着pH的增大:c2(HC2O4-)/[c(H2C2O4)c(C2O42-)] 的值先增大后减小 |
您最近一年使用:0次
单选题
|
困难
(0.15)
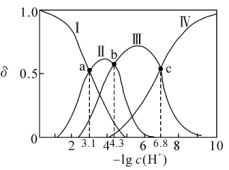
【推荐2】甘氨酸( )是一种最简单的氨基酸。其作为内源性抗氧化剂还原型谷胱甘肽的组成氨基酸,在机体发生严重应激时常需外源补充。如图为某兴趣小组通过实验获得在25℃下10mL
)是一种最简单的氨基酸。其作为内源性抗氧化剂还原型谷胱甘肽的组成氨基酸,在机体发生严重应激时常需外源补充。如图为某兴趣小组通过实验获得在25℃下10mL 甘氨酸溶液中各组分分布分数和pH的对应关系(通过HCl调节pH,溶液体积不变)
甘氨酸溶液中各组分分布分数和pH的对应关系(通过HCl调节pH,溶液体积不变)
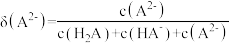
 )是一种最简单的氨基酸。其作为内源性抗氧化剂还原型谷胱甘肽的组成氨基酸,在机体发生严重应激时常需外源补充。如图为某兴趣小组通过实验获得在25℃下10mL
)是一种最简单的氨基酸。其作为内源性抗氧化剂还原型谷胱甘肽的组成氨基酸,在机体发生严重应激时常需外源补充。如图为某兴趣小组通过实验获得在25℃下10mL 甘氨酸溶液中各组分分布分数和pH的对应关系(通过HCl调节pH,溶液体积不变)
甘氨酸溶液中各组分分布分数和pH的对应关系(通过HCl调节pH,溶液体积不变)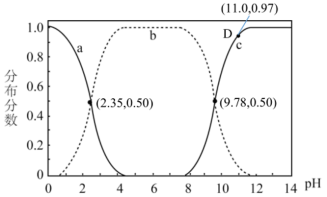
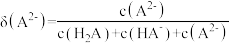
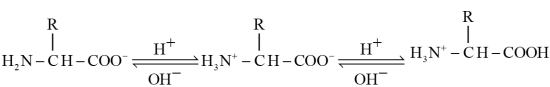
A.a为 ,b为 ,b为 ,c为 ,c为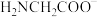 , , , , |
B. 时, 时, |
C.在D点溶液中: |
| D.该兴趣小组测得甘氨酸的pL=6.065,查表得知甘氨酸实际pL=5.97,造成误差的原因可能是因为原甘氨酸样品中有杂质,导致甘氨酸实际浓度偏低 |
您最近一年使用:0次
单选题
|
困难
(0.15)
名校
解题方法
【推荐3】已知室温下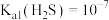 ,
,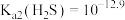 。通过下列实验探究含硫化合物的性质。
。通过下列实验探究含硫化合物的性质。
实验1:测得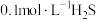 溶液pH=4.1
溶液pH=4.1
实验2:向10mL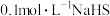 溶液中逐滴加入5mL水,用pH计监测过程中pH变化
溶液中逐滴加入5mL水,用pH计监测过程中pH变化
实验3:向10mL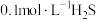 溶液中逐滴加入
溶液中逐滴加入 NaOH溶液,直至pH=7
NaOH溶液,直至pH=7
实验4:向5mL 中滴加10mL
中滴加10mL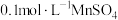 溶液,产生粉色沉淀,再加几滴
溶液,产生粉色沉淀,再加几滴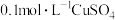 溶液,产生黑色沉淀
溶液,产生黑色沉淀
下列说法不正确的是
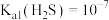 ,
,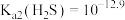 。通过下列实验探究含硫化合物的性质。
。通过下列实验探究含硫化合物的性质。实验1:测得
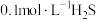 溶液pH=4.1
溶液pH=4.1实验2:向10mL
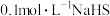 溶液中逐滴加入5mL水,用pH计监测过程中pH变化
溶液中逐滴加入5mL水,用pH计监测过程中pH变化实验3:向10mL
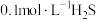 溶液中逐滴加入
溶液中逐滴加入 NaOH溶液,直至pH=7
NaOH溶液,直至pH=7实验4:向5mL
 中滴加10mL
中滴加10mL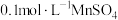 溶液,产生粉色沉淀,再加几滴
溶液,产生粉色沉淀,再加几滴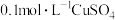 溶液,产生黑色沉淀
溶液,产生黑色沉淀下列说法不正确的是
A.由实验1可知: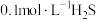 溶液中 溶液中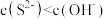 |
| B.实验2加水过程中,监测结果为溶液的pH不断减小 |
C.实验3所得溶液中存在: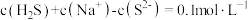 |
D.由实验4可知: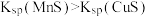 |
您最近一年使用:0次
单选题
|
困难
(0.15)
解题方法
【推荐1】某无色稀溶液X中,可能含有如表所列离子中的某几种。
取该溶液适量,向其中加入某试剂Y,产生沉淀的物质的量(n)与加入试剂体积(Y)的关系如图所示。下列说法正确的是
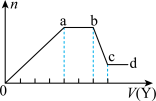
取该溶液适量,向其中加入某试剂Y,产生沉淀的物质的量(n)与加入试剂体积(Y)的关系如图所示。下列说法正确的是
| 阴离子 |  、 、 、[Al(OH)4]-、Cl- 、[Al(OH)4]-、Cl- |
| 阳离子 | Al3+、Fe3+、Mg2+、 、Na+ 、Na+ |

A.若Y是盐酸,则X中一定含有CO 、SiO 、SiO 、[Al(OH)4]-和NH4+ 、[Al(OH)4]-和NH4+ |
B.若Y是NaOH溶液,则X中一定含有A13+、Fe3+、 、Cl- 、Cl- |
C.若Y是NaOH溶液,则ab段发生反应的离子方程式为: +OH-=NH3↑+H2O +OH-=NH3↑+H2O |
D.若Y是NaOH溶液,则X中的Al3+、Mg2+、 物质的量之比为2:1:4 物质的量之比为2:1:4 |
您最近一年使用:0次
单选题
|
困难
(0.15)
解题方法
【推荐2】 时,用
时,用 溶液滴定柠檬酸(化学式为
溶液滴定柠檬酸(化学式为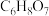 ,结构简式为
,结构简式为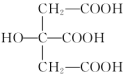 )溶液,溶液中
)溶液,溶液中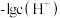 与
与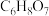 、
、 、
、 、
、 的分布系数
的分布系数 的关系如图所示[如
的关系如图所示[如 的分布系数
的分布系数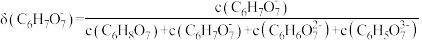 ]。下列说法错误的是
]。下列说法错误的是
 时,用
时,用 溶液滴定柠檬酸(化学式为
溶液滴定柠檬酸(化学式为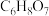 ,结构简式为
,结构简式为 )溶液,溶液中
)溶液,溶液中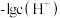 与
与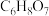 、
、 、
、 、
、 的分布系数
的分布系数 的关系如图所示[如
的关系如图所示[如 的分布系数
的分布系数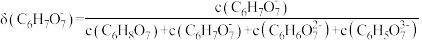 ]。下列说法错误的是
]。下列说法错误的是
A.柠檬酸为三元弱酸, 的数量级为 的数量级为 |
B.b点对应溶液中,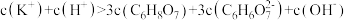 |
C.溶液中水的电离程度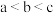 |
D.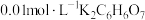 溶液中 溶液中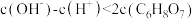 |
您最近一年使用:0次
单选题
|
困难
(0.15)
名校
解题方法
【推荐3】在25℃时,将1.0 L w mol·L-1 CH3COOH 溶液与0.1 mol NaOH固体混合,充分反应。向混合液中加入CH3COOH或CH3COONa固体(忽略体积和温度变化),溶液pH随加入CH3COOH或CH3COONa固体的物质的量的变化关系如图所示。下列叙述正确的是
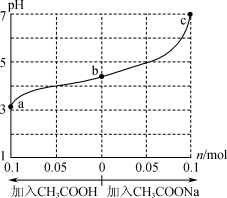

| A.b点混合液中c(H+)≥ c(OH-) + c(CH3COO-) |
B.加入CH3COOH过程中,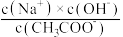 增大 增大 |
C.25℃时,CH3COOH的电离平衡常数 Ka= 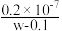 mol·L-1 mol·L-1 |
| D.a、b、c对应的混合液中,水的电离程度由大到小的顺序是c>a>b |
您最近一年使用:0次
单选题
|
困难
(0.15)
解题方法
【推荐1】25℃下,向20 mL 0.1 mol·L-1H2A溶液中滴加0.1 mol·L-1NaOH溶液,有关粒子物质的量的变化如图所示。下列有关说法正确的是
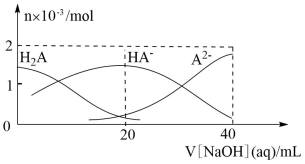

| A.H2A属于强酸 |
| B.c(HA-)/c(H2A)随着V[NaOH(aq)]的增大而减小 |
| C.V[NaOH(aq)]=20mL时,溶液中存在关系:c(HA-)+ c(A2-)+ c(H2A)=0.1mol/L |
| D.V[NaOH(aq)]=20mL时,溶液中存在关系:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) |
您最近一年使用:0次
单选题
|
困难
(0.15)
【推荐2】 ,向一定浓度的
,向一定浓度的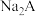 溶液中逐滴加入盐酸,实验测得溶液
溶液中逐滴加入盐酸,实验测得溶液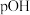 与
与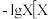 为
为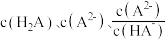 ]变化关系如图所示。下列说法错误的是
]变化关系如图所示。下列说法错误的是
 ,向一定浓度的
,向一定浓度的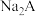 溶液中逐滴加入盐酸,实验测得溶液
溶液中逐滴加入盐酸,实验测得溶液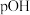 与
与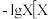 为
为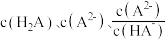 ]变化关系如图所示。下列说法错误的是
]变化关系如图所示。下列说法错误的是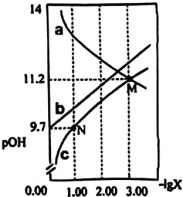
A.曲线 表示 表示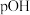 与 与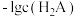 的变化关系 的变化关系 |
B.当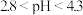 时, 时, |
C.常温下,反应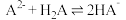 的平衡常数为 的平衡常数为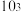 |
D. 点溶液中, 点溶液中,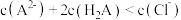 |
您最近一年使用:0次
单选题
|
困难
(0.15)
【推荐3】25℃时,将1.0L cmol·L-1CH3COOH溶液与0.1molNaOH固体混合,使之充分反应。然后向该混合物中加入CH3COOH或CH3COONa固体(忽略体积变化和温度变化),加入的量与溶液pH的变化如下图所示。下列叙述不正确 的是


| A.水的电离程度:c>b>a |
B.该温度下,醋酸的电离平衡常数Ka= |
| C.a点对应的混合溶液中,c(Na+)>c(CH3COOH)>c(OH-) |
| D.当混合溶液呈中性时,c(Na+)=c(CH3COO-)>c(H+)=c(OH-) |
您最近一年使用:0次



