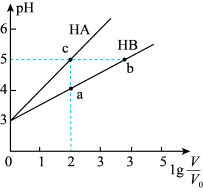
下判说法正确的是
| A.常温下,c(Cl-)均为0.1mol/LNaCl溶液与NH4Cl溶液, pH相等 |
| B.常温下,浓度均为0.1mol/L的CH3COOH溶液与HCl溶液,导电能力相同 |
| C.常温下,HCl溶液中c(Cl-)与CH3COOH溶液中c(CH3COO-)相等,两溶液的pH相等 |
| D.室温下,等物质的量浓度的CH3COOH溶液和NaOH溶液等体积混合,所得溶液呈中性 |
更新时间:2019-04-04 11:12:37
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的个数是
①pH=6的溶液一定是酸性溶液
②25℃时,水溶液中水电离出的c(H+)和水电离出的c(OH-)的乘积一定等于10-14
③0.2mol/L氢硫酸溶液加水稀释,电离程度增大,c(H+)一定增大
④温度保持不变,向水中加入钠盐对水的电离一定没有影响
⑤强电解质熔化时都完全电离,弱电解质在水溶液中部分电离
⑥离子化合物都是强电解质,弱电解质都是共价化合物
⑦室温下用干燥、洁净的玻璃棒蘸取氯水,滴在pH试纸上,测出其pH<7
⑧弱酸电离平衡向右移动,其电离平衡常数一定增大
⑨室温时,0.1mol/L某一元酸HA溶液的pH=4,则该酸的电离度为0.1%
⑩酸度的计算公式是AG=lg[ ],常温下0.1mol/L盐酸的AG=12
],常温下0.1mol/L盐酸的AG=12
①pH=6的溶液一定是酸性溶液
②25℃时,水溶液中水电离出的c(H+)和水电离出的c(OH-)的乘积一定等于10-14
③0.2mol/L氢硫酸溶液加水稀释,电离程度增大,c(H+)一定增大
④温度保持不变,向水中加入钠盐对水的电离一定没有影响
⑤强电解质熔化时都完全电离,弱电解质在水溶液中部分电离
⑥离子化合物都是强电解质,弱电解质都是共价化合物
⑦室温下用干燥、洁净的玻璃棒蘸取氯水,滴在pH试纸上,测出其pH<7
⑧弱酸电离平衡向右移动,其电离平衡常数一定增大
⑨室温时,0.1mol/L某一元酸HA溶液的pH=4,则该酸的电离度为0.1%
⑩酸度的计算公式是AG=lg[
 ],常温下0.1mol/L盐酸的AG=12
],常温下0.1mol/L盐酸的AG=12| A.3 | B.2 | C.1 | D.0 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】常温下,0.1mol•L-1一元酸HA溶液中c(OH-)/c(H+)=1×10-6,下列叙述正确的是( )
| A.该溶液中水的离子积常数为1×10−12 |
| B.该一元酸溶液的pH=1 |
| C.该溶液中由水电离出的c(H+)=1×10−6mol•L-1 |
| D.向该溶液中加入一定量NaA晶体或加水稀释,溶液中c(OH-)均增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】c(H+)相等的盐酸(甲)和醋酸(乙),分别与锌反应,若最后锌已全部溶解且放出气体一样多,则下列说法正确的是
| A.反应开始时的速率:甲>乙 |
| B.反应结束时的c(H+):甲=乙 |
| C.反应开始时的酸的物质的量浓度:甲=乙 |
| D.反应所需时间:甲>乙 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是
| A.在100℃时,pH为6的纯水呈中性(100℃时,Kw=1×10-12) |
| B.加热MgCl2•6H2O能得到纯净的无水氯化镁 |
| C.将1×10-6mol/L盐酸稀释至1000mL,所得溶液的pH为9 |
| D.中和浓度与体积均相同的NaOH溶液和氨水,消耗H2SO4的量前者大于后者 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列实验过程可以达到实验目的的是
实验目的 | 实验过程 | |
| A | 根据褪色时间来研究浓度对反应速率的影响 | 往2支试管中分别加入同体积、等浓度的草酸溶液,再分别加入同体积、不同浓度的KMnO4溶液 |
| B | 比较HClO和CH3COOH酸性的强弱 | 常温下,用pH计分别测定等物质的量浓度的NaClO溶液和CH3COONa溶液的pH |
| C | 证明HA是弱酸 | 等体积、浓度均为0.1mol/L的HA和HB两种酸分别与足量Zn反应,HA放出的H2多 |
| D | 制备Al2O3固体 | 将NaAlO2溶液蒸干并灼烧 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】硫及其化合物在生产生活中具有广泛应用。由自然界的硫磺和金属硫化物矿通过化学反应可得到 ,
, 催化氧化生成
催化氧化生成 ,其热化学方程式为
,其热化学方程式为
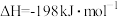 。燃煤、金属冶炼和硫酸生产等产生的尾气中都含有
。燃煤、金属冶炼和硫酸生产等产生的尾气中都含有 ,用
,用 等碱性溶液吸收尾气中的
等碱性溶液吸收尾气中的 ,可得到
,可得到 、
、 等化工产品。下列硫及其化合物的性质与用途具有对应关系的是
等化工产品。下列硫及其化合物的性质与用途具有对应关系的是
 ,
, 催化氧化生成
催化氧化生成 ,其热化学方程式为
,其热化学方程式为
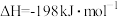 。燃煤、金属冶炼和硫酸生产等产生的尾气中都含有
。燃煤、金属冶炼和硫酸生产等产生的尾气中都含有 ,用
,用 等碱性溶液吸收尾气中的
等碱性溶液吸收尾气中的 ,可得到
,可得到 、
、 等化工产品。下列硫及其化合物的性质与用途具有对应关系的是
等化工产品。下列硫及其化合物的性质与用途具有对应关系的是A. 有氧化性,可用于生产 有氧化性,可用于生产 | B. 溶液显碱性,可用于吸收少量 溶液显碱性,可用于吸收少量 |
C. 有还原性,可用于纸浆漂白 有还原性,可用于纸浆漂白 | D.浓 有脱水性,可用作干燥剂 有脱水性,可用作干燥剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】25 ℃时,相同物质的量浓度的下列溶液:①NaCl 、②NaOH、③H2SO4 、④(NH4)2SO4、⑤Ba(OH)2、⑥CH3COONa、⑦NH4Cl、⑧HCl,其中pH值按由大到小顺序排列的一组是( )
| A.⑤②①⑥⑦④③⑧ | B.⑤②⑥①⑦④⑧③ |
| C.③⑧④⑦①⑥②⑤ | D.⑤②①③⑧⑦④⑥ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】室温下进行下列实验,根据实验操作和现象所得到的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 加热盛有少量NH4HCO3固体的试管,试管口处润湿的红色石蕊试纸变蓝 | NH4HCO3显碱性 |
| B | 相同条件下,分别测量0.1 mol·L-1和0.01 mol·L-1醋酸溶液的导电性,前者的导电性强 | 醋酸浓度越大,电离程度越大 |
| C | 向3 mL KI溶液中滴加几滴溴水,振荡,再滴加1 mL淀粉溶液,溶液显蓝色 | Br2的氧化性比I2的强 |
| D | 用pH试纸测得:CH3COONa溶液的pH约为9,NaNO2溶液的pH约为8 | HNO2电离出H+的能力比CH3COOH的强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温条件下,下列有关电解质溶液的说法正确的是
| A.加水稀释盐酸时,溶液中所有离子的浓度均减小 |
| B.将10mL0.01mol/LNaOH溶液与同浓度的HA溶液混合,若混合后溶液呈中性,则消耗的HA的体积V≤10mL |
C.等浓度的①NH4Cl溶液②NH4HSO4溶液③NH4HCO3溶液中的c( )相等 )相等 |
D.室温下,向0.1mol/L氨水中加少量NH4Cl固体,溶液中 减小 减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】室温下,下列实验的有关说法不正确 的是
A.除去 溶液中的少量 溶液中的少量 ,可选用 ,可选用 调节溶液的pH使 调节溶液的pH使 转化为沉淀 转化为沉淀 |
B.向 溶液中加入等浓度、等体积的氨水后,溶液显碱性: 溶液中加入等浓度、等体积的氨水后,溶液显碱性: |
C.向 稀溶液中加入少量冰醋酸,可以使 稀溶液中加入少量冰醋酸,可以使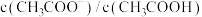 减小 减小 |
D.向 溶液中加入水,可以促进 溶液中加入水,可以促进 的水解平衡正移,使溶液pH增大 的水解平衡正移,使溶液pH增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】室温时,向20 mL 0.1 mol·L-1的醋酸溶液中不断滴入0.1 mol·L-1的NaOH溶液,溶液的pH变化曲线如图所示。在滴定过程中,关于溶液中离子浓度大小关系的描述不正确 的是


| A.a点时:c( CH3COOH)>c( Na+)>c( CH3COO-)>c( H+)>c( OH -) |
| B.b点时:c( Na+) =c( CH3COO-)>c(H+)=c( OH-) |
| C.c点时:c(OH-)=c(CH3COOH) +c(H+) |
| D.d点时:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
您最近一年使用:0次

 的变化如图所示。下列说法中错误的是
的变化如图所示。下列说法中错误的是