某温度下,在固定容积的密闭容器中,可逆反应A(g)+ B(g) 2C(g)达到平衡时,各物质的物质的量之比为n(A)∶n(B)∶n(C)=2∶2∶1。保持温度不变,以2∶2∶1的物质的量之比再充入A、B、C,则下列说法错误的是( )
2C(g)达到平衡时,各物质的物质的量之比为n(A)∶n(B)∶n(C)=2∶2∶1。保持温度不变,以2∶2∶1的物质的量之比再充入A、B、C,则下列说法错误的是( )
 2C(g)达到平衡时,各物质的物质的量之比为n(A)∶n(B)∶n(C)=2∶2∶1。保持温度不变,以2∶2∶1的物质的量之比再充入A、B、C,则下列说法错误的是( )
2C(g)达到平衡时,各物质的物质的量之比为n(A)∶n(B)∶n(C)=2∶2∶1。保持温度不变,以2∶2∶1的物质的量之比再充入A、B、C,则下列说法错误的是( )| A.平衡不移动 |
| B.相当长时间后,n(A)∶n(B)∶n(C)仍为2∶2∶1 |
| C.再达平衡时,C的体积分数增大 |
| D.相当长时间后,正反应速率增大,逆反应速率也增大 |
更新时间:2019-12-13 18:04:36
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列有关化学反应速率的说法中,正确的是
| A.汽车尾气中的NO和CO反应生成N2和CO2的速率很小,使用催化剂可提高化学反应的速率 |
| B.等质量的锌粉和锌片与相同体积、相同物质的量浓度的盐酸反应,反应速率相等 |
| C.某反应是一个放热反应,所以升高温度,逆反应速率增大,正反应速率减小 |
| D.用铁片与硫酸反应制取氢气时,用质量分数为98%的浓硫酸可以提高产生氢气的速率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】t℃时,在一个体积为2L密闭容器中加入反应物A、B,发生如下反应: 。反应过程中的部分数据如下表所示,下列说法正确的是
。反应过程中的部分数据如下表所示,下列说法正确的是
 。反应过程中的部分数据如下表所示,下列说法正确的是
。反应过程中的部分数据如下表所示,下列说法正确的是| 物质 | 起始 | 2分钟 | 4分钟 | 6分钟 |
| A | 2mol | 1.2mol | ||
| B | 6mol | 3.0mol | ||
| C | 0mol | 4.5mol |
| A.前2分钟内,A的反应速率为0.2mol/(L•min) |
| B.升高温度,正反应速率增大,逆反应速率减小 |
| C.4分钟时,反应已达到平衡状态 |
| D.混合气体的压强不变,不能说明该反应达到了化学平衡状态 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知一定温度和压强下,N2(g)和H2 (g)反应生成2molNH3(g),放出92.4kJ热量。在同温同压下向密闭容器中通入1mol N2和3mol H2,达平衡时放出热量为Q1kJ;向另一体积相同的容器中通入0.5molN2和1.5molH2,相同温度下达到平衡时放出热量为Q2kJ。则下列叙述正确的是
| A.2Q2<Q1<92.4kJ | B.2Q2=Q1=92.4kJ |
| C.2Q2>Q1=92.4kJ | D.2Q2=Q1<92.4kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
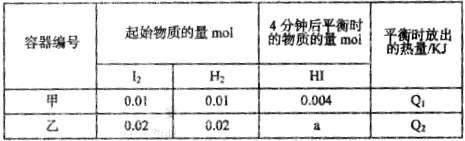
【推荐2】恒温下,在容积为2升的甲、乙两个恒容密闭容器中分别充入H2和I2发生可逆反应:H2 (g) +I2(g)  2HI(g) △H="-Q" kJ/mol,实验时有关数据如表:
2HI(g) △H="-Q" kJ/mol,实验时有关数据如表:
下列判断正确的
 2HI(g) △H="-Q" kJ/mol,实验时有关数据如表:
2HI(g) △H="-Q" kJ/mol,实验时有关数据如表:
下列判断正确的
| A.甲容器中,4分钟内氢气的反应速率为5.0×10-4rmol/(L·min) |
| B.平衡时,放出的热量: Q1=4.0×10-3Q kJ |
| C.平衡后,a=8.0×10-3mol,故乙中HI的质量分数比甲中高 |
| D.该温度下,该反应的平衡常数K=0.25 |
您最近一年使用:0次
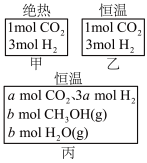
【推荐3】在初始温度为500℃、容积恒定为10L的三个密闭容器中,按图所示投入原料,发生反应:CO2(g)+3H2(g)  CH3OH(g)+H2O(g) △H=-25kJ/mol。已知乙达到平衡时气体的压强为开始时的0.55倍;乙、丙中初始反应方向不同,平衡后对应各组分的体积分数相等。下列分析不正确的是
CH3OH(g)+H2O(g) △H=-25kJ/mol。已知乙达到平衡时气体的压强为开始时的0.55倍;乙、丙中初始反应方向不同,平衡后对应各组分的体积分数相等。下列分析不正确的是
 CH3OH(g)+H2O(g) △H=-25kJ/mol。已知乙达到平衡时气体的压强为开始时的0.55倍;乙、丙中初始反应方向不同,平衡后对应各组分的体积分数相等。下列分析不正确的是
CH3OH(g)+H2O(g) △H=-25kJ/mol。已知乙达到平衡时气体的压强为开始时的0.55倍;乙、丙中初始反应方向不同,平衡后对应各组分的体积分数相等。下列分析不正确的是
| A.刚开始反应时速率:甲=乙 |
| B.平衡后反应放热:甲<乙 |
| C.500℃时乙容器中反应的平衡常数:K=3×102 |
| D.若a≠0,则0.9<b<l |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列实验事实可以用平衡移动原理解释的是
| A.“NO2”球浸泡在热水中,颜色变深 |
B.H2(g)+ I2 (g)  2HI(g),加压后颜色变深 2HI(g),加压后颜色变深 |
| C.过量铁和稀硝酸反应,溶液变成浅绿色 |
| D.合成氨工业中使用铁触媒作催化剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在密闭容器中,加入一定量的A、B混合气体,发生反应:xA(g) + yB(g) zC(g),平衡时测得A的浓度为0.80mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度为0.40mol/L,下列有关判断正确的是
zC(g),平衡时测得A的浓度为0.80mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度为0.40mol/L,下列有关判断正确的是
 zC(g),平衡时测得A的浓度为0.80mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度为0.40mol/L,下列有关判断正确的是
zC(g),平衡时测得A的浓度为0.80mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度为0.40mol/L,下列有关判断正确的是| A.x + y < z | B.平衡向正反应方向移动 |
| C.B的转化率降低 | D.C的产率不变 |
您最近一年使用:0次

 为催化剂的光热化学循环分解
为催化剂的光热化学循环分解 反应为温室气体减排提供了一个新途径,该反应的机理如下图所示,
反应为温室气体减排提供了一个新途径,该反应的机理如下图所示,
 的相对分子质量,应尽量在高温低压条件下测定
的相对分子质量,应尽量在高温低压条件下测定 与稀硫酸反应,加入适量硫酸铜晶体可以加快氢气的生成速率
与稀硫酸反应,加入适量硫酸铜晶体可以加快氢气的生成速率

