下列有关电解质溶液的说法正确的是
| A.在蒸馏水中滴加浓H2SO4,Kw不变 |
| B.常温下,等体积的盐酸和甲酸溶液相比,前者的导电能力强 |
| C.相同温度时,1mol/L醋酸与0.5mol/L的醋酸中,c(H+)之比为2:1 |
| D.NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度不相同 |
19-20高二上·云南昆明·期中 查看更多[2]
更新时间:2019-12-26 21:16:04
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】常温下,向新制氯水中滴加NaOH溶液,溶液中水电离出的 浓度与NaOH溶液体积之间的关系如图所示。下列推断
浓度与NaOH溶液体积之间的关系如图所示。下列推断不正确 的是

 浓度与NaOH溶液体积之间的关系如图所示。下列推断
浓度与NaOH溶液体积之间的关系如图所示。下列推断
| A.E、F点溶液的pH分别为3和7 |
B.F点对应的溶液中: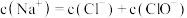 |
C.G点对应的溶液中: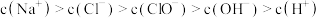 |
D.F~H点对应的溶液中, 为定值 为定值 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】常温下,Ka(HClO)=3×10-3,先向水中缓缓通入Cl2后滴入NaOH溶液,过程中水电离出的c(H+)水如图所示,下列相关离子浓度的关系判断正确的是


A.M点: |
| B.N点:c(Na+) =2c(ClO-) +c(HClO) |
| C.P点:c(Na+)=2c(ClO-)=2c(Cl-) |
| D.Q点:c(Na+)>c(Cl-)>c(ClO-) >c(H+)>c(ОH-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】下列说法不正确的是( )
| A.将pH=4的某酸稀释10倍,测得其pH<5,则该酸为弱酸 |
| B.相同温度相同pH的CH3COONa、NaAlO2和NaHCO3三种溶液的物质的量浓度大小为:c(NaAlO2)<c(NaHCO3)<c(CH3COONa) |
| C.0.1mol/L的NaA溶液和0.1mol/L的HA溶液等体积混合pH=4.75,则溶液:c(HA)+2c(H+)=2c(OH-)+c(A-) |
| D.向NH4HSO4溶液中滴加NaOH溶液至中性,所得混合液:c(Na+)>c(NH4+)>c(SO42-)>c(OH-)=c(H+) |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】25℃时,0.10L某二元弱酸 用1.00
用1.00
 溶液调节其
溶液调节其 ,溶液中
,溶液中 、
、 和
和 的物质的量浓度及溶液
的物质的量浓度及溶液 与所加
与所加 溶液体积的变化关系如图所示,下列说法正确的是
溶液体积的变化关系如图所示,下列说法正确的是

 用1.00
用1.00
 溶液调节其
溶液调节其 ,溶液中
,溶液中 、
、 和
和 的物质的量浓度及溶液
的物质的量浓度及溶液 与所加
与所加 溶液体积的变化关系如图所示,下列说法正确的是
溶液体积的变化关系如图所示,下列说法正确的是
A.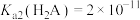 |
B.在Z点时,由水电离出的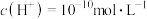 |
C.在Y点时,对应溶液中: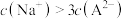 |
D.0.1  溶液中: 溶液中: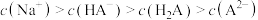 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】常温时,向10 mL0.1 mo/LHX溶液中逐滴加入0.1 mol/L的氨水,其导电能力、pH与V(NH3·H2O)的关系变化如图所示(假设反应过程中温度不变,下列说法不正确的是
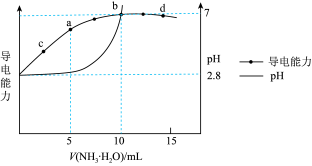

| A.水的电离程度: b>d,a>c | B.Kb(NH3·H2O)=K(HX)=10-4.6 |
| C.d点所得溶液的pH<7 | D.a点对应的溶液中:c(HX)+2c(H+)=c(X-)+2c(NH3·H2O)+2c(OH-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】下列说法不正确的是
| A.25℃时,pH="11" NaOH溶液和pH="3" CH3COOH混合,若溶液显酸性,则所得溶液中离子浓度可能为c(CH3COO-)>c(H+)>c(Na+)>c(OH-) |
| B.取c(H+)=0.01mol/L的盐酸和醋酸各100mL,分别稀释2倍后,再分别加入0.03g锌粉,在相同条件下充分反应,醋酸与锌反应的速率大 |
| C.25℃时,某溶液中由水电离出的c(H+)=10-a mol/L,若a>7时,该溶液pH一定为14-a |
| D.含等物质的量的NaHC2O4和Na2C2O4的溶液中存在:2c(Na+)=3[c(HC2O4-)+c(C2O42-)+c(H2C2O4)] |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】已知亚磷酸(H3PO3)是二元弱酸,298 K时的电离常数分别为Ka1=10-1.4,Ka2=10-6.1.298 K时,向1 L 0.2 mol·L-1 NaH2PO3溶液中通入HCl气体,溶液的pH与通入HCl物质的量的关系如图所示。下列说法正确的是
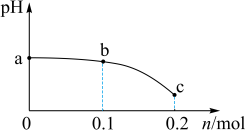

A.a点溶液中:c(H2PO )>c(HPO )>c(HPO )>c(H+)>c(H3PO3) )>c(H+)>c(H3PO3) |
| B.室温下,b点溶液的pH>7 |
C.c点溶液中:c(Cl-)=c(H2PO )+c(H3PO3)+c(HPO )+c(H3PO3)+c(HPO ) ) |
D.NaH2PO3溶液中存在的含P的离子有H2PO 、HPO 、HPO 、PO 、PO |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】常温下,部分弱酸的电离平衡常数如下表所示。下列说法正确的是
| 弱酸 | HCOOH | HCN |
| 电离平衡常数 | Ka=1.77×10-4 | Ka=5×10-10 |
| A.0.1 mol·L-1的NaCN溶液:c(Na+)>c(HCN)>c(CN-)>c(H+) |
| B.pH=8的HCOONa溶液:c(Na+)-c(HCOO-)=9.9×10-7 mol·L-1 |
| C.0.1 mol·L-1 HCOONa溶液甲和0.1 mol·L-1 NaCN溶液乙:c(H+)甲<c(H+)乙 |
| D.0.1 mol·L-1 NaCN溶液和0.1 mol·L-1的HCOONa溶液等体积混合:2c(Na+)=c(CN-)+c(HCOO-) |
您最近一年使用:0次

 )+2c(
)+2c(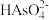 )+3c(
)+3c( )+c(OH-)
)+c(OH-)

