Ⅰ.已知NO(g)+CO2(g)=NO2(g)+CO(g) ΔH1;2CO(g)+O2(g)=2CO2(g) ΔH2
则2NO2(g) 2NO(g)+O2(g)的反应热ΔH=
2NO(g)+O2(g)的反应热ΔH=___ (用含△H1,△H2的代数式表示)。
Ⅱ.某条件下,在2L密闭容器中发生如下反应:2NO2(g) 2NO(g)+O2(g) ΔH,在三种不同条件下进行,其中实验Ⅰ、Ⅱ都在800℃,实验Ⅲ在850℃,NO、O2的起始浓度都为0,NO2的浓度(mol·L-1)随时间(min)的变化如图所示。请回答下列问题:
2NO(g)+O2(g) ΔH,在三种不同条件下进行,其中实验Ⅰ、Ⅱ都在800℃,实验Ⅲ在850℃,NO、O2的起始浓度都为0,NO2的浓度(mol·L-1)随时间(min)的变化如图所示。请回答下列问题:
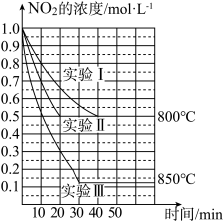
(1)实验Ⅱ隐含的反应条件是___ 。
(2)实验Ⅱ中,从反应开始至达到平衡,用氧气浓度变化表示的化学反应速率为___ 。
(3)800℃时,该反应的平衡常数K=___ 。该反应是___ (填“吸”或“放”)热反应。
(4)若实验Ⅰ中达到平衡后,再向密闭容器中通入2mol由物质的量之比为1:1组成的NO2与NO混合气体(保持温度不变),此时正反应方向速率___ 逆反应方向速率(填“大于”或“等于”或“小于”)。
(5)若实验Ⅰ中达到平衡后,再向密闭容器中再通入一定量的NO2(保持温度不变),一段时间后达到新平衡,则新平衡与原平衡相比混合气体中NO2的体积分数___ (填“增大”或“不变”或“减小”)。
(6)NO2、NO是重要的大气污染物,近年来人们利用NH3在一定条件下与之反应而将其转化为无害的参与大气循环的物质,如:8NH3+6NO2 7N2+12H2O。该反应中氧化产物与还原产物物质的量的比为:
7N2+12H2O。该反应中氧化产物与还原产物物质的量的比为:___ 。
则2NO2(g)
 2NO(g)+O2(g)的反应热ΔH=
2NO(g)+O2(g)的反应热ΔH=Ⅱ.某条件下,在2L密闭容器中发生如下反应:2NO2(g)
 2NO(g)+O2(g) ΔH,在三种不同条件下进行,其中实验Ⅰ、Ⅱ都在800℃,实验Ⅲ在850℃,NO、O2的起始浓度都为0,NO2的浓度(mol·L-1)随时间(min)的变化如图所示。请回答下列问题:
2NO(g)+O2(g) ΔH,在三种不同条件下进行,其中实验Ⅰ、Ⅱ都在800℃,实验Ⅲ在850℃,NO、O2的起始浓度都为0,NO2的浓度(mol·L-1)随时间(min)的变化如图所示。请回答下列问题:
(1)实验Ⅱ隐含的反应条件是
(2)实验Ⅱ中,从反应开始至达到平衡,用氧气浓度变化表示的化学反应速率为
(3)800℃时,该反应的平衡常数K=
(4)若实验Ⅰ中达到平衡后,再向密闭容器中通入2mol由物质的量之比为1:1组成的NO2与NO混合气体(保持温度不变),此时正反应方向速率
(5)若实验Ⅰ中达到平衡后,再向密闭容器中再通入一定量的NO2(保持温度不变),一段时间后达到新平衡,则新平衡与原平衡相比混合气体中NO2的体积分数
(6)NO2、NO是重要的大气污染物,近年来人们利用NH3在一定条件下与之反应而将其转化为无害的参与大气循环的物质,如:8NH3+6NO2
 7N2+12H2O。该反应中氧化产物与还原产物物质的量的比为:
7N2+12H2O。该反应中氧化产物与还原产物物质的量的比为:
更新时间:2020-01-16 16:31:22
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】海洋是生命的摇篮,海水不仅是宝贵的水资源,而且蕴藏着丰富的化学资源。从海水中提取一些重要的化工产品的工艺流程如图所示。

根据上述流程图回答下列问题:
(1)海水淡化处理的方法有蒸馏法、冷冻法、_____________ 。(写出1种即可)
(2)写出反应①化学反应方程式_______________________________________ 。
(3)标准状况下22.4 L Cl2气体发生反应②,转移的电子数是________ NA。
(4)反应③中硫酸酸化可提高Cl2的利用率,理由是____________________________ 。
(5)过程③到过程⑤的变化为“Br-→Br2→Br-→Br2”,其目的是_______________ 。
(6)浓缩氯化镁溶液后冷却可以得到MgCl2﹒6H2O,该晶体受热时会发生如下变化:MgCl2﹒6H2O== Mg(OH)Cl + HCl↑+ 5H2O。则,从溶液制备无水晶体的“操作a”可以采取的措施是__________________________________________ 。

根据上述流程图回答下列问题:
(1)海水淡化处理的方法有蒸馏法、冷冻法、
(2)写出反应①化学反应方程式
(3)标准状况下22.4 L Cl2气体发生反应②,转移的电子数是
(4)反应③中硫酸酸化可提高Cl2的利用率,理由是
(5)过程③到过程⑤的变化为“Br-→Br2→Br-→Br2”,其目的是
(6)浓缩氯化镁溶液后冷却可以得到MgCl2﹒6H2O,该晶体受热时会发生如下变化:MgCl2﹒6H2O== Mg(OH)Cl + HCl↑+ 5H2O。则,从溶液制备无水晶体的“操作a”可以采取的措施是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】焦亚硫酸钠(Na2S2O5)常用作食品漂白剂。其制备工艺流程如下:

已知:反应II包含2NaHSO3=Na2S2O5+ H2O等多步反应。
(1)反应I的总化学方程式为,反应I进行时应先通入的气体是,反应I产生的NH4Cl可用作________________。
(2)灼烧时发生反应的化学方程式为,若灼烧时生成SO21.12×l06L(标准状况下),则转移电子____mol。
(3)已知Na2S2O5与稀硫酸反应放出SO2,其离子方程式为_______________。
(4)副产品X的化学式是________________,在上述流程中可循环使用的物质是___________________。
(5)为了减少产品Na2S2O5中杂质含量,需控制反应II中气体与固体的物质的量之比约为,检验产品中含有碳酸钠杂质所需试剂________________。(填编号)。
①澄清石灰水 ②饱和碳酸氢钠溶液 ③氢氧化钠
④酸性高锰酸钾 ⑤稀硫酸

已知:反应II包含2NaHSO3=Na2S2O5+ H2O等多步反应。
(1)反应I的总化学方程式为,反应I进行时应先通入的气体是,反应I产生的NH4Cl可用作________________。
(2)灼烧时发生反应的化学方程式为,若灼烧时生成SO21.12×l06L(标准状况下),则转移电子____mol。
(3)已知Na2S2O5与稀硫酸反应放出SO2,其离子方程式为_______________。
(4)副产品X的化学式是________________,在上述流程中可循环使用的物质是___________________。
(5)为了减少产品Na2S2O5中杂质含量,需控制反应II中气体与固体的物质的量之比约为,检验产品中含有碳酸钠杂质所需试剂________________。(填编号)。
①澄清石灰水 ②饱和碳酸氢钠溶液 ③氢氧化钠
④酸性高锰酸钾 ⑤稀硫酸
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】短周期主族元素A、B、C、D、E、F的原子序数依次增大,它们的原子核外电子层之和为13;B的化合物种类繁多,数目庞大;C、D是空气中含量最多的两种元素;D、E形成的单质在不同条件下可以生成两种不同的离子化合物;F是同周期元素中原子半径最小的。
(1)A、D以1 :1形成化合物的电子式为____ 。A、C形成最简单化合物的空间构型为____ 。B可形成晶体类型不同的多种单质,它们互称为____ 。
(2)A、C形成的某化合物的相对分子质量与D2的相等,写出该化合物与足量盐酸反应的离子方程式:__________ 。
(3)A、C、F形成的化合物是一种常见的化学肥料,该物质的水溶液中离子浓度的大小顺序为____ 。
(4)C、D两元素可组成价态相同且能相互转变的化合物,它们是____ (填化学式)。
(5)F2与FD2均可用于自来水的杀菌消毒,若它们在杀菌过程中的还原产物相同,则消毒等体积的自来水,所需F2和FD2的物质的量之比为____ 。
(1)A、D以1 :1形成化合物的电子式为
(2)A、C形成的某化合物的相对分子质量与D2的相等,写出该化合物与足量盐酸反应的离子方程式:
(3)A、C、F形成的化合物是一种常见的化学肥料,该物质的水溶液中离子浓度的大小顺序为
(4)C、D两元素可组成价态相同且能相互转变的化合物,它们是
(5)F2与FD2均可用于自来水的杀菌消毒,若它们在杀菌过程中的还原产物相同,则消毒等体积的自来水,所需F2和FD2的物质的量之比为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】(1)已知:
甲醇脱水反应 2CH3OH(g)═CH3OCH3(g)+H2O(g) △H1=-23.9kJ•mol-1
甲醇制烯烃反应 2CH3OH(g) ═C2H4 (g)+2H2O(g) △H2=-29.1kJ•mol-1
乙醇异构化反应 C2H5OH (g)═CH3OCH3(g) △H3=+50.7kJ•mol-1
则乙烯气相直接水合反应的热化学方程式为:____________________ 。
(2)如图为乙烯气相直接水合法制备乙醇中乙烯的平衡转化率与温度、压强的关系(其中n(H2O) : n(C2H4)=1:1)。
若p2=8.0 MPa,列式计算A点的平衡常数Kp=____________ (用平衡分压代替平衡浓度计算;分压=总压×物质的量分数;结果保留到小数点后两位);
(3)以乙烯为燃料,氧气为氧化剂,KOH溶液为电解质溶液,可制成燃料电池(电极材料为惰性电极)。
①若KOH溶液足量,则负极的电极反应式__________________________________ 。
②若电解质溶液中KOH的物质的量为0.75mol,当有0.25mol乙烯参与反应时(假设电解质溶液体积变化忽略不计),则反应后电解质溶液中各种离子的物质的量浓度由大到小的顺序是_____________________________________________________
甲醇脱水反应 2CH3OH(g)═CH3OCH3(g)+H2O(g) △H1=-23.9kJ•mol-1
甲醇制烯烃反应 2CH3OH(g) ═C2H4 (g)+2H2O(g) △H2=-29.1kJ•mol-1
乙醇异构化反应 C2H5OH (g)═CH3OCH3(g) △H3=+50.7kJ•mol-1
则乙烯气相直接水合反应的热化学方程式为:
(2)如图为乙烯气相直接水合法制备乙醇中乙烯的平衡转化率与温度、压强的关系(其中n(H2O) : n(C2H4)=1:1)。

若p2=8.0 MPa,列式计算A点的平衡常数Kp=
(3)以乙烯为燃料,氧气为氧化剂,KOH溶液为电解质溶液,可制成燃料电池(电极材料为惰性电极)。
①若KOH溶液足量,则负极的电极反应式
②若电解质溶液中KOH的物质的量为0.75mol,当有0.25mol乙烯参与反应时(假设电解质溶液体积变化忽略不计),则反应后电解质溶液中各种离子的物质的量浓度由大到小的顺序是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】环境监测显示,某城市的主要气体污染物为SO2、NOx、CO等,其主要来源为燃煤、机动车尾气。进行如下研究:
(1)为减少燃煤对SO2的排放,可将煤转化为清洁燃料水煤气(CO和H2)。
已知: ΔH=-241.8kJ·mol-1
ΔH=-241.8kJ·mol-1
 ΔH=-110.5kJmol-1
ΔH=-110.5kJmol-1
写出焦炭与1mol水蒸气反应生成水煤气的热化学方程式:________ 。
(2)①在101 kPa时,H2(g)在 1.00 mol O2(g)中完全燃烧生成2.00 mol H2O(l)放出571.6 kJ的热量,表示H2燃烧热的热化学方程式为________________________________ 。
②1.00 L 1.00 mol·L−1 H2SO4溶液与2.00 L 1.00 mol·L−1 NaOH溶液完全反应,放出114.6 kJ热量,表示其中和热的热化学方程式为____________________________ 。
(3)利用如图所示装置(电极均为惰性电极)可吸收SO2,并利用阴极排出的溶液吸收NO2。

电极A的电极反应式为________ ;
(1)为减少燃煤对SO2的排放,可将煤转化为清洁燃料水煤气(CO和H2)。
已知:
 ΔH=-241.8kJ·mol-1
ΔH=-241.8kJ·mol-1 ΔH=-110.5kJmol-1
ΔH=-110.5kJmol-1写出焦炭与1mol水蒸气反应生成水煤气的热化学方程式:
(2)①在101 kPa时,H2(g)在 1.00 mol O2(g)中完全燃烧生成2.00 mol H2O(l)放出571.6 kJ的热量,表示H2燃烧热的热化学方程式为
②1.00 L 1.00 mol·L−1 H2SO4溶液与2.00 L 1.00 mol·L−1 NaOH溶液完全反应,放出114.6 kJ热量,表示其中和热的热化学方程式为
(3)利用如图所示装置(电极均为惰性电极)可吸收SO2,并利用阴极排出的溶液吸收NO2。

电极A的电极反应式为
您最近一年使用:0次
【推荐3】乙烯是有机合成工业重要的原料,由乙烷制取乙烯是常见的方法。已知乙烷热裂解法制取乙烯的反应为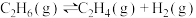
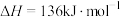 。
。
(1)一定温度下,在乙烷热裂解制取乙烯时,向体系中充入一定量惰性气体,保持体系的总压强为100kPa,测得平衡时各组分的体积分数如下表所示:
该温度下反应的平衡常数
_______ kPa,(用物质的平衡分压代替平衡浓度,平衡分压=总压强X体积分数)
(2)利用膜分离技术可以实现边反应边分离出生成的 。在容积为1L的恒容密闭容器中充入1mol乙烷,测得不同氢气移出率α[
。在容积为1L的恒容密闭容器中充入1mol乙烷,测得不同氢气移出率α[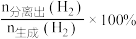 ]条件下,乙烷的平衡转化率与和温度的关系如图-1所示。
]条件下,乙烷的平衡转化率与和温度的关系如图-1所示。
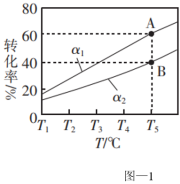
①α1_______ (填“>”、“<”或“=”) α2。
②若A点时平衡常数K=0.8,则α1=_______ 。
(3)以 和
和 为原料可以协同制取
为原料可以协同制取 和CO,发生的反应如下:
和CO,发生的反应如下:
反应1: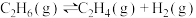
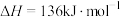
反应2:
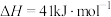
①已知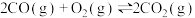
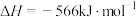 。
。
则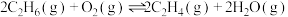 的
的
_______  。
。
②0.1MPa时,按物质的量之比为1:1向密闭容器中充入 和
和 的混合气体,反应相同时间,测得
的混合气体,反应相同时间,测得 和
和 的转化率与温度的关系如图-2所示。X代表的物质是
的转化率与温度的关系如图-2所示。X代表的物质是_______ 。750~820℃时,随着温度的升高,容器中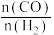 的值的变化情况是
的值的变化情况是_______ 。
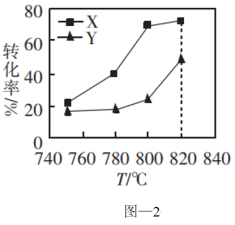
③乙烷热裂解时,会产生积碳,以 和
和 为原料协同制取
为原料协同制取 和CO会减少积碳的产生,原因是
和CO会减少积碳的产生,原因是_______ 。
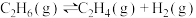
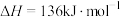 。
。(1)一定温度下,在乙烷热裂解制取乙烯时,向体系中充入一定量惰性气体,保持体系的总压强为100kPa,测得平衡时各组分的体积分数如下表所示:
| 物质 |  |  |  |
| 体积分数 | 5% | 20% | 20% |

(2)利用膜分离技术可以实现边反应边分离出生成的
 。在容积为1L的恒容密闭容器中充入1mol乙烷,测得不同氢气移出率α[
。在容积为1L的恒容密闭容器中充入1mol乙烷,测得不同氢气移出率α[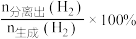 ]条件下,乙烷的平衡转化率与和温度的关系如图-1所示。
]条件下,乙烷的平衡转化率与和温度的关系如图-1所示。
①α1
②若A点时平衡常数K=0.8,则α1=
(3)以
 和
和 为原料可以协同制取
为原料可以协同制取 和CO,发生的反应如下:
和CO,发生的反应如下:反应1:
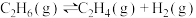
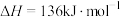
反应2:

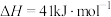
①已知
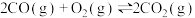
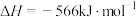 。
。则
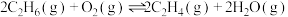 的
的
 。
。②0.1MPa时,按物质的量之比为1:1向密闭容器中充入
 和
和 的混合气体,反应相同时间,测得
的混合气体,反应相同时间,测得 和
和 的转化率与温度的关系如图-2所示。X代表的物质是
的转化率与温度的关系如图-2所示。X代表的物质是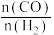 的值的变化情况是
的值的变化情况是
③乙烷热裂解时,会产生积碳,以
 和
和 为原料协同制取
为原料协同制取 和CO会减少积碳的产生,原因是
和CO会减少积碳的产生,原因是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】氮元素单质及其化合物在工农业生产生活中有着重要作用。
(1)根据下图,NO2和CO反应生成NO和CO2的ΔH =___________ kJ•mol-1。
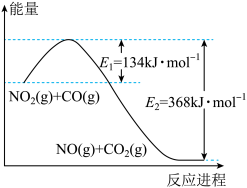
(2)用NH3催化还原NOx还可以消除氮氧化物的污染。例如:

 ①
①

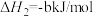 ②
②
若1mol NH3还原NO至N2,则该反应过程中的反应热ΔH3___________  (用含a、b的式子表示)。
(用含a、b的式子表示)。
(3)在固定体积的密闭容器中,进行如下化学反应:N2 (g)+3H2 (g) 2NH3 (g)
2NH3 (g)  ,其平衡常数K与温度T的关系如下表:
,其平衡常数K与温度T的关系如下表:
①该反应的平衡常数表达式:K ___________
②试判断K1___________ K2 (填写“>”“=”或“<”)
③一定温度下,在2L密闭容器中充入1mol N2和3mol H2并发生反应。若容器容积恒定,10min达到平衡时,气体的总物质的量为原来的7/8,则N2的转化率α(N2)=___________ ,以NH3表示该过程的反应速率v(NH3)=___________ 。
(1)根据下图,NO2和CO反应生成NO和CO2的ΔH =

(2)用NH3催化还原NOx还可以消除氮氧化物的污染。例如:

 ①
①
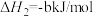 ②
②若1mol NH3还原NO至N2,则该反应过程中的反应热ΔH3
 (用含a、b的式子表示)。
(用含a、b的式子表示)。(3)在固定体积的密闭容器中,进行如下化学反应:N2 (g)+3H2 (g)
 2NH3 (g)
2NH3 (g)  ,其平衡常数K与温度T的关系如下表:
,其平衡常数K与温度T的关系如下表:| T/K | 298 | 398 | 498 |
| 平衡常数K | 4.1 106 106 | K1 | K2 |
②试判断K1
③一定温度下,在2L密闭容器中充入1mol N2和3mol H2并发生反应。若容器容积恒定,10min达到平衡时,气体的总物质的量为原来的7/8,则N2的转化率α(N2)=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】为了减少温室气体排放,习近平主席向世界承诺:中国将在2030年前实现“碳达峰”,到2060年实现“碳中和”。因此研究氮的氧化物\碳的氧化物等大气污染物的处理有着重要意义。
(1)汽车尾气中NO生成过程中的能量变化如图所示。

则该反应为___________ 反应。(选填“放热”或“吸热”)
(2)汽车排气管内安装的催化转化器可使尾气的主要污染物(NO和CO)大部分转化为无毒的大气循环物质,其反应方程式为___________ 。工业尾气中的NOx也可以利用氨气的___________ 性,将其转化为无毒物质。
(3)用CO2和H2合成甲醇有利于减少碳排放,其反应原理为CO2(g) +3H2(g) CH3OH(g) +H2O(g)。向甲、乙两个体积都为2.0L的恒容密闭容器中均充入1 mol CO2和3 mol H2,甲在T1、乙在T2温度下发生上述反应,反应过程中n(CH3OH)随时间(t)的变化见下表:
CH3OH(g) +H2O(g)。向甲、乙两个体积都为2.0L的恒容密闭容器中均充入1 mol CO2和3 mol H2,甲在T1、乙在T2温度下发生上述反应,反应过程中n(CH3OH)随时间(t)的变化见下表:
①甲容器中,0 ~6 min内的平均反应速率v(H2)=___________ 。
②乙容器中反应达到最大限度时,CO2的转化率为___________ 。
(4)一定温度下,在恒容密闭容器中发生反应:2NO2(g)+4CO(g) 4CO2(g)+N2(g)。下列能判断该反应达到化学平衡状态的是
4CO2(g)+N2(g)。下列能判断该反应达到化学平衡状态的是___________ (填序号)。
A. 反应速率2v(NO2)=v(CO)
B. 混合气体中NO2的含量保持不变
C. 混合气体颜色不再改变
D.混合气体的密度不再改变
E. 混合气体的压强不再改变
(5)已知:反应2Fe3++Fe=3Fe2+,该反应___________ (填“能”或“否”)设计成原电池,若能,其正极材料为___________ ,电解质溶液为___________ ,负极的电极反应式为___________ 。
(1)汽车尾气中NO生成过程中的能量变化如图所示。

则该反应为
(2)汽车排气管内安装的催化转化器可使尾气的主要污染物(NO和CO)大部分转化为无毒的大气循环物质,其反应方程式为
(3)用CO2和H2合成甲醇有利于减少碳排放,其反应原理为CO2(g) +3H2(g)
 CH3OH(g) +H2O(g)。向甲、乙两个体积都为2.0L的恒容密闭容器中均充入1 mol CO2和3 mol H2,甲在T1、乙在T2温度下发生上述反应,反应过程中n(CH3OH)随时间(t)的变化见下表:
CH3OH(g) +H2O(g)。向甲、乙两个体积都为2.0L的恒容密闭容器中均充入1 mol CO2和3 mol H2,甲在T1、乙在T2温度下发生上述反应,反应过程中n(CH3OH)随时间(t)的变化见下表: | t/min | 0 | 3 | 6 | 12 | 24 | 36 |
| n甲(CH3OH)/mol | 0 | 0.36 | 0.60 | 0.82 | 0.80 | 0.80 |
| n乙(CH3OH)/mol | 0 | 0.30 | 0.50 | 0.68 | 0.85 | 0.85 |
②乙容器中反应达到最大限度时,CO2的转化率为
(4)一定温度下,在恒容密闭容器中发生反应:2NO2(g)+4CO(g)
 4CO2(g)+N2(g)。下列能判断该反应达到化学平衡状态的是
4CO2(g)+N2(g)。下列能判断该反应达到化学平衡状态的是A. 反应速率2v(NO2)=v(CO)
B. 混合气体中NO2的含量保持不变
C. 混合气体颜色不再改变
D.混合气体的密度不再改变
E. 混合气体的压强不再改变
(5)已知:反应2Fe3++Fe=3Fe2+,该反应
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】甲醇是重要的溶剂和替代燃料,工业上用CO和H2在一定条件下制备CH3OH的反应为:CO(g)+2H2= CH3OH(g),在体积为1L的恒容密闭容器中,充人2molCO和4mol H2,一定条件下发生上述反应,测得CO(g)和CH3OH(g)的浓度随时间变化如图所示:

①从反应开始至达到平衡所需时间为_______ ,用氢气表示的平均反应速率
_______ 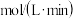
②根据下列热化学方程式计算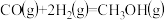 的△H=
的△H=_______ 。
已知:①CO(g)+ O2(g)=CO2(g) △H1=-283.0kJ/mol
O2(g)=CO2(g) △H1=-283.0kJ/mol
③达到平衡状态时CO的转化率为_______ ,该条件下反应的平衡常数k =_______ ,K值越大,说明反应物的转化率越_______ ,欲提高CO的转化率,可采取的措施有_______ 。(任写一种)

①从反应开始至达到平衡所需时间为

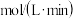
②根据下列热化学方程式计算
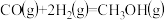 的△H=
的△H=已知:①CO(g)+
 O2(g)=CO2(g) △H1=-283.0kJ/mol
O2(g)=CO2(g) △H1=-283.0kJ/mol②H2(g)+ O2(g)=H2O(g) △H2=-241.8kJ/mol
O2(g)=H2O(g) △H2=-241.8kJ/mol
③CH3OH(g)+ O2(g)=CO2(g)+2H2O(g) △H3=-192.2kJ/mol
O2(g)=CO2(g)+2H2O(g) △H3=-192.2kJ/mol
③达到平衡状态时CO的转化率为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】研究氮的相关化合物在化工生产中有重要意义。
(1)氨的催化氧化是制备硝酸的重要反应,实验中先用酒精喷灯加热催化剂,然后通入反应气体,当催化剂红热后撤离酒精喷灯,催化剂始终保持红热,温度可达到700℃以上。下列图示中,能够正确表示该反应过程能量变化的是_______ (填标号)。
A. B.
B. C.
C.
(2)在2L的恒温恒容密闭容器中,发生反应 ,通入等物质的量的NO和
,通入等物质的量的NO和 气体,
气体,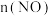 随时间的变化如下表:
随时间的变化如下表:
①0~4s内,
_______  。
。
②某同学由数据推测,反应在第4s时恰好达到平衡状态。该推测_______ (填“正确”或“错误”)。
③在第5s时, 的转化率为
的转化率为_______ 。
④平衡时,容器中混合气体的压强与反应开始时的压强之比为_______ 。
(3)一氧化氮—空气燃料电池将化学能转化为电能的同时,实现了制硝酸、发电、环保三位一体的结合,其工作原理如图所示,写出放电过程中正极的电极反应式_______ ,若过程中产生2mol ,则消耗标准状况下
,则消耗标准状况下 的体积为
的体积为_______ 。

(1)氨的催化氧化是制备硝酸的重要反应,实验中先用酒精喷灯加热催化剂,然后通入反应气体,当催化剂红热后撤离酒精喷灯,催化剂始终保持红热,温度可达到700℃以上。下列图示中,能够正确表示该反应过程能量变化的是
A.
 B.
B. C.
C.
(2)在2L的恒温恒容密闭容器中,发生反应
 ,通入等物质的量的NO和
,通入等物质的量的NO和 气体,
气体,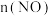 随时间的变化如下表:
随时间的变化如下表:| t/s | 0 | 1 | 2 | 3 | 4 | 5 |
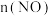 /mol /mol | 0.020 | 0.012 | 0.008 | 0.005 | 0.004 | 0.004 |

 。
。②某同学由数据推测,反应在第4s时恰好达到平衡状态。该推测
③在第5s时,
 的转化率为
的转化率为④平衡时,容器中混合气体的压强与反应开始时的压强之比为
(3)一氧化氮—空气燃料电池将化学能转化为电能的同时,实现了制硝酸、发电、环保三位一体的结合,其工作原理如图所示,写出放电过程中正极的电极反应式
 ,则消耗标准状况下
,则消耗标准状况下 的体积为
的体积为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】科学、安全、有效和合理地使用化学品是每一位生产者和消费者的要求和责任。
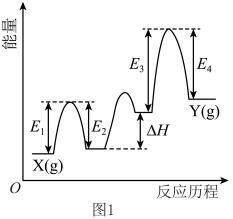
(1)铬及其化合物在催化、金属防腐等方面具有重要应用, 催化丙烷脱氢过程中,部分反应历程如图1所示。则
催化丙烷脱氢过程中,部分反应历程如图1所示。则 过程的焓变
过程的焓变
___________ 。(列出计算式) 和H-SAPO-34复合催化剂极大提高短链烯烃选择性。
和H-SAPO-34复合催化剂极大提高短链烯烃选择性。 和
和 在催化剂
在催化剂 表面转化为甲醇的各步骤所需要克服的能垒及甲醇在
表面转化为甲醇的各步骤所需要克服的能垒及甲醇在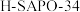 作用下产生乙烯、丙烯示意图如图2所示。
作用下产生乙烯、丙烯示意图如图2所示。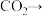 甲氧基
甲氧基 过程中,
过程中,___________ 的生成是决速步骤。(填化学式)
②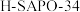 具有氧八元环构成的笼状结构(直径0.94nm),笼口为小的八环孔(直径0.38nm)。短链烯烃选择性提高的原因是
具有氧八元环构成的笼状结构(直径0.94nm),笼口为小的八环孔(直径0.38nm)。短链烯烃选择性提高的原因是___________ 。
(3)废水中铬(VI)主要以 和
和 形式存在,处理的方法之一是将铬(Ⅵ)还原为
形式存在,处理的方法之一是将铬(Ⅵ)还原为 ,再转化为
,再转化为 沉淀。常温下,
沉淀。常温下, 和
和 在溶液中存在如下平衡:
在溶液中存在如下平衡: ,该反应的平衡常数
,该反应的平衡常数 。
。
①若废水中 (Ⅵ)的总物质的量浓度
(Ⅵ)的总物质的量浓度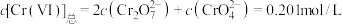 ,要将废水中
,要将废水中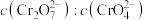 调节为
调节为 ,则需调节溶液的
,则需调节溶液的
___________ 。(忽略调节 时溶液体积的变化)
时溶液体积的变化)
②有关该平衡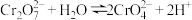 说法正确的是
说法正确的是___________ (填序号)
A.反应达平衡时, 今和
今和 的浓度相同
的浓度相同
B.加入少量水稀释,溶液中离子总数增加
C.溶液的颜色不变,说明反应达到平衡
D.加入少量 固体,平衡时
固体,平衡时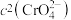 与
与 之比保持不变
之比保持不变
(4)纳米零价铁可处理电镀废水中的甘氨酸铬。
①甘氨酸铬(结构简式如图3所示)分子中与铬配位的原子为___________ 。___________ 。
(1)铬及其化合物在催化、金属防腐等方面具有重要应用,
 催化丙烷脱氢过程中,部分反应历程如图1所示。则
催化丙烷脱氢过程中,部分反应历程如图1所示。则 过程的焓变
过程的焓变
 和H-SAPO-34复合催化剂极大提高短链烯烃选择性。
和H-SAPO-34复合催化剂极大提高短链烯烃选择性。 和
和 在催化剂
在催化剂 表面转化为甲醇的各步骤所需要克服的能垒及甲醇在
表面转化为甲醇的各步骤所需要克服的能垒及甲醇在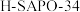 作用下产生乙烯、丙烯示意图如图2所示。
作用下产生乙烯、丙烯示意图如图2所示。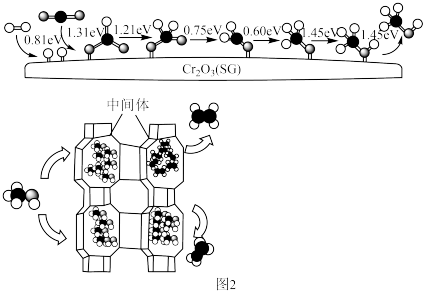
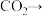 甲氧基
甲氧基 过程中,
过程中,②
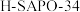 具有氧八元环构成的笼状结构(直径0.94nm),笼口为小的八环孔(直径0.38nm)。短链烯烃选择性提高的原因是
具有氧八元环构成的笼状结构(直径0.94nm),笼口为小的八环孔(直径0.38nm)。短链烯烃选择性提高的原因是(3)废水中铬(VI)主要以
 和
和 形式存在,处理的方法之一是将铬(Ⅵ)还原为
形式存在,处理的方法之一是将铬(Ⅵ)还原为 ,再转化为
,再转化为 沉淀。常温下,
沉淀。常温下, 和
和 在溶液中存在如下平衡:
在溶液中存在如下平衡: ,该反应的平衡常数
,该反应的平衡常数 。
。①若废水中
 (Ⅵ)的总物质的量浓度
(Ⅵ)的总物质的量浓度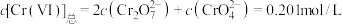 ,要将废水中
,要将废水中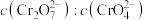 调节为
调节为 ,则需调节溶液的
,则需调节溶液的
 时溶液体积的变化)
时溶液体积的变化)②有关该平衡
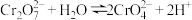 说法正确的是
说法正确的是A.反应达平衡时,
 今和
今和 的浓度相同
的浓度相同B.加入少量水稀释,溶液中离子总数增加
C.溶液的颜色不变,说明反应达到平衡
D.加入少量
 固体,平衡时
固体,平衡时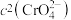 与
与 之比保持不变
之比保持不变(4)纳米零价铁可处理电镀废水中的甘氨酸铬。
①甘氨酸铬(结构简式如图3所示)分子中与铬配位的原子为

|
|
| 图4 | 图5 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.据报道,我国在南海北部神狐海域进行的可燃冰(甲烷的水合物)试采获得成功。
(1)甲烷重整是提高甲烷利用率的重要方式,除部分氧化外还有以下二种:
水蒸气重整:CH4(g)+H2O(g)⇌CO(g)+3H2(g) ΔH1=+205.9kJ·mol-1①
CO(g)+H2O(g)⇌CO2(g)+H2(g) ΔH2=-41.2kJ·mol-1②
二氧化碳重整:CH4(g)+CO2(g)⇌2CO(g)+2H2(g) ΔH3 ③
则反应①自发进行的条件是_______ ,ΔH3=_______ kJ·mol-1。
Ⅱ.氮的固定一直是科学家研究的重要课题,合成氨则是人工固氮比较成熟的技术,其原理为N2 (g)+3H2 (g)⇌2NH3(g)
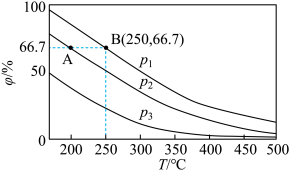
(2)在不同温度、压强和相同催化剂条件下,初始时N2、H2分别为0.1mol、0.3mol时,平衡后混合物中氨的体积分数(ψ)如图所示。
①其中,p1,p2和p3由大到小的顺序是_______ ,其原因是_______ 。
②若分别用vA(N2)和vB(N2)表示从反应开始至达平衡状态A、B时的化学反应速率,则vA(N2)_______ vB(N2)(填“ ”“
”“ ”或“
”或“ ”
” 。
。
③若在250℃、p1为105Pa条件下,反应达到平衡时容器的体积为1L,则该条件下B点N2的分压p(N2)为_______ Pa(分压=总压×物质的量分数,保留一位小数)。
(1)甲烷重整是提高甲烷利用率的重要方式,除部分氧化外还有以下二种:
水蒸气重整:CH4(g)+H2O(g)⇌CO(g)+3H2(g) ΔH1=+205.9kJ·mol-1①
CO(g)+H2O(g)⇌CO2(g)+H2(g) ΔH2=-41.2kJ·mol-1②
二氧化碳重整:CH4(g)+CO2(g)⇌2CO(g)+2H2(g) ΔH3 ③
则反应①自发进行的条件是
Ⅱ.氮的固定一直是科学家研究的重要课题,合成氨则是人工固氮比较成熟的技术,其原理为N2 (g)+3H2 (g)⇌2NH3(g)
(2)在不同温度、压强和相同催化剂条件下,初始时N2、H2分别为0.1mol、0.3mol时,平衡后混合物中氨的体积分数(ψ)如图所示。

①其中,p1,p2和p3由大到小的顺序是
②若分别用vA(N2)和vB(N2)表示从反应开始至达平衡状态A、B时的化学反应速率,则vA(N2)
 ”“
”“ ”或“
”或“ ”
” 。
。③若在250℃、p1为105Pa条件下,反应达到平衡时容器的体积为1L,则该条件下B点N2的分压p(N2)为
您最近一年使用:0次