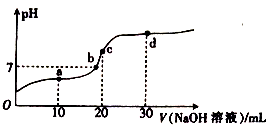
常温下,将1.0 mol/L 盐酸滴入20 mL 1.0 mol/L氨水中,溶液pH随加入盐酸体积变化的曲线如图所示。下列有关说法正确的是


| A.a点,c(NH4+)=c(OH-) |
| B.b点,c(NH4+)>c(Cl-)>c(NH3·H2O) |
| C.c点,pH=7 |
| D.d点,c(NH4+)+c(NH3·H2O)=c(Cl-) |
更新时间:2020-02-07 14:18:07
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列图示与对应的叙述相符的是

A.  图所示的反应,若升高温度,该反应的平衡常数变小 图所示的反应,若升高温度,该反应的平衡常数变小 |
B.  图所示的是 图所示的是 与 与 反应时含铝微粒浓度变化曲线,图中a点溶液中大量存在 反应时含铝微粒浓度变化曲线,图中a点溶液中大量存在 |
C.  表示等pH的盐酸与醋酸中分别加水稀释的pH变化,其中曲线b对应的是盐酸 表示等pH的盐酸与醋酸中分别加水稀释的pH变化,其中曲线b对应的是盐酸 |
D.  表示向 表示向 溶液中逐滴加稀盐酸,生成 溶液中逐滴加稀盐酸,生成 与所甲盐酸物质的量的关系 与所甲盐酸物质的量的关系 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】表中实验操作、现象与结论对应关系正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 以酚酞为指示剂,用盐酸标准液滴定氢氧化钠溶液 | 溶液由红色变为浅红色便立刻读数 | 测得c(NaOH)偏大 |
| B | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体 | 有白色沉淀生成,溶液红色变浅 | 纯碱溶液呈碱性是由CO 水解引起 水解引起 |
| C | 测定等浓度的NaClO溶液、CH3COONa溶液的pH | 前者大 | 酸性:HClO>CH3COOH |
| D | 用广泛pH试纸测定1mol/LNaHSO3溶液的酸碱性 | 测得pH=3.2 | NaHSO3溶液呈酸性,证明HSO 的电离大于水解 的电离大于水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】常温下,用NaOH溶液滴定H2A溶液,混合溶液的pH与离子浓度的负对数pX的关系如图所示。pX代表-lg 或-lg
或-lg ,曲线M代表-lg
,曲线M代表-lg 与pH的关系,曲线N代表-lg
与pH的关系,曲线N代表-lg 与pH的关系,下列说法不正确的是
与pH的关系,下列说法不正确的是
 或-lg
或-lg ,曲线M代表-lg
,曲线M代表-lg 与pH的关系,曲线N代表-lg
与pH的关系,曲线N代表-lg 与pH的关系,下列说法不正确的是
与pH的关系,下列说法不正确的是
| A.a、b两点所加的NaOH溶液体积大小:V(b)<V(a) |
| B.滴定至pH=7时,c(Na+ )=2c(A2-) +c(HA- ) |
| C.NaHA溶液中存在c(Na+ )=2c(A2- )+c(H2A) +c(HA- ) |
| D.H2A的第一步电离常数为 10-1.2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】常温下,0.10mol/L HCOONH4溶液中,c(HCOO-)、c(HCOOH)、 、c(NH3•H2O)四种微粒的pX[
、c(NH3•H2O)四种微粒的pX[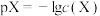 ]随pOH的变化关系如图,已知
]随pOH的变化关系如图,已知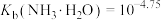 。下列说法错误的是
。下列说法错误的是
 、c(NH3•H2O)四种微粒的pX[
、c(NH3•H2O)四种微粒的pX[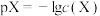 ]随pOH的变化关系如图,已知
]随pOH的变化关系如图,已知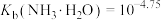 。下列说法错误的是
。下列说法错误的是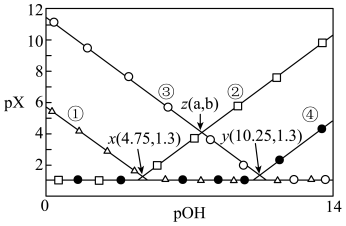
A.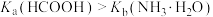 |
B.曲线③表示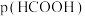 随pOH的变化关系 随pOH的变化关系 |
C.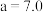 |
D.等浓度的HCOOH和HCOONH4混合液中: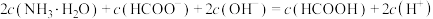 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列说法中不正确的是( )
| A.浓度均为0.1 mol⋅L-1的小苏打溶液与烧碱溶液等体积混合:c(Na+)+c(H+)=2c(CO32-)+c(OH-)+c(HCO3-) |
| B.pH相同的盐酸和硫酸,分别用蒸馏水稀释至原体积的m倍和n倍,稀释后两溶液pH相等,则m>n |
| C.常温下,0.1 mol⋅L-1某一元酸HA在水中有0.1%发生电离,则该温度下HA的电离常数约为10-7 |
D.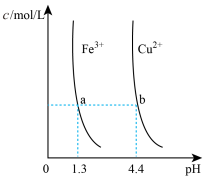 某温度下,Fe(OH)3,Cu(OH)2分别在溶液中达到沉淀溶解平衡后,改变溶液的pH,金属阳离子浓度的变化如图。由图可知:Ksp[Fe(OH)3]<Ksp[Cu(OH)2] 某温度下,Fe(OH)3,Cu(OH)2分别在溶液中达到沉淀溶解平衡后,改变溶液的pH,金属阳离子浓度的变化如图。由图可知:Ksp[Fe(OH)3]<Ksp[Cu(OH)2] |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】常温下,用0.10mol/LNaOH溶液滴定20.00mL 0.10mol/LHA溶液(滴定曲线见图)。下列说法正确的是
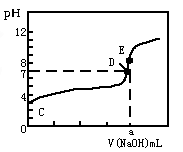
| A.此图可以表示从NaOH滴定盐酸的曲线 |
| B.图中D点状态时溶液中有:c(Na+)<c(A-) |
| C.达到D、E状态时,均有:c(Na+)+c(H+)=c(A-)+c(OH-) |
| D.当O<V(NaOH)<20.00mL时,对应混合溶液中各离子浓度由大到小的顺序均为c(A-)> c(Na+)> c(H+)>c(OH-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】常温下,下列说法不正确的是( )
| A.0.1mol/L的FeCl3溶液与0.01mol/L的FeCl3溶液中,Fe3+的浓度之比大于10 |
B.将a mol·L-1的氨水与0.01mol·L-1的盐酸等体积混合后,c(NH4+)=c(Cl-),则NH3·H2O的电离常数为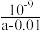 |
| C.pH加和为12的强酸与弱酸混合,pH可能为6 |
| D.0.1mol·L-1 NH4HS溶液中有:c(NH4+)=c(HS-)+c(S2-)+c(H2S) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】常温下,向0.50 mol/L的MOH溶液中逐滴加入0.25 mol/L的盐酸,溶液的pH随 的变化关系如图。已知:中和率=
的变化关系如图。已知:中和率= ×100%。下列说法正确的是
×100%。下列说法正确的是

 的变化关系如图。已知:中和率=
的变化关系如图。已知:中和率= ×100%。下列说法正确的是
×100%。下列说法正确的是
A.a点溶液中: |
| B.b点时,MOH的中和率为50% |
C.c点溶液中: |
| D.a、b、c、d四点溶液中,水的电离程度逐渐减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知:Ag2SO4微溶于水,Ag2SO3难溶于水。对Ag2SO3饱和溶液改变下列条件,可使c( )减小,同时c(Ag+)增大的是
)减小,同时c(Ag+)增大的是
 )减小,同时c(Ag+)增大的是
)减小,同时c(Ag+)增大的是| A.常温下,加入少量蒸馏水 | B.常温下,加入少量Na2SO3 |
C.常温下,通入少量O2,氧化SO | D.由常温降低至10℃ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】常温下,向10mL0.10mol/LCuCl2溶液中滴加0.10mol/LNa2S溶液,滴加过程中-lgc(Cu2+)与Na2S溶液体积(V)的关系如图所示,已知Ksp(ZnS)>Ksp(CuS)。下列说法不正确的是
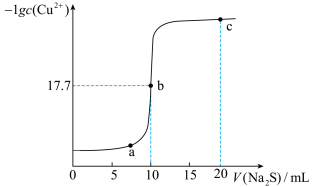

| A.a、b两点CuS的溶度积Ksp相等 |
| B.常温下,CuS的溶度积Ksp的数量级为10-36 |
| C.c点溶液中:c(Cl-)>c(Na+)>c(S2-)>c(OH-)>c(H+) |
| D.闪锌矿(ZnS)遇到硫酸铜溶液可转变为铜蓝(CuS) |
您最近一年使用:0次

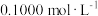 的
的 溶液测定锥形瓶中一定体积的盐酸的物质的量浓度。下列操作将导致测定值高于实际值的是
溶液测定锥形瓶中一定体积的盐酸的物质的量浓度。下列操作将导致测定值高于实际值的是