合理处理燃气中的H2S,不仅可减少对大气的污染,还可进行资源化利用。回答下列问题:
(1)H2S和S的燃烧热如表所示,

请写出常温下H2S与SO2反应的热化学方程式______ 。
(2)可以把H2S设计为一种燃料电池,原理如图a所示:其中,Fe2+在电池工作中的作用是______ ;请写出 I室发生的离子方程式______ 。
(3)为探究H2S的直接热解2H2S(g)=2H2(g )+S2(g)。在一体积为2L的密闭容器中充入2 mol H2S与1 molAr (起到稀释作用),进行实验。
①某同学测出不同温度下H2S的物质的量与反应时间的图象,图b是截取该图象的中间某部分。请计算T2温度下,0-l0s内,H2S的反应速率v=______ mo•L-1•s-1;
②图b中,T1、T2、T3三个温度,最高的是______ ;比较A点与B点的逆反应速率的大小,vA(逆)______ vB(逆)(填“>”、“<”或“=”);
③图c是表示反应2H2S(g)=2H2(g)+S2(g)平衡时,装置内各组分气体物质的量分数=与温度的关系(其中Ar气体变化曲线未画出)。请计算:C点的平衡常数K=______ ;D点平衡时,H2S的转化率=______ 。
(1)H2S和S的燃烧热如表所示,
| 物质 | 燃烧热/△H(kJ•mol-1) |
| H2S | -a |
| S | -b |

请写出常温下H2S与SO2反应的热化学方程式
(2)可以把H2S设计为一种燃料电池,原理如图a所示:其中,Fe2+在电池工作中的作用是
(3)为探究H2S的直接热解2H2S(g)=2H2(g )+S2(g)。在一体积为2L的密闭容器中充入2 mol H2S与1 molAr (起到稀释作用),进行实验。
①某同学测出不同温度下H2S的物质的量与反应时间的图象,图b是截取该图象的中间某部分。请计算T2温度下,0-l0s内,H2S的反应速率v=
②图b中,T1、T2、T3三个温度,最高的是
③图c是表示反应2H2S(g)=2H2(g)+S2(g)平衡时,装置内各组分气体物质的量分数=与温度的关系(其中Ar气体变化曲线未画出)。请计算:C点的平衡常数K=
更新时间:2020-02-14 09:24:34
|
相似题推荐
解答题-原理综合题
|
较易
(0.85)
【推荐1】甲醇(CH3OH)在作为内燃机燃料、制作燃料电池等方面具有重要的用途。
(1)25℃、101 kPa时,1 mol甲醇完全燃烧生成液态水释放的能量是762.5 kJ,写出该反应的热化学方程式______ 。
(2)64 g甲醇完全燃烧生成液态水释放的热量为_______ kJ。
(3)工业上以CO2和H2为原料合成甲醇:CO2(g) + 3H2(g) = CH3OH(g)+H2O(l) ΔH= a kJ/mol,若要计算a,需要知道甲醇完全燃烧生成液态水的焓变以及_______ 的焓变(文字描述)。
(4)甲醇的另一种用途是制成燃料电池,装置图如图所示。采用铂作为电极材料,稀硫酸作电解质溶液,向其中一个电极直接加入纯化后的甲醇,同时向一个电极通入空气。回答下列问题:
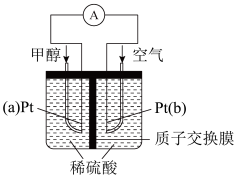
① 电池的正极反应式为:____________ ,负极反应式为:___________ 。
② 该电池工作时,H+的移动方向是由_____ 极经质子交换膜流向_____ 极(填“a”或“b”)。
③ 甲醇可作为内燃机燃料,也可用于制作燃料电池,其反应均为甲醇与氧气的反应,但能量转化形式不同,电池将化学能转化为电能的根本原因是___________ 。
(1)25℃、101 kPa时,1 mol甲醇完全燃烧生成液态水释放的能量是762.5 kJ,写出该反应的热化学方程式
(2)64 g甲醇完全燃烧生成液态水释放的热量为
(3)工业上以CO2和H2为原料合成甲醇:CO2(g) + 3H2(g) = CH3OH(g)+H2O(l) ΔH= a kJ/mol,若要计算a,需要知道甲醇完全燃烧生成液态水的焓变以及
(4)甲醇的另一种用途是制成燃料电池,装置图如图所示。采用铂作为电极材料,稀硫酸作电解质溶液,向其中一个电极直接加入纯化后的甲醇,同时向一个电极通入空气。回答下列问题:

① 电池的正极反应式为:
② 该电池工作时,H+的移动方向是由
③ 甲醇可作为内燃机燃料,也可用于制作燃料电池,其反应均为甲醇与氧气的反应,但能量转化形式不同,电池将化学能转化为电能的根本原因是
您最近一年使用:0次
【推荐2】研究NO2、SO2 、CO等大气污染气体的处理具有重要意义。
(1)NO2可用水吸收,相应的化学反应方程式为______ 。
(2)利用反应6NO2+ 8NH3 7N2+12 H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是
7N2+12 H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是______ L。
(3)已知:2SO2(g)+O2(g) 2SO3(g) ΔH=-196.6 kJ·mol-1
2SO3(g) ΔH=-196.6 kJ·mol-1
2NO(g)+O2(g) 2NO2(g) ΔH=-113.0 kJ·mol-1
2NO2(g) ΔH=-113.0 kJ·mol-1
则反应NO2(g)+SO2(g) SO3(g)+NO(g)的ΔH=
SO3(g)+NO(g)的ΔH=______ kJ·mol-1。
(4)一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是______ 。
a.体系压强保持不变
b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变
d.每消耗1 mol SO3的同时生成1 molNO2
(5)测得上述反应平衡时NO2与SO2体积比为1:6,则平衡常数K=______ 。
(1)NO2可用水吸收,相应的化学反应方程式为
(2)利用反应6NO2+ 8NH3
 7N2+12 H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是
7N2+12 H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是(3)已知:2SO2(g)+O2(g)
 2SO3(g) ΔH=-196.6 kJ·mol-1
2SO3(g) ΔH=-196.6 kJ·mol-12NO(g)+O2(g)
 2NO2(g) ΔH=-113.0 kJ·mol-1
2NO2(g) ΔH=-113.0 kJ·mol-1则反应NO2(g)+SO2(g)
 SO3(g)+NO(g)的ΔH=
SO3(g)+NO(g)的ΔH=(4)一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是
a.体系压强保持不变
b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变
d.每消耗1 mol SO3的同时生成1 molNO2
(5)测得上述反应平衡时NO2与SO2体积比为1:6,则平衡常数K=
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐3】二氧化碳的回收利用是环保领域研究的热点。
(1)用电弧法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下氧化法提纯,请完成该反应的化学方程式:____ 。(系数按顺序填在答题卷上)
C+KMnO4+H2SO4→CO2↑+MnSO4+K2SO4+H2O
(2)溶于海水的CO2主要以4种无机碳形式存在,其中HCO 占95%,在海洋循环中,通过如图所示的途径固碳,写出钙化作用的离子方程式:
占95%,在海洋循环中,通过如图所示的途径固碳,写出钙化作用的离子方程式:____ 。

(3)利用如图所示装置从海水中提取CO2,有利于减少环境温室气体含量。结合方程式简述提取CO2的原理:____ 。
 。
。
(4)CO2可以制甲醇,已知298K和101kPa条件下:
CO2(g)+3H2(g)=CH3OH(g)+H2O(l) △H=-akJ·mol-1
2H2(g)+O2(g)=2H2O(l) △H=-bkJ·mol-1
CH3OH(g)=CH3OH(l) △H=-ckJ·mol-1
则表示CH3OH(l)的燃烧热的热化学方程式为:____ 。
(1)用电弧法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下氧化法提纯,请完成该反应的化学方程式:
C+KMnO4+H2SO4→CO2↑+MnSO4+K2SO4+H2O
(2)溶于海水的CO2主要以4种无机碳形式存在,其中HCO
 占95%,在海洋循环中,通过如图所示的途径固碳,写出钙化作用的离子方程式:
占95%,在海洋循环中,通过如图所示的途径固碳,写出钙化作用的离子方程式:
(3)利用如图所示装置从海水中提取CO2,有利于减少环境温室气体含量。结合方程式简述提取CO2的原理:
 。
。 (4)CO2可以制甲醇,已知298K和101kPa条件下:
CO2(g)+3H2(g)=CH3OH(g)+H2O(l) △H=-akJ·mol-1
2H2(g)+O2(g)=2H2O(l) △H=-bkJ·mol-1
CH3OH(g)=CH3OH(l) △H=-ckJ·mol-1
则表示CH3OH(l)的燃烧热的热化学方程式为:
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐1】全球空气污染日趋严重,消除氮氧化物污染对建设宜居环境具有重要意义。
I.已知: ①
①
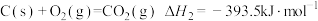 ②
②
 ③
③
(1)某反应的平衡常数表达式为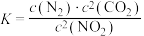 ,写出该反应的热化学方程式:
,写出该反应的热化学方程式:___________ 。
II.往恒容密闭容器中通入一定量 ,发生反应
,发生反应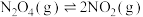 ,随温度升高,气体颜色变深。
,随温度升高,气体颜色变深。
(2)图甲为该反应平衡时有关物理量 随某条件X(其他条件不变)变化的关系图。X,
随某条件X(其他条件不变)变化的关系图。X, 可以分别表示___________(填字母)。
可以分别表示___________(填字母)。

(3)图乙为 时,体系中各物质的物质的量浓度随时间变化关系图。
时,体系中各物质的物质的量浓度随时间变化关系图。
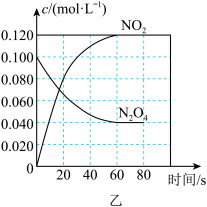
①在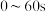 时段,反应速率
时段,反应速率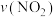 为
为___________  。
。
② 后,改变反应温度为
后,改变反应温度为 ,
, 以
以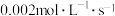 的平均速率降低,经
的平均速率降低,经 后又达到平衡。则
后又达到平衡。则
___________ (填“>”或“<”)100,判断理由是___________ 。
I.已知:
 ①
①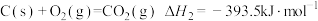 ②
② ③
③(1)某反应的平衡常数表达式为
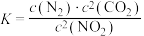 ,写出该反应的热化学方程式:
,写出该反应的热化学方程式:II.往恒容密闭容器中通入一定量
 ,发生反应
,发生反应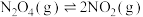 ,随温度升高,气体颜色变深。
,随温度升高,气体颜色变深。(2)图甲为该反应平衡时有关物理量
 随某条件X(其他条件不变)变化的关系图。X,
随某条件X(其他条件不变)变化的关系图。X, 可以分别表示___________(填字母)。
可以分别表示___________(填字母)。
A.温度 ,逆反应速率 ,逆反应速率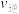 | B.温度 ,混合气体的密度 ,混合气体的密度 |
C.反应物浓度 ,平衡常数 ,平衡常数 | D.反应物浓度 , , 转化率 转化率 |
(3)图乙为
 时,体系中各物质的物质的量浓度随时间变化关系图。
时,体系中各物质的物质的量浓度随时间变化关系图。
①在
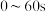 时段,反应速率
时段,反应速率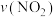 为
为 。
。②
 后,改变反应温度为
后,改变反应温度为 ,
, 以
以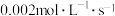 的平均速率降低,经
的平均速率降低,经 后又达到平衡。则
后又达到平衡。则
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】化学反应的快慢和限度对人类生产、生活有重要的意义。
(1)将影响化学反应速率的因素镇在空格处。
(2)某小组将酸性KMnO4溶液与H2C2O4(具有还原性)溶液混合,用反应中溶液紫色消失快慢的方法研究影响化学反应速率的因素。实验中酸性KMnO4溶液(0.0010 mol/L)、H2C2O4溶液的用量均为4 mL(忽略加入固体,溶液混合时体积的变化)。
①该反应中氧化剂与还原剂的物质的量之比为________ 。
②请帮助他们完成以下实验设计表:填写IV中的数据,并将实验目的补充完整。
③该小组同学对实验II进行了3次实验,测得以下数据:
实验II中用KMnO4表示该反应的平均反应速率为____ 。
(1)将影响化学反应速率的因素镇在空格处。
| 实例 | 影响因素 |
| 食物放在冰箱里延长保质期 | ① |
| 实验室将块状药品研细,再进行反应 | ② |
①该反应中氧化剂与还原剂的物质的量之比为
②请帮助他们完成以下实验设计表:填写IV中的数据,并将实验目的补充完整。
| 实验编号 | 温度/K | 催化剂的用量/g | H2C2O4溶液的浓度/ mol.L-1 | 实验目的 |
| I | 298 | 0.5 | 0.010 | A.实验I和II探究 B.实验I和III探究 C.实验I和IV探究催化剂对反应速率的影响 |
| II | 298 | 0.5 | 0.050 | |
| III | 323 | 0.5 | 0.010 | |
| IV |
③该小组同学对实验II进行了3次实验,测得以下数据:
| 实验编号 | 溶液褪色所需时间t/min | ||
| 第1次 | 第2次 | 第3次 | |
| II | 4.9 | 5.1 | 5.0 |
实验II中用KMnO4表示该反应的平均反应速率为
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐3】I.一定条件下,将2molA气体和2molB气体加入2L的恒容密闭容器中进行反应: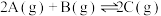 。2min后达化学平衡,测得C的浓度为
。2min后达化学平衡,测得C的浓度为 ,填写下列空白:
,填写下列空白:
(1)2min内用A表示的平均反应速率为_______ 。
(2)平衡时B的物质的量浓度为_______ 。
(3)平衡时A的转化率是B的转化率的_______ 倍。
(4)能说明该反应达到化学平衡状态的是:_______ 。
(5)要使该反应的化学反应速率加快,可采取的措施是:_______ (任写两种)。
II.理论上,任何自发的氧化还原反应都可以设计成原电池。利用反应 设计一种化学电池,回答下列问题:
设计一种化学电池,回答下列问题:
(6)正极上发生的电极反应式为_______ 。
(7)若导线上转移的电子为1mol,则消耗金属铜的质量为_______ 。
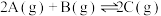 。2min后达化学平衡,测得C的浓度为
。2min后达化学平衡,测得C的浓度为 ,填写下列空白:
,填写下列空白:(1)2min内用A表示的平均反应速率为
(2)平衡时B的物质的量浓度为
(3)平衡时A的转化率是B的转化率的
(4)能说明该反应达到化学平衡状态的是:
| A.A表示的平均反应速率等于C表示的平均反应速率 |
| B.消耗1molA的同时生成0.5molB |
| C.分别用A、B、C表示的反应速率之比为2∶1∶2 |
| D.C的物质的量不再变化 |
II.理论上,任何自发的氧化还原反应都可以设计成原电池。利用反应
 设计一种化学电池,回答下列问题:
设计一种化学电池,回答下列问题:(6)正极上发生的电极反应式为
(7)若导线上转移的电子为1mol,则消耗金属铜的质量为
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐1】二氧化碳催化加氢合成乙烯是综合利用 的热点研究领域。相关的主要化学反应有:
的热点研究领域。相关的主要化学反应有:
Ⅰ.

Ⅱ.

Ⅲ.

(1)将 和
和 按物质的量之比为1:3投入一密闭容器中反应。(只考虑反应Ⅰ)
按物质的量之比为1:3投入一密闭容器中反应。(只考虑反应Ⅰ)
①当通入的气体总物质的量一定时,在固定体积、不同温度下,产物乙烯的体积分数随时间的变化如图1所示。试结合图1判断该反应自发进行的条件并说明理由___________ 。

②下列描述正确的是___________ 。
A.升高温度使反应的平衡常数增大
B.加压有助于反应的平衡正向移动
C.恒压时, 可以说明反应达到平衡
可以说明反应达到平衡
D.恒容时,再充入一定量 ,反应平衡体系中
,反应平衡体系中 增大
增大
(2)现将一定量的 和
和 置于一固定容积的容器中模拟工业生产过程,在不同温度下均反应一段时间后测定生成物的浓度,得到图2和图3。
置于一固定容积的容器中模拟工业生产过程,在不同温度下均反应一段时间后测定生成物的浓度,得到图2和图3。
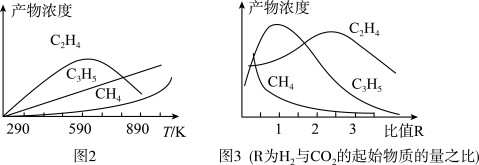
①结合图2和图3,该模拟工业生产制备乙烯的适宜条件为___________ 。
②725K时,将 和
和 的混合气体(体积比为1:3,总物质的量为4mol)在VL的固定容积容器中反应,并在一定催化剂下只进行反应Ⅰ和Ⅲ.达到平衡时,测得容器中
的混合气体(体积比为1:3,总物质的量为4mol)在VL的固定容积容器中反应,并在一定催化剂下只进行反应Ⅰ和Ⅲ.达到平衡时,测得容器中 和
和 的物质的量均为
的物质的量均为 mol,则在该温度下反应Ⅲ的平衡常数K为
mol,则在该温度下反应Ⅲ的平衡常数K为___________ 。
③在一定温度和压强条件下,为了提高反应物气体的转化率,采用了选择性膜技术,可选择性地让某气体通过而离开体系)。当选择性膜吸附乙烯气体时,可以降低副产物 的选择性(
的选择性( 选择性:生成
选择性:生成 消耗的
消耗的 的物质的量与总共转化了的
的物质的量与总共转化了的 的物质的量之比),请结合具体反应说明原因
的物质的量之比),请结合具体反应说明原因___________ 。
 的热点研究领域。相关的主要化学反应有:
的热点研究领域。相关的主要化学反应有:Ⅰ.


Ⅱ.


Ⅲ.


(1)将
 和
和 按物质的量之比为1:3投入一密闭容器中反应。(只考虑反应Ⅰ)
按物质的量之比为1:3投入一密闭容器中反应。(只考虑反应Ⅰ)①当通入的气体总物质的量一定时,在固定体积、不同温度下,产物乙烯的体积分数随时间的变化如图1所示。试结合图1判断该反应自发进行的条件并说明理由

②下列描述正确的是
A.升高温度使反应的平衡常数增大
B.加压有助于反应的平衡正向移动
C.恒压时,
 可以说明反应达到平衡
可以说明反应达到平衡D.恒容时,再充入一定量
 ,反应平衡体系中
,反应平衡体系中 增大
增大(2)现将一定量的
 和
和 置于一固定容积的容器中模拟工业生产过程,在不同温度下均反应一段时间后测定生成物的浓度,得到图2和图3。
置于一固定容积的容器中模拟工业生产过程,在不同温度下均反应一段时间后测定生成物的浓度,得到图2和图3。
①结合图2和图3,该模拟工业生产制备乙烯的适宜条件为
②725K时,将
 和
和 的混合气体(体积比为1:3,总物质的量为4mol)在VL的固定容积容器中反应,并在一定催化剂下只进行反应Ⅰ和Ⅲ.达到平衡时,测得容器中
的混合气体(体积比为1:3,总物质的量为4mol)在VL的固定容积容器中反应,并在一定催化剂下只进行反应Ⅰ和Ⅲ.达到平衡时,测得容器中 和
和 的物质的量均为
的物质的量均为 mol,则在该温度下反应Ⅲ的平衡常数K为
mol,则在该温度下反应Ⅲ的平衡常数K为③在一定温度和压强条件下,为了提高反应物气体的转化率,采用了选择性膜技术,可选择性地让某气体通过而离开体系)。当选择性膜吸附乙烯气体时,可以降低副产物
 的选择性(
的选择性( 选择性:生成
选择性:生成 消耗的
消耗的 的物质的量与总共转化了的
的物质的量与总共转化了的 的物质的量之比),请结合具体反应说明原因
的物质的量之比),请结合具体反应说明原因
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐2】甲醇制烯烃(MTO)是煤制烯烃工艺路线的核心技术。煤制烯烃主要包括煤的气化、液化、烯烃化三个阶段。
(1)煤的液化发生的主要反应之一为
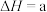 kJ⋅mol
kJ⋅mol ,在不同温度下,K(500°C)
,在不同温度下,K(500°C)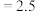 (mol⋅L
(mol⋅L ),K(700°C)
),K(700°C)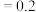 (mol⋅L
(mol⋅L )
)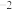 。
。
①
___________ 0(填“>”、“<”、“=”)。
②若反应在容积为2L的密闭容器中进行,500℃测得某一时刻体系内 、CO、
、CO、 物质的量分别为2 mol、1 mol、3 mol,则此时生成
物质的量分别为2 mol、1 mol、3 mol,则此时生成 的速率
的速率___________ 消耗 的速率(填“>”、“<”、“=”)。
的速率(填“>”、“<”、“=”)。
(2)通过研究外界条件对反应的影响,尽可能提高甲醇生成乙烯或丙烯的产率。
甲醇制烯烃的主要反应有:
Ⅰ.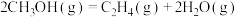
 kJ⋅mol
kJ⋅mol
Ⅱ.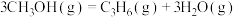
 kJ⋅mol
kJ⋅mol
Ⅲ.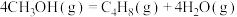
 kJ⋅mol
kJ⋅mol
① 转化为
转化为 的热化学方程式为Ⅳ:
的热化学方程式为Ⅳ: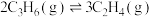
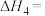
___________ 。
②加入 作为稀释剂,反应Ⅰ中
作为稀释剂,反应Ⅰ中 的产率将
的产率将___________ (填“增大”、“减小”或“不变”)。
(3)为研究不同条件对反应的影响,测得不同温度下平衡时 、
、 和
和 的物质的量分数变化,如图所示:
的物质的量分数变化,如图所示:
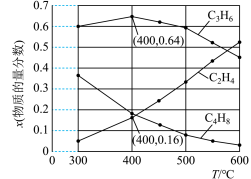
①随着温度的升高, 的物质的量分数呈现先增大后减小的趋势。温度高于400℃时,原因是
的物质的量分数呈现先增大后减小的趋势。温度高于400℃时,原因是___________ 。
②体系总压为0.1 MPa,400℃时反应Ⅳ的平衡常数
___________ 。
(1)煤的液化发生的主要反应之一为

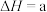 kJ⋅mol
kJ⋅mol ,在不同温度下,K(500°C)
,在不同温度下,K(500°C)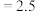 (mol⋅L
(mol⋅L ),K(700°C)
),K(700°C)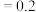 (mol⋅L
(mol⋅L )
)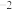 。
。①

②若反应在容积为2L的密闭容器中进行,500℃测得某一时刻体系内
 、CO、
、CO、 物质的量分别为2 mol、1 mol、3 mol,则此时生成
物质的量分别为2 mol、1 mol、3 mol,则此时生成 的速率
的速率 的速率(填“>”、“<”、“=”)。
的速率(填“>”、“<”、“=”)。(2)通过研究外界条件对反应的影响,尽可能提高甲醇生成乙烯或丙烯的产率。
甲醇制烯烃的主要反应有:
Ⅰ.
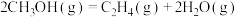
 kJ⋅mol
kJ⋅mol
Ⅱ.
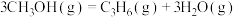
 kJ⋅mol
kJ⋅mol
Ⅲ.
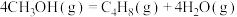
 kJ⋅mol
kJ⋅mol
①
 转化为
转化为 的热化学方程式为Ⅳ:
的热化学方程式为Ⅳ: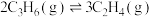
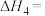
②加入
 作为稀释剂,反应Ⅰ中
作为稀释剂,反应Ⅰ中 的产率将
的产率将(3)为研究不同条件对反应的影响,测得不同温度下平衡时
 、
、 和
和 的物质的量分数变化,如图所示:
的物质的量分数变化,如图所示:
①随着温度的升高,
 的物质的量分数呈现先增大后减小的趋势。温度高于400℃时,原因是
的物质的量分数呈现先增大后减小的趋势。温度高于400℃时,原因是②体系总压为0.1 MPa,400℃时反应Ⅳ的平衡常数

您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐3】 催化加氢制甲醇技术可以帮助实现“碳中和”,催化过程中会发生以下反应:
催化加氢制甲醇技术可以帮助实现“碳中和”,催化过程中会发生以下反应:
主反应:
 (平衡常数为
(平衡常数为 )
)
副反应:
 (平衡常数为
(平衡常数为 )
)
(1)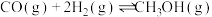 的
的
_______ ;(用 、
、 表示),平衡常数
表示),平衡常数
_______ (用 、
、 表示)。
表示)。
(2)在恒容密闭容器中发生上述反应,下列说法正确的是_______。
(3)恒温恒容的密闭容器中,加入2mol  和4mol
和4mol  ,若只发生主反应,反应起始压强为
,若只发生主反应,反应起始压强为 ,反应达平衡时,压强为
,反应达平衡时,压强为 ,主反应的分压平衡常数
,主反应的分压平衡常数
_______ [用含 的代数式表示,
的代数式表示, 是分压表示的平衡常数,分压(
是分压表示的平衡常数,分压( )=总压(
)=总压(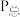 )×体积分数]。
)×体积分数]。
(4)利用电催化也可将 转化为
转化为 ,装置如下图所示,电极Ⅱ上的电极反应式为
,装置如下图所示,电极Ⅱ上的电极反应式为_______ ,当产生3.2g 时,阳极室溶液的质量减少
时,阳极室溶液的质量减少_______ g(忽略气体的溶解)。

 催化加氢制甲醇技术可以帮助实现“碳中和”,催化过程中会发生以下反应:
催化加氢制甲醇技术可以帮助实现“碳中和”,催化过程中会发生以下反应:主反应:

 (平衡常数为
(平衡常数为 )
)副反应:

 (平衡常数为
(平衡常数为 )
)(1)
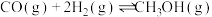 的
的
 、
、 表示),平衡常数
表示),平衡常数
 、
、 表示)。
表示)。(2)在恒容密闭容器中发生上述反应,下列说法正确的是_______。
| A.当反应未达平衡时,加入高选择性催化剂,可以提高单位时间内甲醇的产率 |
| B.反应达平衡后,向体系中充入氦气,副反应平衡不移动 |
C.1h内, 浓度由2 mol∙L−1降低至1 mol∙L−1,氢气的平均反应速率为2 mol∙L−1·h−1 浓度由2 mol∙L−1降低至1 mol∙L−1,氢气的平均反应速率为2 mol∙L−1·h−1 |
| D.升高温度,反应Ⅰ正反应速率减小,逆反应速率增大 |
 和4mol
和4mol  ,若只发生主反应,反应起始压强为
,若只发生主反应,反应起始压强为 ,反应达平衡时,压强为
,反应达平衡时,压强为 ,主反应的分压平衡常数
,主反应的分压平衡常数
 的代数式表示,
的代数式表示, 是分压表示的平衡常数,分压(
是分压表示的平衡常数,分压( )=总压(
)=总压(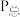 )×体积分数]。
)×体积分数]。(4)利用电催化也可将
 转化为
转化为 ,装置如下图所示,电极Ⅱ上的电极反应式为
,装置如下图所示,电极Ⅱ上的电极反应式为 时,阳极室溶液的质量减少
时,阳极室溶液的质量减少
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)硫酸铜溶液可以加快氢气生成速率的原因是___ 。
(2)实验室中现有Na2SO4、MgSO4、Ag2SO4、K2SO4四种溶液,可与实验中CuSO4溶液起相似作用的是__ 。
(3)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入六个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
①请完成此实验设计,其中:V1=___ ,V6=___ ,V9=___ 。
②反应一段时间后,实验A中的金属呈___ 色,实验E中的金属呈___ 色。
③该同学最后得出的结论为当加入少量CuSO4溶液时,生成氢气的速率会大大提高。但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因:___ 。
(1)硫酸铜溶液可以加快氢气生成速率的原因是
(2)实验室中现有Na2SO4、MgSO4、Ag2SO4、K2SO4四种溶液,可与实验中CuSO4溶液起相似作用的是
(3)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入六个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
| 实验 混合溶液 | A | B | C | D | E | F |
| 4 mol∙L−1H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
②反应一段时间后,实验A中的金属呈
③该同学最后得出的结论为当加入少量CuSO4溶液时,生成氢气的速率会大大提高。但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因:
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐2】I:磷酸氯喹是治疗新型肺炎的潜力药。磷酸是合成该药的初级原料之一,沸点高,难挥发。化学兴趣小组设计了合成磷酸的流程如图。回答下列问题
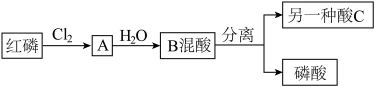
(1)将一定量的红磷与氯气置于容积为2L的恒温恒容(温度,体积均不变)反应器中制取A,各物质的物质的量与时间关系如下图
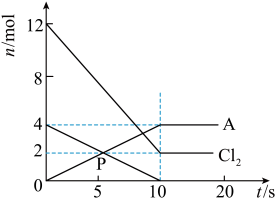
①该反应的化学方程式为___________ (A用化学式表示)
②前10s的平均反应速率v(Cl2)=_______
(2)将A加入热水中,生成两种酸。一种为磷酸,反应过程各元素化合价不变。
①另一种是酸C是___________ (写名称)
②A与热水反应的化学方程式为____________ 。
II(1)将反应Cu+2FeCl3=2FeCl2+CuCl2设计成原电池,完成该原电池的装置示意图______________ ,并作相应标注(标明正负极材料及电解质溶液的名称,电子移动方向、离子移动方向)。
(2)该装置中负极的电极方程式为________ 。
(3)若在反应过程中电极减轻3.2g,则在导线中通过电子__________ mol。

(1)将一定量的红磷与氯气置于容积为2L的恒温恒容(温度,体积均不变)反应器中制取A,各物质的物质的量与时间关系如下图

①该反应的化学方程式为
②前10s的平均反应速率v(Cl2)=
(2)将A加入热水中,生成两种酸。一种为磷酸,反应过程各元素化合价不变。
①另一种是酸C是
②A与热水反应的化学方程式为
II(1)将反应Cu+2FeCl3=2FeCl2+CuCl2设计成原电池,完成该原电池的装置示意图
(2)该装置中负极的电极方程式为
(3)若在反应过程中电极减轻3.2g,则在导线中通过电子
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】某同学用如图所示做水果电池的实验,测得数据如表所示:
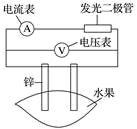
请回答以下问题:
(1)实验⑥中负极的电极反应式为_______ 。
(2)实验①、⑤中电流方向相反的原因是_______ 。
(3)影响水果电池电压的因素有_______ 、_______ 。
(4)若在实验中发光二极管不亮,该同学用铜、锌作电极,用菠萝作介质,并将多个此电池串联起来,再接发光二极管,这样做_______ (填“合理”或“不合理”) 。

| 实验编号 | 电极材料 | 水果品种 | 电极间距/cm | 电压/mV | |
| ① | 锌 | 铜 | 菠萝 | 3 | 900 |
| ② | 锌 | 铜 | 苹果 | 3 | 650 |
| ③ | 锌 | 铜 | 柑橘 | 3 | 850 |
| ④ | 锌 | 铜 | 西红柿 | 3 | 750 |
| ⑤ | 锌 | 铝 | 菠萝 | 3 | 650 |
| ⑥ | 锌 | 铝 | 苹果 | 3 | 450 |
(1)实验⑥中负极的电极反应式为
(2)实验①、⑤中电流方向相反的原因是
(3)影响水果电池电压的因素有
(4)若在实验中发光二极管不亮,该同学用铜、锌作电极,用菠萝作介质,并将多个此电池串联起来,再接发光二极管,这样做
您最近一年使用:0次



