pH=3的HF和pH=11的NaOH溶液等体积混合后,溶液显________ ,溶液中的离子浓度大小关系是_________ 。
更新时间:2020-02-18 16:43:11
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】水的电离平衡曲线如图所示:
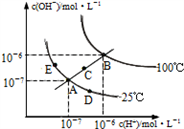
(1)在25℃时,有一pH = 12的NaOH溶液100 mL ,欲使它的pH降为11。如果加入蒸馏水,就加入_______ mL;如果加入pH = 10的NaOH溶液,应加入_______ mL(忽略溶液混合后体积的微小变化);
(2)当温度升高到B点时,水的离子积为________ ;加酸_______ (填能或不能)使水的离子积由E点变到B点;
(3)在100℃下,将pH=8的氢氧化钠溶液与pH=5的盐酸溶液混合并保持100℃,欲使溶液的pH=7,则氢氧化钠溶液与盐酸的体积比为_________ (忽略溶液混合后体积的微小变化)。

(1)在25℃时,有一pH = 12的NaOH溶液100 mL ,欲使它的pH降为11。如果加入蒸馏水,就加入
(2)当温度升高到B点时,水的离子积为
(3)在100℃下,将pH=8的氢氧化钠溶液与pH=5的盐酸溶液混合并保持100℃,欲使溶液的pH=7,则氢氧化钠溶液与盐酸的体积比为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)BiCl3的水解产物中有BiOCl生成。
①写出BiCl3水解反应的方程式:_________________________ 。
②医药上将BiOCl称为次氯酸铋,该名称____________ (填“正确”或“不正确”)。
③如何配制BiCl3溶液?_________________________________ 。
(2)将pH=2的某酸HnA与pH=12的某碱B(OH)m等体积混合后溶液的pH=8。
①若生成的盐中只有一种离子水解,该离子水解的离子方程式为_____________________ 。
②简述该混合液呈碱性的原因______________________ 。
①写出BiCl3水解反应的方程式:
②医药上将BiOCl称为次氯酸铋,该名称
③如何配制BiCl3溶液?
(2)将pH=2的某酸HnA与pH=12的某碱B(OH)m等体积混合后溶液的pH=8。
①若生成的盐中只有一种离子水解,该离子水解的离子方程式为
②简述该混合液呈碱性的原因
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】Ⅰ.在常温下,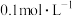 一元酸HB溶液的
一元酸HB溶液的 ,回答下列问题:
,回答下列问题:
(1)HB在水溶液中的电离平衡常数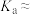
___________ 。
(2)常温下,有 相同、体积相同的盐酸和上述酸HB两种溶液,分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是
相同、体积相同的盐酸和上述酸HB两种溶液,分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是___________ (填字母)。(①表示盐酸,②表示HB)

Ⅱ.25℃时,几种弱酸的电离平衡常数如下表所示,回答下列问题:
(3) 、HClO、
、HClO、 、
、 的酸性由强到弱的顺序为
的酸性由强到弱的顺序为___________ 。
(4)请判断下列反应不正确 的是___________
Ⅲ.回答下列问题
(5)某温度下,纯水中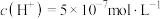 ,则该温度下的
,则该温度下的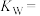
___________ ,若温度不变, 的HCl溶液中,由
的HCl溶液中,由水电离 出的
___________  。
。
(6)25℃时,将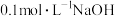 溶液与
溶液与 的
的 溶液等体积混合,(忽略混合后体积的变化),求所得溶液的pH为
溶液等体积混合,(忽略混合后体积的变化),求所得溶液的pH为___________ 。
(7)25℃时,将 的
的 稀释1000倍后,
稀释1000倍后,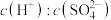 约为
约为___________ 。
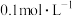 一元酸HB溶液的
一元酸HB溶液的 ,回答下列问题:
,回答下列问题:(1)HB在水溶液中的电离平衡常数
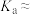
(2)常温下,有
 相同、体积相同的盐酸和上述酸HB两种溶液,分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是
相同、体积相同的盐酸和上述酸HB两种溶液,分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是
Ⅱ.25℃时,几种弱酸的电离平衡常数如下表所示,回答下列问题:
| 弱酸 |  | HClO |  |  |
 |  |  |   | 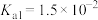  |
(3)
 、HClO、
、HClO、 、
、 的酸性由强到弱的顺序为
的酸性由强到弱的顺序为(4)请判断下列反应
A.少量 通入NaClO溶液中: 通入NaClO溶液中: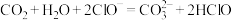 |
B.少量 通入 通入 溶液中: 溶液中: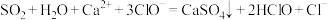 |
C.等浓度、体积的 与 与 混合: 混合: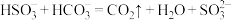 |
D.少量 通入 通入 溶液中: 溶液中: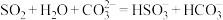 |
Ⅲ.回答下列问题
(5)某温度下,纯水中
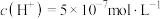 ,则该温度下的
,则该温度下的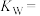
 的HCl溶液中,由
的HCl溶液中,由
 。
。(6)25℃时,将
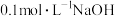 溶液与
溶液与 的
的 溶液等体积混合,(忽略混合后体积的变化),求所得溶液的pH为
溶液等体积混合,(忽略混合后体积的变化),求所得溶液的pH为(7)25℃时,将
 的
的 稀释1000倍后,
稀释1000倍后,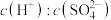 约为
约为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】研究电解质在水溶液中的平衡能了解它的存在形式。
①常温下,0.01 mol . L-1HA溶液中由水电离出的c(H+) =_________ mol/L。
②常温下一定浓度的MA稀溶液的pH=a,则a___ 7(填 “>”、“<”或“=”),用离子方程式表示其原因为_______________ 。
③K点时,溶液中c(H+)+c(M+)-c(OH-)=_____________ mol/L。
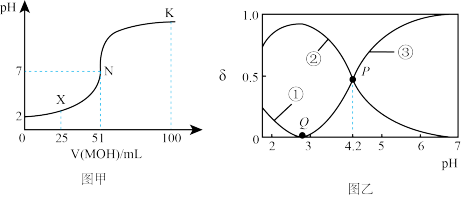
(2)20°C时,有c(H2C2O4)+c( )+c(
)+c( ) = 0.100 mol/L的H2C2O4、NaOH混合溶液,图乙中曲线①、②、③分别对应H2C2O4、
) = 0.100 mol/L的H2C2O4、NaOH混合溶液,图乙中曲线①、②、③分别对应H2C2O4、 、
、  三种微粒的物质的量分数δ随溶液pH变化的关系。请回答以下两个问题:
三种微粒的物质的量分数δ随溶液pH变化的关系。请回答以下两个问题:
①Q点:c(H2C2O4)___ c( ) (填 “>”、“<”或“=”)
) (填 “>”、“<”或“=”)
②该温度下 的电离常数K =
的电离常数K =_______________ 。
①常温下,0.01 mol . L-1HA溶液中由水电离出的c(H+) =
②常温下一定浓度的MA稀溶液的pH=a,则a
③K点时,溶液中c(H+)+c(M+)-c(OH-)=
(2)20°C时,有c(H2C2O4)+c(
 )+c(
)+c( ) = 0.100 mol/L的H2C2O4、NaOH混合溶液,图乙中曲线①、②、③分别对应H2C2O4、
) = 0.100 mol/L的H2C2O4、NaOH混合溶液,图乙中曲线①、②、③分别对应H2C2O4、 、
、  三种微粒的物质的量分数δ随溶液pH变化的关系。请回答以下两个问题:
三种微粒的物质的量分数δ随溶液pH变化的关系。请回答以下两个问题:①Q点:c(H2C2O4)
 ) (填 “>”、“<”或“=”)
) (填 “>”、“<”或“=”)②该温度下
 的电离常数K =
的电离常数K =
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题。
(1)室温下,有a.盐酸 b.硫酸 c.醋酸三种酸:
①当三种酸物质的量浓度相同时,c(H+)由大到小的顺序是___________ (用字母表示,下同)。
②同体积、同物质的量浓度的三种酸,中和NaOH 的能力由大到小的顺序是___________ 。
③将c(H+)相同且体积也相同的三种酸,分别与等浓度的NaOH稀溶液反应至pH=7,则消耗NaOH溶液液的体积由大到小关系为___________ 。
④将c(H+)相同的三种酸均加水稀释至原来的100倍后,c(H+)由大到小的顺序是___________ 。
(2)当H2S浓度较低时常用纯碱溶液进行吸收。表为H2S、H2CO3 的电离平衡常数。
纯碱溶液吸收少量H2S的离子方程式为___________ 。
(1)室温下,有a.盐酸 b.硫酸 c.醋酸三种酸:
①当三种酸物质的量浓度相同时,c(H+)由大到小的顺序是
②同体积、同物质的量浓度的三种酸,中和NaOH 的能力由大到小的顺序是
③将c(H+)相同且体积也相同的三种酸,分别与等浓度的NaOH稀溶液反应至pH=7,则消耗NaOH溶液液的体积由大到小关系为
④将c(H+)相同的三种酸均加水稀释至原来的100倍后,c(H+)由大到小的顺序是
(2)当H2S浓度较低时常用纯碱溶液进行吸收。表为H2S、H2CO3 的电离平衡常数。
| 电离平衡常数 | Kal | Ka2 |
| H2S | 9.1×10-8 | 1.1×10-12 |
| H2CO3 | 4.4×10-7 | 4.7×10-11 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】研究弱电解质的电离,有重要的实际意义。
(1)保持温度不变,向醋酸溶液中通入一定量的氨气,下列量将变小的是_______。
(2)将
 溶液加水稀释,
溶液加水稀释, )的比值将
)的比值将_______ (填“变大”、“不变”或“变小”)。
(3)某些弱酸在25℃时的电离常数如下:
下列反应可以发生的是_______(填字母)。
(1)保持温度不变,向醋酸溶液中通入一定量的氨气,下列量将变小的是_______。
A. | B. |
C. | D. 电离平衡常数 电离平衡常数 |

 溶液加水稀释,
溶液加水稀释, )的比值将
)的比值将(3)某些弱酸在25℃时的电离常数如下:
| 化学式 |  | HSCN | HCN | HClO |  |
| 电离常数 |  | 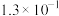 |  |  |   |
A. |
B. |
C. |
D.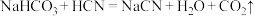 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】已知: 的电离常数
的电离常数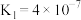 、
、 ,现有常温下20mL0.1 mol∙L−1的
,现有常温下20mL0.1 mol∙L−1的 溶液,回答下列问题。
溶液,回答下列问题。
(1)该溶液呈碱性的原因是(用离子方程式表示):_______ 。
(2)该 溶液中粒子之间的下列关系式中,正确的是______(填选项字母)。
溶液中粒子之间的下列关系式中,正确的是______(填选项字母)。
(3)水解反应是典型的可逆反应。水解反应的化学平衡常数称为水解常数(用Kh表示),请写出 第一步水解反应的水解平衡常数的表达式:
第一步水解反应的水解平衡常数的表达式:______ 。
(4)向该溶液中逐滴加入0.1 mol∙L−1 盐酸40mL,溶液pH逐渐降低,此时溶液中含碳元素微粒的物质的量浓度的百分含量(纵轴)如图所示,CO2因逸出未画出。_______ 。
②当溶液的pH=9时,溶液中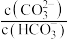 =
=______ 。
 的电离常数
的电离常数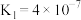 、
、 ,现有常温下20mL0.1 mol∙L−1的
,现有常温下20mL0.1 mol∙L−1的 溶液,回答下列问题。
溶液,回答下列问题。(1)该溶液呈碱性的原因是(用离子方程式表示):
(2)该
 溶液中粒子之间的下列关系式中,正确的是______(填选项字母)。
溶液中粒子之间的下列关系式中,正确的是______(填选项字母)。A.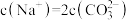 | B.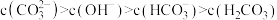 |
C. | D.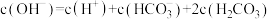 |
(3)水解反应是典型的可逆反应。水解反应的化学平衡常数称为水解常数(用Kh表示),请写出
 第一步水解反应的水解平衡常数的表达式:
第一步水解反应的水解平衡常数的表达式:(4)向该溶液中逐滴加入0.1 mol∙L−1 盐酸40mL,溶液pH逐渐降低,此时溶液中含碳元素微粒的物质的量浓度的百分含量(纵轴)如图所示,CO2因逸出未画出。
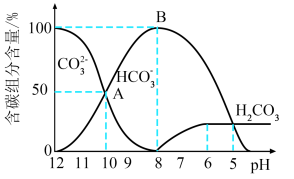
②当溶液的pH=9时,溶液中
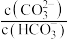 =
=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)常温下,有浓度均为0.1mol/L的三种溶液:a.NaHCO3;b.NaClO;c.CH3COONa。
①三种溶液pH由大到小的顺序为:__________________ 填序号)。
②溶液a的pH大于8,则溶液中c(H2CO3)____ c(CO32-) (填“>”、“<”或“=”)。
(2)已知25℃时,Ksp[AgCl]=1.8×10-10,现将足量氯化银分别放入:a.100mL蒸馏水中;b.100mL 0.2 mol/LAgNO3溶液中;c.100mL 0.1 mol/L氯化铝溶液中;d.100mL 0.1 mol/L盐酸溶液中。充分搅拌后,相同温度下银离子浓度由大到小的顺序是________ 。 (填写序号);b中氯离子的浓度为_______ mol/L。
①三种溶液pH由大到小的顺序为:
②溶液a的pH大于8,则溶液中c(H2CO3)
(2)已知25℃时,Ksp[AgCl]=1.8×10-10,现将足量氯化银分别放入:a.100mL蒸馏水中;b.100mL 0.2 mol/LAgNO3溶液中;c.100mL 0.1 mol/L氯化铝溶液中;d.100mL 0.1 mol/L盐酸溶液中。充分搅拌后,相同温度下银离子浓度由大到小的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)常温下,0.10 mol·L-1 NH4Cl溶液pH___________ 7(填“>”、“<”或“=”),溶液中各离子浓度由大到小的顺序___________ 。
(2)在Na2CO3溶液中滴入酚酞,溶液变红的原因___________ (写出相关的离子方程式),加热溶液颜色___________
(3)25℃时,0.05mol/LH2SO4溶液的pH=___________ ;0.05mol/LBa(OH)2溶液c(H+)=___________
(2)在Na2CO3溶液中滴入酚酞,溶液变红的原因
(3)25℃时,0.05mol/LH2SO4溶液的pH=
您最近一年使用:0次



