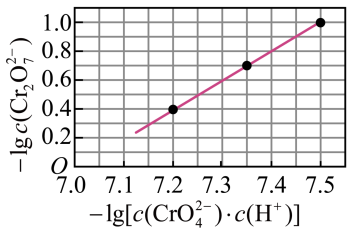
已知:溶液中存在2CrO42- +2H+ Cr2O72- + H2O。25℃时,调节初始浓度为1.0mol·L-1 Na2CrO4溶液的pH(溶液体积变化忽略不计),溶液中-lgc(Cr2O72-)与-lg[c(CrO42-)·c(H+)]的关系如图所示。下列说法错误的是
Cr2O72- + H2O。25℃时,调节初始浓度为1.0mol·L-1 Na2CrO4溶液的pH(溶液体积变化忽略不计),溶液中-lgc(Cr2O72-)与-lg[c(CrO42-)·c(H+)]的关系如图所示。下列说法错误的是
 Cr2O72- + H2O。25℃时,调节初始浓度为1.0mol·L-1 Na2CrO4溶液的pH(溶液体积变化忽略不计),溶液中-lgc(Cr2O72-)与-lg[c(CrO42-)·c(H+)]的关系如图所示。下列说法错误的是
Cr2O72- + H2O。25℃时,调节初始浓度为1.0mol·L-1 Na2CrO4溶液的pH(溶液体积变化忽略不计),溶液中-lgc(Cr2O72-)与-lg[c(CrO42-)·c(H+)]的关系如图所示。下列说法错误的是
A.若将原溶液加少量水稀释,溶液中 的值增大 的值增大 |
| B.当c(Cr2O72-)=c(CrO42- )时溶液的pH<7 |
| C.反应的平衡常数K=1×1014 |
| D.若只升高温度,c(CrO42-)增大,则该反应的∆H<0 |
19-20高三·湖南长沙·阶段练习 查看更多[2]
更新时间:2020-03-02 17:18:39
|
相似题推荐
【推荐1】某温度下,在1 L恒容密闭容器中3.0 mol A发生反应 ,有关数据如下:
,有关数据如下:
下列说法错误的是
 ,有关数据如下:
,有关数据如下:| 时间段/min | 产物C的平均生成速率/mol·L-1·min-1 |
| 0~2 | 0.20 |
| 0~4 | 0.15 |
| 0~6 | 0.10 |
| A.当容器内压强不再变化时,反应达到平衡状态 |
| B.2 min时,加入0.2 mol C,此时平衡逆向移动 |
| C.该温度下的平衡常数K=0.108 |
| D.5 min时,A的物质的量为2.1 mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】恒温下, 反应aX(g)  bY(g) +cZ(g)达到平衡后, 把容器体积扩到原来的2倍且达到新平衡时, Y的物质的量浓度由0.35mol/L减小到0.2mol/L, 下列判断正确的是
bY(g) +cZ(g)达到平衡后, 把容器体积扩到原来的2倍且达到新平衡时, Y的物质的量浓度由0.35mol/L减小到0.2mol/L, 下列判断正确的是
 bY(g) +cZ(g)达到平衡后, 把容器体积扩到原来的2倍且达到新平衡时, Y的物质的量浓度由0.35mol/L减小到0.2mol/L, 下列判断正确的是
bY(g) +cZ(g)达到平衡后, 把容器体积扩到原来的2倍且达到新平衡时, Y的物质的量浓度由0.35mol/L减小到0.2mol/L, 下列判断正确的是| A.a>b+c | B.a<b+c | C.a=b+c | D.a=b=c |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】臭氧层中O3分解过程如图所示,下列说法不正确的是


| A.催化反应①是吸热反应,催化反应②是放热反应 |
| B.E1是催化反应①对应的正反应活化能 |
| C.温度升高,总反应的正反应速率的增加幅度大于逆反应速率的增加幅度 |
| D.(E2+|△H|)是催化反应②对应的逆反应活化能 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
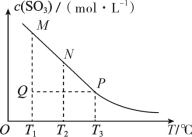
【推荐2】已知反应: ,在恒容密闭容器中,在不同温度下,达平衡时
,在恒容密闭容器中,在不同温度下,达平衡时 的浓度随温度变化的图像(曲线上任何一点都代表平衡状态)。下列说法正确的是
的浓度随温度变化的图像(曲线上任何一点都代表平衡状态)。下列说法正确的是
 ,在恒容密闭容器中,在不同温度下,达平衡时
,在恒容密闭容器中,在不同温度下,达平衡时 的浓度随温度变化的图像(曲线上任何一点都代表平衡状态)。下列说法正确的是
的浓度随温度变化的图像(曲线上任何一点都代表平衡状态)。下列说法正确的是
A. | B.平衡常数: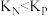 |
C.反应速率: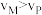 | D.Q点时, |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】已知[Co(H2O)6]2+呈粉红色,[CoCl4]2-呈蓝色,[ZnCl4]2-为无色。现将CoCl2溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡:[Co(H2O)6]2++4Cl- [CoCl4]2-+6H2O ΔH,用该溶液做实验,溶液的颜色变化如图:
[CoCl4]2-+6H2O ΔH,用该溶液做实验,溶液的颜色变化如图:
 [CoCl4]2-+6H2O ΔH,用该溶液做实验,溶液的颜色变化如图:
[CoCl4]2-+6H2O ΔH,用该溶液做实验,溶液的颜色变化如图: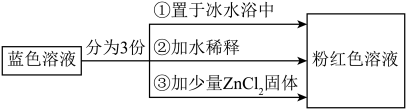
| A.由实验①可推知ΔH>0 |
| B.等物质的量的[Co(H2O)6]2+和[CoCl4]2-中,所含配位键数目不同 |
| C.实验②是由于加水稀释,使得Q<K,导致平衡逆向移动 |
| D.由实验③可知该实验条件下配离子的稳定性:[ZnCl4]2->[CoCl4]2- |
您最近一年使用:0次
【推荐1】某温度下,在一个2 L的密闭容器中,加入4 mol A和2 mol B进行如下反应:2A(g)+B(g)  C(s)+3D(g),反应2 min后达到平衡,测得生成1.6 mol C,下列说法不正确的是
C(s)+3D(g),反应2 min后达到平衡,测得生成1.6 mol C,下列说法不正确的是
 C(s)+3D(g),反应2 min后达到平衡,测得生成1.6 mol C,下列说法不正确的是
C(s)+3D(g),反应2 min后达到平衡,测得生成1.6 mol C,下列说法不正确的是| A.前2 min D的平均反应速率为1.2 mol·L-1·min-1 |
| B.此时A的平衡转化率是80% |
| C.增大该体系的压强,平衡向逆方向移动 |
| D.该温度下平衡常数K=432 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在300 mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni(s)+ 4CO(g)  Ni(CO)4(g),已知该反应的平衡常数与温度的关系如下表所示:
Ni(CO)4(g),已知该反应的平衡常数与温度的关系如下表所示:
下列说法正确的是
 Ni(CO)4(g),已知该反应的平衡常数与温度的关系如下表所示:
Ni(CO)4(g),已知该反应的平衡常数与温度的关系如下表所示:| 温度/℃ | 25 | 80 | 230 |
| 平衡常数 | 5 × 104 | 2 | 1. 9 ×10-5 |
| A.上述生成Ni(CO)4(g)的反应为吸热反应 |
| B.在80 ℃时,测得某时刻,Ni(CO)4、CO的浓度均为0.5 mol·L-1,则此时v(正)<v(逆) |
C.25℃时反应Ni(CO)4(g) Ni(s)+4CO(g)的平衡常数为2× 10-3 Ni(s)+4CO(g)的平衡常数为2× 10-3 |
| D.80℃达到平衡时,测得n(CO)=0.3 mol,则Ni(CO)4的平衡浓度为0.6 mol·L-1 |
您最近一年使用:0次

 H2(g)+CO2(g)△H﹤0,在其他条件不变的情况下,下列说法正确的是
H2(g)+CO2(g)△H﹤0,在其他条件不变的情况下,下列说法正确的是

