X、Y、Z、W为元素周期表前四周期的元素。其中X原子核外的L层电子数是K层电子数的两倍,Y的内层电子数是最外层电子数的9倍。Z在元素周期表的各元素中电负性最大。W原子的第三电子层处于全充满状态且第四电子层只有2个电子。请回答下列问题:
(1)W元素属于_______ 区元素。其基态原子的电子排布式为____________
(2)W2+能与氨气分子形成配离子[W(NH3)4]2+。其中配体分子的空间构为________ ,写出该配离子的结构简式(标明配位键)_________
(3)X能与氢、氮、氧三种元素构成化合物XO(NH2)2,其中X原子的杂化方式为_____ ;1mol该分子中σ键的数目为__________
(4)X的某种晶体为层状结构可与熔融金属钾作用。钾原子填充在各层之间形成间隙化合物,其常见结构的平面投影如图所示,则其化学式可表示为____________ 。
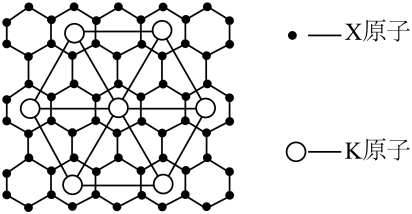
(5)元素Y与元素Z形成的晶体结构如图所示。设晶胞中最近的Y的离子与Z的距离为a pm。该化合物的摩尔质量为b g/ mol,则该晶胞密度的计算式为_________ g/cm3

(1)W元素属于
(2)W2+能与氨气分子形成配离子[W(NH3)4]2+。其中配体分子的空间构为
(3)X能与氢、氮、氧三种元素构成化合物XO(NH2)2,其中X原子的杂化方式为
(4)X的某种晶体为层状结构可与熔融金属钾作用。钾原子填充在各层之间形成间隙化合物,其常见结构的平面投影如图所示,则其化学式可表示为

(5)元素Y与元素Z形成的晶体结构如图所示。设晶胞中最近的Y的离子与Z的距离为a pm。该化合物的摩尔质量为b g/ mol,则该晶胞密度的计算式为

19-20高三下·湖南长沙·阶段练习 查看更多[2]
更新时间:2020-03-03 16:07:58
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】
氮原子可以形成 σ 键、π 键、大 π 键和配位键,成键的多样性使其形成了多种具有独特组成的物质。回答下 列问题:
(1)第一电离能:氮______ 氧(填“大于”或“小于”),基态氮原子价电子排布图不是 ,是因 为该排布方式违背了
,是因 为该排布方式违背了__________ 。
(2)肼(H2N−NH2)分子中孤电子对与 σ 键的数目之比为______ ,肼的相对分子质量与乙烯接近,但沸点远高于乙烯的原因是______ 。
( 3)硝酸的结构可表 示 为 ,硝酸与水分子可 形 成一水合二硝酸结晶 水 合物 (2HNO3 •H2O) , 水分子以三个氢键与两个硝酸分子结合,请写出一水合二硝酸的结构式
,硝酸与水分子可 形 成一水合二硝酸结晶 水 合物 (2HNO3 •H2O) , 水分子以三个氢键与两个硝酸分子结合,请写出一水合二硝酸的结构式______ (氢键用“…”表示)。
(4)正硝酸钠(Na3NO4)为白色晶体,是一种重要的化工原料。
①Na3NO4阴离子的空间构型为______ ,其中心原子杂化方式为______ 。
②分别写出一种与 Na3NO4的阴离子互为等电子体的阴离子和分子______ (填化学式)。
③在 573 K 条件下,实验室中用 NaNO3和 Na2O 在银皿中反应制得 Na3NO4,Na2O 的立方晶胞如图所 示。

图中“●”表示______ (填“Na+”或“O2−”),距离“●”最近且等距离的“○”有______ 个,Na2O 晶胞的参数为 a pm,则晶胞密度为_____ g•cm−3。(列出计算式即可,NA为阿伏加 德罗常数的值)
氮原子可以形成 σ 键、π 键、大 π 键和配位键,成键的多样性使其形成了多种具有独特组成的物质。回答下 列问题:
(1)第一电离能:氮
 ,是因 为该排布方式违背了
,是因 为该排布方式违背了(2)肼(H2N−NH2)分子中孤电子对与 σ 键的数目之比为
( 3)硝酸的结构可表 示 为
 ,硝酸与水分子可 形 成一水合二硝酸结晶 水 合物 (2HNO3 •H2O) , 水分子以三个氢键与两个硝酸分子结合,请写出一水合二硝酸的结构式
,硝酸与水分子可 形 成一水合二硝酸结晶 水 合物 (2HNO3 •H2O) , 水分子以三个氢键与两个硝酸分子结合,请写出一水合二硝酸的结构式(4)正硝酸钠(Na3NO4)为白色晶体,是一种重要的化工原料。
①Na3NO4阴离子的空间构型为
②分别写出一种与 Na3NO4的阴离子互为等电子体的阴离子和分子
③在 573 K 条件下,实验室中用 NaNO3和 Na2O 在银皿中反应制得 Na3NO4,Na2O 的立方晶胞如图所 示。

图中“●”表示
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】C、N、O、P、S、Cl、Cu、Zn八种元素的单质及化合物在现代工业生产中有着广泛的应用,请回答下列问题:
(1)第一电离能:Zn_______ Cu(填“>”或“<”下同)电负性S ______ Cl。
(2)写出基态Cu原子的价电子排布式_________________
(3)SO3的空间构型是________________ ,白磷P4分子呈正四面体结构,P原子位于正四面体的四个顶点,则P原子的杂化形式为_________________ 。
(4)与SCN—互为等电子体的微粒有_________________________ (任写两种)。
(5)NH3、PH3、AsH3三者的沸点由高到低的顺序是___________ ,原因是______________ 。
(6)Cu与Cl形成的一种化合物的晶胞结构如图所示(黑点代表铜原子)。
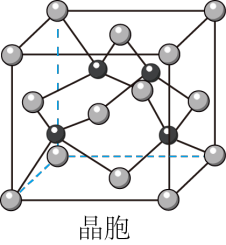
①该晶体的化学式为_________ 。
②已知该晶体中Cu原子和Cl氯原子之间的最短距离apm且恰好为体对角线的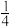 ,阿伏伽德罗常数为NA,则该晶体的密度为
,阿伏伽德罗常数为NA,则该晶体的密度为__________________ g/cm3(列出计算式即可)。
(1)第一电离能:Zn
(2)写出基态Cu原子的价电子排布式
(3)SO3的空间构型是
(4)与SCN—互为等电子体的微粒有
(5)NH3、PH3、AsH3三者的沸点由高到低的顺序是
(6)Cu与Cl形成的一种化合物的晶胞结构如图所示(黑点代表铜原子)。

①该晶体的化学式为
②已知该晶体中Cu原子和Cl氯原子之间的最短距离apm且恰好为体对角线的
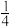 ,阿伏伽德罗常数为NA,则该晶体的密度为
,阿伏伽德罗常数为NA,则该晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】中国科学家首次在月球上发现新矿物,并命名为“嫦娥石”,该矿物是一种新的磷酸盐矿物,其理想化学式为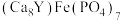 ,是人类在月球上发现的第六种新矿物。
,是人类在月球上发现的第六种新矿物。
(1)钪元素与嫦娥石中的钇(Y)同族。基态钪( )原子的核外电子排布式为
)原子的核外电子排布式为___________ ; 在元素周期表中的位置为
在元素周期表中的位置为___________ 。
(2)嫦娥石中电负性最大的元素其氢化物的熔沸点大于同主族元素氢化物的熔沸点的原因为___________ 。
(3)嫦娥石中 的中心原子杂化方式为
的中心原子杂化方式为___________ 。
(4)斜锆石是与嫦娥石伴生的一种矿物,它的一种变体立方氧化锆可通过人工方法合成,被广泛用作钻石的代替品如图2所示(元素符号O、 ),回答下列问题:
),回答下列问题:
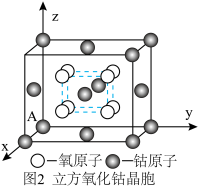
①以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图中锆原子A的坐标为 ,则任意一个氧原子的分数坐标为
,则任意一个氧原子的分数坐标为___________ 。
②若晶胞参数为 的摩尔质量为
的摩尔质量为 ,则该晶体的密度为
,则该晶体的密度为___________  。
。
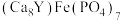 ,是人类在月球上发现的第六种新矿物。
,是人类在月球上发现的第六种新矿物。(1)钪元素与嫦娥石中的钇(Y)同族。基态钪(
 )原子的核外电子排布式为
)原子的核外电子排布式为 在元素周期表中的位置为
在元素周期表中的位置为(2)嫦娥石中电负性最大的元素其氢化物的熔沸点大于同主族元素氢化物的熔沸点的原因为
(3)嫦娥石中
 的中心原子杂化方式为
的中心原子杂化方式为(4)斜锆石是与嫦娥石伴生的一种矿物,它的一种变体立方氧化锆可通过人工方法合成,被广泛用作钻石的代替品如图2所示(元素符号O、
 ),回答下列问题:
),回答下列问题:
①以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图中锆原子A的坐标为
 ,则任意一个氧原子的分数坐标为
,则任意一个氧原子的分数坐标为②若晶胞参数为
 的摩尔质量为
的摩尔质量为 ,则该晶体的密度为
,则该晶体的密度为 。
。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】A、B、C、D都是短周期元素。A的原子核外有两个电子层,最外层已达到饱和。B位于A元素的下一周期,是地壳中含量最多的金属元素。C的离子带有两个单位正电荷,它的核外电子排布与A元素原子相同。D与C属同一周期,D原子的最外层电子数比A的最外层电子数少1。
(1)根据上述事实判断:A是______ ,B是______ ,C是______ ,D是______ (填元素符号)。
(2)C的离子基态核外电子排布式为____________________ ;B、C、D的原子半径由大到小的顺序为____________ (填元素符号)。
(3)D在周期表中的位置______ ,D基态原子的轨道表示式为:_______________
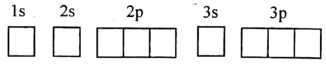
(4)B的最高价氧化物对应的水化物与NaOH溶液反应的离子方程式:_________________________ 。
(1)根据上述事实判断:A是
(2)C的离子基态核外电子排布式为
(3)D在周期表中的位置

(4)B的最高价氧化物对应的水化物与NaOH溶液反应的离子方程式:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】锌钡白( ),又名立德粉,为白色粉末,是一种常用的白色颜料。回答下列问题:
),又名立德粉,为白色粉末,是一种常用的白色颜料。回答下列问题:
(1)基态Zn原子的核外电子排布式为_______ ;基态 有
有_______ 种能量不同的电子。
(2)原子中电子有两种相反的自旋状态,分别用 和
和 表示,称为电子的自旋磁量子数。则基态S原子中电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。则基态S原子中电子自旋磁量子数的代数和为_______ 。
(3) 的三聚体环状结构如图所示,图中S原子的轨道杂化方式为
的三聚体环状结构如图所示,图中S原子的轨道杂化方式为_______ ,1个该分子中含有_______ 个 键,S和O形成的共价键有两类(分别以a和b表示),其中键长较短的键为
键,S和O形成的共价键有两类(分别以a和b表示),其中键长较短的键为_______ (填“a”或“b”);硫的另一种常见的氧化物为 ,则
,则 分子的VSEPR模型名称是
分子的VSEPR模型名称是_______ 。

(4)立方硫化锌的晶胞结构如图所示。 填充在S2-围成的
填充在S2-围成的_______ 空隙中。 与
与 之间的核间距为dcm,则该晶体的密度为
之间的核间距为dcm,则该晶体的密度为_______  (列出计算式即可,设
(列出计算式即可,设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。

 ),又名立德粉,为白色粉末,是一种常用的白色颜料。回答下列问题:
),又名立德粉,为白色粉末,是一种常用的白色颜料。回答下列问题:(1)基态Zn原子的核外电子排布式为
 有
有(2)原子中电子有两种相反的自旋状态,分别用
 和
和 表示,称为电子的自旋磁量子数。则基态S原子中电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。则基态S原子中电子自旋磁量子数的代数和为(3)
 的三聚体环状结构如图所示,图中S原子的轨道杂化方式为
的三聚体环状结构如图所示,图中S原子的轨道杂化方式为 键,S和O形成的共价键有两类(分别以a和b表示),其中键长较短的键为
键,S和O形成的共价键有两类(分别以a和b表示),其中键长较短的键为 ,则
,则 分子的VSEPR模型名称是
分子的VSEPR模型名称是
(4)立方硫化锌的晶胞结构如图所示。
 填充在S2-围成的
填充在S2-围成的 与
与 之间的核间距为dcm,则该晶体的密度为
之间的核间距为dcm,则该晶体的密度为 (列出计算式即可,设
(列出计算式即可,设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
【推荐3】下表中A、B、C、D、E为原子序数依次增大的短周期主族元素,F、G为第四周期元素,其相关信息如下:
(1)E元素在周期表中的位置是___________ ,其基态原子最高能层的电子占据的原子轨道电子云为_____________ 形。
(2)F元素位于元素周期的_____________ 区,其基态原子的价层电子轨道表示式为______________ 。
(3)C元素单质的结构式为_____________ ,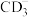 中心原子的杂化方式为
中心原子的杂化方式为___________ ,分子空间构型为_______________ 。
(4)B、C、D、E四种元素的原子半径由大到小的顺序:____________ (填元素符号)。
(5)气态F2+比气态G2+再失去一个电子难,原因是____________ 。
(6)下列关于B2A4的说法中正确的是____________(填序号)。
| A.元素原子是元素周期表中半径最小的原子 |
| B.基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| C.元素原子最高能级的不同轨道都有电子,且只有一种自旋方向 |
| D.原子核外s能级上的电子总数与p能级上的电子总数相等 |
| E.与D为同主族元素 |
| F.其+2价离子的3d轨道为半充满状态 |
| G.目前年产量最大、使用最广泛的金属 |
(2)F元素位于元素周期的
(3)C元素单质的结构式为
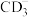 中心原子的杂化方式为
中心原子的杂化方式为(4)B、C、D、E四种元素的原子半径由大到小的顺序:
(5)气态F2+比气态G2+再失去一个电子难,原因是
(6)下列关于B2A4的说法中正确的是____________(填序号)。
| A.B2A4分子中中心原子的杂化类型为sp2 |
| B.B2A4是只由极性键形成的非极性分子 |
| C.B2A4中的所有原子都满足8电子稳定结构 |
| D.B2A4分子中σ键和π键数目比为5:1 |
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】回答下列问题:
(1)甲烷在一定条件下可生成以下微粒:
A.碳正离子( ) B.碳负离子(
) B.碳负离子( ) C.甲基(
) C.甲基(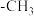 ) D.碳烯(
) D.碳烯(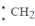 )
)
①四种微粒中,键角为120°的是___________ (填序号)。
②碳负离子( )的空间构型为
)的空间构型为___________ 。
(2)在制取合成氨原料气的过程中,常混有一些杂质,如CO会使催化剂中毒。除去CO的化学方程式为(HAc表示醋酸)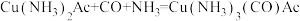 。请回答下列问题:
。请回答下列问题:
①该反应中含有的第二周期非金属元素的第一电离能由大到小的顺序为___________ 。
②在一定条件下NH3和CO2能合成尿素CO(NH2)2,尿素中碳原子轨道的杂化类型为___________ ;1mol尿素分子中 键的数目为
键的数目为___________ 。
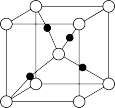
③Cu与O形成的某种化合物的晶胞结构如图所示,若阿伏加德罗常数的值为 ,晶胞的边长为apm,则该晶体的密度为
,晶胞的边长为apm,则该晶体的密度为___________ g/cm3。
(1)甲烷在一定条件下可生成以下微粒:
A.碳正离子(
 ) B.碳负离子(
) B.碳负离子( ) C.甲基(
) C.甲基(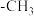 ) D.碳烯(
) D.碳烯(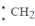 )
)①四种微粒中,键角为120°的是
②碳负离子(
 )的空间构型为
)的空间构型为(2)在制取合成氨原料气的过程中,常混有一些杂质,如CO会使催化剂中毒。除去CO的化学方程式为(HAc表示醋酸)
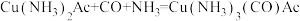 。请回答下列问题:
。请回答下列问题:①该反应中含有的第二周期非金属元素的第一电离能由大到小的顺序为
②在一定条件下NH3和CO2能合成尿素CO(NH2)2,尿素中碳原子轨道的杂化类型为
 键的数目为
键的数目为③Cu与O形成的某种化合物的晶胞结构如图所示,若阿伏加德罗常数的值为
 ,晶胞的边长为apm,则该晶体的密度为
,晶胞的边长为apm,则该晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】E、G、M、Q、T是五种原子序数依次增大的前四周期元素。E、G、M是位于p区的同一周期的元素,M的价层电子排布为ns2np2n,E与M原子核外的未成对电子数相等;QM2与GM2−具有相等的价电子总数;T为过渡元素,其原子核外没有未成对电子。请回答下列问题:
(1)T元素原子的价电子排布式是___ 。
(2)E、G、M三种元素的第一电离能由大到小的顺序为___ (用元素符号表示),其原因为___ 。
(3)G的最简单氢化物的分子立体构型名称为___ ,M的最简单氢化物的分子中中心原子的杂化类型为___ 。M和Q的最简单氢化物的沸点大小顺序为___ (写化学式)。
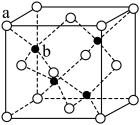
(4)TQ在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方TQ晶体结构如图所示,该晶体的密度为pg·cm−3。如果TQ的摩尔质量为Mg·mol−1,阿伏加 德罗常数为NAmol−1,则a、b之间的距离为___ cm。
(1)T元素原子的价电子排布式是
(2)E、G、M三种元素的第一电离能由大到小的顺序为
(3)G的最简单氢化物的分子立体构型名称为
(4)TQ在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方TQ晶体结构如图所示,该晶体的密度为pg·cm−3。如果TQ的摩尔质量为Mg·mol−1,阿伏加 德罗常数为NAmol−1,则a、b之间的距离为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】A、B、C、D、E、F为前四周期原子序数依次增大的六种元素,已知A元素的某种核素没有中子,B元素基态原子中有3个不同能级且各能级中的电子数相等,D元素的最外层电子数是其电子层数的3倍,E元素的焰色反应呈黄色,F元素是第四周期未成对电子数最多的元素。试回答下列问题:
(1)F原子的价层电子排布式为__________ ,D元素和E元素形成E2D2化学键类型_____ 。
(2)基态原子第一电离能C____ D(“>”或“<”),电负性C____ D(“>”或“<”) 。
(3)CD 中心原子杂化方式
中心原子杂化方式_____ ,CA3立体构型_____ 。
(4)E元素的焰色反应呈黄色,金属元素能产生焰色反应的微观原因为________ 。
(5)已知B元素的某种单质结构如图所示,且晶胞边长为a pm,B原子的摩尔质量为M g/mol,NA为阿伏加德罗常数,则两个最近的B原子之间的距离为__________ pm,该晶体的密度为__________ g/cm3。

(1)F原子的价层电子排布式为
(2)基态原子第一电离能C
(3)CD
 中心原子杂化方式
中心原子杂化方式(4)E元素的焰色反应呈黄色,金属元素能产生焰色反应的微观原因为
(5)已知B元素的某种单质结构如图所示,且晶胞边长为a pm,B原子的摩尔质量为M g/mol,NA为阿伏加德罗常数,则两个最近的B原子之间的距离为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
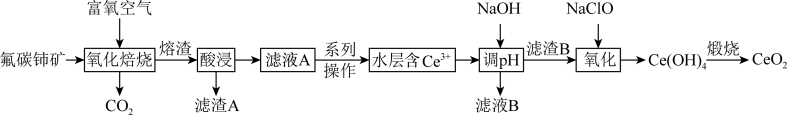
【推荐1】二氧化铈(CeO2)是一种典型的金属氧化物,具有较强的氧化性广泛应用于多相催化反应,并作为汽车尾气净化的三效催化剂的重要组成成分。以氟碳铈矿(主要含CeFCO3、BaO等)为原料制备CeO2的一种工艺流程如下图所示: ;②滤液A中含:
;②滤液A中含: 、
、 等离子。
等离子。
回答下列问题:
(1)滤渣A的主要成分是___________ (填化学式);“酸浸”不用盐酸的理由是_________ (答一点即可)。
(2)“系列操作”包含以下几个过程:已知: 不能溶于有机物TBP;
不能溶于有机物TBP; 能溶于有机物TBP,且存在反应:
能溶于有机物TBP,且存在反应: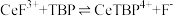 。“滤液A”中加入有机物TBP后的分离方法是
。“滤液A”中加入有机物TBP后的分离方法是___________ ,“有机层B”中发生反应的离子方程式为___________ 。水层中的一种溶质,理论上可以在工艺流程图中的_________ 工序中循环利用,减小“调pH”工序中 的用量,节约生产成本。
的用量,节约生产成本。 沉淀完全(通常认为溶液中离子浓度小于
沉淀完全(通常认为溶液中离子浓度小于 为沉淀完全),应控制pH大于
为沉淀完全),应控制pH大于________ (已知25℃时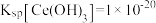 )。
)。
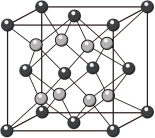
(4)二氧化铈立方晶胞如图所示,则铈原子Ce在晶胞中的位置是________ ;晶体中一个Ce周围与其最近的O的个数为________ 。
 ;②滤液A中含:
;②滤液A中含: 、
、 等离子。
等离子。回答下列问题:
(1)滤渣A的主要成分是
(2)“系列操作”包含以下几个过程:已知:
 不能溶于有机物TBP;
不能溶于有机物TBP; 能溶于有机物TBP,且存在反应:
能溶于有机物TBP,且存在反应: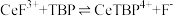 。“滤液A”中加入有机物TBP后的分离方法是
。“滤液A”中加入有机物TBP后的分离方法是 的用量,节约生产成本。
的用量,节约生产成本。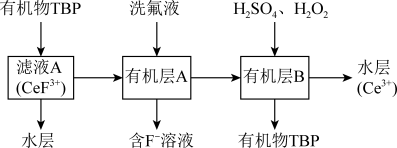
 沉淀完全(通常认为溶液中离子浓度小于
沉淀完全(通常认为溶液中离子浓度小于 为沉淀完全),应控制pH大于
为沉淀完全),应控制pH大于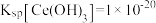 )。
)。(4)二氧化铈立方晶胞如图所示,则铈原子Ce在晶胞中的位置是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】元素是构成我们生活中一切物质的“原材料”。回答下列问题:
(1)(SCN)2中各元素的第一电离能最大的是___________ (填元素符号)。
(2)钛位于元素周期表中的第四周期、第ⅣB族。
①六氟合钛酸钾(K2TiF6)中存在[TiF6]2-,该晶体中不存在的化学键有___________ (填字母序号)。
a.离子键 b.极性键 c.非极性键 d配位键
②纳米TiO2是一种应用广泛的催化剂,其催化的一个实例如下:

有机物甲中标“*”碳原子的杂化方式为___________ 。有机物乙的沸点___________ (填“高于”或“低于”)有机物甲,主要原因为___________ 。
(3)在乙醚溶液中,InCl3与LiH反应生成LiInH4和某物质,该反应的化学方程式为___________ ,LiInH4中阴离子的空间结构为___________ 形。
(4)氯化锂的晶胞如图所示,氯化锂晶体密度为ρg/cm3。设NA为阿伏加德罗常数的值,该晶体中相邻锂原子间的最短距离为___________ cm(列出计算式)。

(1)(SCN)2中各元素的第一电离能最大的是
(2)钛位于元素周期表中的第四周期、第ⅣB族。
①六氟合钛酸钾(K2TiF6)中存在[TiF6]2-,该晶体中不存在的化学键有
a.离子键 b.极性键 c.非极性键 d配位键
②纳米TiO2是一种应用广泛的催化剂,其催化的一个实例如下:

有机物甲中标“*”碳原子的杂化方式为
(3)在乙醚溶液中,InCl3与LiH反应生成LiInH4和某物质,该反应的化学方程式为
(4)氯化锂的晶胞如图所示,氯化锂晶体密度为ρg/cm3。设NA为阿伏加德罗常数的值,该晶体中相邻锂原子间的最短距离为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】著名化学家徐光宪在稀土化学等领域取得了卓越成就,被誉为“稀土界的袁隆平”。稀土元素包括钪、钇和镧系元素。请回答下列问题:
(1)写出基态Sc原子的核外电子排布式_________ ,其中电子占据的轨道数目为_________ 。
(2)在用重量法测定镧系元素和使镧系元素分离时,总是使之先转换成草酸盐,然后经过灼烧而得其氧化物,如2LnCl3+3H2C2O4+nH2O=Ln2(C2O4)3·nH2O+6HCl。
①HOOC-COOH中碳原子的杂化轨道类型为____ ,其中H、C、O的电负性由大到小的顺序为____ 。
②H2O的VSEPR模型为_____ ,写出与H2O互为等电子体的一种阴离子的化学式_____ 。
③HCl和H2O可以形成相对稳定的水合氢离子盐晶体,如HCl·2H2O,HCl·2H2O中含有H5O ,结构为
,结构为 ,在该离子中,存在的作用力有
,在该离子中,存在的作用力有__________ 。
a.配位键 b.极性键 c.非极性键 d.离子键 e.金属键 f.氢键 g.范德华力 h.π键 i.σ键
(3)据报道,在MnO2的催化下,甲醛(HCHO)可被氧化成CO2,则甲醛(HCHO)中的键角____ CO2中的键角(填“=”“>”或“<”)
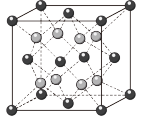
(4)PrO2(二氧化镨)的晶胞结构与CaF2相似,晶胞中Pr(镨)原子位于面心和顶点。Pr(镨)的配位数________ 。假设相距最近的Pr原子与O原子之间的距离为a pm,则该晶体的密度为____ g⋅cm−3(用NA表示阿伏加 德罗常数的值,不必计算出结果)。已知M(Pr)=141g/mol,M(O)=16g/mol
(1)写出基态Sc原子的核外电子排布式
(2)在用重量法测定镧系元素和使镧系元素分离时,总是使之先转换成草酸盐,然后经过灼烧而得其氧化物,如2LnCl3+3H2C2O4+nH2O=Ln2(C2O4)3·nH2O+6HCl。
①HOOC-COOH中碳原子的杂化轨道类型为
②H2O的VSEPR模型为
③HCl和H2O可以形成相对稳定的水合氢离子盐晶体,如HCl·2H2O,HCl·2H2O中含有H5O
 ,结构为
,结构为 ,在该离子中,存在的作用力有
,在该离子中,存在的作用力有a.配位键 b.极性键 c.非极性键 d.离子键 e.金属键 f.氢键 g.范德华力 h.π键 i.σ键
(3)据报道,在MnO2的催化下,甲醛(HCHO)可被氧化成CO2,则甲醛(HCHO)中的键角
(4)PrO2(二氧化镨)的晶胞结构与CaF2相似,晶胞中Pr(镨)原子位于面心和顶点。Pr(镨)的配位数

您最近一年使用:0次



