甲硅烷广泛用于电子工业、汽车领域,三氯氢硅( )是制备甲硅烷的重要原料。回答下列问题:
)是制备甲硅烷的重要原料。回答下列问题:
(1)工业上以硅粉和氯化氢气体为原料生产 时伴随发生的反应有:
时伴随发生的反应有:
①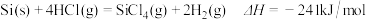
②
以硅粉和氯化氢气体生产 的热化学方程式是
的热化学方程式是_______________________ 。
(2)工业上可用四氯化硅和氢化铝锂( )制甲硅烷,反应后得甲硅烷及两种盐。该反应的化学方程式为
)制甲硅烷,反应后得甲硅烷及两种盐。该反应的化学方程式为_________________________________________________ 。
(3)三氯氢硅歧化也可制得甲硅烷。反应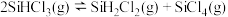 为歧化制甲硅烷过程的关键步骤,此反应采用一定量的
为歧化制甲硅烷过程的关键步骤,此反应采用一定量的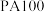 催化剂,在不同反应温度下测得
催化剂,在不同反应温度下测得 的转化率随时间的变化关系如图所示。
的转化率随时间的变化关系如图所示。
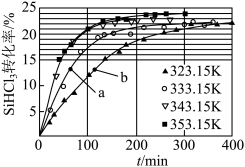
① 时,平衡转化率为
时,平衡转化率为_________ 。该反应是__________ 反应(填“放热”或“吸热”)。
② 时,要缩短反应达到平衡的时间,可采取的措施有
时,要缩短反应达到平衡的时间,可采取的措施有________________________ 。(答一种即可)
③比较a、b处反应速率的大小:
_______________ 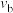 (填“>”“<”或“=”)。已知反应速率
(填“>”“<”或“=”)。已知反应速率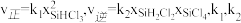 分别是正、逆反应的速率常数,与反应温度有关,x为物质的量分数,则在
分别是正、逆反应的速率常数,与反应温度有关,x为物质的量分数,则在 时
时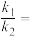
___________ (保留3位小数)。
 )是制备甲硅烷的重要原料。回答下列问题:
)是制备甲硅烷的重要原料。回答下列问题:(1)工业上以硅粉和氯化氢气体为原料生产
 时伴随发生的反应有:
时伴随发生的反应有:①
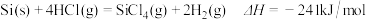
②

以硅粉和氯化氢气体生产
 的热化学方程式是
的热化学方程式是(2)工业上可用四氯化硅和氢化铝锂(
 )制甲硅烷,反应后得甲硅烷及两种盐。该反应的化学方程式为
)制甲硅烷,反应后得甲硅烷及两种盐。该反应的化学方程式为(3)三氯氢硅歧化也可制得甲硅烷。反应
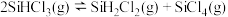 为歧化制甲硅烷过程的关键步骤,此反应采用一定量的
为歧化制甲硅烷过程的关键步骤,此反应采用一定量的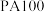 催化剂,在不同反应温度下测得
催化剂,在不同反应温度下测得 的转化率随时间的变化关系如图所示。
的转化率随时间的变化关系如图所示。
①
 时,平衡转化率为
时,平衡转化率为②
 时,要缩短反应达到平衡的时间,可采取的措施有
时,要缩短反应达到平衡的时间,可采取的措施有③比较a、b处反应速率的大小:

 (填“>”“<”或“=”)。已知反应速率
(填“>”“<”或“=”)。已知反应速率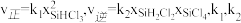 分别是正、逆反应的速率常数,与反应温度有关,x为物质的量分数,则在
分别是正、逆反应的速率常数,与反应温度有关,x为物质的量分数,则在 时
时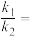
2020·四川绵阳·二模 查看更多[5]
2019年四川省绵阳市高三第二次诊断性考试理综化学试题2020届高三《新题速递·化学》1月第02期(考点11-13)陕西省西安中学2020届高三第三次模拟考试化学试题甘肃省天水市第一中学2020届高三下学期诊断考试化学试题(已下线)第04练 化学平衡-2022年【寒假分层作业】高二化学(人教版2019选择性必修1)
更新时间:2020-03-26 14:57:26
|
相似题推荐
【推荐1】“低碳经济”已成为全世界科学家研究的重要课题。为减小和消除 CO2对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对 CO2 创新利用的研究。
(1)已知:①CO(g)+H2O(g) H2(g)+CO2(g) △H=-41kJ/mol
H2(g)+CO2(g) △H=-41kJ/mol
②C(s)+2H2(g) CH4(g) △H=-73kJ/mol
CH4(g) △H=-73kJ/mol
③2CO(g) C(s)+CO2(g) △H=-171kJ/mol
C(s)+CO2(g) △H=-171kJ/mol
写出CO2与H2反应生成CH4和H2O(g)的热化学方程式:_____ 。
(2)目前工业上有一种方法是用 CO2来生产燃料甲醇。为探究该反应原理,在容积为 2L密闭容器中,充入1molCO2和 3.25molH2在一定条件下发生反应,测得 CO2、CH3OH(g)和 H2O(g)的物质的量(n)随时间的变化如图所示:
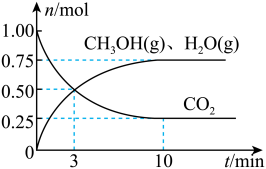
①从反应开始到平衡,氢气的平均反应速率v(H2)=____ 。
②下列措施一定不能使CO2的平衡转化率增大的是____ (填字母)。
A.在原容器中再充入1molCO2
B.在原容器中再充入1molH2
C.在原容器中充入1mol氦气
D.使用更有效的催化剂
E.缩小容器的容积
F.将水蒸气从体系中分离
(3)煤化工通常研究不同条件下CO转化率以解决实际问题。已知在催化剂存在条件下反应:CO(g)+H2O(g)⇌H2(g)+CO2(g)的平衡转化率随p(H2O)/p(CO)及温度变化关系如图所示:
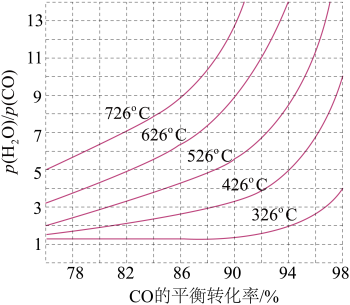
①上述反应的正反应方向是____ (填“吸热”或“放热”)反应;
②对于气相反应,用某组分(B)的平衡压强(pB)代替物质的量浓度(cB)也可以表示平衡常数(记作 Kp),则在恒温密闭容器中,该反应的Kp与Kc的关系是_______ ,如果提高p(H2O)/p(CO),则Kp_______ (填“变大”“变小”或“不变”);使用铁镁催化剂的实际工业流程中,一般采用400℃左右,p(H2O)/p(CO) =3~5,采取此条件的原因可能是 _________ 。
(4)科学家用氮化镓材料与铜组装成如图所示的人工光合系统,利用该装置实现了用CO2和H2O合成CH4。下列关于该电池的叙述正确的是____ (填字母)。
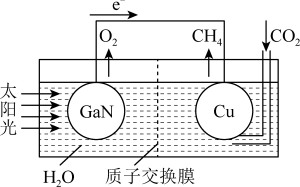
A.该装置能量转化形式仅存在太阳能转化为电能
B.铜电极为正极,电极反应式为CO2+8e-+8H+=CH4+2H2O
C.电池内部H+透过质子交换膜从左向右移动
D.反应结束后,理论上溶液的 pH 值保持不变
(1)已知:①CO(g)+H2O(g)
 H2(g)+CO2(g) △H=-41kJ/mol
H2(g)+CO2(g) △H=-41kJ/mol②C(s)+2H2(g)
 CH4(g) △H=-73kJ/mol
CH4(g) △H=-73kJ/mol③2CO(g)
 C(s)+CO2(g) △H=-171kJ/mol
C(s)+CO2(g) △H=-171kJ/mol写出CO2与H2反应生成CH4和H2O(g)的热化学方程式:
(2)目前工业上有一种方法是用 CO2来生产燃料甲醇。为探究该反应原理,在容积为 2L密闭容器中,充入1molCO2和 3.25molH2在一定条件下发生反应,测得 CO2、CH3OH(g)和 H2O(g)的物质的量(n)随时间的变化如图所示:

①从反应开始到平衡,氢气的平均反应速率v(H2)=
②下列措施一定不能使CO2的平衡转化率增大的是
A.在原容器中再充入1molCO2
B.在原容器中再充入1molH2
C.在原容器中充入1mol氦气
D.使用更有效的催化剂
E.缩小容器的容积
F.将水蒸气从体系中分离
(3)煤化工通常研究不同条件下CO转化率以解决实际问题。已知在催化剂存在条件下反应:CO(g)+H2O(g)⇌H2(g)+CO2(g)的平衡转化率随p(H2O)/p(CO)及温度变化关系如图所示:

①上述反应的正反应方向是
②对于气相反应,用某组分(B)的平衡压强(pB)代替物质的量浓度(cB)也可以表示平衡常数(记作 Kp),则在恒温密闭容器中,该反应的Kp与Kc的关系是
(4)科学家用氮化镓材料与铜组装成如图所示的人工光合系统,利用该装置实现了用CO2和H2O合成CH4。下列关于该电池的叙述正确的是

A.该装置能量转化形式仅存在太阳能转化为电能
B.铜电极为正极,电极反应式为CO2+8e-+8H+=CH4+2H2O
C.电池内部H+透过质子交换膜从左向右移动
D.反应结束后,理论上溶液的 pH 值保持不变
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】Ⅰ、氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要的作用。
(1)下图是 和
和 反应生成
反应生成 过程中能量的变化示意图,请写出
过程中能量的变化示意图,请写出 和
和 反应的热化学方程式:
反应的热化学方程式:_____ 。

(2)若已知下列数据:
试根据表中及图中数据计算 的键能:
的键能:_____  。
。
Ⅱ、我国力争于2030年前做到碳达峰,2060年前实现碳中和。 与
与 重整是
重整是 利用的研究热点之一。该重整反应体系主要涉及以下反应:
利用的研究热点之一。该重整反应体系主要涉及以下反应:
a)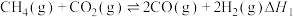
b)
c)
d)
e)
(3)根据盖斯定律,反应 的
的
_____ (写出一个代数式即可)。
(4)上述反应体系在一定条件下建立平衡后,下列说法正确的有_____。
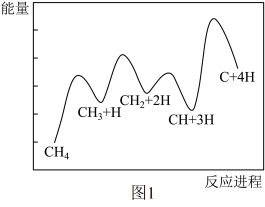
(5)一定条件下, 分解形成碳的反应历程如图1所示。该历程分
分解形成碳的反应历程如图1所示。该历程分_____ 步进行,其中,第_____ 步的正反应活化能最大。
(6)设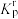 为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为
为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为 )除以
)除以 。反应a、c、e的
。反应a、c、e的 随
随 (温度的倒数)的变化如图2所示。
(温度的倒数)的变化如图2所示。
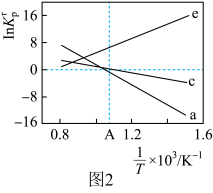
①反应a、c、e中,属于吸热反应的有_____ (填字母)。
②反应c的相对压力平衡常数表达式为
_____ 。
③在图2中 点对应温度下、原料组成为
点对应温度下、原料组成为 、初始总压为
、初始总压为 的恒容密闭容器中进行反应,体系达到平衡时
的恒容密闭容器中进行反应,体系达到平衡时 的分压为
的分压为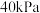 。计算
。计算 的平衡转化率等于
的平衡转化率等于_____
(7) 用途广泛,写出基于其物理性质的一种用途:
用途广泛,写出基于其物理性质的一种用途:_____ 。
(1)下图是
 和
和 反应生成
反应生成 过程中能量的变化示意图,请写出
过程中能量的变化示意图,请写出 和
和 反应的热化学方程式:
反应的热化学方程式:
(2)若已知下列数据:
| 化学键 |  |  |
键能 | 435 | 943 |
 的键能:
的键能: 。
。Ⅱ、我国力争于2030年前做到碳达峰,2060年前实现碳中和。
 与
与 重整是
重整是 利用的研究热点之一。该重整反应体系主要涉及以下反应:
利用的研究热点之一。该重整反应体系主要涉及以下反应:a)
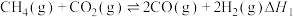
b)

c)

d)

e)

(3)根据盖斯定律,反应
 的
的
(4)上述反应体系在一定条件下建立平衡后,下列说法正确的有_____。
A.增大 与 与 的浓度,反应 的浓度,反应 的正反应速率都增加 的正反应速率都增加 |
B.移去部分 ,反应 ,反应 的平衡均向右移动 的平衡均向右移动 |
C.加入反应 的催化剂,可提高 的催化剂,可提高 的平衡转化率 的平衡转化率 |
| D.降低反应温度,反应a~e的正、逆反应速率都减小 |
(5)一定条件下,
 分解形成碳的反应历程如图1所示。该历程分
分解形成碳的反应历程如图1所示。该历程分
(6)设
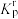 为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为
为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为 )除以
)除以 。反应a、c、e的
。反应a、c、e的 随
随 (温度的倒数)的变化如图2所示。
(温度的倒数)的变化如图2所示。
①反应a、c、e中,属于吸热反应的有
②反应c的相对压力平衡常数表达式为

③在图2中
 点对应温度下、原料组成为
点对应温度下、原料组成为 、初始总压为
、初始总压为 的恒容密闭容器中进行反应,体系达到平衡时
的恒容密闭容器中进行反应,体系达到平衡时 的分压为
的分压为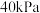 。计算
。计算 的平衡转化率等于
的平衡转化率等于(7)
 用途广泛,写出基于其物理性质的一种用途:
用途广泛,写出基于其物理性质的一种用途:
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐3】氢能是一种绿色能源,研发新型制氢技术具有重要意义。
(1)甘油 、水蒸气、氧气自热式催化重整制氢时无需加热,主要反应如下:
、水蒸气、氧气自热式催化重整制氢时无需加热,主要反应如下:
反应I: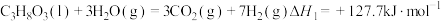
反应Ⅱ: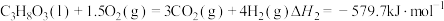
①
___________ 。
②除 外,可能还会产生
外,可能还会产生 等副产物,为了提高原子利用率,最需要抑制
等副产物,为了提高原子利用率,最需要抑制 的生成,原因是
的生成,原因是___________ 。
(2)“表面改性铝粉分解水制氢”因 储量丰富和较强的还原活性得到广泛应用。铝粉表面的致密氧化膜是影响
储量丰富和较强的还原活性得到广泛应用。铝粉表面的致密氧化膜是影响 还原活性的主要因素,工业上常用
还原活性的主要因素,工业上常用 溶液或锡酸钠
溶液或锡酸钠 溶液作为
溶液作为 粉的改性试剂。已知:
粉的改性试剂。已知: 。
。
①利用 溶液改性
溶液改性 粉的原理可用化学方程式表示为
粉的原理可用化学方程式表示为___________ 。
② 下,向两份质量和粒径均相同的
下,向两份质量和粒径均相同的 粉中,分别加入等体积
粉中,分别加入等体积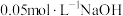 溶液和
溶液和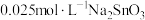 溶液来改性
溶液来改性 粉,氢气产率随时间的变化关系如图1所示。
粉,氢气产率随时间的变化关系如图1所示。 溶液改性效果明显优于
溶液改性效果明显优于 溶液的可能原因是
溶液的可能原因是___________ 。 溶液浓度的变化关系如图2所示。当
溶液浓度的变化关系如图2所示。当 溶液浓度为
溶液浓度为 时,氢气产率接近
时,氢气产率接近 。但
。但 溶液过大或过小会大大降低氢气产率,其可能原因分别是
溶液过大或过小会大大降低氢气产率,其可能原因分别是___________ 。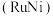 催化氨硼烷水解制氢”主要经过吸附和还原的过程,其反应机理如图所示(每个步骤只画出了可能参与该步反应的1个水分子,氨硼烷中与
催化氨硼烷水解制氢”主要经过吸附和还原的过程,其反应机理如图所示(每个步骤只画出了可能参与该步反应的1个水分子,氨硼烷中与 原子相连的3个
原子相连的3个 原子分别用
原子分别用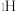 、
、 和
和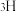 标记)。根据元素电负性的变化规律推测题图的虚线框内微粒
标记)。根据元素电负性的变化规律推测题图的虚线框内微粒 和
和 的化学式分别为
的化学式分别为___________ ;步骤Ⅱ可描述为___________ 。
(1)甘油
 、水蒸气、氧气自热式催化重整制氢时无需加热,主要反应如下:
、水蒸气、氧气自热式催化重整制氢时无需加热,主要反应如下:反应I:
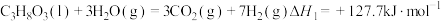
反应Ⅱ:
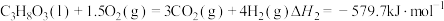
①

②除
 外,可能还会产生
外,可能还会产生 等副产物,为了提高原子利用率,最需要抑制
等副产物,为了提高原子利用率,最需要抑制 的生成,原因是
的生成,原因是(2)“表面改性铝粉分解水制氢”因
 储量丰富和较强的还原活性得到广泛应用。铝粉表面的致密氧化膜是影响
储量丰富和较强的还原活性得到广泛应用。铝粉表面的致密氧化膜是影响 还原活性的主要因素,工业上常用
还原活性的主要因素,工业上常用 溶液或锡酸钠
溶液或锡酸钠 溶液作为
溶液作为 粉的改性试剂。已知:
粉的改性试剂。已知: 。
。①利用
 溶液改性
溶液改性 粉的原理可用化学方程式表示为
粉的原理可用化学方程式表示为②
 下,向两份质量和粒径均相同的
下,向两份质量和粒径均相同的 粉中,分别加入等体积
粉中,分别加入等体积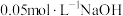 溶液和
溶液和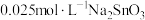 溶液来改性
溶液来改性 粉,氢气产率随时间的变化关系如图1所示。
粉,氢气产率随时间的变化关系如图1所示。 溶液改性效果明显优于
溶液改性效果明显优于 溶液的可能原因是
溶液的可能原因是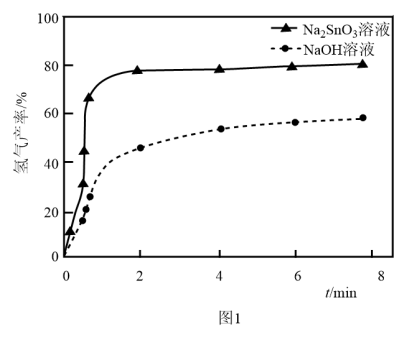
 溶液浓度的变化关系如图2所示。当
溶液浓度的变化关系如图2所示。当 溶液浓度为
溶液浓度为 时,氢气产率接近
时,氢气产率接近 。但
。但 溶液过大或过小会大大降低氢气产率,其可能原因分别是
溶液过大或过小会大大降低氢气产率,其可能原因分别是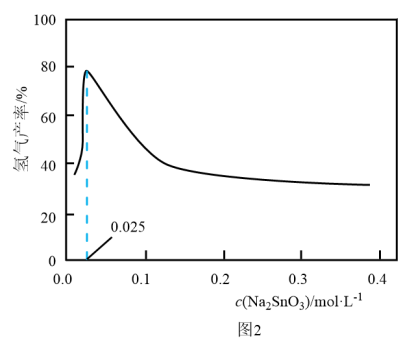
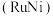 催化氨硼烷水解制氢”主要经过吸附和还原的过程,其反应机理如图所示(每个步骤只画出了可能参与该步反应的1个水分子,氨硼烷中与
催化氨硼烷水解制氢”主要经过吸附和还原的过程,其反应机理如图所示(每个步骤只画出了可能参与该步反应的1个水分子,氨硼烷中与 原子相连的3个
原子相连的3个 原子分别用
原子分别用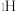 、
、 和
和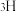 标记)。根据元素电负性的变化规律推测题图的虚线框内微粒
标记)。根据元素电负性的变化规律推测题图的虚线框内微粒 和
和 的化学式分别为
的化学式分别为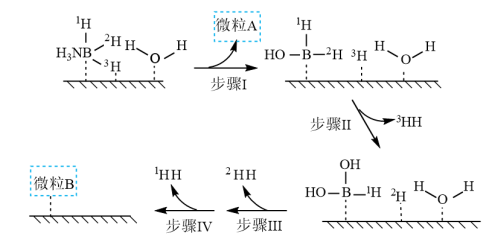
您最近一年使用:0次
【推荐1】完成下列问题
(1)已知:
反应Ⅰ:N2(g)+O2(g) 2NO(g) ΔH1=akJ/mol
2NO(g) ΔH1=akJ/mol
反应Ⅱ;2NO(g)+O2(g) 2NO2(g) ΔH2=bkJ/mol
2NO2(g) ΔH2=bkJ/mol
反应Ⅲ:2N2O(g) 2N2(g)+O2(g) ΔH3=ckJ/mol
2N2(g)+O2(g) ΔH3=ckJ/mol
反应Ⅳ:N2O(g)+NO2(g) 3NO(g) ΔH=
3NO(g) ΔH=___________ kJ/mol
(2)汽车尾气中的NO和CO可在催化剂作用下生成无污染的气体。在密闭容器中充入反应物,测得平衡时NO的体积分数与温度、压强的关系如图。
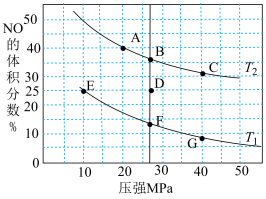
①反应2NO(g)+2CO(g) N2(g)+2CO2(g) ΔH<0,则T1
N2(g)+2CO2(g) ΔH<0,则T1___________ T2(填“>”“=”或“<”)
②该反应达到平衡后,为同时提高反应速率和NO的转化率,可采取的措施有___________ (答两点即可)。
③在D点,对反应容器降温的同时缩小体积至体系压强增大,重新达到的平衡状态可能是图中A~G点中的___________ 点。
(3)在催化剂作用下,利用反应C(s)+2NO(g) N2(g)+CO2(g) ΔH=-34.0kJ/mol,用活性炭对NO进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒容,在相同时间内测得NO的转化率随温度的变化如图所示:
N2(g)+CO2(g) ΔH=-34.0kJ/mol,用活性炭对NO进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒容,在相同时间内测得NO的转化率随温度的变化如图所示:
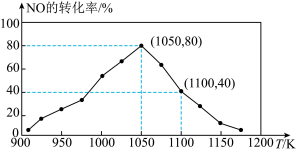
①由图可知,1050K前反应中NO的转化率随温度升高而增大,其原因为___________ ;在1050K时,CO2的体积分数为___________ 。
②用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数(记作Kp)。在1100K、1.1×106Pa时,该反应的化学平衡常数Kp=___________ [已知:气体分压(P分)=气体总压(Pa)×体积分数]。
(4)含铈溶液可以处理大气中的氮氧化物,并可通过电解法再生。铈元素(Ce)常见的化合价有+3价、+4价。NO可以被含Ce4+的溶液吸收,生成等物质的量的 、
、 。可采用电解法将上述吸收液中等物质的量
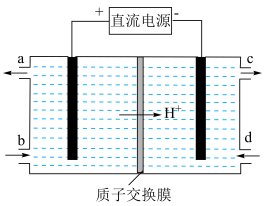
。可采用电解法将上述吸收液中等物质的量 、
、 转化为无毒物质,其原理如图所示。阴极的电极反应式为
转化为无毒物质,其原理如图所示。阴极的电极反应式为___________ 。
(1)已知:
反应Ⅰ:N2(g)+O2(g)
 2NO(g) ΔH1=akJ/mol
2NO(g) ΔH1=akJ/mol反应Ⅱ;2NO(g)+O2(g)
 2NO2(g) ΔH2=bkJ/mol
2NO2(g) ΔH2=bkJ/mol反应Ⅲ:2N2O(g)
 2N2(g)+O2(g) ΔH3=ckJ/mol
2N2(g)+O2(g) ΔH3=ckJ/mol反应Ⅳ:N2O(g)+NO2(g)
 3NO(g) ΔH=
3NO(g) ΔH=(2)汽车尾气中的NO和CO可在催化剂作用下生成无污染的气体。在密闭容器中充入反应物,测得平衡时NO的体积分数与温度、压强的关系如图。

①反应2NO(g)+2CO(g)
 N2(g)+2CO2(g) ΔH<0,则T1
N2(g)+2CO2(g) ΔH<0,则T1②该反应达到平衡后,为同时提高反应速率和NO的转化率,可采取的措施有
③在D点,对反应容器降温的同时缩小体积至体系压强增大,重新达到的平衡状态可能是图中A~G点中的
(3)在催化剂作用下,利用反应C(s)+2NO(g)
 N2(g)+CO2(g) ΔH=-34.0kJ/mol,用活性炭对NO进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒容,在相同时间内测得NO的转化率随温度的变化如图所示:
N2(g)+CO2(g) ΔH=-34.0kJ/mol,用活性炭对NO进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒容,在相同时间内测得NO的转化率随温度的变化如图所示:
①由图可知,1050K前反应中NO的转化率随温度升高而增大,其原因为
②用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数(记作Kp)。在1100K、1.1×106Pa时,该反应的化学平衡常数Kp=
(4)含铈溶液可以处理大气中的氮氧化物,并可通过电解法再生。铈元素(Ce)常见的化合价有+3价、+4价。NO可以被含Ce4+的溶液吸收,生成等物质的量的
 、
、 。可采用电解法将上述吸收液中等物质的量
。可采用电解法将上述吸收液中等物质的量 、
、 转化为无毒物质,其原理如图所示。阴极的电极反应式为
转化为无毒物质,其原理如图所示。阴极的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐2】“事物的双方既相互对立又相互统一”的哲学观点在化学中有着诸多体现。
Ⅰ.硫和氮两种元素与人们的生活密切相关,自然界中硫、氮的循环是维持生态平衡的重要物质基础。
(1)下列说法错误的是______(填标号)。
(2)一种具有高弹性的自修复聚氨酯材料(TPU)结构如下:
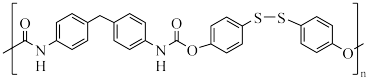
该聚合物由X(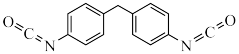 )和Y(
)和Y(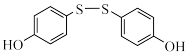 )聚合而成,下列说法正确的是______(填标号)。
)聚合而成,下列说法正确的是______(填标号)。
Ⅱ.含硫、氮物质的使用在为人类带来益处的同时,也给人们带来了一些困扰。利用化学原理处理含硫、氮的废气、废液等具有重要意义。
(3)二氧化氯(ClO2)可用于烟气中SO2和NO的脱除。研究发现ClO2氧化SO2和NO时涉及以下基元反应。
脱硝:ⅰ

ⅱ
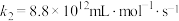
脱硫:ⅲ

ⅳ

其中k为速率常数。对于基元反应: ,其速率方程表达式为
,其速率方程表达式为
实验测得:ClO2分别单独氧化纯SO2、纯NO以及同时氧化二者混合物的氧化率随时间(t)的变化情况如图所示。

①其它因素都相同时,ClO2氧化SO2的活化能______ (填“>”或“<”)ClO2氧化NO的活化能。
②请结合ⅰ、ⅲ、ⅳ的速率常数,判断NO的存在是否会影响ClO2氧化SO2的速率并说明理由:______ 。
(4)CO也可以与NO反应生成无污染物: 。
。
已知:ⅰ 在浓度平衡常数表达式中,用相对分压代替浓度,可得到相对压力平衡常数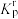 。
。
ⅱ 气体的相对分压等于其分压(单位为kPa)除以 (
(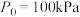 )。
)。
在某温度下,原料组成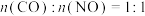 ,初始总压为100 kPa的恒容容器中进行上述反应,达到平衡时CO2的分压为40 kPa,则该反应的相对压力平衡常数
,初始总压为100 kPa的恒容容器中进行上述反应,达到平衡时CO2的分压为40 kPa,则该反应的相对压力平衡常数
______ 。
(5)污水中的硝基苯可用铁炭混合物在酸性条件下处理。硝基苯转化过程如下:

①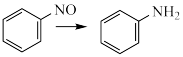 的电极反应式为
的电极反应式为______ 。
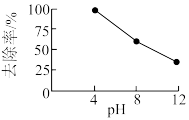
②其他条件一定,相同时间内,硝基苯的去除率与pH的关系如图所示。pH越大,硝基苯的去除率越低的原因可能是______ 。
Ⅰ.硫和氮两种元素与人们的生活密切相关,自然界中硫、氮的循环是维持生态平衡的重要物质基础。
(1)下列说法错误的是______(填标号)。
| A.合成氨很大程度上解决了地球上因粮食不足而导致的饥饿问题 |
| B.组成生命体的蛋白质中含有硫和氮 |
| C.豆科植物的根瘤菌可实现自然固氮 |
| D.二氧化硫有毒,不可用作食品添加剂 |
(2)一种具有高弹性的自修复聚氨酯材料(TPU)结构如下:

该聚合物由X(
 )和Y(
)和Y( )聚合而成,下列说法正确的是______(填标号)。
)聚合而成,下列说法正确的是______(填标号)。| A.X中碳氧双键比碳氮双键更容易与Y发生反应 |
| B.生成该聚合物反应的原子利用率为100% |
| C.其自修复性可能与—S—S—有关 |
| D.废弃的聚合物直接焚烧处理即可 |
Ⅱ.含硫、氮物质的使用在为人类带来益处的同时,也给人们带来了一些困扰。利用化学原理处理含硫、氮的废气、废液等具有重要意义。
(3)二氧化氯(ClO2)可用于烟气中SO2和NO的脱除。研究发现ClO2氧化SO2和NO时涉及以下基元反应。
脱硝:ⅰ


ⅱ

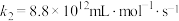
脱硫:ⅲ


ⅳ


其中k为速率常数。对于基元反应:
 ,其速率方程表达式为
,其速率方程表达式为
实验测得:ClO2分别单独氧化纯SO2、纯NO以及同时氧化二者混合物的氧化率随时间(t)的变化情况如图所示。

①其它因素都相同时,ClO2氧化SO2的活化能
②请结合ⅰ、ⅲ、ⅳ的速率常数,判断NO的存在是否会影响ClO2氧化SO2的速率并说明理由:
(4)CO也可以与NO反应生成无污染物:
 。
。已知:ⅰ 在浓度平衡常数表达式中,用相对分压代替浓度,可得到相对压力平衡常数
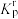 。
。ⅱ 气体的相对分压等于其分压(单位为kPa)除以
 (
(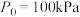 )。
)。在某温度下,原料组成
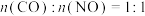 ,初始总压为100 kPa的恒容容器中进行上述反应,达到平衡时CO2的分压为40 kPa,则该反应的相对压力平衡常数
,初始总压为100 kPa的恒容容器中进行上述反应,达到平衡时CO2的分压为40 kPa,则该反应的相对压力平衡常数
(5)污水中的硝基苯可用铁炭混合物在酸性条件下处理。硝基苯转化过程如下:

①
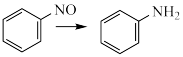 的电极反应式为
的电极反应式为②其他条件一定,相同时间内,硝基苯的去除率与pH的关系如图所示。pH越大,硝基苯的去除率越低的原因可能是

您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】我国科学家成功利用光伏发电,将电解水获得的H2与CO2反应合成甲醇,再由甲醇经若干酶促反应合成淀粉。该研究成果已在国际学术期刊《科学》上发表。回答下列问题:
(1)CO2人工合成转化为淀粉只需要11步,其中前两步涉及的反应如图1所示。 H=
H=___________ (用含 H1、
H1、 H2、
H2、 H3、
H3、 H4的代数式表示)。
H4的代数式表示)。
(2)有学者结合实验和计算机模拟结果,得出CO2(g)+H2(g) CO(g)+H2O(g)的一种反应历程如图2所示,其中吸附在催化剂表面的物种用“·”标注,TS1、TS2、TS3、TS4均为过渡态。决速步骤对应的化学方程式为
CO(g)+H2O(g)的一种反应历程如图2所示,其中吸附在催化剂表面的物种用“·”标注,TS1、TS2、TS3、TS4均为过渡态。决速步骤对应的化学方程式为___________ ;TS3对应的步骤适合在___________ (填“高温”或“低温”)条件下进行。 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)  H<0,在催化剂作用下单位时间内CO2的转化率与温度、催化剂的关系如图3所示。
H<0,在催化剂作用下单位时间内CO2的转化率与温度、催化剂的关系如图3所示。___________ (填“>”“<”或“=”,下同)CH3OH的消耗速率;催化效率:Cat2___________ Cat1。
②b点之后CO2的转化率降低,可能的原因是___________ 。
(4)已知CO2催化加氢的主要反应如下:
反应I.CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
反应II.CO2(g)+H2(g) CO(g)+H2O(g)
CO(g)+H2O(g)
①230℃时,将CO2和H2按物质的量之比为1:3混合通入恒温刚性密闭容器中,在催化剂作用下同时发生反应I和反应II,容器内压强随时间的变化如下表所示。
平衡时p(CO2)=0.1p0,则该温度下反应I的化学平衡常数Kp=___________ MPa-2(用含p0的代数式表示)。
②二氧化碳催化加氢合成甲醇反应往往伴随副反应II。一定温度和压强条件下,为了提高反应速率和甲醇选择性,应当___________ 。
(5)铜(Cu)是CO2催化加氢催化剂中的一种成份。已知Cu属于立方晶系,晶胞参数为anm,密度为dg·cm-3,则Cu晶胞中含有Cu原子数为___________ (用含a、d、NA的式子表示,NA表示阿伏加德罗常数的值)。
(1)CO2人工合成转化为淀粉只需要11步,其中前两步涉及的反应如图1所示。

 H=
H= H1、
H1、 H2、
H2、 H3、
H3、 H4的代数式表示)。
H4的代数式表示)。(2)有学者结合实验和计算机模拟结果,得出CO2(g)+H2(g)
 CO(g)+H2O(g)的一种反应历程如图2所示,其中吸附在催化剂表面的物种用“·”标注,TS1、TS2、TS3、TS4均为过渡态。决速步骤对应的化学方程式为
CO(g)+H2O(g)的一种反应历程如图2所示,其中吸附在催化剂表面的物种用“·”标注,TS1、TS2、TS3、TS4均为过渡态。决速步骤对应的化学方程式为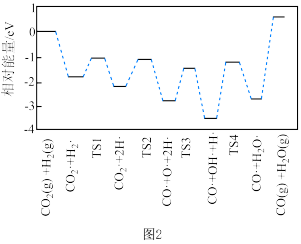
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)  H<0,在催化剂作用下单位时间内CO2的转化率与温度、催化剂的关系如图3所示。
H<0,在催化剂作用下单位时间内CO2的转化率与温度、催化剂的关系如图3所示。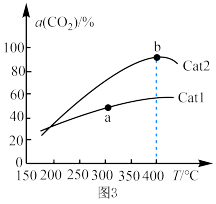
②b点之后CO2的转化率降低,可能的原因是
(4)已知CO2催化加氢的主要反应如下:
反应I.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)反应II.CO2(g)+H2(g)
 CO(g)+H2O(g)
CO(g)+H2O(g)①230℃时,将CO2和H2按物质的量之比为1:3混合通入恒温刚性密闭容器中,在催化剂作用下同时发生反应I和反应II,容器内压强随时间的变化如下表所示。
| 时间/min | 0 | 20 | 40 | 60 | 80 |
| 压强/MPa |  | 0.95 | 0.92 | 0.90 | 0.90 |
②二氧化碳催化加氢合成甲醇反应往往伴随副反应II。一定温度和压强条件下,为了提高反应速率和甲醇选择性,应当
(5)铜(Cu)是CO2催化加氢催化剂中的一种成份。已知Cu属于立方晶系,晶胞参数为anm,密度为dg·cm-3,则Cu晶胞中含有Cu原子数为
您最近一年使用:0次
【推荐1】我国将力争2030年前实现碳达峰、2060年前实现碳中和,是党中央经过深思熟虑做出的重要决策,事关中华民族永续发展和构建人类命运共同体。研究CO2的综合利用对促进“低碳经济”的发展有重要意义。
I.利用二氧化碳催化加氢制甲醇。回答下列问题:
某温度下,二氧化碳与氢气反应制甲醇的总反应为 ,
,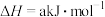 。
。
(1)已知 、
、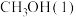 的燃烧热分别为
的燃烧热分别为 、
、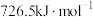 ,且
,且
 ,则
,则
_____ 。
在体积为4.0L的密闭容器中充入0.8molCO2和2.0molH2,发生反应CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH<0,测得CO2、CH3OH的物质的量随时间变化如图:
CH3OH(g)+H2O(g) ΔH<0,测得CO2、CH3OH的物质的量随时间变化如图:
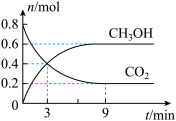
(2) 时间段内,
时间段内, 的平均反应速率为
的平均反应速率为_____ 。
(3)该反应的平衡常数表达式K=_____ ;若在上述平衡体系中再充入0.4molCO2和1.2molH2O(g)(保持温度不变),则此平衡将_____ 移动(填“向正反应方向”、“不”、“向逆反应方向”)。
(4)下列措施能使 增大的是_____。
增大的是_____。
Ⅱ.利用CO2、NH3为原料生产尿素[CO(NH2)2],反应原理为:2NH3(g)+CO2(g) H2O(l)+CO(NH2)2(s) ΔH=-178kJ∙mol-1.T1℃时,在1L的密闭容器中充入CO2和NH3模拟工业生产,n(NH3)/n(CO2)=x,图中是CO2平衡转化率(α)与x的关系。
H2O(l)+CO(NH2)2(s) ΔH=-178kJ∙mol-1.T1℃时,在1L的密闭容器中充入CO2和NH3模拟工业生产,n(NH3)/n(CO2)=x,图中是CO2平衡转化率(α)与x的关系。
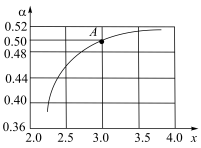
(5)图中A点NH3的平衡转化率α=_____ %。
(6)当x=1.0时,若起始的压强为p0kPa,水为液态,平衡时压强变为起始的1/2。则该反应的平衡常数Kp=_____ (kPa)-3(Kp为以分压表示的平衡常数,分压=总压×体积分数)。
I.利用二氧化碳催化加氢制甲醇。回答下列问题:
某温度下,二氧化碳与氢气反应制甲醇的总反应为
 ,
,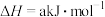 。
。(1)已知
 、
、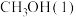 的燃烧热分别为
的燃烧热分别为 、
、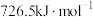 ,且
,且
 ,则
,则
在体积为4.0L的密闭容器中充入0.8molCO2和2.0molH2,发生反应CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH<0,测得CO2、CH3OH的物质的量随时间变化如图:
CH3OH(g)+H2O(g) ΔH<0,测得CO2、CH3OH的物质的量随时间变化如图:
(2)
 时间段内,
时间段内, 的平均反应速率为
的平均反应速率为(3)该反应的平衡常数表达式K=
(4)下列措施能使
 增大的是_____。
增大的是_____。A.将 从体系中分离 从体系中分离 |
| B.充入He,使体系压强增大 |
| C.降低温度、增大压强 |
D.再充入 |
Ⅱ.利用CO2、NH3为原料生产尿素[CO(NH2)2],反应原理为:2NH3(g)+CO2(g)
 H2O(l)+CO(NH2)2(s) ΔH=-178kJ∙mol-1.T1℃时,在1L的密闭容器中充入CO2和NH3模拟工业生产,n(NH3)/n(CO2)=x,图中是CO2平衡转化率(α)与x的关系。
H2O(l)+CO(NH2)2(s) ΔH=-178kJ∙mol-1.T1℃时,在1L的密闭容器中充入CO2和NH3模拟工业生产,n(NH3)/n(CO2)=x,图中是CO2平衡转化率(α)与x的关系。
(5)图中A点NH3的平衡转化率α=
(6)当x=1.0时,若起始的压强为p0kPa,水为液态,平衡时压强变为起始的1/2。则该反应的平衡常数Kp=
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】NO、NO2是大气污染物,但只要合理利用也是重要的资源。
(1)亚硝酰氯(ClNO)是合成有机物的中间体。将一定量的NO与Cl2充入-密闭容器中,发生反应:2NO(g)+Cl2(g) 2ClNO(g) △H<0。平衡后,改变外界条件X,实验测得NO的转化率a(NO)随X的变化如图1所示,则条件X可能是
2ClNO(g) △H<0。平衡后,改变外界条件X,实验测得NO的转化率a(NO)随X的变化如图1所示,则条件X可能是________ (填字母)。
a 温度 b 压强 c d 与催化剂的接触面积
d 与催化剂的接触面积
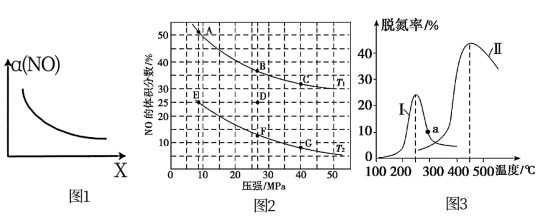
(2)在密闭容器中充入4 mol CO和5 mol NO,发生反应2NO(g)+2CO(g) N2(g)+2CO2(g) △H1=-746.5 kJ· mol-1,图2为平衡时NO的体积分数与温度、压强的关系曲线图。
N2(g)+2CO2(g) △H1=-746.5 kJ· mol-1,图2为平衡时NO的体积分数与温度、压强的关系曲线图。
①温度:T1_______ (填“<”或“>”)T2。
②若反应在D点达到平衡,此时对反应进行升温且同时扩大容器体积使平衡压强减小,重新达到平衡,则D点应向图中A~G点中的_______ 点移动。
③某研究小组探究催化剂对CO、NO转化的影响。将NO和CO以一定的流速通过两种不同的催化剂进行反应,相同时间内测量逸出气体中NO含量,从而确定尾气脱氮率(脱氮率即NO的转化率),结果如图3所示。温度低于200℃时,图3中曲线I脱氮率随温度升高而变化不大的主要原因为____________ ;a点_______ (填“是”或“不是”)对应温度下的平衡脱氮率,说明其理由:__________ 。
(3)以连二硫酸根(S2O42-)为媒介,使用间接电化学法处理燃煤烟气中的NO,装置如图4所示:
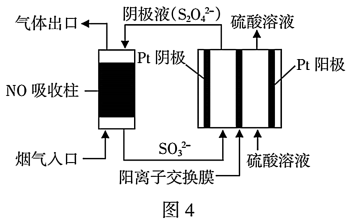
①阴极区的电极反应式为_______________ 。
②NO被吸收转化后的主要产物为NH4+,若通电时电路中转移了0.3 mol e-,则此通电过程中理论上被吸收的NO在标准状况下的体积为____________ mL。
(1)亚硝酰氯(ClNO)是合成有机物的中间体。将一定量的NO与Cl2充入-密闭容器中,发生反应:2NO(g)+Cl2(g)
 2ClNO(g) △H<0。平衡后,改变外界条件X,实验测得NO的转化率a(NO)随X的变化如图1所示,则条件X可能是
2ClNO(g) △H<0。平衡后,改变外界条件X,实验测得NO的转化率a(NO)随X的变化如图1所示,则条件X可能是a 温度 b 压强 c
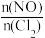 d 与催化剂的接触面积
d 与催化剂的接触面积
(2)在密闭容器中充入4 mol CO和5 mol NO,发生反应2NO(g)+2CO(g)
 N2(g)+2CO2(g) △H1=-746.5 kJ· mol-1,图2为平衡时NO的体积分数与温度、压强的关系曲线图。
N2(g)+2CO2(g) △H1=-746.5 kJ· mol-1,图2为平衡时NO的体积分数与温度、压强的关系曲线图。①温度:T1
②若反应在D点达到平衡,此时对反应进行升温且同时扩大容器体积使平衡压强减小,重新达到平衡,则D点应向图中A~G点中的
③某研究小组探究催化剂对CO、NO转化的影响。将NO和CO以一定的流速通过两种不同的催化剂进行反应,相同时间内测量逸出气体中NO含量,从而确定尾气脱氮率(脱氮率即NO的转化率),结果如图3所示。温度低于200℃时,图3中曲线I脱氮率随温度升高而变化不大的主要原因为
(3)以连二硫酸根(S2O42-)为媒介,使用间接电化学法处理燃煤烟气中的NO,装置如图4所示:

①阴极区的电极反应式为
②NO被吸收转化后的主要产物为NH4+,若通电时电路中转移了0.3 mol e-,则此通电过程中理论上被吸收的NO在标准状况下的体积为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐3】将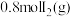 和
和 置于某
置于某 密闭容器中,。在一定温度下发生反应:
密闭容器中,。在一定温度下发生反应: 并达到平衡。
并达到平衡。 的体积分数随时间的变化如表格所示:
的体积分数随时间的变化如表格所示:
(1)在条件I到达平衡时,计算该反应 转化率,要求列出计算过程
转化率,要求列出计算过程___________ (三段式计算)。
(2)在条件I从开始反应到到达平衡时, 的反应速率为
的反应速率为___________ 。
(3)为达到条件Ⅱ的数据,对于反应体系可能改变的操作是___________ 。
(4)该反应的
___________ 0(填“>”,“<”或“=”)
(5) 时,将
时,将 气体充入体积为
气体充入体积为 的恒容密闭容器中,发生反应
的恒容密闭容器中,发生反应 ,
, 后反应达到化学平衡,测得容器中混合气体总压强为
后反应达到化学平衡,测得容器中混合气体总压强为 ,此混合气体中
,此混合气体中 与
与 的物质的量之比为
的物质的量之比为 。该温度下,反应的化学平衡常数
。该温度下,反应的化学平衡常数
___________  (
( 为以分压表示的平衡常数,分压=总压×体积分数)。
为以分压表示的平衡常数,分压=总压×体积分数)。
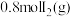 和
和 置于某
置于某 密闭容器中,。在一定温度下发生反应:
密闭容器中,。在一定温度下发生反应: 并达到平衡。
并达到平衡。 的体积分数随时间的变化如表格所示:
的体积分数随时间的变化如表格所示: 体积分数 体积分数 | 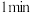 |  |  | 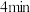 |  | 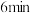 |  |
| 条件I |  |  |  | 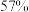 |  |  |  |
| 条件Ⅱ |  |  | 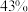 |  | 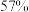 |  |  |
 转化率,要求列出计算过程
转化率,要求列出计算过程(2)在条件I从开始反应到到达平衡时,
 的反应速率为
的反应速率为(3)为达到条件Ⅱ的数据,对于反应体系可能改变的操作是
(4)该反应的

(5)
 时,将
时,将 气体充入体积为
气体充入体积为 的恒容密闭容器中,发生反应
的恒容密闭容器中,发生反应 ,
, 后反应达到化学平衡,测得容器中混合气体总压强为
后反应达到化学平衡,测得容器中混合气体总压强为 ,此混合气体中
,此混合气体中 与
与 的物质的量之比为
的物质的量之比为 。该温度下,反应的化学平衡常数
。该温度下,反应的化学平衡常数
 (
( 为以分压表示的平衡常数,分压=总压×体积分数)。
为以分压表示的平衡常数,分压=总压×体积分数)。
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】铁在工业、农业和国防科技中有重要应用,我国已是生产钢铁最多的国家。回答下列问题:
(1) 工业上以磁铁矿和焦炭为原料冶炼铁存在以下变化:
①Fe3O4(s)+4C(s)=3Fe(s)+4CO(g) ΔH1=+678kJ·mol-1 ②CO(g)+ O2(g)=CO2(g) ΔH2=-283kJ·mol-1
O2(g)=CO2(g) ΔH2=-283kJ·mol-1
③C(s) + O2(g)=CO(g) ΔH3=-110kJ·mol-1 ④Fe3O4(s)+4CO(g)⇌3Fe(s)+4CO2(g) ΔH4
O2(g)=CO(g) ΔH3=-110kJ·mol-1 ④Fe3O4(s)+4CO(g)⇌3Fe(s)+4CO2(g) ΔH4
则ΔH4=____ kJ·mol-1。
(2)铁矿石中常含有硫, 使高炉尾气中混有SO2, 除去高炉尾气中SO2 的物质是___ 。生产中发现, 无论怎么改变原料配比与条件, 在高炉尾气中始终有CO, 原因是___ 。
(3)在温度 aK时,反应Fe3O4(s)+4CO(g)⇌3Fe(s)+4CO2(g)的浓度平衡常数Kc=16(用浓度计算所得),则用分压(分压等于总压×体积分数)代替浓度算得的平衡常数Kp___ Kc(填 “大于”“小于” 或 “等于”)。平衡混合气体中CO的体积分数为___ (保留两位有效数字)。
(4) aK 时,在体积为 2L 的密闭容器中,加入 Fe、 Fe3O4、 CO、 CO2各1.0mol,气体的压强为PkPa。
①此时,v 正(CO2)___ v 逆(CO)(填 “大于”“小于” 或 “等于”), 反应经过5min后达到平衡, 该时间范围内的平均反应速率 v(CO2)=___ mol/(L·min)(保留两位有效数字)。
②已知:恒容条件下,相同分子数的气体,其压强与温度成正比。平衡后温度从 aK逐渐升高到3aK, 请在下图中绘制出CO分压(PCO的变化曲线)_______ 。
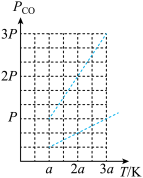
(1) 工业上以磁铁矿和焦炭为原料冶炼铁存在以下变化:
①Fe3O4(s)+4C(s)=3Fe(s)+4CO(g) ΔH1=+678kJ·mol-1 ②CO(g)+
 O2(g)=CO2(g) ΔH2=-283kJ·mol-1
O2(g)=CO2(g) ΔH2=-283kJ·mol-1③C(s) +
 O2(g)=CO(g) ΔH3=-110kJ·mol-1 ④Fe3O4(s)+4CO(g)⇌3Fe(s)+4CO2(g) ΔH4
O2(g)=CO(g) ΔH3=-110kJ·mol-1 ④Fe3O4(s)+4CO(g)⇌3Fe(s)+4CO2(g) ΔH4则ΔH4=
(2)铁矿石中常含有硫, 使高炉尾气中混有SO2, 除去高炉尾气中SO2 的物质是
(3)在温度 aK时,反应Fe3O4(s)+4CO(g)⇌3Fe(s)+4CO2(g)的浓度平衡常数Kc=16(用浓度计算所得),则用分压(分压等于总压×体积分数)代替浓度算得的平衡常数Kp
(4) aK 时,在体积为 2L 的密闭容器中,加入 Fe、 Fe3O4、 CO、 CO2各1.0mol,气体的压强为PkPa。
①此时,v 正(CO2)
②已知:恒容条件下,相同分子数的气体,其压强与温度成正比。平衡后温度从 aK逐渐升高到3aK, 请在下图中绘制出CO分压(PCO的变化曲线)

您最近一年使用:0次
【推荐2】综合利用含碳资源、促进碳中和在保护生态环境等方面具有重要意义。回答下列问题:
(1)中国科学院在国际上宣布首次实现CO2到淀粉的全合成,其中前两步涉及的反应如图1所示。_______ (用△H1、△H2、△H3、△H4表示)。
②反应I进行时,同时发生反应:2CO2(g)+6H2(g) C2H4(g)+4H2O(g)。在1L恒容密闭容器中充入4.0molCO2和6.0molH2,一定温度下,达到平衡时,c(CO2)=c(H2O)=2.4mol/L,请回答下列问题:反应I的平衡常数的表达式K=
C2H4(g)+4H2O(g)。在1L恒容密闭容器中充入4.0molCO2和6.0molH2,一定温度下,达到平衡时,c(CO2)=c(H2O)=2.4mol/L,请回答下列问题:反应I的平衡常数的表达式K=_______ 。CH3OH物质的量分数为_______ %(计算结果保留1位小数)。
(2)乙烯是合成工业的重要原料,一定条件下可发生反应:3C2H4(g) 2C3H6(g)分别在不同温度、不同催化剂下,保持其他初始条件不变,重复实验,经相同时间测得C2H4体积分数与温度的关系如图2所示。
2C3H6(g)分别在不同温度、不同催化剂下,保持其他初始条件不变,重复实验,经相同时间测得C2H4体积分数与温度的关系如图2所示。_______ V逆(填“>”“<”或“=”),根据图中所给信息,应选择的反应条件为_______ 。
(3)CO2氧化1-丁烯脱氢生产1,3-丁二烯,其反应原理为:CH2=CHCH2CH3(g)+CO2(g)→CH2=CHCH=CH2(g)+H2O(g)+CO(g)氧化脱氢反应可能的反应路径有两种,如图3所示:_______ (填化学式)。
②若为“两步路径”,在温度和总压相同时,1-丁烯氧化脱氢的平衡转化率高于直接脱氢的原因是_______ 。
(1)中国科学院在国际上宣布首次实现CO2到淀粉的全合成,其中前两步涉及的反应如图1所示。
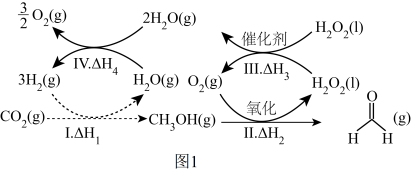
②反应I进行时,同时发生反应:2CO2(g)+6H2(g)
 C2H4(g)+4H2O(g)。在1L恒容密闭容器中充入4.0molCO2和6.0molH2,一定温度下,达到平衡时,c(CO2)=c(H2O)=2.4mol/L,请回答下列问题:反应I的平衡常数的表达式K=
C2H4(g)+4H2O(g)。在1L恒容密闭容器中充入4.0molCO2和6.0molH2,一定温度下,达到平衡时,c(CO2)=c(H2O)=2.4mol/L,请回答下列问题:反应I的平衡常数的表达式K=(2)乙烯是合成工业的重要原料,一定条件下可发生反应:3C2H4(g)
 2C3H6(g)分别在不同温度、不同催化剂下,保持其他初始条件不变,重复实验,经相同时间测得C2H4体积分数与温度的关系如图2所示。
2C3H6(g)分别在不同温度、不同催化剂下,保持其他初始条件不变,重复实验,经相同时间测得C2H4体积分数与温度的关系如图2所示。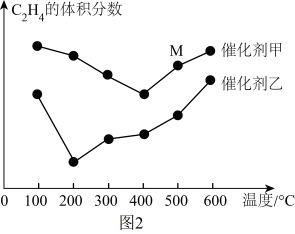
(3)CO2氧化1-丁烯脱氢生产1,3-丁二烯,其反应原理为:CH2=CHCH2CH3(g)+CO2(g)→CH2=CHCH=CH2(g)+H2O(g)+CO(g)氧化脱氢反应可能的反应路径有两种,如图3所示:
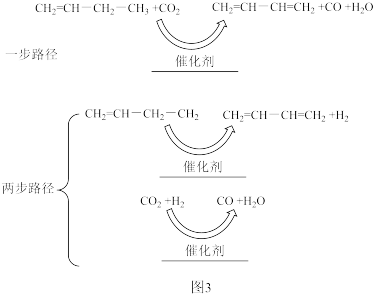
②若为“两步路径”,在温度和总压相同时,1-丁烯氧化脱氢的平衡转化率高于直接脱氢的原因是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】燃煤废气中的氮氧化物(NOx)、CO2、SO2等气体,常用下列方法处理,以实现节能减排、废物利用等。已知:25℃ 时,Kb(NH3·H2O)=1.8×10-5; H2SO3:Ka1=1.5×10-2,Ka2=1.0×10-7。
(1)处理烟气中的SO2常用液吸法。室温条件下,将烟气通入浓氨水中得到(NH4)2SO3溶液,0.1mol/L(NH4)2SO3溶液的pH____ (填“>”“<”或“=”)7。
(2)用活性炭可以还原处理氮氧化物,有关反应为C(s)+2NO(g) ⇌ N2(g)+CO2(g)。在恒容条件下,能判断该反应一定达到平衡状态的依据是________ (填选项编号)。
A.单位时间内生成2nmolNO(g)的同时消耗nmolCO2(g)
B.混合气体的密度不再发生改变
C.反应体系的压强不再发生改变
D.混合气体的平均相对分子质量不再改变
(3)有科学家经过研究发现,用CO2和H2在210~290℃,催化剂条件下可转化生成甲醇蒸气和水蒸气。
①230℃,向容器中投入0.5molCO2和1.5molH2,当转化率达80% 时放出热量19.6kJ能量,写出该反应的热化学方程式__________________ 。
②一定条件下,往 2L恒容密闭容器中充入1.0molCO2和3.0molH2,在不同催化剂作用下,相同时间内 CO2的转化率随温度的变化如图1所示:
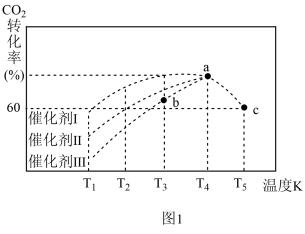
催化剂效果最佳的是催化剂________ (填“Ⅰ”“Ⅱ”“Ⅲ”)。b点v( 正 )________ v( 逆 )( 填“>”“<”或“=”) 。此反应在 a 点时已达平衡状态,a 点的转化率比 c 点高的原因_____ 。已知容器内的起始压强为100kPa,则图中c点对应温度下反应的平衡常数Kp=____________ KPa-2。(保留两位有效数字,Kp为以分压表示的平衡常数,分压=总压×物质的量分数)
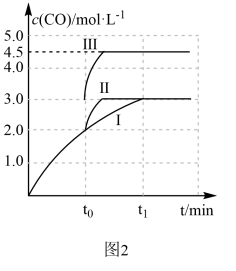
(4)一定条件下,CO2和H2也可以发生反应CO2(g)+H2(g) ⇌ CO(g)+H2O(g) ΔH<0,一定温度下,在3L容积可变的密闭容器中发生如上反应,已知c(CO)与反应时间t变化曲线Ⅰ如图2所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ或曲线Ⅲ。当曲线Ⅰ变为曲线Ⅲ时,改变的条件是____________________ 。
(1)处理烟气中的SO2常用液吸法。室温条件下,将烟气通入浓氨水中得到(NH4)2SO3溶液,0.1mol/L(NH4)2SO3溶液的pH
(2)用活性炭可以还原处理氮氧化物,有关反应为C(s)+2NO(g) ⇌ N2(g)+CO2(g)。在恒容条件下,能判断该反应一定达到平衡状态的依据是
A.单位时间内生成2nmolNO(g)的同时消耗nmolCO2(g)
B.混合气体的密度不再发生改变
C.反应体系的压强不再发生改变
D.混合气体的平均相对分子质量不再改变
(3)有科学家经过研究发现,用CO2和H2在210~290℃,催化剂条件下可转化生成甲醇蒸气和水蒸气。
①230℃,向容器中投入0.5molCO2和1.5molH2,当转化率达80% 时放出热量19.6kJ能量,写出该反应的热化学方程式
②一定条件下,往 2L恒容密闭容器中充入1.0molCO2和3.0molH2,在不同催化剂作用下,相同时间内 CO2的转化率随温度的变化如图1所示:

催化剂效果最佳的是催化剂
(4)一定条件下,CO2和H2也可以发生反应CO2(g)+H2(g) ⇌ CO(g)+H2O(g) ΔH<0,一定温度下,在3L容积可变的密闭容器中发生如上反应,已知c(CO)与反应时间t变化曲线Ⅰ如图2所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ或曲线Ⅲ。当曲线Ⅰ变为曲线Ⅲ时,改变的条件是

您最近一年使用:0次



