2020年2月15日,由国家科研攻关组的主要成员单位的专家组共同研判磷酸氯喹在细胞水平上能有效抑制新型冠状病毒(SARS-CoV-2)的感染。磷酸氯喹的结构如图所示,据此回答下列问题。
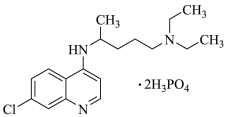
(1)C、N、O三种元素第一电离能从大到小的顺序为_____________ ;电负性χ(P)_____ χ(Cl)(填“>”或“<”);
(2)磷酸氯喹中N原子的杂化方式为_____ ,NH3是一种极易溶于水的气体,其沸点比AsH3的沸点高,其原因是___________ ;
(3)磷化镓与砷化镓是两种由ⅢA族元素与ⅤA族元素人工合成的Ⅲ-Ⅴ族化合物半导体材料。其晶胞结构可看作金刚石晶胞内部的碳原子被P(As)原子代替,顶点和面心的碳原子被Ga原子代替。
①基态Ga原子核外电子排布式为__________ ;
②砷化镓晶体中含有的化学键类型为___________ (填选项字母);
A.离子键 B.配位键 C.σ键 D.π键 E.极性键 F.非极性键
③磷化镓与砷化镓具有相似的晶体结构,其中熔点较高的是__________ (填化学式),原因是_______________ ;
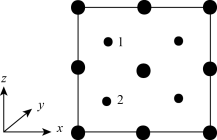
④以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置。称作原子分数坐标。如图为沿y轴投影的磷化镓晶胞中所有原子的分布图。若原子1的原子分数坐标为(0.25,0.25,0.75),则原子2的原子分数坐标为__________ ;若磷化镓的晶体密度为ρ g·cm-3,阿伏加 德罗常数的值为NA,则晶胞中Ga和P原子的最近距离为__________ pm(用代数式表示)。

(1)C、N、O三种元素第一电离能从大到小的顺序为
(2)磷酸氯喹中N原子的杂化方式为
(3)磷化镓与砷化镓是两种由ⅢA族元素与ⅤA族元素人工合成的Ⅲ-Ⅴ族化合物半导体材料。其晶胞结构可看作金刚石晶胞内部的碳原子被P(As)原子代替,顶点和面心的碳原子被Ga原子代替。
①基态Ga原子核外电子排布式为
②砷化镓晶体中含有的化学键类型为
A.离子键 B.配位键 C.σ键 D.π键 E.极性键 F.非极性键
③磷化镓与砷化镓具有相似的晶体结构,其中熔点较高的是
④以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置。称作原子分数坐标。如图为沿y轴投影的磷化镓晶胞中所有原子的分布图。若原子1的原子分数坐标为(0.25,0.25,0.75),则原子2的原子分数坐标为

更新时间:2020-04-08 10:50:11
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】根据反应:2Na2CO3+ SnO2+4S Na2SO4 + Na2SnS3+2CO2↑。回答下列问题:
Na2SO4 + Na2SnS3+2CO2↑。回答下列问题:
(1)上述反应涉及的元素中,非金属性最强的元素的最外层电子排布式为_____________ 在上述反应的生成物中,属于分子晶体的结构式___________________ 。
(2)在上述反应中单质物质的原子核外共有______ 种不同运动状态的电子,有_____ 种不同能量的电子。
(3)上述反应中,金属性最强的元素与铝元素相比较,可作为判断金属性强弱依据的是__________ (选填编号)。
a.能否置换出铝盐溶液中铝
b.Al(OH)3能否溶解在该元素最高价氧化物对应水化物中
c.单质与氢气化合的难易程度
d.单质与同浓度的稀盐酸发生反应的快慢程度
(4)常温下,测得Na2SnS3溶液pH>7,请用离子方程式表示其原因:___ 。
 Na2SO4 + Na2SnS3+2CO2↑。回答下列问题:
Na2SO4 + Na2SnS3+2CO2↑。回答下列问题:(1)上述反应涉及的元素中,非金属性最强的元素的最外层电子排布式为
(2)在上述反应中单质物质的原子核外共有
(3)上述反应中,金属性最强的元素与铝元素相比较,可作为判断金属性强弱依据的是
a.能否置换出铝盐溶液中铝
b.Al(OH)3能否溶解在该元素最高价氧化物对应水化物中
c.单质与氢气化合的难易程度
d.单质与同浓度的稀盐酸发生反应的快慢程度
(4)常温下,测得Na2SnS3溶液pH>7,请用离子方程式表示其原因:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】我国具有丰富的铜矿资源,请回答下列有关铜及其化合物的问题:
(1)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。Cu和Zn在元素周期表中位于_____ 区,请写出基态Cu原子的价电子排布式_______________ 。第一电离能Il(Zn)_______ Il(Cu)(填“大于”或“小于”),原因是________ 。
(2)新型农药松脂酸铜具有低残留的特点,下图是松脂酸铜的结构简式,请分析1个松脂酸铜中π键的个数是______ ,加“*”碳原子的杂化方式为________ 。

(3)硫酸铜溶于氨水形成[Cu(NH3)4]SO4深蓝色溶液。
①在[Cu(NH3)4]2+中Cu2+、NH3之间形成的化学键为____ ,提供孤电子对的成键原子是______ 。
② 立体构型是
立体构型是_____________ 。
③NH3的沸点_________ (填“高于”或“低于”)PH3;
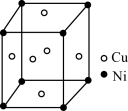
(4)一种铜镍合金(俗称白铜)的晶胞如下图所示,铜、镍原子个数比为__________ 。
(1)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。Cu和Zn在元素周期表中位于
(2)新型农药松脂酸铜具有低残留的特点,下图是松脂酸铜的结构简式,请分析1个松脂酸铜中π键的个数是

(3)硫酸铜溶于氨水形成[Cu(NH3)4]SO4深蓝色溶液。
①在[Cu(NH3)4]2+中Cu2+、NH3之间形成的化学键为
②
 立体构型是
立体构型是③NH3的沸点
(4)一种铜镍合金(俗称白铜)的晶胞如下图所示,铜、镍原子个数比为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】氮化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为起始物,经过一系列反应可以得到BN,如图所示:
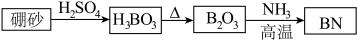
(1)由B2O3制备BN的化学方程式是________________________________________ 。BN有二种结构,其中一种超硬、耐磨、耐高温,这种BN属于__________ 晶体。
(2)硼元素原子的电子排布式为___________ ,这些电子有_________ 种不同的能量。
(3)与B元素在同一周期,其原子的最外层有2个未成对电子的元素是______ (写元素符号);甲同学列了一个比较微粒半径的式子:Li+>Be2+>B3+,乙同学对此提出了异义。乙同学的异义是________________________ 。
(4)原子个数相同、最外层电子总数也相同的化合物是“等电子体”,等电子体的结构相似。B3N3H6 与苯是等电子体,被称为“无机苯”。B3N3H6的结构式如图,则B3N3H6的二氯代物有_________ 种。
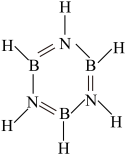

(1)由B2O3制备BN的化学方程式是
(2)硼元素原子的电子排布式为
(3)与B元素在同一周期,其原子的最外层有2个未成对电子的元素是
(4)原子个数相同、最外层电子总数也相同的化合物是“等电子体”,等电子体的结构相似。B3N3H6 与苯是等电子体,被称为“无机苯”。B3N3H6的结构式如图,则B3N3H6的二氯代物有

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】生物质能是一种洁净、可再生的能源。生物质气(主要成分为CO、CO2等)与H2混合,催化合成甲醇是生物质能利用的方法之一。
(1)①上述反应的催化剂含有Cu、Zn、Al等元素。写出基态Cu原子的核外电子排布式:______ 。
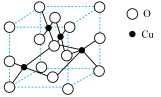
②铜的一种氧化物晶胞中(结构如图所示),所包含的Cu原子数目为______ 。
③其中O原子的配位数为______ 。
(2)根据等电子原理,写出CO分子的结构式______ 。
(3)甲醇催化氧化可得到甲醛(HCHO),甲醛与新制Cu(OH)2的碱性溶液反应生成Cu2O沉淀。
①甲醇沸点比甲醛高得多的原因是______ 。
②甲醇分子中原子轨道的杂化类型为sp3的原子个数为______ 。
③甲醛分子的空间构型是______ ;1mol甲醛分子中σ键的数目为______ 。
④甲醇中C、H、O三种元素电负性由大到小的顺序为______ 。
⑤Cu2O的熔点比Cu2S高的原因是______ 。
(1)①上述反应的催化剂含有Cu、Zn、Al等元素。写出基态Cu原子的核外电子排布式:
②铜的一种氧化物晶胞中(结构如图所示),所包含的Cu原子数目为
③其中O原子的配位数为

(2)根据等电子原理,写出CO分子的结构式
(3)甲醇催化氧化可得到甲醛(HCHO),甲醛与新制Cu(OH)2的碱性溶液反应生成Cu2O沉淀。
①甲醇沸点比甲醛高得多的原因是
②甲醇分子中原子轨道的杂化类型为sp3的原子个数为
③甲醛分子的空间构型是
④甲醇中C、H、O三种元素电负性由大到小的顺序为
⑤Cu2O的熔点比Cu2S高的原因是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】联合国将2019年定为“国际化学元素周期表年”。元素周期表前四周期的元素a、b、c、d、e、f的原子序数依次增大。a、b、d的价电子层中未成对电子均只有1个,a的基态原子核外有3种不同能量的电子,b、d的单质均能与水剧烈反应,b-和d+核外电子数相差8,c的最外层电子数为其电子层数的2倍,补充维生素D可促进人体对元素e的吸收,f的价电子层中的未成对电子数为4.回答下列问题:
(1)a、b、c的电负性由小到大的顺序为___________ (用元素符号表示)。基态f原子的核外电子排布式为___________ 。
(2)ab3分子中心原子的杂化方式为___________ ,其键角为___________ 。
(3)c的简单氢化物与同族相邻两种元素所形成的简单氢化物沸点由高到低的顺序为___________ (用化学式表示),理由:___________ 。
(4)CO与f形成的f(CO)5常温下是一种浅黄色液体,f(CO)5的空间构型为___________ ,提供孤电子对的原子是___________ (填元素符号),CO分子中σ键与π键数目之比为___________ 。
(1)a、b、c的电负性由小到大的顺序为
(2)ab3分子中心原子的杂化方式为
(3)c的简单氢化物与同族相邻两种元素所形成的简单氢化物沸点由高到低的顺序为
(4)CO与f形成的f(CO)5常温下是一种浅黄色液体,f(CO)5的空间构型为
您最近一年使用:0次
【推荐3】请回答下列问题。
I.有几种元素的微粒核外电子排布式均为 ,下列问题其中:
,下列问题其中:
(1)某电中性微粒一般不和其他元素的原子反应,这种微粒的符号是_______ 。
(2)某微粒的盐溶液,能使溴水褪色,并出现浑浊,这种微粒的符号是_______ 。
(3)某微粒氧化性很弱,但得到电子后还原性很强,且该微粒对应的元素原子有一个单电子,这种微粒的符号是_______ 。
(4)某微粒还原性虽弱,但失去电子后氧化性强,且该微粒对应的元素原子得到一个电子即达稳定结构,这种微粒的符号是_______ 。
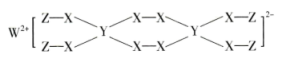
II.一种新型漂白剂(结构如下)可用于漂白羊毛等,其中W、Y、Z为不同周期、不同主族的短周期元素,Z原子的核外电子排布式为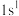 ,W、Y、Z的最外层电子数之和等于X的最外层电子数,X基态原子核外有两个单电子,W、X对应的简单离子核外电子排布相同。
,W、Y、Z的最外层电子数之和等于X的最外层电子数,X基态原子核外有两个单电子,W、X对应的简单离子核外电子排布相同。
回答下列问题:
(5)写出元素X在周期表中的位置:_______ 。
(6)写出W简单离子的核外电子排布式:_______ 。
(7)Y元素基态原子核外电子的运动状态有_______ 种,占据的原子轨道有_______ 个。
(8)W、X、Y电负性由大到小的顺序是_______ 。
I.有几种元素的微粒核外电子排布式均为
 ,下列问题其中:
,下列问题其中:(1)某电中性微粒一般不和其他元素的原子反应,这种微粒的符号是
(2)某微粒的盐溶液,能使溴水褪色,并出现浑浊,这种微粒的符号是
(3)某微粒氧化性很弱,但得到电子后还原性很强,且该微粒对应的元素原子有一个单电子,这种微粒的符号是
(4)某微粒还原性虽弱,但失去电子后氧化性强,且该微粒对应的元素原子得到一个电子即达稳定结构,这种微粒的符号是
II.一种新型漂白剂(结构如下)可用于漂白羊毛等,其中W、Y、Z为不同周期、不同主族的短周期元素,Z原子的核外电子排布式为
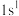 ,W、Y、Z的最外层电子数之和等于X的最外层电子数,X基态原子核外有两个单电子,W、X对应的简单离子核外电子排布相同。
,W、Y、Z的最外层电子数之和等于X的最外层电子数,X基态原子核外有两个单电子,W、X对应的简单离子核外电子排布相同。
回答下列问题:
(5)写出元素X在周期表中的位置:
(6)写出W简单离子的核外电子排布式:
(7)Y元素基态原子核外电子的运动状态有
(8)W、X、Y电负性由大到小的顺序是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】A、B、D、E、F五种元素的原子序数依次增大,且均为元素周期表前四周期元素,其中基态A原子的最外层电子数是最内层电子数的2倍;基态B原子的2p轨道上有3个未成对电子;基态D原子的s能级和p能级的电子总数相等;E和D可形成淡黄色固体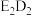 ;基态F原子的3d轨道的电子数是4s轨道电子数的3倍。回答下列问题:
;基态F原子的3d轨道的电子数是4s轨道电子数的3倍。回答下列问题:
(1)写出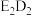 的电子式:
的电子式:___________ 。
(2)B的简单氢化物分子的空间结构是___________ ,其中心原子采取___________ 杂化。
(3)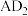 分子的
分子的 模型为
模型为___________ ,它的键角为___________ 。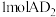 含有
含有 键的数目为
键的数目为___________ 。
(4)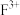 比
比 稳定,请用原子结构知识解释其原因:
稳定,请用原子结构知识解释其原因:___________ 。
(5)A、B、D简单氢化物稳定性由弱到强的顺序为___________ (用化学式表示),原因是___________ (从原子结构与键参数角度解释原因)。
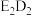 ;基态F原子的3d轨道的电子数是4s轨道电子数的3倍。回答下列问题:
;基态F原子的3d轨道的电子数是4s轨道电子数的3倍。回答下列问题:(1)写出
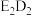 的电子式:
的电子式:(2)B的简单氢化物分子的空间结构是
(3)
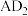 分子的
分子的 模型为
模型为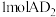 含有
含有 键的数目为
键的数目为(4)
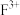 比
比 稳定,请用原子结构知识解释其原因:
稳定,请用原子结构知识解释其原因:(5)A、B、D简单氢化物稳定性由弱到强的顺序为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】碳族元素及其化合物有十分丰富的化学性质,请回答:
(1)在有机反应中有许多活性中间体,如在异丁烯与水加成中生成的(CH3)3C+,其中C存在的杂化方式_______ ,其中C+的VSEPR模型是_______ ;在有机化合物中碳上的氢的酸性可由pK描述,K为该氢的电离平衡常数,则CCl3H与CF3H中pK较大的是_______ ,理由是_______ 。
(2)碱金属M( ,
, ,
, 等)可与石墨和
等)可与石墨和 形成化合物。
形成化合物。 与
与 作用形成的
作用形成的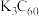 具有三维超导性能,图1为其晶胞,该晶体类型是
具有三维超导性能,图1为其晶胞,该晶体类型是_______ 。
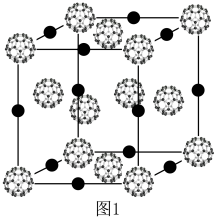
(3)石墨可看成碳层的叠加,六方石墨是abab……的两层循环,三方石墨是abcabc……(a、b、c表示不同的碳层)的三层循环,图2中属于六方石墨的是_______ :石墨与钾蒸汽作用可形成石墨夹层离子化合物,图3所示的化合物的化学式是_______ 。

(4)硅也可形成的一系列氢化物,如甲硅烷能与 猛烈反应,在空气中可以自燃,请说明硅烷化学性质比相应的烷烃活泼的原因
猛烈反应,在空气中可以自燃,请说明硅烷化学性质比相应的烷烃活泼的原因_______ 。
(1)在有机反应中有许多活性中间体,如在异丁烯与水加成中生成的(CH3)3C+,其中C存在的杂化方式
(2)碱金属M(
 ,
, ,
, 等)可与石墨和
等)可与石墨和 形成化合物。
形成化合物。 与
与 作用形成的
作用形成的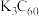 具有三维超导性能,图1为其晶胞,该晶体类型是
具有三维超导性能,图1为其晶胞,该晶体类型是
(3)石墨可看成碳层的叠加,六方石墨是abab……的两层循环,三方石墨是abcabc……(a、b、c表示不同的碳层)的三层循环,图2中属于六方石墨的是

(4)硅也可形成的一系列氢化物,如甲硅烷能与
 猛烈反应,在空气中可以自燃,请说明硅烷化学性质比相应的烷烃活泼的原因
猛烈反应,在空气中可以自燃,请说明硅烷化学性质比相应的烷烃活泼的原因
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】回答下列问题
(1)太阳能电池板主要材料为单晶硅或多晶硅。Si的价电子层的电子排布式为___________ ;单晶硅的晶体类型为___________ 。SiCl4是生产高纯硅的前驱体,其中Si采取的杂化类型为___________ 。SiCl4可发生水解反应,机理如下:
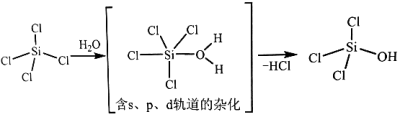
含s、p、d轨道的杂化类型有:①dsp2、②sp3d、③sp3d2,中间体SiCl4(H2O)中Si采取的杂化类型为___________ (填标号)。
(2)CO2分子中存在___________ 个 键和
键和___________ 个 键。
键。
(3)甲醇的沸点(64.7℃)介于水(100℃)和甲硫醇(CH3SH,7.6℃)之间,其原因是___________ 。
(1)太阳能电池板主要材料为单晶硅或多晶硅。Si的价电子层的电子排布式为

含s、p、d轨道的杂化类型有:①dsp2、②sp3d、③sp3d2,中间体SiCl4(H2O)中Si采取的杂化类型为
(2)CO2分子中存在
 键和
键和 键。
键。(3)甲醇的沸点(64.7℃)介于水(100℃)和甲硫醇(CH3SH,7.6℃)之间,其原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】第三代永磁体材料——钕铁硼(NdFeB)因其优异的综合磁性能,被广泛应用于计算机、通信信息等高科技产业
(1)铁、钴、镍元素性质非常相似,原子半径接近但依次减小,NiO、FeO的晶体结构类型与氯化钠相同。基态钴原子价电子轨道表示式为___________ ,熔、沸点:NiO___________ (填“<”“>”或“=”)FeO
(2)新型储氢材料氨硼烷(NH3BH3)常温下以固体形式稳定存在,极易溶于水
①氨硼烷分子中B原子采取___________ 杂化
②氨硼烷晶体中存在的作用力有范德华力、极性键、___________ 和___________
(3)氨硼烷受热析氢的过程之一如图甲所示
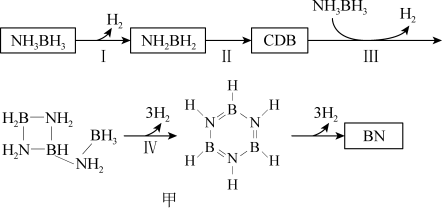
①NH2BH2的氮硼键键能大于NH3BH3,其原因为___________
②CDB的结构简式为___________
③立方氮化硼(BN)晶体的晶胞结构如图乙所示。设阿伏加德罗常数的值为NA,该晶体的密度为___________ g·cm-3(用含a和NA的最简式表示)。图丙是立方氮化硼晶胞的俯视投影图,请在图中用“ ”标明B原子的相对位置
”标明B原子的相对位置___________

(1)铁、钴、镍元素性质非常相似,原子半径接近但依次减小,NiO、FeO的晶体结构类型与氯化钠相同。基态钴原子价电子轨道表示式为
(2)新型储氢材料氨硼烷(NH3BH3)常温下以固体形式稳定存在,极易溶于水
①氨硼烷分子中B原子采取
②氨硼烷晶体中存在的作用力有范德华力、极性键、
(3)氨硼烷受热析氢的过程之一如图甲所示

①NH2BH2的氮硼键键能大于NH3BH3,其原因为
②CDB的结构简式为
③立方氮化硼(BN)晶体的晶胞结构如图乙所示。设阿伏加德罗常数的值为NA,该晶体的密度为
 ”标明B原子的相对位置
”标明B原子的相对位置
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】钛酸钡具有优良的介电、压电特性,主要用于电容器、自动温控等领域。
(1)基态钛原子的电子排布式为___________
(2)钡元素在自然界中主要以重晶石形式存在,其成分为BaSO4,其中所含三种元素的电负性从大到小的顺序为___________ (用元素符号表示);SO 的空间构型为
的空间构型为___________ ,其中S原子的杂化方式为___________ 。
(3)卤化钠(NaX)和四卤化钛(TiX4)的熔点如图所示,已知TiF4的晶体类型与TiCl4、TiBr4、TiI4不同,下列判断不正确的是___________ (选填字母序号)。
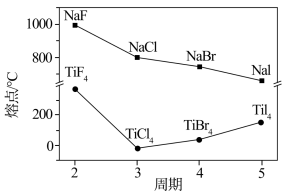
a.NaX均为离子晶体
b.随X半径的增大,NaX的离子键减弱,熔点逐渐降低
c.TiF4的熔点反常升高是由于氢键的作用
d.TiCl4、TiBr4、TiI4的相对分子质量依次增大,分子间作用力增大,熔点逐渐升高
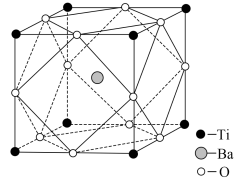
(4)钛酸钡的晶胞结构如图所示,钛酸钡的化学式为___________ ;晶体中每个钡离子周围与其距离最近且相等的氧离子的数量是___________ ;其晶胞参数约为a pm,钛酸钡晶体的密度ρ=___________ g·cm-3(阿伏加德罗常数的值为NA,1pm=1×10-12m)
(1)基态钛原子的电子排布式为
(2)钡元素在自然界中主要以重晶石形式存在,其成分为BaSO4,其中所含三种元素的电负性从大到小的顺序为
 的空间构型为
的空间构型为(3)卤化钠(NaX)和四卤化钛(TiX4)的熔点如图所示,已知TiF4的晶体类型与TiCl4、TiBr4、TiI4不同,下列判断不正确的是

a.NaX均为离子晶体
b.随X半径的增大,NaX的离子键减弱,熔点逐渐降低
c.TiF4的熔点反常升高是由于氢键的作用
d.TiCl4、TiBr4、TiI4的相对分子质量依次增大,分子间作用力增大,熔点逐渐升高
(4)钛酸钡的晶胞结构如图所示,钛酸钡的化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】近年来,有机-无机杂化金属卤素钙钛矿作为优良的光电材料受到广泛研究和关注,回答下列问题。
(1) Ca、Ti元素基态原子核外电子占据能级数之比为___________ ,与 Ti 处于同周期单电子数与Ti相同的元素还有___________ 种,Ca的前三级电离能数据分别为589.8 kJ/mol、1145.4 kJ/mol、4912.4 kJ/mol,第三电离能增大较多的原因是___________ 。
(2)卤族元素可与N和P元素形成多种稳定卤化物,其中NCl3分子构型为___________ , P元素可形成稳定的PCl3和PCl5,而氮元素只存在稳定的NCl3,理由是___________ 。
(3)Ti的配合物有多种。Ti(CO)6、Ti(H2O) 、TiF
、TiF 中的配体所含原子中电负性最小的是
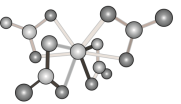
中的配体所含原子中电负性最小的是___________ ;Ti(NO3)4的球棍结构如图,Ti4+的配位数是___________ 。
(4)研究表明,TiO2通过氮掺杂反应生成TiO2-aNb,能使TiO2对可见光具有活性,反应如图所示。
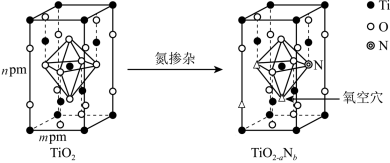
已知TiO2晶胞为长方体,设阿伏加德罗常数的值为NA,TiO2的密度为___________ g/cm3(列出计算式)。TiO2-aNb晶体中a=___________ ,b=___________ 。
(1) Ca、Ti元素基态原子核外电子占据能级数之比为
(2)卤族元素可与N和P元素形成多种稳定卤化物,其中NCl3分子构型为
(3)Ti的配合物有多种。Ti(CO)6、Ti(H2O)
 、TiF
、TiF 中的配体所含原子中电负性最小的是
中的配体所含原子中电负性最小的是
(4)研究表明,TiO2通过氮掺杂反应生成TiO2-aNb,能使TiO2对可见光具有活性,反应如图所示。

已知TiO2晶胞为长方体,设阿伏加德罗常数的值为NA,TiO2的密度为
您最近一年使用:0次



