解题方法
1 . 降低大气中的 的含量是当今世界重要的科研课题之一,我国力争在2060年前实现碳中和。研究二氧化碳的回收对这一宏伟目标的实现具有现实意义。二氧化碳催化加氢制甲醇,涉及的反应如下:
的含量是当今世界重要的科研课题之一,我国力争在2060年前实现碳中和。研究二氧化碳的回收对这一宏伟目标的实现具有现实意义。二氧化碳催化加氢制甲醇,涉及的反应如下:
I.

II.

III.

反应I、II的 (K代表化学平衡常数)随
(K代表化学平衡常数)随 (温度的倒数)的变化如图1所示;当初始进料比
(温度的倒数)的变化如图1所示;当初始进料比 时,在不同温度下仅发生反应I和II达到平衡,体系中
时,在不同温度下仅发生反应I和II达到平衡,体系中 、CO的选择性和
、CO的选择性和 的平衡转化率
的平衡转化率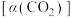 与温度的关系如图2所示,
与温度的关系如图2所示, 的选择性
的选择性 。下列说法正确的是
。下列说法正确的是


 的含量是当今世界重要的科研课题之一,我国力争在2060年前实现碳中和。研究二氧化碳的回收对这一宏伟目标的实现具有现实意义。二氧化碳催化加氢制甲醇,涉及的反应如下:
的含量是当今世界重要的科研课题之一,我国力争在2060年前实现碳中和。研究二氧化碳的回收对这一宏伟目标的实现具有现实意义。二氧化碳催化加氢制甲醇,涉及的反应如下:I.


II.


III.


反应I、II的
 (K代表化学平衡常数)随
(K代表化学平衡常数)随 (温度的倒数)的变化如图1所示;当初始进料比
(温度的倒数)的变化如图1所示;当初始进料比 时,在不同温度下仅发生反应I和II达到平衡,体系中
时,在不同温度下仅发生反应I和II达到平衡,体系中 、CO的选择性和
、CO的选择性和 的平衡转化率
的平衡转化率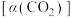 与温度的关系如图2所示,
与温度的关系如图2所示, 的选择性
的选择性 。下列说法正确的是
。下列说法正确的是

A.反应III的活化能 |
| B.反应I在高温条件下易自发进行 |
C.当 ,初始进料比 ,初始进料比 时, 时, |
D.图2中表示 选择性变化的曲线是b 选择性变化的曲线是b |
您最近一年使用:0次
2 . 设NA为阿伏加德罗常数的值。已知反应:
①CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H1=akJ•mol-1
②CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H2=bkJ•mol-1
其他数据如表所示,下列说法正确的是
①CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H1=akJ•mol-1
②CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H2=bkJ•mol-1
其他数据如表所示,下列说法正确的是
| 化学键 | C=O | O=O | C-H | O-H |
| 键能/(kJ•mol-1) | 798 | x | 413 | 463 |
| A.b<a,且甲烷的摩尔燃烧焓为bkJ•mol-1 |
| B.H2O(g)=H2O(l) △H=(a-b)kJ•mol-1 |
C.上表中x=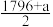 |
| D.当有4NA个C-H键断裂时,反应放出的热量为bkJ |
您最近一年使用:0次
3 . 合成氨的反应为N2(g)+3H2(g) 2NH3(g)ΔH=-92kJ·mol-1是一个可逆反应,反应条件是高温、高压,并且需要合适的催化剂。则:
2NH3(g)ΔH=-92kJ·mol-1是一个可逆反应,反应条件是高温、高压,并且需要合适的催化剂。则:
(1)如果将1mol氮气和3mol氢气混合,使其充分反应,反应放出的能量总小于上述数值,为什么?___________ 。
(2)实验室模拟工业合成氨时,在容积为2L的密闭容器内,充入2mol氮气和3mol氢气,反应经过2分钟后,容器内压强变为原来的 ,则0~2分钟内用氮气表示的化学反应速率是
,则0~2分钟内用氮气表示的化学反应速率是___________ ,此时氢气的转化率为___________ 。
(3)在容积为2L的密闭容器内,充入1mol氮气和3mol氢气,在500℃、有催化剂作用条件下,当合成氨的反应达到化学平衡时,下列说法正确的是___________ 。
a.正反应速率和逆反应速率相等且为零 b.氮气和氢气的转化率相等
c.氮气的转化率达到最大值 d.氮气和氢气的浓度相等
e.NH3的体积分数保持不变 f.反应达到该条件下的最大限度
(4)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体。在25℃、101kPa下,已知该反应每消耗9.95gCuCl(s)放热4.44kJ,该反应的热化学方程式是___________ 。
(5)根据所学知识,比较下列反应热的大小。
①同一反应的生成物状态不同时反应热不同,如2H2(g)+O2(g)=2H2O(g) ΔH1,2H2(g)+O2(g)=2H2O(l) ΔH2,则ΔH1___________ ΔH2(填“>”、“<”或“=”,下同)。
②同一反应的反应物状态不同时,反应热不同,如S(g)+O2(g)=SO2(g) ΔH1,S(s)+O2(g)=SO2(g) ΔH2,则ΔH1___________ ΔH2。
 2NH3(g)ΔH=-92kJ·mol-1是一个可逆反应,反应条件是高温、高压,并且需要合适的催化剂。则:
2NH3(g)ΔH=-92kJ·mol-1是一个可逆反应,反应条件是高温、高压,并且需要合适的催化剂。则:(1)如果将1mol氮气和3mol氢气混合,使其充分反应,反应放出的能量总小于上述数值,为什么?
(2)实验室模拟工业合成氨时,在容积为2L的密闭容器内,充入2mol氮气和3mol氢气,反应经过2分钟后,容器内压强变为原来的
 ,则0~2分钟内用氮气表示的化学反应速率是
,则0~2分钟内用氮气表示的化学反应速率是(3)在容积为2L的密闭容器内,充入1mol氮气和3mol氢气,在500℃、有催化剂作用条件下,当合成氨的反应达到化学平衡时,下列说法正确的是
a.正反应速率和逆反应速率相等且为零 b.氮气和氢气的转化率相等
c.氮气的转化率达到最大值 d.氮气和氢气的浓度相等
e.NH3的体积分数保持不变 f.反应达到该条件下的最大限度
(4)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体。在25℃、101kPa下,已知该反应每消耗9.95gCuCl(s)放热4.44kJ,该反应的热化学方程式是
(5)根据所学知识,比较下列反应热的大小。
①同一反应的生成物状态不同时反应热不同,如2H2(g)+O2(g)=2H2O(g) ΔH1,2H2(g)+O2(g)=2H2O(l) ΔH2,则ΔH1
②同一反应的反应物状态不同时,反应热不同,如S(g)+O2(g)=SO2(g) ΔH1,S(s)+O2(g)=SO2(g) ΔH2,则ΔH1
您最近一年使用:0次
名校
解题方法
4 . 下列各组热化学方程式中,ΔH的比较正确的是
①C(s)+O2(g)= CO2(g) ΔH1;C(s)+ O2(g)=CO(g) ΔH2
O2(g)=CO(g) ΔH2
②S(s)+O2(g)=SO2(g) ΔH3; S(g)+O2(g)= SO2(g) ΔH4
③H2(g)+ O2(g)= H2O(l) ΔH5:2H2(g)+O2(g)= 2H2O(l) ΔH6
O2(g)= H2O(l) ΔH5:2H2(g)+O2(g)= 2H2O(l) ΔH6
④CaO(s)+ H2O(1)= Ca(OH)2(s) ΔH7; CaCO3(s)= CaO(s)+CO2(s) ΔH8
①C(s)+O2(g)= CO2(g) ΔH1;C(s)+
 O2(g)=CO(g) ΔH2
O2(g)=CO(g) ΔH2②S(s)+O2(g)=SO2(g) ΔH3; S(g)+O2(g)= SO2(g) ΔH4
③H2(g)+
 O2(g)= H2O(l) ΔH5:2H2(g)+O2(g)= 2H2O(l) ΔH6
O2(g)= H2O(l) ΔH5:2H2(g)+O2(g)= 2H2O(l) ΔH6④CaO(s)+ H2O(1)= Ca(OH)2(s) ΔH7; CaCO3(s)= CaO(s)+CO2(s) ΔH8
| A.ΔH1<ΔH2 | B.ΔH3<ΔH4 |
| C.ΔH5<ΔH6 | D.ΔH7>ΔH8 |
您最近一年使用:0次
2023-05-16更新
|
648次组卷
|
2卷引用:广东省广州市第十七中学2022-2023学年高二上学期期中考试化学试题
名校
解题方法
5 . 下列推论正确的是
| A.S(g)+O2(g)=SO2(g) △H1,S(s)+O2(g)=SO2(g) △H2;则:△H1>△H2 |
| B.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) △H =-57.4kJ/mol,则:含20gNaOH的溶液与稀盐酸完全反应,放出的热量为28.7kJ |
| C.C(石墨,s)=C(金刚石,s) △H=+1.9kJ/mol,则:由石墨制取金刚石的反应是吸热反应,金刚石比石墨稳定 |
| D.CaCO3(s)=CaO(s)+CO2(g) △H >0,△S>0,则:该反应任何温度下都能自发进行 |
您最近一年使用:0次
2023-05-05更新
|
293次组卷
|
3卷引用:陕西省宝鸡市金台区2022-2023学年高二下学期期中质量检测化学试题
陕西省宝鸡市金台区2022-2023学年高二下学期期中质量检测化学试题山东省鄄城县第一中学2023-2024学年高二上学期9月月考化学试题(已下线)期中考试模拟试题(一)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)
6 . 相关有机物分别与氢气发生加成反应生成1mol环己烷(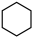 )的能量变化如图所示:
)的能量变化如图所示:
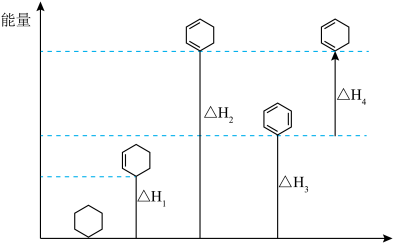
下列说法不正确的是
 )的能量变化如图所示:
)的能量变化如图所示:
下列说法不正确的是
| A.图中给出的几种有机物中环己烷最稳定 |
B.苯因为存在共轭 键,比环己二烯稳定 键,比环己二烯稳定 |
| C.环己二烯加氢制备环己烯需要吸收能量 |
| D.由苯制备环己烷放出的能量小于由环己二烯制备环己烷放出的能量 |
您最近一年使用:0次
7 . 下列说法错误的是
| A.化学反应一定伴随能量变化,有能量变化的过程未必是化学反应 |
B.已知  ,则石墨比金刚石更稳定 ,则石墨比金刚石更稳定 |
| C.中和热测定实验中,应当缓慢分次倒入NaOH溶液并搅拌 |
D. 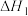 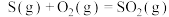  ,则 ,则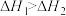 |
您最近一年使用:0次
名校
解题方法
8 . 下列说法正确的是
A.已知C(石墨,s) (金刚石,s) (金刚石,s) 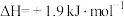 ,则金刚石比石墨稳定 ,则金刚石比石墨稳定 |
B.已知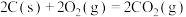  , ,  ,则 ,则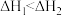 |
C.氢气的燃烧热为285.8  ,则表示氢气燃烧热的热化学方程式为 ,则表示氢气燃烧热的热化学方程式为 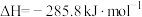 |
D.在一定条件下,将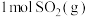 和 和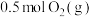 置于密闭容器中充分反应,放出热量79.2 kJ,则该反应的热化学方程式为 置于密闭容器中充分反应,放出热量79.2 kJ,则该反应的热化学方程式为 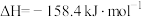 |
您最近一年使用:0次
2023-02-20更新
|
332次组卷
|
5卷引用:河北省石家庄市新乐市第一中学2022-2023学年高二上学期期末考试化学试题
河北省石家庄市新乐市第一中学2022-2023学年高二上学期期末考试化学试题江西省宜春市宜丰中学2023-2024学年高二上学期9月月考化学试题(已下线)专题02 反应热的计算-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(人教版2019)河南省焦作市博爱县第一中学2023-2024学年高三上学期11月期中考试化学试题四川省自贡市2023-2024学年高二上学期期末考试化学试题
解题方法
9 . 某同学设计如图所示实验,探究反应中的能量变化。
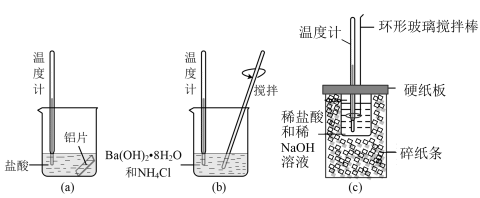
下列判断正确的是

下列判断正确的是
| A.由实验可知,(a)、(b)、(c)所涉及的反应都是放热反应 |
| B.实验(c)所涉及实验一组完整的实验数据需要测两次温度 |
| C.实验(c)中将环形玻璃搅拌棒改为铜质搅拌器对实验结果没有影响 |
| D.若用NaOH固体代替NaOH溶液与盐酸反应测定中和反应的反应热,则测得中和热的ΔH偏低 |
您最近一年使用:0次
解题方法
10 . 甲烷、乙烯和丙烯都是重要的化工原料,都能燃烧,丙烯的燃烧热 比乙烯的燃烧热
比乙烯的燃烧热 小。下列相关说法正确的是
小。下列相关说法正确的是
 比乙烯的燃烧热
比乙烯的燃烧热 小。下列相关说法正确的是
小。下列相关说法正确的是A. 和 和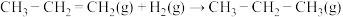 的焓变很接近 的焓变很接近 |
B.已知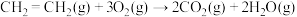 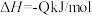 ,乙烯的燃烧热 ,乙烯的燃烧热 为 为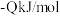 |
| C.丙烯燃烧放出的热量一定比乙烯燃烧放出的热量多 |
D.若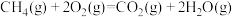  , ,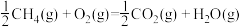  ,则 ,则 |
您最近一年使用:0次



