名校
1 . 常温下,用0.1000mol•L﹣1 NaOH溶液滴定20.00mL 0.1000mol•L﹣1 CH3COOH溶液所得滴定曲线如图,下列说法不正确的是
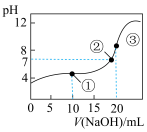

| A.点③溶液显碱性的原因是CH3COO﹣+H2O=CH3COOH+OH﹣ |
| B.点②时溶液中c(Na+)大于c(CH3COO﹣) |
| C.点①溶液中 c(CH3COOH)+c(H+)>c(CH3COO﹣)+c(OH﹣) |
| D.在逐滴加入NaOH溶液至40mL的过程中,水的电离程度先增大后减小 |
您最近一年使用:0次
2 . 为了测定胆矾( )的纯度,进行如下实验:将wg胆矾样品置于100mL烧杯中,加入少量稀硫酸及蒸馏水,使样品溶解,定量转入250mL容量瓶中,用蒸馏水稀释至刻度,摇匀。移取25.00mL上述所配溶液置于250mL锥形瓶中,加入50mL蒸馏水及足量
)的纯度,进行如下实验:将wg胆矾样品置于100mL烧杯中,加入少量稀硫酸及蒸馏水,使样品溶解,定量转入250mL容量瓶中,用蒸馏水稀释至刻度,摇匀。移取25.00mL上述所配溶液置于250mL锥形瓶中,加入50mL蒸馏水及足量 溶液,充分反应,滴入2滴X,用
溶液,充分反应,滴入2滴X,用
 ,溶液滴定至终点,消耗滴定液VmL。已知:
,溶液滴定至终点,消耗滴定液VmL。已知: ,
, 。下列叙述错误的是
。下列叙述错误的是
 )的纯度,进行如下实验:将wg胆矾样品置于100mL烧杯中,加入少量稀硫酸及蒸馏水,使样品溶解,定量转入250mL容量瓶中,用蒸馏水稀释至刻度,摇匀。移取25.00mL上述所配溶液置于250mL锥形瓶中,加入50mL蒸馏水及足量
)的纯度,进行如下实验:将wg胆矾样品置于100mL烧杯中,加入少量稀硫酸及蒸馏水,使样品溶解,定量转入250mL容量瓶中,用蒸馏水稀释至刻度,摇匀。移取25.00mL上述所配溶液置于250mL锥形瓶中,加入50mL蒸馏水及足量 溶液,充分反应,滴入2滴X,用
溶液,充分反应,滴入2滴X,用
 ,溶液滴定至终点,消耗滴定液VmL。已知:
,溶液滴定至终点,消耗滴定液VmL。已知: ,
, 。下列叙述错误的是
。下列叙述错误的是| A.X为淀粉溶液 | B.滴定终点溶液颜色由无色变为蓝色 |
| C.若锥形瓶未干燥,则测得结果偏低 | D.该胆矾样品的纯度为 |
您最近一年使用:0次
3 . 常温下向25mL0.12
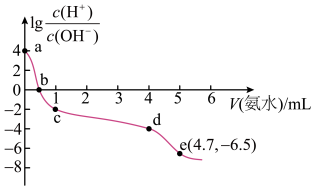
 溶液中逐滴加入一定浓度的氨水,反应过程中加入氨水的体积V与溶液中
溶液中逐滴加入一定浓度的氨水,反应过程中加入氨水的体积V与溶液中 的关系如图。已知e点对应的溶液迅速由浑浊变澄清,此时溶液中
的关系如图。已知e点对应的溶液迅速由浑浊变澄清,此时溶液中 )、
)、 均约为
均约为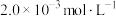 。下列说法正确的是
。下列说法正确的是

 溶液中逐滴加入一定浓度的氨水,反应过程中加入氨水的体积V与溶液中
溶液中逐滴加入一定浓度的氨水,反应过程中加入氨水的体积V与溶液中 的关系如图。已知e点对应的溶液迅速由浑浊变澄清,此时溶液中
的关系如图。已知e点对应的溶液迅速由浑浊变澄清,此时溶液中 )、
)、 均约为
均约为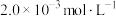 。下列说法正确的是
。下列说法正确的是
A. 浓度最大的是a点 浓度最大的是a点 |
B.b点对应溶液中: |
| C.与葡萄糖发生银镜反应,最好选择d点 |
D.由e点可知,反应 的平衡常数数值为 的平衡常数数值为 |
您最近一年使用:0次
4 . 实验室中为了测定过氧化尿素产品的纯度进行如下操作:取 过氧化尿素产品溶于水配成
过氧化尿素产品溶于水配成 溶液,量取
溶液,量取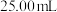 所配溶液于锥形瓶中,加入适量稀硫酸和过量KI,在暗处充分反应。滴加几滴指示剂R,用
所配溶液于锥形瓶中,加入适量稀硫酸和过量KI,在暗处充分反应。滴加几滴指示剂R,用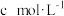 标准
标准 溶液滴定至终点,消耗滴定液
溶液滴定至终点,消耗滴定液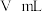 。已知:
。已知: ;
; 。下列叙述正确的是
。下列叙述正确的是
 过氧化尿素产品溶于水配成
过氧化尿素产品溶于水配成 溶液,量取
溶液,量取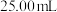 所配溶液于锥形瓶中,加入适量稀硫酸和过量KI,在暗处充分反应。滴加几滴指示剂R,用
所配溶液于锥形瓶中,加入适量稀硫酸和过量KI,在暗处充分反应。滴加几滴指示剂R,用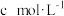 标准
标准 溶液滴定至终点,消耗滴定液
溶液滴定至终点,消耗滴定液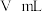 。已知:
。已知: ;
; 。下列叙述正确的是
。下列叙述正确的是| A.指示剂R淀粉溶液 |
| B.滴定终点的现象是溶液由无色变蓝色,且半分钟内不变 |
C.该过氧化尿素的纯度为 |
| D.若加入KI后,放置时间过长,则测定结果偏低 |
您最近一年使用:0次
5 . 机车车辆配件制造过程中,为了增加配件耐腐蚀能力,要使用盐酸浸透除锈。某研究所加入屏蔽剂后使用乙基紫(变色范围 )为指示剂采取酸碱滴定的方法滴定并计算酸洗废液中的盐酸浓度,所得滴定曲线如图所示。下列说法正确的是
)为指示剂采取酸碱滴定的方法滴定并计算酸洗废液中的盐酸浓度,所得滴定曲线如图所示。下列说法正确的是
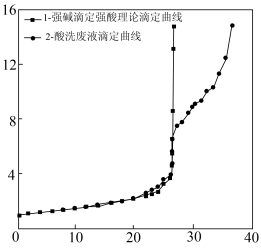
 )为指示剂采取酸碱滴定的方法滴定并计算酸洗废液中的盐酸浓度,所得滴定曲线如图所示。下列说法正确的是
)为指示剂采取酸碱滴定的方法滴定并计算酸洗废液中的盐酸浓度,所得滴定曲线如图所示。下列说法正确的是
A.酸洗废液中的主要杂质离子为 和 和 |
B.若酸洗废液中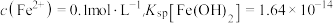 ,理论上无需屏蔽 ,理论上无需屏蔽 |
| C.滴定过程中,眼睛要紧盯滴定管的刻度变化 |
| D.图中两条曲线不能完全重合,故该方法不能达到实验目的 |
您最近一年使用:0次
6 . 将一颗市售维他命C(分子式 ,分子量
,分子量 )加水使其完全溶解,配制成
)加水使其完全溶解,配制成 溶液。取此溶液
溶液。取此溶液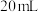 置入一锥形瓶中,加入适量的淀粉液作为指示剂,需用
置入一锥形瓶中,加入适量的淀粉液作为指示剂,需用 的
的 碘液滴定,达到滴定终点,维他命C与碘的化学反应式如下:
碘液滴定,达到滴定终点,维他命C与碘的化学反应式如下:

下列叙述,哪些正确?
 ,分子量
,分子量 )加水使其完全溶解,配制成
)加水使其完全溶解,配制成 溶液。取此溶液
溶液。取此溶液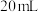 置入一锥形瓶中,加入适量的淀粉液作为指示剂,需用
置入一锥形瓶中,加入适量的淀粉液作为指示剂,需用 的
的 碘液滴定,达到滴定终点,维他命C与碘的化学反应式如下:
碘液滴定,达到滴定终点,维他命C与碘的化学反应式如下:
下列叙述,哪些正确?
A.滴定终点时锥形瓶内溶液的 值上升 值上升 |
| B.反应中,碘为氧化剂 |
| C.反应中每莫耳维他命C分子释出2莫耳电子 |
| D.当蓝色不再消失,表示锥形瓶中溶液含有少许过量的碘 |
E.此颗市售维他命C中约含有 的维他命C 的维他命C |
您最近一年使用:0次
7 . 电位滴定是利用溶液电位突变指示终点的滴定法。常温下,用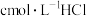 标准溶液测定
标准溶液测定 某生活用品中
某生活用品中 的含量(假设其它物质均不反应,且不含碳、钠元素),得到滴定过程中溶液电位与
的含量(假设其它物质均不反应,且不含碳、钠元素),得到滴定过程中溶液电位与 的关系如图所示。已知:根据两个滴定终点时消耗盐酸的体积差可计算出
的关系如图所示。已知:根据两个滴定终点时消耗盐酸的体积差可计算出 的量。下列说法不正确的是
的量。下列说法不正确的是

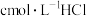 标准溶液测定
标准溶液测定 某生活用品中
某生活用品中 的含量(假设其它物质均不反应,且不含碳、钠元素),得到滴定过程中溶液电位与
的含量(假设其它物质均不反应,且不含碳、钠元素),得到滴定过程中溶液电位与 的关系如图所示。已知:根据两个滴定终点时消耗盐酸的体积差可计算出
的关系如图所示。已知:根据两个滴定终点时消耗盐酸的体积差可计算出 的量。下列说法不正确的是
的量。下列说法不正确的是
| A.滴定过程中水的电离程度逐渐增大 |
B.滴定过程中溶液中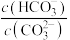 逐渐增大 逐渐增大 |
C.1mL该生活用品中含有 的质量为 的质量为 |
D.曲线任一点溶液中均存在: |
您最近一年使用:0次
8 . 用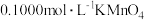 (酸性)标准溶液滴定20.00 mL未知浓度的
(酸性)标准溶液滴定20.00 mL未知浓度的 溶液。下列说法或操作正确的是
溶液。下列说法或操作正确的是
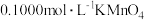 (酸性)标准溶液滴定20.00 mL未知浓度的
(酸性)标准溶液滴定20.00 mL未知浓度的 溶液。下列说法或操作正确的是
溶液。下列说法或操作正确的是A.滴定前,用 溶液润洗锥形瓶2~3次 溶液润洗锥形瓶2~3次 |
B. 标准溶液装于碱式滴定管中 标准溶液装于碱式滴定管中 |
C.反应的离子方程式为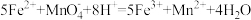 |
D.若平行实验测得消耗 溶液体积为10.00 mL,则 溶液体积为10.00 mL,则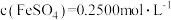 |
您最近一年使用:0次
9 . 碘量法测定水中的溶解氧的步骤如下;①氧的固定∶101 kPa、25℃时,取 100.00mL水样与 Mn(OH)2碱性悬浊液(含 KI)混合,反应生成 MnO(OH)2;②酸化、滴定∶将固氧后的水样用适量稀硫酸酸化,MnO(OH)2被 I-还原为 Mn2+,在暗处静置5min,然后用amol·L-1  标准液滴定(
标准液滴定( ),达到滴定终点时消耗
),达到滴定终点时消耗 标准液 b mL。下列说法正确的是
标准液 b mL。下列说法正确的是
 标准液滴定(
标准液滴定( ),达到滴定终点时消耗
),达到滴定终点时消耗 标准液 b mL。下列说法正确的是
标准液 b mL。下列说法正确的是| A.氧的固定时,每固定 16mgO2转移电子的物质的量为4×10-3mol |
B.酸化时主要反应的离子方程式为∶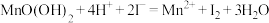 |
| C.滴定时溶液酸性太强,所测水样中溶解氧的含量偏低 |
| D.水样中溶解氧的含量为 80ab mg·L-1 |
您最近一年使用:0次
10 . 已知25℃时,MOH的Kb=10-7。该温度下,向20.00mL0.1mol•L-1MCl溶液中滴入0.1mol•L-1NaOH溶液,溶液中由水电离出的c(H+)的负对数与所加NaOH溶液的体积关系如图所示。下列说法正确的是( )


| A.m=3 |
| B.V1=10 |
C.p点对应溶液中 =10n-7:1 =10n-7:1 |
| D.n点对应溶液中c(MOH)=c(Cl-)-c(Na+) |
您最近一年使用:0次



