名校
解题方法
1 . 下列实验操作规范的是
 |  |  |  |
| A.钠的燃烧 | B.排空气法收集CO2 | C.混合浓硫酸和乙醇 | D.溶液的转移 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
2 . 下列离子方程式书写正确的是
A.Ca(HCO3)2溶液中加入少量NaOH溶液:Ca2++ +OH-=CaCO3↓+H2O +OH-=CaCO3↓+H2O |
| B.向沸水中滴加饱和氯化铁溶液得到胶体:Fe3++3H2O=Fe(OH)3↓+3H+ |
| C.氧化铁溶于氢碘酸溶液:Fe2O3+6H+=2Fe3++3H2O |
D.向氢氧化钠溶液中通入少量CO2:OH-+CO2= |
您最近一年使用:0次
名校
解题方法
3 . 抗疫居家期间,同学们在参与家务劳动的过程中体会到化学知识无处不在。下列劳动与所涉及的化学知识不相符的是
| 选项 | 家务劳动 | 化学知识 |
| A | 用白醋除去水壶中的水垢 | 白醋可溶解CaCO3沉淀 |
| B | 用小苏打粉作膨松剂焙制糕点 | NaHCO3会中和发面产生的酸放出CO2 |
| C | 用含NaClO的84消毒液拖地 | NaClO有还原性 |
| D | 用洁厕灵洗马桶 | 洁厕灵中含有盐酸,可以与尿垢反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
4 . 工业制胆矾时,将粗制CuO粉末(含杂质FeO、Fe2O3)慢慢加入适量的稀H2SO4中完全溶解,除去杂质离子后,再蒸发结晶可得纯净的胆矾晶体。已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;pH接近4时,Fe3+以Fe(OH)3的形式完全沉淀。为除去溶液中的Fe2+,可先加入_______,(从下面四个选项选择)将Fe2+氧化为Fe3+
| A.CuO | B.Cl2 | C.Cu(OH)2 | D.H2O2 |
您最近一年使用:0次
名校
5 . 高铁酸钾( )在能源、环保等方面有着广泛的用途。如图是实验室制备
)在能源、环保等方面有着广泛的用途。如图是实验室制备 的实验装置图,请回答下列问题:
的实验装置图,请回答下列问题:
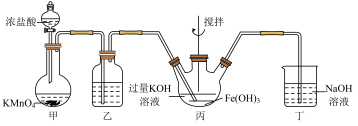
(1)图中装有浓盐酸的仪器名称为___________ 。
(2)浓盐酸与高锰酸钾发生反应: ,当消耗
,当消耗 时,理论上被氧化的HCl为
时,理论上被氧化的HCl为___________ mol。
(3)乙装置中的试剂为___________ ,作用是___________ 。
(4)写出丁装置中发生反应的离子方程式:___________ 。
(5)请完成并配平丙装置中的离子方程式:_______
___________ ___________ ___________+___________
___________ ___________+___________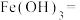 ___________
___________ ___________
___________ ___________ ___________
___________ ___________
(6)漂白液、漂白粉和漂粉精既可作棉、麻、纸张的漂白剂,又可用作环境消毒剂。工业生产漂白粉的化学方程式为___________ 。
 )在能源、环保等方面有着广泛的用途。如图是实验室制备
)在能源、环保等方面有着广泛的用途。如图是实验室制备 的实验装置图,请回答下列问题:
的实验装置图,请回答下列问题: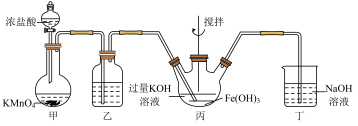
(1)图中装有浓盐酸的仪器名称为
(2)浓盐酸与高锰酸钾发生反应:
 ,当消耗
,当消耗 时,理论上被氧化的HCl为
时,理论上被氧化的HCl为(3)乙装置中的试剂为
(4)写出丁装置中发生反应的离子方程式:
(5)请完成并配平丙装置中的离子方程式:
___________
 ___________ ___________+___________
___________ ___________+___________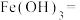 ___________
___________ ___________
___________ ___________ ___________
___________ ___________(6)漂白液、漂白粉和漂粉精既可作棉、麻、纸张的漂白剂,又可用作环境消毒剂。工业生产漂白粉的化学方程式为
您最近一年使用:0次
名校
解题方法
6 . 铁有两种氯化物,都是重要的化工试剂。某化学活动小组用如图所示的装置(夹持装置略去)模拟工业生产制备无水氯化铁。请回答下列问题:
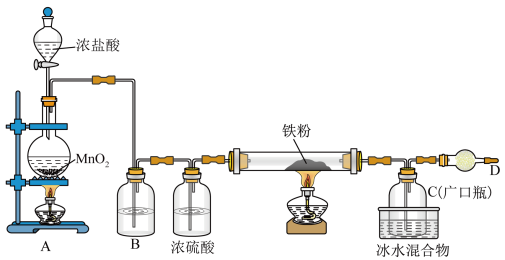
查阅有关资料如下:
①氯化铁熔点为306℃,沸点为315℃;易吸收空气中的水分而潮解。
②氯化亚铁熔点为670℃,易升华。
(1)A中发生反应的化学方程式为___________ 。
(2)过量铁粉与氯气,加热条件下反应的化学方程式为___________ 。
(3)D中装的药品是碱石灰,其作用是___________ 。
(4)将氯化铁制成氢氧化铁胶体,当光束通过 胶体时,可以看见一条光亮的“通路”,叫做
胶体时,可以看见一条光亮的“通路”,叫做___________ 效应。
(5)该小组在实验中发现稀盐酸与 混合加热不生成氯气,对用稀盐酸实验没有氯气生成的原因经讨论后有如下猜想:
混合加热不生成氯气,对用稀盐酸实验没有氯气生成的原因经讨论后有如下猜想:
猜想①:是由于 浓度低所致。
浓度低所致。
猜想②:是由于___________ 所致。
小组设计了以下实验方案进行验证:
a.稀盐酸滴入 中,然后通入HCl气体加热
中,然后通入HCl气体加热
b.稀盐酸滴入 中,然后加入NaCl固体加热
中,然后加入NaCl固体加热
c.稀盐酸滴入 中,然后加入浓硫酸加热
中,然后加入浓硫酸加热
d. 与NaCl的浓溶液混合加热
与NaCl的浓溶液混合加热
e.浓硫酸与NaCl固体、 固体共热
固体共热
实验现象:a、c、e有黄绿色气体生成,b、d没有黄绿色气体生成。
由此可知猜想___________ 成立。

查阅有关资料如下:
①氯化铁熔点为306℃,沸点为315℃;易吸收空气中的水分而潮解。
②氯化亚铁熔点为670℃,易升华。
(1)A中发生反应的化学方程式为
(2)过量铁粉与氯气,加热条件下反应的化学方程式为
(3)D中装的药品是碱石灰,其作用是
(4)将氯化铁制成氢氧化铁胶体,当光束通过
 胶体时,可以看见一条光亮的“通路”,叫做
胶体时,可以看见一条光亮的“通路”,叫做(5)该小组在实验中发现稀盐酸与
 混合加热不生成氯气,对用稀盐酸实验没有氯气生成的原因经讨论后有如下猜想:
混合加热不生成氯气,对用稀盐酸实验没有氯气生成的原因经讨论后有如下猜想:猜想①:是由于
 浓度低所致。
浓度低所致。猜想②:是由于
小组设计了以下实验方案进行验证:
a.稀盐酸滴入
 中,然后通入HCl气体加热
中,然后通入HCl气体加热b.稀盐酸滴入
 中,然后加入NaCl固体加热
中,然后加入NaCl固体加热c.稀盐酸滴入
 中,然后加入浓硫酸加热
中,然后加入浓硫酸加热d.
 与NaCl的浓溶液混合加热
与NaCl的浓溶液混合加热e.浓硫酸与NaCl固体、
 固体共热
固体共热实验现象:a、c、e有黄绿色气体生成,b、d没有黄绿色气体生成。
由此可知猜想
您最近一年使用:0次
7 . 探究钠及其化合物的性质,下列方案设计、现象及结论都正确的是
| 方案设计 | 现象 | 结论 | |
| A | 向露置在空气中的 固体中加入稀盐酸 固体中加入稀盐酸 | 溶液中产生气泡 |  固体已经变质 固体已经变质 |
| B | 将一小块金属钠在燃烧匙中点燃,伸入盛有 的集气瓶中 的集气瓶中 | 产生黑、白两种固体 | 钠的还原性强,与二氧化碳发生了置换反应 |
| C | 向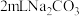 溶液中滴加少量的稀盐酸 溶液中滴加少量的稀盐酸 | 溶液中产生气泡 | 该 溶液中混有 溶液中混有 杂质 杂质 |
| D | 向插有温度计的 溶液中加入一定量NaOH固体 溶液中加入一定量NaOH固体 | 有刺激性气味产生,温度计示数增大 | 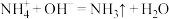 为放热反应 为放热反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
8 . 下列叙述错误 的是
①金属单质在氧化还原反应中只作还原剂
② 与
与 反应生成了
反应生成了 ,故
,故 是酸性氧化物
是酸性氧化物
③碱性氧化物一定是金属氧化物
④0.1molNaCl的摩尔质量为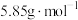
⑤ 与足量的Fe反应时,转移电子数目为
与足量的Fe反应时,转移电子数目为
⑥在相同的温度和压强下,任何物质的摩尔体积约相等
⑦质量相等,密度不相等的 和
和 分子数目一定相等
分子数目一定相等
①金属单质在氧化还原反应中只作还原剂
②
 与
与 反应生成了
反应生成了 ,故
,故 是酸性氧化物
是酸性氧化物③碱性氧化物一定是金属氧化物
④0.1molNaCl的摩尔质量为
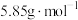
⑤
 与足量的Fe反应时,转移电子数目为
与足量的Fe反应时,转移电子数目为
⑥在相同的温度和压强下,任何物质的摩尔体积约相等
⑦质量相等,密度不相等的
 和
和 分子数目一定相等
分子数目一定相等| A.①③⑥⑦ | B.②③⑤⑦ | C.①②④⑤ | D.②④⑥ |
您最近一年使用:0次
9 .  是金属储氢材料,遇水能剧烈反应释放出
是金属储氢材料,遇水能剧烈反应释放出 ,
, 在125℃时分解为LiH、
在125℃时分解为LiH、 和Al。下列说法正确的是
和Al。下列说法正确的是
 是金属储氢材料,遇水能剧烈反应释放出
是金属储氢材料,遇水能剧烈反应释放出 ,
, 在125℃时分解为LiH、
在125℃时分解为LiH、 和Al。下列说法正确的是
和Al。下列说法正确的是A. 中Al的化合价为-5价 中Al的化合价为-5价 |
B. 与水反应时, 与水反应时, 作氧化剂 作氧化剂 |
C. 在125℃时完全分解,每生成 在125℃时完全分解,每生成 转移电子的物质的量为4mol 转移电子的物质的量为4mol |
| D.LiH是反应的还原产物 |
您最近一年使用:0次
名校
解题方法
10 . 下列分类或归类正确的是
①液氯、氨水、干冰、碘化银均为纯净物
② 、NaOH、HCl、IBr均为强电解质
、NaOH、HCl、IBr均为强电解质
③明矾、水银、烧碱、硫酸均为电解质
④因为醋酸铵是强电解质,所以其在水溶液中的电离方程式为:
⑤碘酒、淀粉、云雾、纳米材料均为胶体
①液氯、氨水、干冰、碘化银均为纯净物
②
 、NaOH、HCl、IBr均为强电解质
、NaOH、HCl、IBr均为强电解质③明矾、水银、烧碱、硫酸均为电解质
④因为醋酸铵是强电解质,所以其在水溶液中的电离方程式为:

⑤碘酒、淀粉、云雾、纳米材料均为胶体
| A.④ | B.②③⑤ | C.②④ | D.④⑤ |
您最近一年使用:0次



