名校
解题方法
1 .  、
、 和CO组成的混合气体在同温同压下与氮气的密度相同,则该混合气体中
和CO组成的混合气体在同温同压下与氮气的密度相同,则该混合气体中 、
、 和CO的体积比为
和CO的体积比为
 、
、 和CO组成的混合气体在同温同压下与氮气的密度相同,则该混合气体中
和CO组成的混合气体在同温同压下与氮气的密度相同,则该混合气体中 、
、 和CO的体积比为
和CO的体积比为| A.22∶1∶14 | B.29∶8∶13 | C.26∶8∶57 | D.13∶8∶29 |
您最近一年使用:0次
2022-01-03更新
|
2549次组卷
|
34卷引用:山西省运城市稷山中学2022届高三上学期月考(一)化学试题
山西省运城市稷山中学2022届高三上学期月考(一)化学试题(已下线)2019高考备考一轮复习精品资料 第一章 从实验学化学 第3讲 化学计算中常用的几种方法【教学案】湖南省衡阳县第四中学2019届高三第一次月考(9月)化学试题夯基提能2020届高三化学选择题对题专练——化学计算中的常见方法和应用(提升练)贵州省毕节市威宁第四中学2022届高三第一次月考化学试题河北省秦皇岛市昌黎第一中学2023届高三第一次调研考试化学试题(已下线)2012-2013学年江西省四校高一零班第一次月考化学试卷(已下线)2013-2014黑龙江省哈六中高二下学期期末考试化学试卷(已下线)2014-2015学年河南省方城县第一高级中学高一10月月考化学试卷2015-2016学年浙江省余姚中学高一上10月月考化学试卷2015-2016学年辽宁省辽阳一中高一上学期9月教学质检化学试卷2015-2016学年内蒙古集宁一中高一上第一次月考化学试卷2016-2017学年河北省廊坊一中高一上学期第一次月考化学试卷2016-2017学年河北省定州中学高二(承智班)下学期开学考试化学试卷辽宁省葫芦岛市第一中学2017-2018学年高一上学期第一次月考化学试题辽宁省葫芦岛市第一高级中学2017-2018学年高一上学期第一次月考化学试题江西省九江市2017-2018学年高一上学期第一次阶段联考化学试题四川省乐山沫若中学2017-2018学年高一上学期第一次月考化学试题【全国百强校】四川省成都市双流区棠湖中学2018-2019学年高一上学期第一次月考化学试题【校级联考】湖北省重点高中协作体2018-2019学年高一上学期期中联考化学试题吉林省白城市通榆县第一中学2019-2020学年高一上学期第一次月考化学试题河南省鲁山县第一高级中学2019-2020学年高一9月月考化学试卷试题江西省宜春九中(外国语学校)2019-2020学年高一上学期第一次月考化学试题宁夏回族自治区吴忠市吴忠中学2019-2020学年高一上学期期中考试化学试题黑龙江省大兴安岭漠河县第一中学2019-2020学年高一上学期第一次阶段考试化学试题吉林省长春市东北师大附中净月校区2019-2020学年高一12月月考化学试题湖南省株洲市攸县三中2019-2020学年高一上学期第一次月考化学试题(已下线)【南昌新东方】江西省九江市2017-2018学年高一上学期第一次阶段联考化学试题黑龙江省漠河市高级中学2021-2022学年高一上学期第一次月考化学试题福建省厦门外国语学校石狮分校2021-2022学年高一上学期第一次月考化学试题福建省师范大学附属中学2021–2022学年高一上学期期中考试化学试题上海市进才中学2022-2023学年高一上学期期中考试化学试题上海师范大学附属中学2022-2023学年高一上学期期中考试化学试题四川省成都市树德中学2022-2023学年高一上学期期末复习化学试题
真题
名校
2 . 二氧化氯(ClO2,黄绿色易溶于水的气体)是高效、低毒的消毒剂,回答下列问题:
(1)工业上可用KClO3与Na2SO3在H2SO4存在下制得ClO2,该反应氧化剂与还原剂物质的量之比为_____ 。
(2)实验室用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料,通过以下过程制备ClO2:

①电解时发生反应的化学方程式为________________________ 。
②溶液X中大量存在的阴离子有__________ 。
③除去ClO2中的NH3可选用的试剂是______ (填标号)。
a.水b.碱石灰C.浓硫酸d.饱和食盐水
(3)用下图装置可以测定混合气中ClO2的含量:

Ⅰ.在锥形瓶中加入足量的碘化钾,用50 mL水溶解后,再加入3 mL稀硫酸:
Ⅱ.在玻璃液封装置中加入水,使液面没过玻璃液封管的管口;
Ⅲ.将一定量的混合气体通入锥形瓶中吸收;
Ⅳ.将玻璃液封装置中的水倒入锥形瓶中:
Ⅴ.用0.1000 mol·L-1硫代硫酸钠标准溶液滴定锥形瓶中的溶液(I2+2S2O32-=2I-+S4O62-),指示剂显示终点时共用去20.00 mL硫
代硫酸钠溶液。在此过程中:
①锥形瓶内ClO2与碘化钾反应的离子方程式为______________________ 。
②玻璃液封装置的作用是______________ 。
③V中加入的指示剂通常为_________ ,滴定至终点的现象是_____________ 。
④测得混合气中ClO2的质量为_________ g。
(4)用ClO2处理过的饮用水会含有一定量的亚氯酸盐。若要除去超标的亚氯酸盐,下列物质最适宜的是_______ (填标号)。
a.明矾b.碘化钾c.盐酸d.硫酸亚铁
(1)工业上可用KClO3与Na2SO3在H2SO4存在下制得ClO2,该反应氧化剂与还原剂物质的量之比为
(2)实验室用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料,通过以下过程制备ClO2:

①电解时发生反应的化学方程式为
②溶液X中大量存在的阴离子有
③除去ClO2中的NH3可选用的试剂是
a.水b.碱石灰C.浓硫酸d.饱和食盐水
(3)用下图装置可以测定混合气中ClO2的含量:

Ⅰ.在锥形瓶中加入足量的碘化钾,用50 mL水溶解后,再加入3 mL稀硫酸:
Ⅱ.在玻璃液封装置中加入水,使液面没过玻璃液封管的管口;
Ⅲ.将一定量的混合气体通入锥形瓶中吸收;
Ⅳ.将玻璃液封装置中的水倒入锥形瓶中:
Ⅴ.用0.1000 mol·L-1硫代硫酸钠标准溶液滴定锥形瓶中的溶液(I2+2S2O32-=2I-+S4O62-),指示剂显示终点时共用去20.00 mL硫
代硫酸钠溶液。在此过程中:
①锥形瓶内ClO2与碘化钾反应的离子方程式为
②玻璃液封装置的作用是
③V中加入的指示剂通常为
④测得混合气中ClO2的质量为
(4)用ClO2处理过的饮用水会含有一定量的亚氯酸盐。若要除去超标的亚氯酸盐,下列物质最适宜的是
a.明矾b.碘化钾c.盐酸d.硫酸亚铁
您最近一年使用:0次
2019-01-30更新
|
7072次组卷
|
6卷引用:山西省临猗县临晋中学2019届高三9月月考化学试题
山西省临猗县临晋中学2019届高三9月月考化学试题2015年全国普通高等学校招生统一考试化学(新课标II卷)(已下线)解密03 氧化还原反应——备战2018年高考化学之高频考点解密(已下线)学科网2019年高考化学一轮复习讲练测2.4 氧化还原反应的规律及应用 练2020届高考化学二轮复习大题精准训练 —— 化学工艺流程题福建省龙岩市上杭县第一中学2021届高三上学期10月月考化学试题
3 . 某无色混合气体,可能含有CO、H2、SO2、Cl2、HCl中的一种或几种,把此混合气体通过少量澄清石灰水,无沉淀生成;再通过少量品红溶液,完全褪色;随后将该气体通过足量的氢氧化钠溶液后,再通过足量红热的CuO粉末,粉末变成红色;最后通入CaCl2溶液中,无沉淀生成,则下列关于此混合气体的叙述正确的是
| A.澄清石灰水中无沉淀,说明一定不含有SO2 |
| B.品红褪色,可能是Cl2导致的 |
| C.氧化铜粉末变红,说明CO和H2中至少有一种 |
| D.CaCl2溶液中无沉淀,说明通过CuO后得到的气体中一定不含有CO2 |
您最近一年使用:0次
2017-05-05更新
|
5344次组卷
|
12卷引用:山西省实验中学2021届高三9月月考化学试题
山西省实验中学2021届高三9月月考化学试题山西省实验中学2020-2021学年高三上学期第一次月考化学试题山东省济宁市嘉祥县第一中学2021-2022学年高三上学期期中考试化学试题辽宁省沈阳市第一二〇中学2023-2024学年高三上学期第一次质量检测化学试题上海市复旦大学附中浦东分校2016-2017学年高一下学期期中考试化学试题【全国百强校】云南省曲靖市第一中学2018-2019学年高一下学期期中考试化学试题安徽省合肥市第六中学2019-2020学年高一下学期开学考试化学试题高一必修第一册(苏教2019) 模块综合测评安徽省灵璧县第一中学2020-2021学年高一上学期12月月考试题广东省大联考2021-2022学年高一下学期期中检测化学试题黑龙江省哈尔滨市德强学校2021-2022学年高一下学期期中考试化学试题上海市复旦大学附属中学2022-2023学年高一下学期阶段测试化学试题
4 . CoCl2·6H2O是一种饲料营养强化剂。一种利用水钴矿(主要成分为Co2O3、Co(OH)3,还含少量Fe2O3、Al2O3、MnO等)制取CoCl2·6H2O的工艺流程如下:

已知:①浸出液含有的阳离子主要有H+、CO2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表(金属离子浓度为0.01 mol/L):
③CoCl2·6H2O熔点为86℃,加热至110~120℃时,失去结晶水生成无水氯化钴。
(1)写出浸出过程中Co2O3发生反应的离子方程式:_______ 。
(2)写出NaClO3发生反应的主要离子方程式:_______ ;若不慎向“浸出液”中加过量NaClO3时,可能会生成有毒气体,写出生成该有毒气体的离子方程式:_______ 。
(3)惰性电极电解CoCl2溶液的阳极电极反应式为_______ 。

(4)“操作1”中包含3个基本实验操作,它们依次是_______ 、_______ 和过滤。制得的CoCl2·6H2O在烘干时需减压烘干的原因是_______ 。
(5)萃取剂对金属离子的萃取率与pH的关系如图向“滤液”中加入萃取剂的目的是_______ ,其使用的最佳pH范围是_______ 。
A.2.0~2.5 B.3.0~3.5
C.4.0~4.5 D.5.0~5.5
(6)为测定粗产品中CoCl2·H2O的含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量。通过计算发现粗产品中CoCl2·6H2O的质量分数大于100%,其原因可能是_______ 。(答一条即可)

已知:①浸出液含有的阳离子主要有H+、CO2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表(金属离子浓度为0.01 mol/L):
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
③CoCl2·6H2O熔点为86℃,加热至110~120℃时,失去结晶水生成无水氯化钴。
(1)写出浸出过程中Co2O3发生反应的离子方程式:
(2)写出NaClO3发生反应的主要离子方程式:
(3)惰性电极电解CoCl2溶液的阳极电极反应式为

(4)“操作1”中包含3个基本实验操作,它们依次是
(5)萃取剂对金属离子的萃取率与pH的关系如图向“滤液”中加入萃取剂的目的是
A.2.0~2.5 B.3.0~3.5
C.4.0~4.5 D.5.0~5.5
(6)为测定粗产品中CoCl2·H2O的含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量。通过计算发现粗产品中CoCl2·6H2O的质量分数大于100%,其原因可能是
您最近一年使用:0次
2016-12-09更新
|
1122次组卷
|
3卷引用:山西省三区八校2017届高三第二次模拟考试理科综合化学试题
5 . 某无色溶液,其中可能存在的离子有:Na+、Ag+、Ba2+、Fe3+、Al3+、 、S2﹣、
、S2﹣、 、
、 、
、 ,现取该溶液进行实验,实验结果如下:
,现取该溶液进行实验,实验结果如下:

试回答下列问题:
(1)生成沉淀甲的离子方程式为:_______ 。
(2)由溶液甲生成沉淀乙的离子方程式为_______ 。
(3)已知气体甲由两种氧化物组成(不包括水蒸气和HBr),请你设计实验逐一鉴别这两种成分,将所需试剂以及现象填入如表(表中每一行对应正确即可得分)
(4)综上所述,该溶液肯定存在的离子有:___ 。
(5)针对溶液中可能存在的离子,用实验证明是否存在的方法是__ 。
 、S2﹣、
、S2﹣、 、
、 、
、 ,现取该溶液进行实验,实验结果如下:
,现取该溶液进行实验,实验结果如下:
试回答下列问题:
(1)生成沉淀甲的离子方程式为:
(2)由溶液甲生成沉淀乙的离子方程式为
(3)已知气体甲由两种氧化物组成(不包括水蒸气和HBr),请你设计实验逐一鉴别这两种成分,将所需试剂以及现象填入如表(表中每一行对应正确即可得分)
| 步骤 | 实验目的 | 试剂 | 现象 |
| 1 | |||
| 2 | |||
| 3 | 检验CO2 | 澄清石灰水 | 溶液变浑浊 |
(5)针对溶液中可能存在的离子,用实验证明是否存在的方法是
您最近一年使用:0次
名校
6 . 将一定量的Cl2通入体积为40mL、浓度为7.5mol/L的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),测得反应后溶液中有三种含氯元素的离子,其中ClO-物质的量为0.06mol和ClO3-物质的量0.03mol,下列说法不正确的是
| A.该反应的离子方程式为:5Cl2+10OH-=7Cl-+2ClO-+ClO3—+5H2O |
| B.该反应中,氧化剂与还原剂物质的量之比为5:3 |
| C.上述苛性钾溶液中含有0.3mol的KOH |
| D.反应后生成的ClO-和ClO3-两种离子在一定条件下均有氧化性 |
您最近一年使用:0次
2016-12-09更新
|
2567次组卷
|
5卷引用:山西省实验中学2018届高三上学期第一次月考化学试题
解题方法
7 . 某氯化铁与氯化亚铁的混合物。现要测定其中铁元素的质量分数,实验按以下步骤进行:

请根据上面流程,回答以下问题:
(1)操作Ⅰ所用到的玻璃仪器除烧杯、玻璃棒外,还必须有____________ 、__________ 。 (填仪器名称)
(2)请写出加入溴水发生的离子反应方程式_________________ 。
(3)将沉淀物加热,冷却至室温,用天平称量其质量为b1g。再次加热并冷却至室温称量其质量为b2g,若b1-b2=0.3g,则接下来还应进行的操作是__________ 。若蒸发皿质量是 W1 g,蒸发皿与加热后固体总质量是W2g,则样品中铁元素的质量分数是___________ 。有同学提出,还可以采用以下方法来测定:

①溶解样品改用了硫酸,而不用盐酸,原因是______________ 。
②选择的还原剂是否能用铁 (填“是”或“否”),原因是:__________________ 。
③若滴定用掉c mol/ L KMnO4溶液bmL,则样品中铁元素的质量分数是_______________ 。

请根据上面流程,回答以下问题:
(1)操作Ⅰ所用到的玻璃仪器除烧杯、玻璃棒外,还必须有
(2)请写出加入溴水发生的离子反应方程式
(3)将沉淀物加热,冷却至室温,用天平称量其质量为b1g。再次加热并冷却至室温称量其质量为b2g,若b1-b2=0.3g,则接下来还应进行的操作是

①溶解样品改用了硫酸,而不用盐酸,原因是
②选择的还原剂是否能用铁 (填“是”或“否”),原因是:
③若滴定用掉c mol/ L KMnO4溶液bmL,则样品中铁元素的质量分数是
您最近一年使用:0次
2016-12-09更新
|
624次组卷
|
6卷引用:2016届山西省晋中市四校高三上学期期中联考化学试卷
2016届山西省晋中市四校高三上学期期中联考化学试卷(已下线)2011届浙江省名校名师新编“百校联盟”交流高三联考(理综)化学部分(已下线)2011届浙江省杭州市长河高中高三市二测模考(理综)化学部分2016届四川省绵阳南山中学高三秋季零诊考试化学试卷2016届海南中学高三考前高考模拟十化学试卷2017届河北省石家庄市辛集中学高三上第一次阶段考试化学卷
解题方法
8 . 铅及其化合物可用于蓄电池、耐酸设备及X射线防护材料等。回答下列问题:
(1)铅是碳的同族元素,比碳多4个电子层,铅在元素周期表的位置为_________________ ,Fe3O4可写成FeO·Fe2O3的形式,如果将Pb3O4也写成相对应的形式应为:______________
(2)PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为___________________ 。PbO2可由PbO与次氯酸钠溶液反应制得,其反应的离子方程式为______________ 。
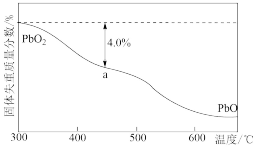
(3)PbO2在加热过程发生分解的失重曲线如右图所示,已知失重曲线上的a点为样品失重4.0%(即 ×100%)的残留固体,若a点固体组成表示为PbOx或mPbO2·nPbO,计算x值和m︰n
×100%)的残留固体,若a点固体组成表示为PbOx或mPbO2·nPbO,计算x值和m︰n_______________ ,____________ 。
(1)铅是碳的同族元素,比碳多4个电子层,铅在元素周期表的位置为
(2)PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为

(3)PbO2在加热过程发生分解的失重曲线如右图所示,已知失重曲线上的a点为样品失重4.0%(即
 ×100%)的残留固体,若a点固体组成表示为PbOx或mPbO2·nPbO,计算x值和m︰n
×100%)的残留固体,若a点固体组成表示为PbOx或mPbO2·nPbO,计算x值和m︰n
您最近一年使用:0次
名校
9 . 在100mL密度为1.2g/mL稀硝酸中,加入一定量的镁和铜组成的混合物,充分反应后金属完全溶解(假设还原产物只有NO),向反应后溶液中加入3mol/L NaOH溶液至沉淀完全,测得生成沉淀质量比原金属质量增加5.1g。则下列叙述不正确的是
| A.当金属全部溶解时收集到NO气体的体积为2.24L(标准状况) |
| B.当生成沉淀的量最多时,消耗NaOH溶液体积最小为100mL |
| C.原稀硝酸的物质的量浓度一定为4 mol/L |
| D.参加反应金属总质量(m)为9.6g>m>3.6g |
您最近一年使用:0次
2016-12-09更新
|
2919次组卷
|
11卷引用:2015届山西省临汾一中等四校高三第二次联考化学试卷
2015届山西省临汾一中等四校高三第二次联考化学试卷2015届陕西省西工大附中高三下学期三模考试化学试卷2016届湖南省长沙市明德中学高三上学期第三次月考化学试卷2016届湖南省益阳市箴言中学高三上学期第三次模拟化学试卷2016届河北省保定市高三上学期摸底考试化学试卷湖南省长沙市明德中学2016届高三上学期第三次月考化学试题2015-2016学年浙江省宁波市北仑中学高二下学期期中考试化学试卷湖南省长沙市一中2019-2020学年高一上学期期末考试化学试题黑龙江省大庆实验中学2019-2020学年高一下学期第一次阶段考试化学试题四川省乐山市第四中学2019-2020学年高一下学期期中考试化学试题陕西西北工业大学附属中学2022-2023学年高一下学期期中考试化学试题
10 . X、Y、Z是三种常见元素的单质,甲、乙是两种常见的化合物,这些单质和甲乙化合物之间存在如图所示的关系。下列说法一定正确的是


| A.X、Y、Z都是非金属单质 |
| B.X、Y、Z中至少有一种是金属单质 |
| C.若X、Y为金属单质,则Z必为非金属单质 |
| D.若X、Y为非金属单质,则Z必为金属单质 |
您最近一年使用:0次



