名校
1 . 下列有关铁及其化合物的说法中正确的是
| A.高温下,Fe与水蒸气反应生成Fe2O3和H2 |
| B.Fe2(SO4)3与KSCN反应产生血红色沉淀 |
| C.除去FeCl2溶液中的FeCl3杂质,可以向溶液中加入过量的铁粉,然后过滤 |
| D.Fe(OH)2为白色固体,不溶于水,能在空气中稳定存在 |
您最近一年使用:0次
2022-03-24更新
|
260次组卷
|
3卷引用:吉林省长春市希望高中2021-2022学年高一上学期期末考试化学试题
名校
2 . 电子工业常用 溶液腐蚀覆铜板上的铜箔,制造印刷电路板。从腐蚀废液(主要含
溶液腐蚀覆铜板上的铜箔,制造印刷电路板。从腐蚀废液(主要含 、
、 、
、 )中回收铜,并重新获得
)中回收铜,并重新获得 溶液,处理流程如下:
溶液,处理流程如下:
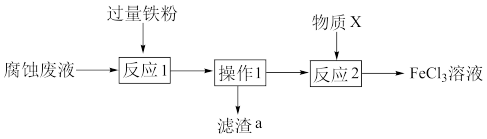
下列说法不正确的是
 溶液腐蚀覆铜板上的铜箔,制造印刷电路板。从腐蚀废液(主要含
溶液腐蚀覆铜板上的铜箔,制造印刷电路板。从腐蚀废液(主要含 、
、 、
、 )中回收铜,并重新获得
)中回收铜,并重新获得 溶液,处理流程如下:
溶液,处理流程如下:
下列说法不正确的是
A. 溶液腐蚀铜箔的原理为 溶液腐蚀铜箔的原理为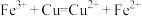 |
| B.反应1和反应2都发生了氧化还原反应 |
| C.实验室中进行操作1时,用到的主要玻璃仪器有漏斗、烧杯和玻璃棒 |
D.滤渣a的主要成分是Cu和Fe,物质X可以选用酸性 溶液 溶液 |
您最近一年使用:0次
2022-03-23更新
|
587次组卷
|
4卷引用:吉林省长春市第二中学2022-2023学年高一上学期期末考试化学试题
名校
3 . 长期放置的FeSO4溶液易被氧化而变质,某兴趣小组进行了如下实验:
(1)设计实验检验FeSO4溶液的变质程度,请将方案补充完整。
③若要使部分变质的FeSO4复原,方法是___________ 。(写离子反应方程式)
(2)利用部分变质的FeSO4溶液制备Fe2O3,请在内填写所需试剂或条件
①________ ;②________ ;③________ ;
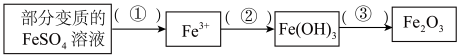
④若100mL该变质溶液制得1.6gFe2O3,则变质前FeSO4溶液的浓度为___________ 。
(3)FeSO4可用作补铁剂,使用时建议与维生素C同服,同学甲猜测维生素C可将Fe3+转化为Fe2+,以利于人体吸收。为了验证这一猜想,设计了如下实验:
由上述实验能否得出“维生素C可将Fe3+转化为Fe2+”的结论?请说明结论和理由___________ 。
(1)设计实验检验FeSO4溶液的变质程度,请将方案补充完整。
| 实验方案 | 实验现象 | 实验结论 | |
| 步骤1 | 取待检测液于试管中,向其中滴加KSCN溶液 | ① | FeSO4溶液部分变质 |
| 步骤2 | 取待检测液于试管中,向其中滴加少量酸性高锰酸钾溶液 | ② | |
(2)利用部分变质的FeSO4溶液制备Fe2O3,请在内填写所需试剂或条件
①

④若100mL该变质溶液制得1.6gFe2O3,则变质前FeSO4溶液的浓度为
(3)FeSO4可用作补铁剂,使用时建议与维生素C同服,同学甲猜测维生素C可将Fe3+转化为Fe2+,以利于人体吸收。为了验证这一猜想,设计了如下实验:
| 实验方案 | 实验现象 |
| 取适量Fe2(SO4)3溶液于试管中,加入维生素C片,振荡溶解后,滴加酸性高锰酸钾溶液。 | 紫色褪去 |
您最近一年使用:0次
名校
4 . 电子工业常用30%的 溶液腐蚀附在绝缘板上的铜箔,制造印刷电路板。
溶液腐蚀附在绝缘板上的铜箔,制造印刷电路板。
(1)写出 溶液与金属铜反应的离子方程式:
溶液与金属铜反应的离子方程式:___________ 。
(2)检验溶液中存在 的试剂是
的试剂是___________ ,证明 存在的现象是
存在的现象是___________ 。
(3)某小组采取下列步骤从使用过的腐蚀废液中回收钢,并重新获得 溶液:
溶液:

操作Ⅰ和Ⅱ使用到的主要玻璃仪器有___________ ,请写出通入⑥后发生反应的离子方程式:___________ 。
(4)实验室里保存 溶液时,常在溶液中加入铁钉或铁粉防止溶液里的
溶液时,常在溶液中加入铁钉或铁粉防止溶液里的 被氧化,请用离子方程式说明其中的道理:
被氧化,请用离子方程式说明其中的道理:___________ 。
(5)若某腐蚀液中含 、
、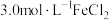 、
、 ,取200mL腐蚀液按上述步骤回收铜,为充分回收铜,加入①的质量最小为
,取200mL腐蚀液按上述步骤回收铜,为充分回收铜,加入①的质量最小为___________ 。
 溶液腐蚀附在绝缘板上的铜箔,制造印刷电路板。
溶液腐蚀附在绝缘板上的铜箔,制造印刷电路板。(1)写出
 溶液与金属铜反应的离子方程式:
溶液与金属铜反应的离子方程式:(2)检验溶液中存在
 的试剂是
的试剂是 存在的现象是
存在的现象是(3)某小组采取下列步骤从使用过的腐蚀废液中回收钢,并重新获得
 溶液:
溶液:
操作Ⅰ和Ⅱ使用到的主要玻璃仪器有
(4)实验室里保存
 溶液时,常在溶液中加入铁钉或铁粉防止溶液里的
溶液时,常在溶液中加入铁钉或铁粉防止溶液里的 被氧化,请用离子方程式说明其中的道理:
被氧化,请用离子方程式说明其中的道理:(5)若某腐蚀液中含
 、
、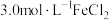 、
、 ,取200mL腐蚀液按上述步骤回收铜,为充分回收铜,加入①的质量最小为
,取200mL腐蚀液按上述步骤回收铜,为充分回收铜,加入①的质量最小为
您最近一年使用:0次
5 . 为探究某食品包装袋内一小包脱氧剂中的还原铁粉是否变质,分别取少量样品溶于盐酸,再进行下列实验,其中结论正确的是
| A.若滴加KSCN溶液,溶液变红,说明铁粉变质 |
| B.若滴加KSCN溶液,溶液未变红,说明铁粉未变质 |
| C.若依次滴加氯水,KSCN溶液,溶液变红,说明铁粉全部变质 |
| D.若滴加KSCN溶液,溶液未变红;再滴加氯水,溶液变红,说明铁粉全部变质 |
您最近一年使用:0次
2022-02-27更新
|
1448次组卷
|
24卷引用:吉林市田家炳高级中学2022-2023学年高一上学期期末考试化学试题
吉林市田家炳高级中学2022-2023学年高一上学期期末考试化学试题天津市红桥区2020-2021学年高三上学期期中考试化学试题第一节 铁及其化合物 第2课时 铁盐、亚铁盐内蒙古包头市2021-2022学年高一上学期期末考试化学试题辽宁省沈阳市2021-2022学年高一上学期期末质量监测化学试题2广东省化州市第一中学2020-2021学年高一上学期期末考试化学试题北京市北京师范大学第二附属中学2022-2023学年高一上学期12月月考化学试题湖南省株洲世纪星高级中学2022-2023学年高一上学期期末考试化学试题广东省广州中学2022-2023学年高一上学期期末考试化学试题天津市南开中学2022-2023学年高一上学期期末考试化学试题内蒙古赤峰市红山区2022-2023学年高一上学期期末质量检测化学试题内蒙古包头市2022-2023学年高一上学期期末考试化学试题内蒙古呼伦贝尔市满洲里市第一中学2022-2023学年高一下学期第一次月考化学试题广东省东莞市南城开心实验学校2022-2023学年高一上学期12月半月考化学试题四川省绵阳南山中学2022-2023学年高一上学期期末模拟化学试题湖南省长沙市珺琟高级中学2023-2024学年高一上学期第二次月考化学试题 四川省宜宾市第四中学校2023-2024学年高一上学期1月期末化学试题云南省昆明市五华区2023-2024学年高一上学期1月期末化学试题天津市静海区第一中学2023-2024学年高一上学期12月月考化学试题浙江省丽水市三校联考2023-2024学年高一上学期12月月考化学试题四川省江油市太白中学2023-2024学年高一上学期第三次月考化学试题湖南省常德石门一中2023-2024年上学期高一年级化学期末考试卷(适用湖南地区))湖南省长沙市长郡中学2023-2024学年高一下学期选科适应性检测化学试卷河南省开封市联考2023-2024学年高一上学期1月期末化学试题
名校
6 . 部分含铁微粒所带的电荷数与其中铁元素化合价的关系如图所示,由该图可预测含铁微粒间相互转化时所需试剂。下列推断不合理的是
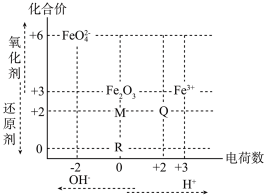

| A.M一定为FeO |
| B.若R为单质,则常温下浓硫酸可使R钝化 |
| C.若Q为金属阳离子,则可用K3[Fe(CN)6]溶液检验 |
D.Fe3+与氧化剂在碱性条件下反应可生成FeO |
您最近一年使用:0次
2022-02-26更新
|
1326次组卷
|
8卷引用:吉林省长春市第二中学2023-2024学年高三上学期10月月考化学试题
吉林省长春市第二中学2023-2024学年高三上学期10月月考化学试题广东省深圳市普通高中2022届高三下学期第一次调研考试化学试题(已下线)专项05 氧化还原反应-备战2022年高考化学阶段性新题精选专项特训(全国卷)(3月期)(已下线)押广东卷化学第10题 元素及其化合物-备战2022年高考化学临考题号押题(广东卷)河北省衡水中学2021-2022学年高三下学期二调考试化学试题浙江省舟山市定海第一中学2021-2022学年高一下学期4月质量检测化学试题(已下线)题型27 铁及其化合物的性质、用途及相关计算广东省汕尾市华大实验学校2021-2022学年高三下学期第二次周考化学试题
名校
解题方法
7 . 实验是解决化学问题的基本途径。下列对于某些离子的检验及结论正确的是
A.向某溶液中加入 溶液,有白色沉淀生成,则溶液中一定含 溶液,有白色沉淀生成,则溶液中一定含 |
B.用铂丝蘸取某溶液在火焰上灼烧,火焰呈黄色,则溶液中一定含 无 无 |
C.向溶液中滴加KSCN溶液,溶液无明显变化,溶液中一定不含 |
D.向某溶液中加入足量稀盐酸,有能使澄清石灰水变浑浊的气体生成,则溶液中一定含 |
您最近一年使用:0次
2022-02-23更新
|
570次组卷
|
5卷引用:吉林省梅河口市第五中学2021-2022学年高一上学期期末联考化学试题
8 .  溶液中含有少量
溶液中含有少量 杂质,除杂所需的试剂是
杂质,除杂所需的试剂是
 溶液中含有少量
溶液中含有少量 杂质,除杂所需的试剂是
杂质,除杂所需的试剂是| A.铜片 | B.铁粉 | C.氯气 | D.锌粒 |
您最近一年使用:0次
2022-02-16更新
|
107次组卷
|
3卷引用:吉林省长春市第二十九中学2021-2022学年高一上学期第二学程考试化学(文)试题
9 . 电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
(1)写出FeCl3溶液与金属铜发生反应的离子方程式:____ 。
Ⅰ.某工程师为了从使用过的腐蚀废液中回收铜,并重新获得纯净的FeCl3溶液,准备采用下列步骤:
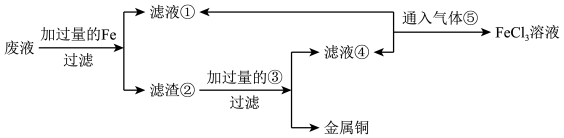
(2)请写出上述实验中有关物质的化学式:③_____ 。
(3)要证明某溶液中不含Fe3+而可能含有Fe2+,进行如下实验操作时的最佳顺序为_____ 。
①加入足量氯水②加入足量KMnO4溶液③加入少量KSCN溶液
(4)写出向①④的混合液中通入⑤的离子方程式:_____ 。
Ⅱ.用如图所示装置制取和观察Fe(OH)2在空气中被氧化时的颜色变化,实验时必须使用铁屑及6mol•L-1的硫酸,其他试剂任选。填写下列空白:
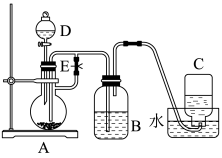
(5)B中盛有一定量的NaOH溶液,A中应预先加入的试剂是____ ,实验开始时先将活塞E打开,再打开分液漏斗D活塞让酸液流下,在C中收集到气体。
(6)简述生成Fe(OH)2的操作过程:____ 。
(7)拔去装置B中的橡皮塞,让空气进入,写出有关反应的化学方程式:____ 。
(1)写出FeCl3溶液与金属铜发生反应的离子方程式:
Ⅰ.某工程师为了从使用过的腐蚀废液中回收铜,并重新获得纯净的FeCl3溶液,准备采用下列步骤:

(2)请写出上述实验中有关物质的化学式:③
(3)要证明某溶液中不含Fe3+而可能含有Fe2+,进行如下实验操作时的最佳顺序为
①加入足量氯水②加入足量KMnO4溶液③加入少量KSCN溶液
| A.①③ | B.③② | C.③① | D.①②③ |
Ⅱ.用如图所示装置制取和观察Fe(OH)2在空气中被氧化时的颜色变化,实验时必须使用铁屑及6mol•L-1的硫酸,其他试剂任选。填写下列空白:

(5)B中盛有一定量的NaOH溶液,A中应预先加入的试剂是
(6)简述生成Fe(OH)2的操作过程:
(7)拔去装置B中的橡皮塞,让空气进入,写出有关反应的化学方程式:
您最近一年使用:0次
名校
10 . 一定条件下,将一定量Fe3O4溶于过量盐酸生成FeCl2和FeCl3, 分别取少量反应后的溶液进行以下实验,有关实验描述正确的是
| A.滴加KSCN溶液,若溶液变红色证明溶液中含有Fe3+ |
| B.加入5.6g铁粉恰好完全反应,则Fe3O4的质量为23.2g |
| C.用溶液在铜片上写字,一段时间后洗去溶液,观察到铜片表面无明显现象 |
| D.先向溶液中通入氯气,再滴加KSCN溶液,若变红色证明溶液中含有Fe2+ |
您最近一年使用:0次
2022-01-13更新
|
579次组卷
|
3卷引用:吉林省长春市第六中学2022-2023学年高一上学期期末考试化学试题
吉林省长春市第六中学2022-2023学年高一上学期期末考试化学试题江苏省江阴市普通高中2021-2022学年高一上学期期终教学质量抽测建议卷化学试题(已下线)2022年广东卷高考真题变式题(11-16)



