1 . 健康人体内含铁元素大约 ,人体内铁元素以
,人体内铁元素以 和
和 的形式存在,
的形式存在, 易被吸收,所以给贫血者补充铁元素时,应补充亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中
易被吸收,所以给贫血者补充铁元素时,应补充亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中 的存在,设计并进行了如下实验:
的存在,设计并进行了如下实验:_______ ,试剂2的化学式为_______ 。
(2)加入新制氯水,溶液中发生的氧化还原反应的离子方程式是_______ 。
(3)加入试剂2时溶液为淡红色,说明“速力菲”中的 已部分被氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有
已部分被氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有_______ 性。
(4)不仅溶液中 易被氧化成
易被氧化成 ,溶液中白色沉淀
,溶液中白色沉淀 更易被
更易被 氧化,请写出反应的化学方程式:
氧化,请写出反应的化学方程式:_______ ,现象为_______ 。
 ,人体内铁元素以
,人体内铁元素以 和
和 的形式存在,
的形式存在, 易被吸收,所以给贫血者补充铁元素时,应补充亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中
易被吸收,所以给贫血者补充铁元素时,应补充亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中 的存在,设计并进行了如下实验:
的存在,设计并进行了如下实验: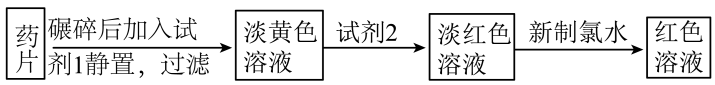
(2)加入新制氯水,溶液中发生的氧化还原反应的离子方程式是
(3)加入试剂2时溶液为淡红色,说明“速力菲”中的
 已部分被氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有
已部分被氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有(4)不仅溶液中
 易被氧化成
易被氧化成 ,溶液中白色沉淀
,溶液中白色沉淀 更易被
更易被 氧化,请写出反应的化学方程式:
氧化,请写出反应的化学方程式:
您最近一年使用:0次
2 . 下列说法不正确的是
| A.铁元素在自然界中以化合态和游离态形式存在 |
B. 中铁的化合价有 中铁的化合价有 和 和 价,是一种混合物 价,是一种混合物 |
C.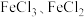 和 和 都可以通过化合反应制取 都可以通过化合反应制取 |
D. 铁与足量稀盐酸反应,转移电子数为 铁与足量稀盐酸反应,转移电子数为 |
您最近一年使用:0次
3 . 某班同学用如下实验探究Fe2+与Fe3+的转化,回答下列问题,
(1)实验I:Fe3+转化为Fe2+
实验步骤及现象:甲组同学将少量铜粉加入1mL0.lmol/LFeCl3溶液中,观察到铜粉消失,溶液黄色变浅,加入蒸馏水后无明显现象:乙组同学将过量铜粉加入1mL0.lmol/LFeCl3溶液中,观察到铜粉有剩余,溶液黄色褪去,加入蒸馏水后出现白色沉淀;丙组同学将过量铜粉加入lmL0.05mol/LFe2(SO4)3溶液中,观察到铜粉有剩余,溶液黄色褪去,变成蓝色,测入蒸馏水后无白色沉淀。
①分别取三组实验反应后的溶液于三支试管中加入几滴K3[Fe(CN)6]溶液,出现蓝色沉淀,证明生成了Fe2+;分析三组实验结果,实验中均发生的反应离子方程式为_______ 。
②对比三组实验,说明加入蒸馏水后沉淀的产生与_______ 有关。
③向丙组实验后的溶液中加入饱和NaCl溶液可能出现的现象为_______ 。
④丙组在检验反应后的溶液中是否存在Fe3+时,取反应后上层清液于试管中,滴加3滴KSCN溶液,结果出现白色沉淀,查阅资料:i.SCN-的化学性质与I-相似,CuSCN为白色固体;ii.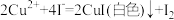 ,写出该实验中出现白色沉淀的离子方程式为
,写出该实验中出现白色沉淀的离子方程式为_______ 。
(2)实验II:Fe2+转化为Fe3+
实验步骤及现象:向3mL0.1mol/LFeSO4溶液中加入稍过量稀硝酸,溶液变为棕色,放置一段时间后,棕色消失,溶液变为黄色,已知硝酸具有氧化性, (棕色):
(棕色):
⑤使用的FeSO4溶液中存在少量铁屑,其目的是_______ 。
⑥实验中产生NO的原因为_______ (用离子方程式表示)。
(1)实验I:Fe3+转化为Fe2+
实验步骤及现象:甲组同学将少量铜粉加入1mL0.lmol/LFeCl3溶液中,观察到铜粉消失,溶液黄色变浅,加入蒸馏水后无明显现象:乙组同学将过量铜粉加入1mL0.lmol/LFeCl3溶液中,观察到铜粉有剩余,溶液黄色褪去,加入蒸馏水后出现白色沉淀;丙组同学将过量铜粉加入lmL0.05mol/LFe2(SO4)3溶液中,观察到铜粉有剩余,溶液黄色褪去,变成蓝色,测入蒸馏水后无白色沉淀。
①分别取三组实验反应后的溶液于三支试管中加入几滴K3[Fe(CN)6]溶液,出现蓝色沉淀,证明生成了Fe2+;分析三组实验结果,实验中均发生的反应离子方程式为
②对比三组实验,说明加入蒸馏水后沉淀的产生与
③向丙组实验后的溶液中加入饱和NaCl溶液可能出现的现象为
④丙组在检验反应后的溶液中是否存在Fe3+时,取反应后上层清液于试管中,滴加3滴KSCN溶液,结果出现白色沉淀,查阅资料:i.SCN-的化学性质与I-相似,CuSCN为白色固体;ii.
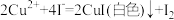 ,写出该实验中出现白色沉淀的离子方程式为
,写出该实验中出现白色沉淀的离子方程式为(2)实验II:Fe2+转化为Fe3+
实验步骤及现象:向3mL0.1mol/LFeSO4溶液中加入稍过量稀硝酸,溶液变为棕色,放置一段时间后,棕色消失,溶液变为黄色,已知硝酸具有氧化性,
 (棕色):
(棕色):⑤使用的FeSO4溶液中存在少量铁屑,其目的是
⑥实验中产生NO的原因为
您最近一年使用:0次
4 . 能正确表示下列反应的离子方程式为
A.向 溶液中通入过量 溶液中通入过量 : : |
B.食醋去除水垢中的 : :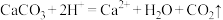 |
C.向碳酸钠溶液中通入少量 : : |
D.次磷酸(一元弱酸)与足量NaOH溶液反应: |
您最近一年使用:0次
2024-04-03更新
|
63次组卷
|
2卷引用:安徽省六安市叶集皖西当代中学2023-2024学年高一下学期3月月考化学试题
解题方法
5 . 能正确表示下列反应的离子方程式的是
A.FeBr2溶液通入足量Cl2: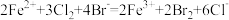 |
B.NaAlO2溶液中通入过量的CO2: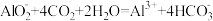 |
C.FeSO4溶液中加入H2O2产生沉淀: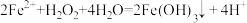 |
D.氯化铜溶液中通入硫化氢: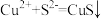 |
您最近一年使用:0次
名校
解题方法
6 . 无色溶液滴到石蕊试纸上显红色,此溶液中能大量共存的一组离子是
A. 、 、 、 、 、 、 | B. 、 、 、 、 、 、 |
C. 、 、 、 、 、 、 | D. 、 、 、 、 、 、 |
您最近一年使用:0次
7 . 依据下列实验,预测的实验现象正确的是
| 选项 | 实验内容 | 预测的实验现象 |
| A | 向 溶液中滴加NaOH溶液至过量 溶液中滴加NaOH溶液至过量 | 先产生白色沉淀后沉淀消失 |
| B | 向 溶液中滴加KSCN溶液 溶液中滴加KSCN溶液 | 溶液变红色 |
| C | 向漂白粉溶液中通入少量 气体 气体 | 溶液出现白色沉淀 |
| D | 向酸性 溶液中滴加 溶液中滴加 溶液至过量 溶液至过量 | 溶液紫红色褪去 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
8 . 下列关于铁及其化合物说法正确的是
A.过量的铁丝在 中燃烧生成 中燃烧生成 |
B. 不稳定,在空气里能被氧化成 不稳定,在空气里能被氧化成 |
| C.铁性质活泼,铁元素在自然界中都以化合态的形式存在 |
D.向饱和 溶液中滴加适量 溶液中滴加适量 溶液即可得到氢氧化铁胶体 溶液即可得到氢氧化铁胶体 |
您最近一年使用:0次
名校
9 . 工业上用赤铁矿(主要成分为 ,含
,含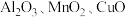 等杂质)制备绿矾
等杂质)制备绿矾 的流程如下:
的流程如下: 能与
能与 溶液反应生成可溶性盐
溶液反应生成可溶性盐 。
。
回答下列问题:
(1)试剂a为___________ 。
(2)试剂b需过量,其目的是___________ ;“滤渣”的成分是___________ 。
(3)“结晶”需隔绝空气,原因是___________ 。
(4)绿矾隔绝空气加强热可用于制备红色颜料铁红。取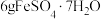 样品隔绝空气加热(杂质不反应),受热过程中样品质量随温度变化的曲线如图所示(已知固体
样品隔绝空气加热(杂质不反应),受热过程中样品质量随温度变化的曲线如图所示(已知固体 不含结晶水)。
不含结晶水)。 主要成分的化学式为
主要成分的化学式为___________ 。
②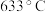 时,除生成铁红外,同时生成能使
时,除生成铁红外,同时生成能使 溶液变浑浊的气体和使品红溶液裉色的气体。该温度下反应的化学方程式为
溶液变浑浊的气体和使品红溶液裉色的气体。该温度下反应的化学方程式为___________ ;该样品中 的质量分数为
的质量分数为___________  (保留一位小数)。
(保留一位小数)。
 ,含
,含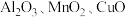 等杂质)制备绿矾
等杂质)制备绿矾 的流程如下:
的流程如下: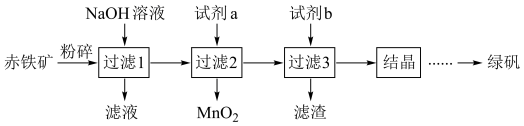
 能与
能与 溶液反应生成可溶性盐
溶液反应生成可溶性盐 。
。回答下列问题:
(1)试剂a为
(2)试剂b需过量,其目的是
(3)“结晶”需隔绝空气,原因是
(4)绿矾隔绝空气加强热可用于制备红色颜料铁红。取
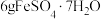 样品隔绝空气加热(杂质不反应),受热过程中样品质量随温度变化的曲线如图所示(已知固体
样品隔绝空气加热(杂质不反应),受热过程中样品质量随温度变化的曲线如图所示(已知固体 不含结晶水)。
不含结晶水)。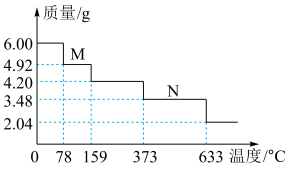
 主要成分的化学式为
主要成分的化学式为②
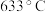 时,除生成铁红外,同时生成能使
时,除生成铁红外,同时生成能使 溶液变浑浊的气体和使品红溶液裉色的气体。该温度下反应的化学方程式为
溶液变浑浊的气体和使品红溶液裉色的气体。该温度下反应的化学方程式为 的质量分数为
的质量分数为 (保留一位小数)。
(保留一位小数)。
您最近一年使用:0次
2024-02-02更新
|
263次组卷
|
3卷引用:安徽师范大学附属中学2023-2024学年高一下学期3月阶段性教学质量监测化学试题
名校
解题方法
10 . 将绿矾( )溶于水配制成溶液喷施在叶面上,可解决植物叶面变黄问题,因此绿矾又被誉为“铁肥”。下列有关“铁肥”说法错误的是
)溶于水配制成溶液喷施在叶面上,可解决植物叶面变黄问题,因此绿矾又被誉为“铁肥”。下列有关“铁肥”说法错误的是
 )溶于水配制成溶液喷施在叶面上,可解决植物叶面变黄问题,因此绿矾又被誉为“铁肥”。下列有关“铁肥”说法错误的是
)溶于水配制成溶液喷施在叶面上,可解决植物叶面变黄问题,因此绿矾又被誉为“铁肥”。下列有关“铁肥”说法错误的是| A.“铁肥”易被空气氧化变质 |
B.可用 溶液检验“铁肥”是否发生变质 溶液检验“铁肥”是否发生变质 |
| C.为保证“铁肥”的效果,可向配制后的溶液中加入少量铁粉 |
D. 的摩尔质量为 的摩尔质量为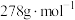 |
您最近一年使用:0次
2023-12-31更新
|
292次组卷
|
8卷引用:安徽省灵璧中学名校联考2023-2024学年高一上学期1月阶段性考试化学试题



