名校
1 . 信息时代产生的大量电子垃圾对环境造成了极大的威胁。某“变废为宝”学生探究小组将一批废弃的线路板简单处理后,70%Cu、25%Al、4%Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线。_______ ;得到滤渣1的主要成分为_______ 。
(2)步骤①中能否用稀盐酸代替稀硫酸?_______ (填“能”或“否”)。
(3)步骤②加入H2O2的作用是_______ 。
(4)从滤液2获得硫酸铜晶体的方法是蒸发浓缩、_______ 。该过程可能会用到以下实验仪器中的:_______ 。(写名称)_______ 方案不可行,原因是_______ 。
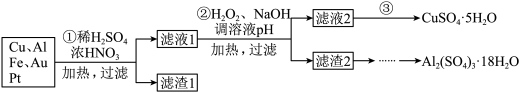
(2)步骤①中能否用稀盐酸代替稀硫酸?
(3)步骤②加入H2O2的作用是
(4)从滤液2获得硫酸铜晶体的方法是蒸发浓缩、

您最近一年使用:0次
名校
2 . 下列实验方案不可行的是
| A.用碱石灰干燥氨气 | B.用蓝色石蕊试液检验酸性溶液 |
| C.通入Cl2除去FeCl3溶液中的FeCl2 | D.加入Fe粉除去Al3+溶液中的杂质Cu2+ |
您最近一年使用:0次
3 . 下列离子方程式正确的是
A. 溶于水: 溶于水: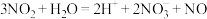 |
B. 溶液中加入过量NaOH溶液并加热: 溶液中加入过量NaOH溶液并加热: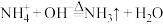 |
C. 气体通入氨水: 气体通入氨水: |
D.过量铁粉与稀硝酸混合,产生气体: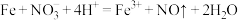 |
您最近一年使用:0次
名校
4 . 下列各组离子在强酸性条件下能大量共存的是
A.Ba2+、Na+、I-、NO | B.Ca2+、SO 、NO 、NO 、Cl- 、Cl- |
C.K+、Na+、Cl-、SO | D.NH 、Fe2+、Cl-、NO 、Fe2+、Cl-、NO |
您最近一年使用:0次
5 . 宏观辨识与微观探析是化学核心素养之一、下列物质性质与用途对应的离子方程式书写正确的是
A. 氧化海带灰酸性浸出液提取碘: 氧化海带灰酸性浸出液提取碘: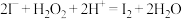 |
B. 与水反应用作潜水艇氧气来源: 与水反应用作潜水艇氧气来源: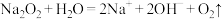 |
C.绿矾处理含 的酸性废水: 的酸性废水: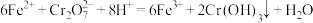 |
D.向 溶液中通入氨气可制备抗酸药 溶液中通入氨气可制备抗酸药 : :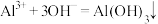 |
您最近一年使用:0次
名校
解题方法
6 . 实验室用 和
和 溶液制备碳酸亚铁的装置如图所示(夹持装置已省略),三颈烧瓶中产生白色沉淀及无色气体。下列说法不正确的是
溶液制备碳酸亚铁的装置如图所示(夹持装置已省略),三颈烧瓶中产生白色沉淀及无色气体。下列说法不正确的是
 和
和 溶液制备碳酸亚铁的装置如图所示(夹持装置已省略),三颈烧瓶中产生白色沉淀及无色气体。下列说法不正确的是
溶液制备碳酸亚铁的装置如图所示(夹持装置已省略),三颈烧瓶中产生白色沉淀及无色气体。下列说法不正确的是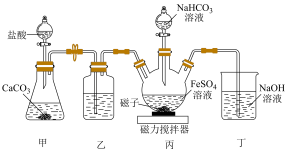
A.装置甲产生 可排除装置中的空气 可排除装置中的空气 |
B.装置乙中盛装的试剂为饱和 溶液 溶液 |
C.装置丙中发生反应的离子方程式: |
| D.反应结束后,将丙中反应液静置、过滤、洗涤、干燥,可得到碳酸亚铁 |
您最近一年使用:0次
2024-03-15更新
|
723次组卷
|
4卷引用:广东省江门市2023-2024学年高三一模考试化学卷
广东省江门市2023-2024学年高三一模考试化学卷江西省宜春市宜丰中学2023-2024学年高一下学期4月期中考试化学试题(已下线)压轴题03?物质的制备、检验、分离与提纯(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)(已下线)选择题1-5
7 . 铁泥是钢铁厂废弃物,经分析其成分如下表:
已知杂质不溶于酸。
综合利用废弃物,对资源利用和环境保护具有现实意义,铁泥常用于制备铁红,实验室模拟其工艺流程如下:

(1)酸浸过程中 与硫酸反应的离子方程式为
与硫酸反应的离子方程式为_______ 、_______ 。
(2)转化过程中发生反应的离子方程式为______________ 。从经济环保角度考虑,“转化”中可替代 的物质是
的物质是_______ 。检验溶液中的 常用的试剂是
常用的试剂是_______ 。
(3)滤液2中含有的主要离子有_______ 。
(4)煅烧步骤的化学反应方程式为______________
| 成分 |  |  |  |  | 水分 | 杂质 |
质量分数 | 74.25 | 7.28 | 3.56 | 3.67 | 8.12 | 3.12 |
综合利用废弃物,对资源利用和环境保护具有现实意义,铁泥常用于制备铁红,实验室模拟其工艺流程如下:

(1)酸浸过程中
 与硫酸反应的离子方程式为
与硫酸反应的离子方程式为(2)转化过程中发生反应的离子方程式为
 的物质是
的物质是 常用的试剂是
常用的试剂是(3)滤液2中含有的主要离子有
(4)煅烧步骤的化学反应方程式为
您最近一年使用:0次
名校
8 . 工业上用赤铁矿(主要成分为 ,含
,含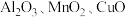 等杂质)制备绿矾
等杂质)制备绿矾 的流程如下:
的流程如下: 能与
能与 溶液反应生成可溶性盐
溶液反应生成可溶性盐 。
。
回答下列问题:
(1)试剂a为___________ 。
(2)试剂b需过量,其目的是___________ ;“滤渣”的成分是___________ 。
(3)“结晶”需隔绝空气,原因是___________ 。
(4)绿矾隔绝空气加强热可用于制备红色颜料铁红。取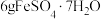 样品隔绝空气加热(杂质不反应),受热过程中样品质量随温度变化的曲线如图所示(已知固体
样品隔绝空气加热(杂质不反应),受热过程中样品质量随温度变化的曲线如图所示(已知固体 不含结晶水)。
不含结晶水)。 主要成分的化学式为
主要成分的化学式为___________ 。
②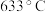 时,除生成铁红外,同时生成能使
时,除生成铁红外,同时生成能使 溶液变浑浊的气体和使品红溶液裉色的气体。该温度下反应的化学方程式为
溶液变浑浊的气体和使品红溶液裉色的气体。该温度下反应的化学方程式为___________ ;该样品中 的质量分数为
的质量分数为___________  (保留一位小数)。
(保留一位小数)。
 ,含
,含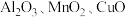 等杂质)制备绿矾
等杂质)制备绿矾 的流程如下:
的流程如下: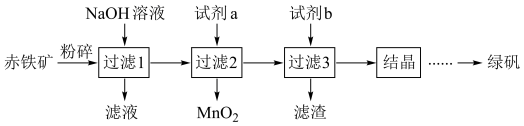
 能与
能与 溶液反应生成可溶性盐
溶液反应生成可溶性盐 。
。回答下列问题:
(1)试剂a为
(2)试剂b需过量,其目的是
(3)“结晶”需隔绝空气,原因是
(4)绿矾隔绝空气加强热可用于制备红色颜料铁红。取
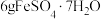 样品隔绝空气加热(杂质不反应),受热过程中样品质量随温度变化的曲线如图所示(已知固体
样品隔绝空气加热(杂质不反应),受热过程中样品质量随温度变化的曲线如图所示(已知固体 不含结晶水)。
不含结晶水)。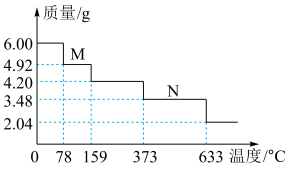
 主要成分的化学式为
主要成分的化学式为②
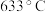 时,除生成铁红外,同时生成能使
时,除生成铁红外,同时生成能使 溶液变浑浊的气体和使品红溶液裉色的气体。该温度下反应的化学方程式为
溶液变浑浊的气体和使品红溶液裉色的气体。该温度下反应的化学方程式为 的质量分数为
的质量分数为 (保留一位小数)。
(保留一位小数)。
您最近一年使用:0次
2024-02-02更新
|
263次组卷
|
3卷引用:广东省化州市第一中学2023-2024学年高一下学期月考(一)化学试题
名校
9 . 下列各组物质,不会因反应条件(温度或者反应物用量)改变而引起产物改变的是
A. 溶液和 溶液和 | B.Fe和 |
C.Na和 | D.NaOH溶液和 |
您最近一年使用:0次
2023-06-08更新
|
336次组卷
|
7卷引用:广东省湛江市2023-2024学年高一上学期1月期末调研考试化学试题
10 . 部分含铁物质的分类与相应化合价关系如图所示。下列推断不合理的是


| A.通过化合反应和复分解反应均能直接得到 d |
| B.a→f→g→d 的每步转化均可一步实现 |
| C.h 具有强氧化性,在日常生活中可用于生活用水的消毒与净化 |
| D.c 溶于氢碘酸的离子方程式为Fe2O3 + 6H+= 2Fe3+ +3H2O |
您最近一年使用:0次
2023-06-07更新
|
321次组卷
|
3卷引用:广东省广州市黄广中学2023-2024学年高一上学期期末错题专项考化学试卷



