1 . “协同去污,变废为宝”为处理工业废水提供了新思路。现有含 、
、 的电镀废液以及含
的电镀废液以及含 的废液。现联合处理废水,回收
的废液。现联合处理废水,回收 并生产铁红和媒染剂
并生产铁红和媒染剂 ,回收过程如下,请回答以下问题:
,回收过程如下,请回答以下问题:________ 。
(2)对于该工艺的说法错误的是________。
(3)写出铁铜废液中加入试剂1发生的离子方程式________ 。滤液与含酸性 的废液反应的离子方程式为
的废液反应的离子方程式为________ 。
(4)证明滤液已被试剂3完全氧化的实验方法是________ 。
(5)从 溶液制取
溶液制取 晶体的实验操作方法为蒸发浓缩、
晶体的实验操作方法为蒸发浓缩、________ 、过滤、________ 、干燥。
(6)已知 化学性质与
化学性质与 类似,若将流程中
类似,若将流程中 的溶液转化为氢氧化铬,则转化过程中发生的离子方程式为
的溶液转化为氢氧化铬,则转化过程中发生的离子方程式为________ 。
 、
、 的电镀废液以及含
的电镀废液以及含 的废液。现联合处理废水,回收
的废液。现联合处理废水,回收 并生产铁红和媒染剂
并生产铁红和媒染剂 ,回收过程如下,请回答以下问题:
,回收过程如下,请回答以下问题: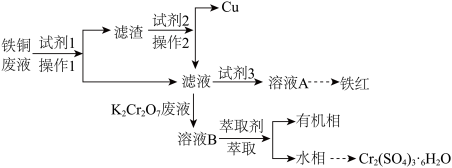
(2)对于该工艺的说法错误的是________。
| A.操作1和操作2都是过滤 |
B.试剂1是过量的 粉,试剂2是过量的 粉,试剂2是过量的 |
| C.可从有机相中提取出某成分加入到溶液A中,提高产量,剩余成分可循环利用 |
D.试剂3只能是 ,目的是将 ,目的是将 氧化成 氧化成 |
(3)写出铁铜废液中加入试剂1发生的离子方程式
 的废液反应的离子方程式为
的废液反应的离子方程式为(4)证明滤液已被试剂3完全氧化的实验方法是
(5)从
 溶液制取
溶液制取 晶体的实验操作方法为蒸发浓缩、
晶体的实验操作方法为蒸发浓缩、(6)已知
 化学性质与
化学性质与 类似,若将流程中
类似,若将流程中 的溶液转化为氢氧化铬,则转化过程中发生的离子方程式为
的溶液转化为氢氧化铬,则转化过程中发生的离子方程式为
您最近一年使用:0次
2 .  磁材料应用广泛,制备流程如图。下列说法错误的是
磁材料应用广泛,制备流程如图。下列说法错误的是
 磁材料应用广泛,制备流程如图。下列说法错误的是
磁材料应用广泛,制备流程如图。下列说法错误的是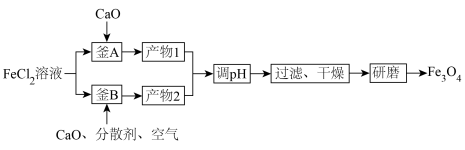
| A.“产物1”需要密封保存防止氧化 |
B.“釜B”中主要反应的化学方程式为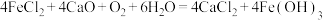 |
C.“产物1”与“产物2”中参与生成 反应的物质的物质的量之比为2:1 反应的物质的物质的量之比为2:1 |
| D.“分散剂”可破坏形成的胶体来促进氧化 |
您最近一年使用:0次
名校
3 . 碱式硫酸铁[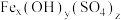 ](其中Fe元素为+3价)是一种新型高效絮凝剂。一种利用废铁屑(含Fe和少量
](其中Fe元素为+3价)是一种新型高效絮凝剂。一种利用废铁屑(含Fe和少量 、
、 )生产碱式硫酸铁的工艺流程如下:
)生产碱式硫酸铁的工艺流程如下:
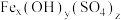 ](其中Fe元素为+3价)是一种新型高效絮凝剂。一种利用废铁屑(含Fe和少量
](其中Fe元素为+3价)是一种新型高效絮凝剂。一种利用废铁屑(含Fe和少量 、
、 )生产碱式硫酸铁的工艺流程如下:
)生产碱式硫酸铁的工艺流程如下: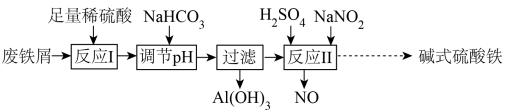
A.x、y、z一定符合关系式: |
B.“过滤”所得滤液中只含溶质 |
| C.“反应Ⅰ”中包含的反应类型有置换反应、化合反应和复分解反应 |
D.在实际生产中,反应Ⅱ常同时通入 以减少 以减少 的用量,若有11.2L(标准状况)的 的用量,若有11.2L(标准状况)的 参与反应,则相当于节约2mol 参与反应,则相当于节约2mol |
您最近一年使用:0次
4 . 下图是一种综合处理SO2废气的工艺流程。下列说法正确的是
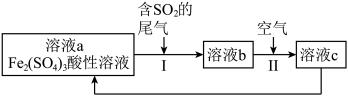
| A.操作Ⅱ发生反应的离子方程式为:2Fe2++4H++O2=2Fe3++2H2O |
| B.溶液b中阳离子只有Fe2+ |
| C.溶液a转化为溶液b的反应中,SO2被氧化 |
| D.加入FeO可以使溶液c转化为溶液a |
您最近一年使用:0次
解题方法
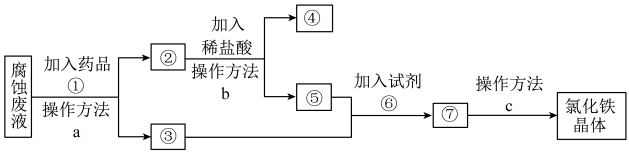
5 . 一种从腐蚀废液回收金属铜并获得氯化铁晶体的工艺流程如下。请根据流程,回答下列问题。(提示:为充分除去杂质,所加试剂均为过量)__________________ 。
(2)④所代表的物质是______ (用化学式表示)。
(3)操作方法a、b、c中是过滤的是______ (填序号)。
(4)若取2 mL溶液⑤加入试管中,然后滴加氢氧化钠溶液,产生白色沉淀,______ (补全实验现象),此过程涉及氧化还原反应的化学方程式是_________________ 。
(5)试剂⑥是 时,发生反应的化学方程式是
时,发生反应的化学方程式是__________________ 。
(2)④所代表的物质是
(3)操作方法a、b、c中是过滤的是
(4)若取2 mL溶液⑤加入试管中,然后滴加氢氧化钠溶液,产生白色沉淀,
(5)试剂⑥是
 时,发生反应的化学方程式是
时,发生反应的化学方程式是
您最近一年使用:0次
名校
6 . 能正确表示下列反应的离子方程式的是
| A.氯化铁溶液腐蚀铜箔:Fe3++Cu=Fe2++Cu2+ |
| B.向FeBr2溶液中通入过量Cl2:2Fe2++Cl2=2Fe3++2Cl﹣ |
C.向Na2CO3溶液中滴入少量盐酸:CO +2H+=H2O+CO2↑ +2H+=H2O+CO2↑ |
| D.用“胃舒平”治疗胃酸过多:Al(OH)3+3H+=Al3++3H2O |
您最近一年使用:0次
名校
解题方法
7 . 利用下列装置(夹持装置略)进行实验,下列说法不正确的是


| A.用甲装置检验H2中的HCl |
| B.用乙装置可以制取H2、CO2、SO2、NH3、NO等气体 |
| C.装置丙从FeSO4溶液中获得纯净的FeSO4固体 |
| D.甲丁所示仪器不能提纯Fe(OH)3胶体 |
您最近一年使用:0次
8 . 碳酸亚铁晶体[ ]为白色固体,不溶于水,干燥品在空气中稳定,湿品在空气中缓慢氧化为
]为白色固体,不溶于水,干燥品在空气中稳定,湿品在空气中缓慢氧化为 呈茶色,可用作阻燃剂、动物饲料铁添加剂、补血剂等。回答下列问题:
呈茶色,可用作阻燃剂、动物饲料铁添加剂、补血剂等。回答下列问题:
(1)实验室利用 溶液和
溶液和 溶液制备
溶液制备 ,实验装置(夹持仪器已省略)如图所示:
,实验装置(夹持仪器已省略)如图所示:

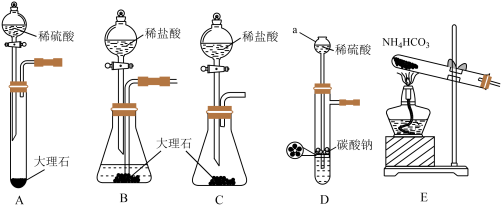
①方框内为制取 的装置,下列装置和药品较为适宜的是
的装置,下列装置和药品较为适宜的是_________ (填字母)。
②装置D中仪器a的名称是___________ 。
③根据①的选择,装置甲中试剂a的名称是_____________ 。
(2) 的制备,步骤如下:
的制备,步骤如下:
通入一段时间 后,向
后,向 溶液中加入过量
溶液中加入过量 溶液,搅拌,反应后过滤,将沉淀洗涤、干燥,得到
溶液,搅拌,反应后过滤,将沉淀洗涤、干燥,得到 。
。
①生成 的离子方程式为
的离子方程式为_________________ 。
②装置丙的作用是_________________ 。
(3)将 溶液换成
溶液换成 溶液能提高产品纯度,原因是
溶液能提高产品纯度,原因是________________ 。
(4)某同学查阅资料得知,煅烧 的产物中含有+2价铁元素,于是他设计了由
的产物中含有+2价铁元素,于是他设计了由 制备
制备 的方案。先向
的方案。先向 中依次加入试剂:稀硫酸、①
中依次加入试剂:稀硫酸、①___________ 和②____________ ;然后再③__________ (填操作)灼烧,即可得到 。
。
 ]为白色固体,不溶于水,干燥品在空气中稳定,湿品在空气中缓慢氧化为
]为白色固体,不溶于水,干燥品在空气中稳定,湿品在空气中缓慢氧化为 呈茶色,可用作阻燃剂、动物饲料铁添加剂、补血剂等。回答下列问题:
呈茶色,可用作阻燃剂、动物饲料铁添加剂、补血剂等。回答下列问题:(1)实验室利用
 溶液和
溶液和 溶液制备
溶液制备 ,实验装置(夹持仪器已省略)如图所示:
,实验装置(夹持仪器已省略)如图所示:

①方框内为制取
 的装置,下列装置和药品较为适宜的是
的装置,下列装置和药品较为适宜的是②装置D中仪器a的名称是
③根据①的选择,装置甲中试剂a的名称是
(2)
 的制备,步骤如下:
的制备,步骤如下:通入一段时间
 后,向
后,向 溶液中加入过量
溶液中加入过量 溶液,搅拌,反应后过滤,将沉淀洗涤、干燥,得到
溶液,搅拌,反应后过滤,将沉淀洗涤、干燥,得到 。
。①生成
 的离子方程式为
的离子方程式为②装置丙的作用是
(3)将
 溶液换成
溶液换成 溶液能提高产品纯度,原因是
溶液能提高产品纯度,原因是(4)某同学查阅资料得知,煅烧
 的产物中含有+2价铁元素,于是他设计了由
的产物中含有+2价铁元素,于是他设计了由 制备
制备 的方案。先向
的方案。先向 中依次加入试剂:稀硫酸、①
中依次加入试剂:稀硫酸、① 。
。
您最近一年使用:0次
9 . 下列各组离子能在溶液中大量共存的是
| A.钠离子、二价铁离子、硝酸根离子、氢离子 | B.钠离子、氢离子、碳酸氢根离子、硝酸根 |
| C.钾离子、铵根离子、硫酸根离子、钡离子 | D.氢离子、铜离子、硝酸根、硫酸根 |
您最近一年使用:0次
名校
解题方法
10 . 下列反应对应的离子方程式书写正确的是
A. 溶于氢碘酸: 溶于氢碘酸: |
B.向 溶液中通入等物质的量的氯气: 溶液中通入等物质的量的氯气: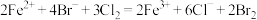 |
C.向氢氧化钡溶液中加入少量稀硫酸: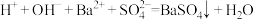 |
D.用氢氧化钠溶液吸收工业废气中的二氧化氮: |
您最近一年使用:0次



