1 . 电子工业中,用 溶液腐蚀覆铜板制造印刷电路板后,采用下列流程从废液中回收铜并重新得到
溶液腐蚀覆铜板制造印刷电路板后,采用下列流程从废液中回收铜并重新得到 溶液。
溶液。
(1) 溶液腐蚀覆铜板反应的化学方程式为
溶液腐蚀覆铜板反应的化学方程式为___________ 。
(2)废液中加入过量 发生反应的离子方程式为
发生反应的离子方程式为___________ 、___________ 。
(3)滤渣为混合物。物质 是
是___________ 。
(4)通入 可以使废液再生,发生反应的化学方程式为
可以使废液再生,发生反应的化学方程式为___________ ;工业上通常用双氧水代替 ,这样做的优点是
,这样做的优点是___________ 。
 溶液腐蚀覆铜板制造印刷电路板后,采用下列流程从废液中回收铜并重新得到
溶液腐蚀覆铜板制造印刷电路板后,采用下列流程从废液中回收铜并重新得到 溶液。
溶液。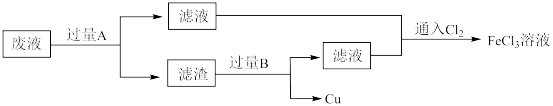
(1)
 溶液腐蚀覆铜板反应的化学方程式为
溶液腐蚀覆铜板反应的化学方程式为(2)废液中加入过量
 发生反应的离子方程式为
发生反应的离子方程式为(3)滤渣为混合物。物质
 是
是(4)通入
 可以使废液再生,发生反应的化学方程式为
可以使废液再生,发生反应的化学方程式为 ,这样做的优点是
,这样做的优点是
您最近一年使用:0次
解题方法
2 . 下列各组离子能在溶液中大量共存的是
A. 、 、 、 、 、 、 | B. 、 、 、 、 、 、 |
C. 、 、 、 、 、 、 | D. 、 、 、 、 、 、 |
您最近一年使用:0次
3 . 高纯硅制备过程中会产生副产物 ,某同学在实验室以
,某同学在实验室以 和硅镁石(含
和硅镁石(含 、
、 及少量Fe的氧化物)为原料,制备氯化镁晶体(
及少量Fe的氧化物)为原料,制备氯化镁晶体( )并回收
)并回收 的工艺流程如图所示:
的工艺流程如图所示:
回答下列问题:
(1)写出 “水溶”过程中发生反应的化学方程式:
“水溶”过程中发生反应的化学方程式:_______ 。
(2)“氧化”时加 发生反应的离子方程式为
发生反应的离子方程式为_______ ,反应温度不易过高,主要原因是_______ 。
(3)试剂X的作用为“调pH”将杂质转化为沉淀而除去,同时不引入杂质,试剂X可以是下列试剂中的_______ (填字母),“调pH”的范围为_______ 。
A.NaOH B. C.
C. D.MgO
D.MgO
(4)“沉淀1”灼烧后所得固体与“沉淀2”共同用于回收 ,“沉淀1”灼烧时应在
,“沉淀1”灼烧时应在_______ (填仪器名称)中进行。
(5)若以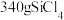 为原料,理论上制得
为原料,理论上制得 的质量为
的质量为_______ g(假设反应过程中Cl元素无损耗)。
 ,某同学在实验室以
,某同学在实验室以 和硅镁石(含
和硅镁石(含 、
、 及少量Fe的氧化物)为原料,制备氯化镁晶体(
及少量Fe的氧化物)为原料,制备氯化镁晶体( )并回收
)并回收 的工艺流程如图所示:
的工艺流程如图所示: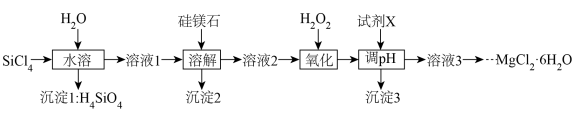
 |  | |
| 开始沉淀的pH | 2.2 | 9.6 |
| 沉淀完全的pH | 3.5 | 11.6 |
(1)写出
 “水溶”过程中发生反应的化学方程式:
“水溶”过程中发生反应的化学方程式:(2)“氧化”时加
 发生反应的离子方程式为
发生反应的离子方程式为(3)试剂X的作用为“调pH”将杂质转化为沉淀而除去,同时不引入杂质,试剂X可以是下列试剂中的
A.NaOH B.
 C.
C. D.MgO
D.MgO(4)“沉淀1”灼烧后所得固体与“沉淀2”共同用于回收
 ,“沉淀1”灼烧时应在
,“沉淀1”灼烧时应在(5)若以
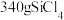 为原料,理论上制得
为原料,理论上制得 的质量为
的质量为
您最近一年使用:0次
名校
4 . 某溶液X中可能含有Na+、 、Ba2+、Fe2+、Mg2+、Cl-、
、Ba2+、Fe2+、Mg2+、Cl-、 、
、 、
、 中的一种或几种。取该溶液进行连续实验,实验过程如图所示,下列有关推理错误的是
中的一种或几种。取该溶液进行连续实验,实验过程如图所示,下列有关推理错误的是
 、Ba2+、Fe2+、Mg2+、Cl-、
、Ba2+、Fe2+、Mg2+、Cl-、 、
、 、
、 中的一种或几种。取该溶液进行连续实验,实验过程如图所示,下列有关推理错误的是
中的一种或几种。取该溶液进行连续实验,实验过程如图所示,下列有关推理错误的是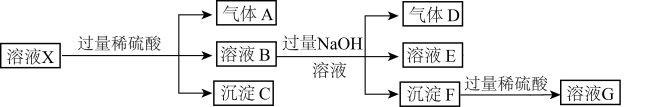
A.溶液X中一定不存在的阴离子为 和 和 |
B.生成气体A的离子方程式为3Fe2++ +4H+=3Fe3++NO↑+2H2O +4H+=3Fe3++NO↑+2H2O |
| C.气体D能使湿润的红色石蕊试纸变蓝 |
| D.溶液G中一定含有的阳离子为H+、Mg2+、Fe3+、Fe2+ |
您最近一年使用:0次
2024-04-04更新
|
1033次组卷
|
4卷引用:河南省漯河市高级中学2023-2024学年高三下学期4月月考化学试题
河南省漯河市高级中学2023-2024学年高三下学期4月月考化学试题湖南省长沙市长郡中学2024届高三高考适应性考试(二)化学试题(已下线)题型4 离子反应 氧化还原反应(25题)-2024年高考化学常考点必杀300题(新高考通用)(已下线)压轴题01?离子方程式与离子共存的判断(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)
5 . 氮是生物体的重要组成元素,也是维持高等动物生命活动的必需元素。氮的循环涉及地球上生物圈的方方面面。

| A.硝化过程中,含氮物质被还原 |
B. 属于氮的固定 属于氮的固定 |
C.土壤中 和 和 的存在有利于从与其接触的水体中除去氮元素 的存在有利于从与其接触的水体中除去氮元素 |
| D.氨氧化过程中,亚硝态氮元素与铵态氮元素理论物质的量之比为3∶4 |
您最近一年使用:0次
2024-03-26更新
|
143次组卷
|
3卷引用:河南省洛阳市宜阳县第一高级中学2023-2024学年高一下学期期中考试化学试卷(研学班)
6 . 某企业排放的废水中含有 和
和 。为了变废为宝,技术人员计划从该废水中回收
。为了变废为宝,技术人员计划从该废水中回收 和金属Cu,工艺流程如图所示。回答下列问题:
和金属Cu,工艺流程如图所示。回答下列问题:
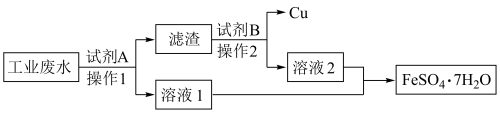
(1)“操作2”的名称为__________ ,在实验室中进行该操作时,所需要的玻璃仪器除烧杯外,还有__________ 。
(2)加入试剂A的目的是将 全部转化为Cu,以便回收铜单质,发生反应的离子方程式为
全部转化为Cu,以便回收铜单质,发生反应的离子方程式为__________ 。
(3)合并溶液1、溶液2后,使溶液析出 晶体的实验操作是
晶体的实验操作是__________ 。
(4)A小组同学要鉴别“溶液2”中的金属阳离子,所需实验操作及实验现象是__________ 。
(5)B小组同学设计如下实验,研究亚铁盐与 溶液的反应。
溶液的反应。
试剂:酸化的 溶液1和5%
溶液1和5% 溶液
溶液
①上述实验中 溶液与溶液1反应的离子方程式是
溶液与溶液1反应的离子方程式是__________ 。
②请结合相关反应解释“稍后,产生气泡”的原因是__________ 。
 和
和 。为了变废为宝,技术人员计划从该废水中回收
。为了变废为宝,技术人员计划从该废水中回收 和金属Cu,工艺流程如图所示。回答下列问题:
和金属Cu,工艺流程如图所示。回答下列问题:
(1)“操作2”的名称为
(2)加入试剂A的目的是将
 全部转化为Cu,以便回收铜单质,发生反应的离子方程式为
全部转化为Cu,以便回收铜单质,发生反应的离子方程式为(3)合并溶液1、溶液2后,使溶液析出
 晶体的实验操作是
晶体的实验操作是(4)A小组同学要鉴别“溶液2”中的金属阳离子,所需实验操作及实验现象是
(5)B小组同学设计如下实验,研究亚铁盐与
 溶液的反应。
溶液的反应。试剂:酸化的
 溶液1和5%
溶液1和5% 溶液
溶液操作 | 现象 |
取 酸化的溶液1于试管中,加入5滴5% 酸化的溶液1于试管中,加入5滴5% 溶液 溶液 | 溶液立即变为棕黄色,稍后,产生气泡 |
向反应后的溶液中加入 溶液 溶液 | 溶液变红 |
 溶液与溶液1反应的离子方程式是
溶液与溶液1反应的离子方程式是②请结合相关反应解释“稍后,产生气泡”的原因是
您最近一年使用:0次
名校
解题方法
7 . 下列离子方程式书写不正确 的是
A.向 溶液中通入氯气: 溶液中通入氯气: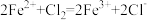 |
B.向 溶液中滴加 溶液中滴加 溶液: 溶液: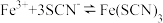 |
C.向 溶液中加入少量氨水: 溶液中加入少量氨水: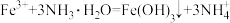 |
D.向 溶液中过量铜粉: 溶液中过量铜粉: |
您最近一年使用:0次
2024-02-02更新
|
141次组卷
|
2卷引用:河南省漯河市高级中学2023-2024学年高一上学期1月月考化学试题
名校
8 . 铁粉具有平肝镇心解毒之功效,主治惊痫、癫狂、脚气冲心、贫血等。某兴趣小组设计利用 制备还原铁粉的流程如下。
制备还原铁粉的流程如下。

实验室中可用 (用废铁屑和稀硫酸反应制得)和
(用废铁屑和稀硫酸反应制得)和 在如图装置模拟上述流程中的“转化”环节。
在如图装置模拟上述流程中的“转化”环节。

(1)植物油的作用是___________ 。
(2)实验过程中,欲将得到的 溶液和
溶液和 溶液混合,操作方法是
溶液混合,操作方法是___________ 。混合后反应生成 的离子方程式为
的离子方程式为___________ 。
(3) 溶液要现用现配的原因是
溶液要现用现配的原因是___________ 。
(4)“干燥”的主要目的是脱去游离水,该过程中会有少量 在空气中被氧化为
在空气中被氧化为 ,该反应的化学方程式为
,该反应的化学方程式为___________ ;取干燥后的 样品11.33g,与木炭混合后焙烧,所有铁都被还原为还原铁粉,最终得到还原铁粉5.6g,样品中杂质
样品11.33g,与木炭混合后焙烧,所有铁都被还原为还原铁粉,最终得到还原铁粉5.6g,样品中杂质 的质量为
的质量为___________ g。在高温条件下,过量的木炭与 反应,写出此反应的化学方程式:
反应,写出此反应的化学方程式:___________ 。
 制备还原铁粉的流程如下。
制备还原铁粉的流程如下。
实验室中可用
 (用废铁屑和稀硫酸反应制得)和
(用废铁屑和稀硫酸反应制得)和 在如图装置模拟上述流程中的“转化”环节。
在如图装置模拟上述流程中的“转化”环节。
(1)植物油的作用是
(2)实验过程中,欲将得到的
 溶液和
溶液和 溶液混合,操作方法是
溶液混合,操作方法是 的离子方程式为
的离子方程式为(3)
 溶液要现用现配的原因是
溶液要现用现配的原因是(4)“干燥”的主要目的是脱去游离水,该过程中会有少量
 在空气中被氧化为
在空气中被氧化为 ,该反应的化学方程式为
,该反应的化学方程式为 样品11.33g,与木炭混合后焙烧,所有铁都被还原为还原铁粉,最终得到还原铁粉5.6g,样品中杂质
样品11.33g,与木炭混合后焙烧,所有铁都被还原为还原铁粉,最终得到还原铁粉5.6g,样品中杂质 的质量为
的质量为 反应,写出此反应的化学方程式:
反应,写出此反应的化学方程式:
您最近一年使用:0次
2024-01-23更新
|
325次组卷
|
3卷引用:河南省百师联考2023-2024学年高一上学期1月期末化学试题
名校
9 . 在酸性高锰酸钾溶液中,可能大量共存的离子是
A. | B. | C. | D. |
您最近一年使用:0次
解题方法
10 . 从印刷电路板的废液中回收铜单质,并重新获得 溶液的工艺流程如下:
溶液的工艺流程如下:
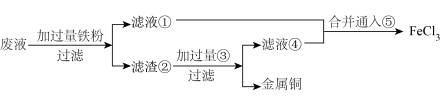
下列说法不正确的是
 溶液的工艺流程如下:
溶液的工艺流程如下:
下列说法不正确的是
| A.滤液④为混合物 | B.③物质可能为稀 溶液 溶液 |
C.物质⑤可用 代替 代替 | D.过滤用到的玻璃仪器有漏斗、烧杯和玻璃棒 |
您最近一年使用:0次
2023-12-16更新
|
316次组卷
|
2卷引用:河南省周口市鹿邑县2023-2024学年高一上学期1月期末化学试题



