名校
解题方法
1 . 科技是第一生产力,我国科学家在诸多领域取得了重大成就。下列说法正确的是
A. 的发现开启了碳纳米材料应用的新时代, 的发现开启了碳纳米材料应用的新时代, 属于混合型晶体 属于混合型晶体 |
B.“神舟十七号”发动机的耐高温结构材料 属于分子晶体 属于分子晶体 |
C.飞船火箭使用偏二甲肼[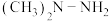 ]作燃料, ]作燃料,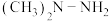 属于烃类 属于烃类 |
| D.量子计算机“悟空”即将面世,其传输信号的光纤主要成分为二氧化硅 |
您最近一年使用:0次
2024-03-25更新
|
356次组卷
|
4卷引用:广东省广州市铁一中学2023-2024学年高二下学期3月月考化学试题
名校
解题方法
2 . 氮化镓在光电器件领域应用广泛,N与Si组成的Si3N4硬度媲美金刚石,下列说法不正确的是

A.As基态核外电子排布式为 |
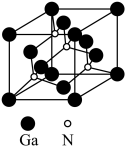
| B.氮化镓晶胞结构如图所示,其化学式为GaN |
| C. Si3N4、晶体Si、金刚石均是共价晶体 |
D. 中H-N-H键的键角大于 中H-N-H键的键角大于 中H-O-H键的键角 中H-O-H键的键角 |
您最近一年使用:0次
名校
3 . 下列说法正确的是
| A.相同条件下,PH3 比 NH3易溶于水、易液化 |
| B.NCl3的空间结构和 VSEPR 模型都为四面体形 |
| C.基态气态25Mn2+再失去1个电子比基态气态26Fe2+再失去1个电子难 |
| D.AlN 和 GaN的成键结构与金刚石相似,为共价晶体,GaN 的熔点高于AlN |
您最近一年使用:0次
2024-02-18更新
|
217次组卷
|
2卷引用:湖南省湖南师范大学附属中学2023-2024学年高三上学期月考五化学试题
4 . 我国在新型锂离子电池电极材料研究方面取得重大突破:NiFe2O4/膨胀石墨(EG)纳米复合材料、PET复合Cu箔、黑磷-石墨复合材料的使用极大提高了电池的能量和安全性。回答下列问题:
(1)Ni元素在周期表中的位置是_______ ,与Ni同周期元素中,基态原子的未成对电子数与Ni相同的有_______ 种。
(2)第二电离能:Fe_______ Cu(选填“>”或“<”),原因是_______ 。
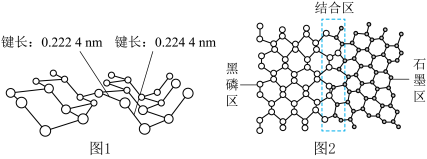
(3)白磷、红磷、黑磷是P元素形成的三种常见单质。黑磷结构与石墨类似,也具有层状结构(如图1),黑磷-石墨复合材料单层结构俯视图如图2。
下列说法正确的是_______(填字母).
(4) 是目前正在开发的电池正极活性物质,其晶胞结构如图3
是目前正在开发的电池正极活性物质,其晶胞结构如图3
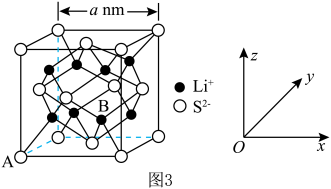
①图3中S2-的配位数为_______ ;
②已知A的坐标为(0,0,0),B的坐标为_______ ;
③设阿伏伽德罗常数的值为NA,则Li2S晶体的密度为_______ g∙cm-3 (用含a,NA的代数式表示)
(1)Ni元素在周期表中的位置是
(2)第二电离能:Fe
(3)白磷、红磷、黑磷是P元素形成的三种常见单质。黑磷结构与石墨类似,也具有层状结构(如图1),黑磷-石墨复合材料单层结构俯视图如图2。

下列说法正确的是_______(填字母).
| A.黑磷中P-P键键能完全相同 |
| B.P的三种常见单质中,黑磷的熔沸点最高 |
| C.黑磷中存在大π键,易导电 |
| D.在结合区,P原子与C原子之间的作用力属范德华力 |
 是目前正在开发的电池正极活性物质,其晶胞结构如图3
是目前正在开发的电池正极活性物质,其晶胞结构如图3
①图3中S2-的配位数为
②已知A的坐标为(0,0,0),B的坐标为
③设阿伏伽德罗常数的值为NA,则Li2S晶体的密度为
您最近一年使用:0次
名校
解题方法
5 . 下列原因分析能正确解释性质差异的是
| 选项 | 性质差异 | 原因分析 |
| A | 金属活动性:Mg>Al | 第一电离能:Mg>Al |
| B | 气态氢化物稳定性: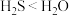 | 分子间作用力: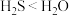 |
| C | 熔点:金刚石>碳化硅>硅 | 化学键键能:C-C>C-Si>Si-Si |
| D | 酸性: | 非金属性:C<S |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-03-24更新
|
744次组卷
|
5卷引用:北京市清华大学附属中学2023-2024学年高三上学期12月统练(六)化学试题
6 . 铁铝铅榴石主要成分为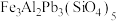 ,其组成也可写成的氧化物形式:
,其组成也可写成的氧化物形式: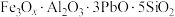 。下列说法正确的是
。下列说法正确的是
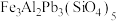 ,其组成也可写成的氧化物形式:
,其组成也可写成的氧化物形式: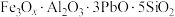 。下列说法正确的是
。下列说法正确的是| A.组成元素均位于元素周期表的p区 |
| B.晶体硅的熔点比二氧化硅晶体高 |
| C.基态铝原子核外电子有7种不同的空间运动状态 |
D.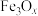 中Fe(II)与Fe(III)的个数比为2:1 中Fe(II)与Fe(III)的个数比为2:1 |
您最近一年使用:0次
2023-02-26更新
|
645次组卷
|
3卷引用:山东省淄博实验中学2022-2023学年高二下学期3月月考化学试题
7 . 下列陈述Ⅰ和陈述Ⅱ均正确且有因果关系的是
| 选项 | 选项I | 选项II |
| A | Si-O键键能比Si-H键高 |  的熔沸点比 的熔沸点比 高 高 |
| B | Cl的非金属性比Si强 |  溶液中滴加盐酸产生白色凝胶 溶液中滴加盐酸产生白色凝胶 |
| C | 生铁中含有碳元素而纯铁中不含 | 生铁比纯铁熔点更低,硬度更大 |
| D | 增大压强, 平衡正移 平衡正移 | 压缩 和 和 混合气体体积,红棕色变深 混合气体体积,红棕色变深 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . ⅢA族元素的单质及其化合物在生产、生活中有广泛应用。如图是几种由ⅢA族元素(或与其他族元素)形成的物质的结构,请回答下列问题:
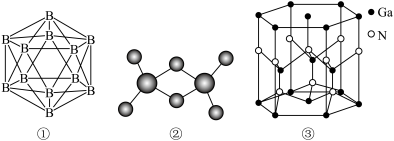
(1)已知晶体硼的基本结构单元是正二十面体(如图①),每个三角形均为正三角形,每个顶角处各有一个硼原子。则该结构单元由________ 个硼原子构成,共含有________ 个B—B键。
(2)科学家合成了一系列具有独特化学特性的氢铝化合物 。已知最简单的氢铝化合物的分子式为
。已知最简单的氢铝化合物的分子式为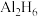 ,它的熔点为150℃,燃烧热极高。
,它的熔点为150℃,燃烧热极高。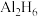 的球棍模型如图②。
的球棍模型如图②。
a.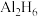 在固态时所形成的晶体是
在固态时所形成的晶体是________ 。
b.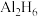 中含有的化学键类型为
中含有的化学键类型为________ 。
c.氢铝化合物________ (填“可能”或“不可能”)成为未来的储氢材料和火箭燃料。
(3)氮化镓属于第三代半导体材料,也是坚硬的高熔点材料,其某种结构如图③所示。它的化学式为________ ,属于________ 晶体。

(1)已知晶体硼的基本结构单元是正二十面体(如图①),每个三角形均为正三角形,每个顶角处各有一个硼原子。则该结构单元由
(2)科学家合成了一系列具有独特化学特性的氢铝化合物
 。已知最简单的氢铝化合物的分子式为
。已知最简单的氢铝化合物的分子式为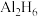 ,它的熔点为150℃,燃烧热极高。
,它的熔点为150℃,燃烧热极高。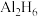 的球棍模型如图②。
的球棍模型如图②。a.
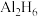 在固态时所形成的晶体是
在固态时所形成的晶体是b.
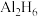 中含有的化学键类型为
中含有的化学键类型为c.氢铝化合物
(3)氮化镓属于第三代半导体材料,也是坚硬的高熔点材料,其某种结构如图③所示。它的化学式为
您最近一年使用:0次
9 . 砷(33As)元素可以形成多种化合物,有着广泛的用途。回答下列问题:
(1)As的基态原子的价电子排布式为_______ 。
(2)雌黄和雄黄早期都曾用作绘画颜料,又都因有抗病毒疗效而用来入药。As元素有+2、+3两种常见价态,在一定条件下,雌黄和雄黄的转化关系如图所示:
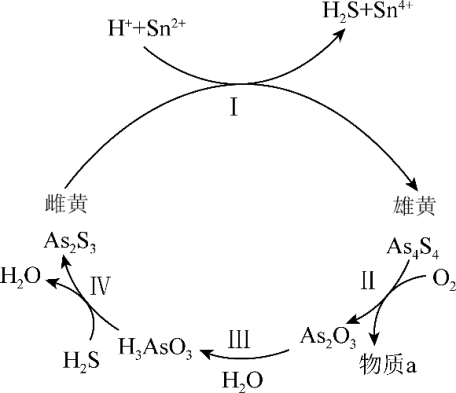
①Ⅰ→Ⅳ中属于氧化还原反应的是_______ 。
②反应Ⅰ中,As2S3和Sn2+恰好完全反应时,其物质的量之比是_______ 。
③反应Ⅱ化学方程式是_______ 。
(3)砷化镓 (GaAs)是一种重要的半导体材料。
①GaAs与GaN都是由原子之间以共价键的成键方式结合而成的晶体。GaAs熔点为1238℃,GaN熔点为1500℃,GaAs熔点低于GaN的原因为_______ 。
②砷化镓晶胞结构如下图所示。平均每个晶胞所含Ga的原子个数为_______ 。
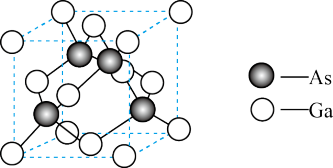
③晶体密度ρ可以用晶胞的质量除以体积来求算。已知GaAs晶胞棱长为apm(1pm=1×10-10cm),阿伏加德罗常数为NA,则该晶体的密度ρ=_______ g∙cm-3(列出计算式即可,GaAs的摩尔质量为145g∙mol-1)。
(1)As的基态原子的价电子排布式为
(2)雌黄和雄黄早期都曾用作绘画颜料,又都因有抗病毒疗效而用来入药。As元素有+2、+3两种常见价态,在一定条件下,雌黄和雄黄的转化关系如图所示:

①Ⅰ→Ⅳ中属于氧化还原反应的是
②反应Ⅰ中,As2S3和Sn2+恰好完全反应时,其物质的量之比是
③反应Ⅱ化学方程式是
(3)砷化镓 (GaAs)是一种重要的半导体材料。
①GaAs与GaN都是由原子之间以共价键的成键方式结合而成的晶体。GaAs熔点为1238℃,GaN熔点为1500℃,GaAs熔点低于GaN的原因为
②砷化镓晶胞结构如下图所示。平均每个晶胞所含Ga的原子个数为

③晶体密度ρ可以用晶胞的质量除以体积来求算。已知GaAs晶胞棱长为apm(1pm=1×10-10cm),阿伏加德罗常数为NA,则该晶体的密度ρ=
您最近一年使用:0次
2022-09-01更新
|
147次组卷
|
2卷引用:北京市第三十五中学2022-2023学年高三上学期 10月月考化学试题
10 . 钻石并不久远,至少在地表上无法达到永恒,其同胞兄弟石墨其实更稳定。用NA表示阿伏加德罗常数的值,请回答下列问题:
(1)石墨的层状结构中,层内碳原子之间以_______ (作用力)结合,层间靠_______ (作用力)维系,属于_______ 晶体;
(2)石墨烯分子中所有原子可以处于同一平面上,最小环为_______ 元环,环中碳碳键的键角为_______ ,每个环内碳原子与C-C键的比值为_______ ,12g石墨烯含σ键的数目为_______ ;
(3)钻石(金刚石)属于_______ 晶体,已知金刚石的晶胞如图所示,每个晶胞中含_______ 个碳原子,已知晶胞参数为apm,则C-C键的键长为_______ pm ;

(4)已知金刚砂(SiC)晶胞结构与金刚石相似,其熔点_______ 金刚石(填“高于”“低于”“等于”)。
(1)石墨的层状结构中,层内碳原子之间以
(2)石墨烯分子中所有原子可以处于同一平面上,最小环为
(3)钻石(金刚石)属于

(4)已知金刚砂(SiC)晶胞结构与金刚石相似,其熔点
您最近一年使用:0次



