名校
1 . 下列实验操作正确且能达到实验目的的是
| A | B |
|
|
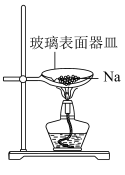
| 钠的燃烧反应 | 验证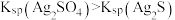 |
| C | D |
|
|
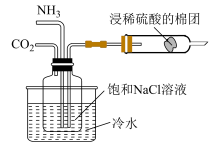
制备 | 证明非金属性: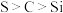 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-12-31更新
|
486次组卷
|
7卷引用:山西省运城市新绛县第二中学2023-2024学年高三上学期1月月考理综试题
山西省运城市新绛县第二中学2023-2024学年高三上学期1月月考理综试题陕西省名校协作体2023-2024学年高三上学期12月月考化学试题甘肃省酒泉育英中学等多校2023-2024学年高三上学期12月一轮复习联考(四)化学试题(已下线)化学(九省联考考后提升卷,河南卷)-2024年1月“九省联考”真题完全解读与考后提升湖南省邵阳市第二中学2023-2024学年高三下学期2月月考化学试题甘肃省张掖市高台县第一中学2023-2024学年高三下学期模拟考化学试题(已下线)专题03 化学实验基础-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)
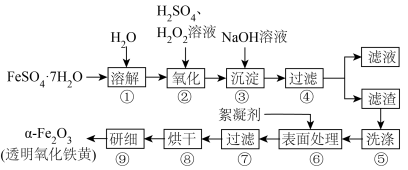
2 . 透明氧化铁黄具有优良着色性能和保色性且使用安全,受到广泛重视,某研究性学习小组拟用硫酸亚铁做原料进行制备,实验流程如图所示:
(1)步骤④用到的仪器除铁架台(带铁圈)、烧杯、玻璃棒之外还需要_______ ;步骤⑨用到的仪器是_______ 。
(2)步骤②发生反应的离子方程式为_______ 。
(3)步骤④所得滤渣的主要成分是_______ (写化学式)。
(4)证明步骤⑤已洗涤干净的方法是_______ 。
(5)步骤②中除用 氧化之外,还可以用
氧化之外,还可以用 氧化,若有2.78g
氧化,若有2.78g 溶解后通氧气,至少需通入标准状况下
溶解后通氧气,至少需通入标准状况下
_______ mL。
(6)将透明氧化铁黄溶于水制得的胶体不具有的性质或用途是_______(填字母)。
(1)步骤④用到的仪器除铁架台(带铁圈)、烧杯、玻璃棒之外还需要
(2)步骤②发生反应的离子方程式为
(3)步骤④所得滤渣的主要成分是
(4)证明步骤⑤已洗涤干净的方法是
(5)步骤②中除用
 氧化之外,还可以用
氧化之外,还可以用 氧化,若有2.78g
氧化,若有2.78g 溶解后通氧气,至少需通入标准状况下
溶解后通氧气,至少需通入标准状况下
(6)将透明氧化铁黄溶于水制得的胶体不具有的性质或用途是_______(填字母)。
| A.分散质的直径为1nm~100nm | B.用激光笔照射时,有一条光亮的通路 |
| C.可用作除氧剂 | D.肉眼很难区分该胶体和溶液 |
您最近一年使用:0次
2024-04-03更新
|
97次组卷
|
2卷引用:山西省部分学校2023-2024学年高一上学期1月期末化学试题
3 . 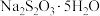 俗称“大苏打”,它是一种常用的试剂.
俗称“大苏打”,它是一种常用的试剂.
(1)工业上,常用 溶液吸收尾气中的
溶液吸收尾气中的 ,氧化产物为
,氧化产物为 .写出离子方程式:
.写出离子方程式:__________________ .理论上,能发生的氧化还原反应都可以设计成原电池.如果将上述反应设计成原电池,则正极反应式为____________ .
(2)已知: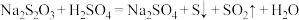
某小组设计实验探究影响化学反应速率的外界因素:
①
_________ ,设计实验I,Ⅱ的目的是_________ .
②实验测得: .由实验I、Ⅲ得出结论是
.由实验I、Ⅲ得出结论是________________ .
③根据表格信息,__________ (填“能”或“不能”)比较a和d的大小,原因是________ .
(3)已知: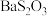 是白色难溶物.大苏打易变质生成
是白色难溶物.大苏打易变质生成 .设计实验证明某大苏打样品是否变质:
.设计实验证明某大苏打样品是否变质:__________________ .
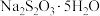 俗称“大苏打”,它是一种常用的试剂.
俗称“大苏打”,它是一种常用的试剂.(1)工业上,常用
 溶液吸收尾气中的
溶液吸收尾气中的 ,氧化产物为
,氧化产物为 .写出离子方程式:
.写出离子方程式:(2)已知:
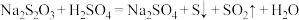
某小组设计实验探究影响化学反应速率的外界因素:
| 序号 | 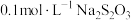 溶液 溶液 | 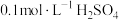 溶液 溶液 | 蒸馏水 | 温度 | 变浑浊时间 |
| I |  |  | 0 | 35℃ | a s |
| II |  | 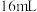 | V mL | 35℃ | b s |
| III |  |  | 0 | 45℃ | c s |
| IV |  |  | 5 mL | 40℃ | d s |

②实验测得:
 .由实验I、Ⅲ得出结论是
.由实验I、Ⅲ得出结论是③根据表格信息,
(3)已知:
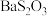 是白色难溶物.大苏打易变质生成
是白色难溶物.大苏打易变质生成 .设计实验证明某大苏打样品是否变质:
.设计实验证明某大苏打样品是否变质:
您最近一年使用:0次
解题方法
4 . 铁及其化合物在生产、生活中有重要作用。回答下列问题:
I.硫酸亚铁晶体 在医药上常用作补血剂。某课外小组的同学通过实验测定补血剂中硫酸亚铁晶体的质量分数,实验步骤如图所示:
在医药上常用作补血剂。某课外小组的同学通过实验测定补血剂中硫酸亚铁晶体的质量分数,实验步骤如图所示:

(1)证明经步骤①得到的滤液中含有 的方法如下:取样,先滴加
的方法如下:取样,先滴加___________ ,再滴加少量氯水,该过程的现象为___________ 。
(2)步骤②加入氯水发生反应的离子方程式是___________ 。
(3)步骤③产生的红褐色物质成分是___________ (写化学式)。
(4)步骤④中一系列操作为___________ 、洗涤、干燥、灼烧。
(5)若所取补血剂质量为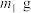 ,最终得到红棕色固体C的质量为
,最终得到红棕色固体C的质量为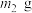 ,则补血剂中硫酸亚铁晶体的质量分数为
,则补血剂中硫酸亚铁晶体的质量分数为___________ (用含 、
、 的代数式表示,不考虑实验中铁元素的损失)。
的代数式表示,不考虑实验中铁元素的损失)。
II.高铁酸钾 是一种新型、高效、多功能绿色水处理剂。工业上制备高铁酸钾以及高铁酸钾处理污水的部分流程如下:
是一种新型、高效、多功能绿色水处理剂。工业上制备高铁酸钾以及高铁酸钾处理污水的部分流程如下:

(6)过程①制取1mol ,理论上需要
,理论上需要 物质的量为
物质的量为___________ ,步骤②中反应能够发生的原因是___________ ,分离出 固体的操作中使用的玻璃仪器有
固体的操作中使用的玻璃仪器有___________ 。
I.硫酸亚铁晶体
 在医药上常用作补血剂。某课外小组的同学通过实验测定补血剂中硫酸亚铁晶体的质量分数,实验步骤如图所示:
在医药上常用作补血剂。某课外小组的同学通过实验测定补血剂中硫酸亚铁晶体的质量分数,实验步骤如图所示:
(1)证明经步骤①得到的滤液中含有
 的方法如下:取样,先滴加
的方法如下:取样,先滴加(2)步骤②加入氯水发生反应的离子方程式是
(3)步骤③产生的红褐色物质成分是
(4)步骤④中一系列操作为
(5)若所取补血剂质量为
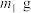 ,最终得到红棕色固体C的质量为
,最终得到红棕色固体C的质量为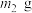 ,则补血剂中硫酸亚铁晶体的质量分数为
,则补血剂中硫酸亚铁晶体的质量分数为 、
、 的代数式表示,不考虑实验中铁元素的损失)。
的代数式表示,不考虑实验中铁元素的损失)。II.高铁酸钾
 是一种新型、高效、多功能绿色水处理剂。工业上制备高铁酸钾以及高铁酸钾处理污水的部分流程如下:
是一种新型、高效、多功能绿色水处理剂。工业上制备高铁酸钾以及高铁酸钾处理污水的部分流程如下:
(6)过程①制取1mol
 ,理论上需要
,理论上需要 物质的量为
物质的量为 固体的操作中使用的玻璃仪器有
固体的操作中使用的玻璃仪器有
您最近一年使用:0次
11-12高一上·云南昆明·期末
名校
解题方法
5 . 将淀粉和稀 溶液混合,装在半透膜袋中,浸泡在盛蒸馏水的烧杯内,过一段时间后,取烧杯中液体进行实验,能证明半透膜完好无损的是
溶液混合,装在半透膜袋中,浸泡在盛蒸馏水的烧杯内,过一段时间后,取烧杯中液体进行实验,能证明半透膜完好无损的是
 溶液混合,装在半透膜袋中,浸泡在盛蒸馏水的烧杯内,过一段时间后,取烧杯中液体进行实验,能证明半透膜完好无损的是
溶液混合,装在半透膜袋中,浸泡在盛蒸馏水的烧杯内,过一段时间后,取烧杯中液体进行实验,能证明半透膜完好无损的是A.加入 溶液产生白色沉淀 溶液产生白色沉淀 | B.加入碘水不变蓝 |
C.加入 溶液没有白色沉淀产生 溶液没有白色沉淀产生 | D.加入碘水变蓝 |
您最近一年使用:0次
2023-12-11更新
|
396次组卷
|
67卷引用:山西大学附属中学2020-2021学年高上学期10月月考化学试题
山西大学附属中学2020-2021学年高上学期10月月考化学试题山西省太原市山西大学附属中学2020-2021学年高一上学期10月(总第一次)模块诊断化学试题山西省朔州市怀仁市第一中学校2021-2022学年高一上学期第一次月考化学试题(已下线)2010—20111学年云南省昆明一中高一上学期期末考试化学试卷(已下线)2011-2012学年湖南省醴陵二中、醴陵四中高一上学期期中联考化学试卷(已下线)2011-2012学年山东省日照一中高一上学期期中考试化学试卷2014-2015学年福建省厦门二中高一上学期期中化学试卷2014-2015江西省赣州市赣县中学北校区高一12月月考化学试卷2015-2016学年河北省冀州中学高一上第一次月考化学试卷2015-2016学年河北衡水冀州中学高一上月考三理化学卷2015-2016学年河北省冀州中学高一上第三次月考化学试卷2015-2016学年河南省信阳市高一上学期期末教学质量监测化学试卷2017届西藏日喀则区第一高级中学高三上第一次月考化学卷2016-2017学年海南省海南中学高一上期中化学试卷2016-2017学年辽宁省实验中学分校高一上期中化学卷吉林省实验中学2017-2018学年高一上学期期中考试化学试题新疆生产建设兵团第二中学2017-2018学年高一上学期期中考试化学试题吉林省实验中学2017-2018学年高一上学期期中考试(文)化学试题(已下线)2018年9月23日 《每日一题》人教必修1-每周一测安徽省青阳县第一中学2018-2019学年高一上学期期中考试化学试题【全国百强校】黑龙江省实验中学2018-2019学年高一上学期期中考试化学试题2.1.2 胶体练习(1)——《高中新教材同步备课》(鲁科版 必修第一册)甘肃省兰州市第五十八中学2019-2020学年高一上学期期中考试化学试题(已下线)2.1.2 分散系及其分类(重点练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版)高一必修第一册(鲁科2019)第2章第1节 元素与物质分类 教材帮福建省南安市侨光中学2020-2021学年高一上学期第一次阶段考试化学试题重庆市万州二中2020-2021学年高一上学期10月月考化学试题河北省保定市徐水区第一中学2020-2021学年高一上学期10月月考化学试题高一必修第一册(苏教2019)专题1 第三单元 物质的分散系宁夏石嘴山第三中学2020-2021学年高一上学期期中考试化学试题内蒙古通辽市开鲁县第一中学2020-2021学年高一上学期期中考试化学试题新疆生产建设兵团第十师北屯高级中学2020-2021学年高一上学期阶段性检测化学试题河北省石家庄市藁城区第一中学2020-2021学年高一上学期开学考试化学试题青海省湟川中学2019-2020学年高一上学期期中考试化学试题(已下线)衔接点21 分散系 胶体-2021年初升高化学无忧衔接(已下线)1.1.1 物质的分类-2021-2022学年高一化学课后培优练(人教版2019必修第一册)第1课时 物质的分类(课后)——课前、课中、课后同步专题精编(人教版2019必修第一册)河北省正定中学2020-2021学年高一上学期第一次月考化学试题(已下线)1.3.1 常见的分散系 胶体-2021-2022学年高一化学课后培优练(苏教版2019必修第一册)江西省宜春市上高二中2021-2022学年高一上学期第一次月考化学试题吉林省长春北师大附属学校2021-2022学年高一上学期第一次月考化学试题河北省衡水市第十四中学2021-2022学年高一上学期一调考试(2)化学试题(已下线)上海市华东师范大学第二附属中学2021-2022学年高一上学期期中考试化学试题2020年北京高考化学真题变式题1-10江西省吉安市遂川中学2021-2022学年高一上学期第一次月考化学(B卷)试题新疆师范大学附属中学2021-2022学年高一10月月考化学试题广东省普宁市华侨中学2021—2022学年高一上学期第三次月考化学试题(已下线)第08讲 元素与物质的分类-【暑假自学课】2022年新高一化学暑假精品课(鲁科版2019必修第一册)(已下线)衔接点04 分散系 胶体-2022年初升高化学无忧衔接(已下线)第1章基础巩固测评卷-【帮课堂】2022-2023学年高一化学同步精品讲义(沪科版2020必修第一册)上海市华东师范大学松江实验高级中学2021-2022学年高一上学期期中考试化学试题安徽师范大学附属中学2022-2023学年高一上学期10月测试化学试题河南省南阳市2022-2023学年高一上学期11月期中化学试题福建省福州第十五中学2022-2023学年高一上学期第一次月考化学试题上海市控江中学2022-2023学年高一上学期期中考试化学试题第七章 有机化合物(A卷·知识通关练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第二册)湖北省云学新高考联盟2023-2024学年高一上学期10月联考化学试题天津市耀华中学2023-2024学年高一上学期第一次月考化学试题湖北省襄阳市第一中学2023-2024学年高一上学期9月月考化学试题福建省福州第七中学2023-2024学年高一上学期10月月考化学试题广东省梅州市梅江区梅州中学2023-2024学年高一上学期第一次月考化学试题广东省汕头市潮阳实验学校2023-2024学年高一上学期11月期中考试化学试题上海市松江一中2023-2024学年高一上学期期中考试化学试题安徽省安庆市第一中学2023-2024学年高一上学期10月月考化学试题(已下线)5.1.3硫酸根离子的检验、粗盐的提纯-随堂练习广西钦州市第四中学2023-2024学年高三上学期12月考试化学试卷广东实验中学越秀学校2023-2024学年高一3月段考化学试题
名校
解题方法
6 . 下列实验操作和实验结论或目的均正确的是
选项 | 实验操作 | 实验结论或目的 |
A | 向含有酚酞的 | 证明 |
B | 等体积 | 证明HX酸性比HY强 |
C | 将氯水滴在湿润的pH试纸上,与标准比色卡对照 | 测定氯水的pH |
D | D.向 | 证明在相同温度下: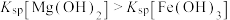 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-01-24更新
|
65次组卷
|
2卷引用:山西省长治市2023-2024学年高二上学期1月期末化学试题
7 . 下列各组实验所得结论或推论正确的是
| 实验现象或事实 | 结论或推论 | |
| A | 向某有机物(C5H8O2)中滴加FeCl3溶液,显色 | 该有机物分子中含酚羟基 |
| B | 常温下,分别向浓度均为0.1mol·L-1的FeSO4和CuSO4溶液中通入H2S气体至饱和,仅后者生成沉淀 | 溶度积常数: |
| C | 向某稀溶液中加入NaOH溶液,加热能产生使湿润的蓝色石蕊试纸变红的气体 | 溶液中含有 |
| D | 向装有FeS固体的装置中滴加稀盐酸,有气体产生 | 证明非金属性:Cl>S |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-21更新
|
263次组卷
|
2卷引用:山西省平遥中学2023-2024学年高三二模考试化学试题
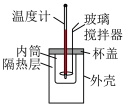
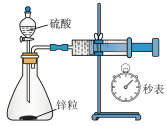
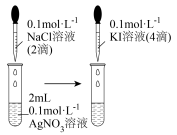
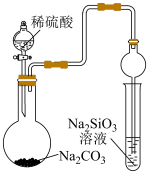
8 . 下列实验装置或实验操作不能达到相应实验目的的是
|
|
向醋酸溶液中滴加碳酸钠溶液产生气泡 |
先产生白色沉淀,再生成黄色沉淀 |
| 使用简易量热计进行中和反应热的测定 | 测定一定时间内生成 的反应速率 的反应速率 | 实验证明醋酸的 大于碳酸的 大于碳酸的 | 实验证明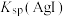 小于 小于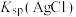 |
A. | B. | C. | D. |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-12-05更新
|
145次组卷
|
2卷引用:山西省朔州市怀仁市2023-2024学年高二上学期1月期末化学试题
9 . 侯德榜为我国化工事业的发展做出了卓越贡献,是我国近代化学工业的奠基人之一,他结合中国国情对氨碱法进行改进,确定了新的工艺流程——侯氏制碱法:将氨碱法和合成氨法两种工艺联合起来,方法流程如图所示。
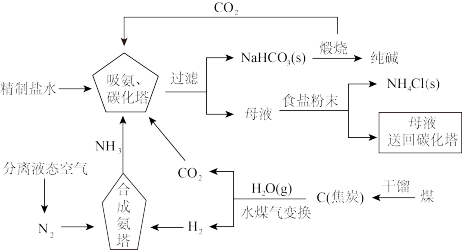
回答下列问题:
(1)向精制盐水中通入 、
、 的顺序及理由为
的顺序及理由为___________ (提示:从两种气体的溶解度进行分析)。
(2)写出 煅烧时发生反应的化学方程式:
煅烧时发生反应的化学方程式:___________ 。
(3)该流程中循环利用的物质为___________ 。
(4)侯氏制碱法除了制取得到纯碱,还生成了一种副产品___________ (填名称),可以用来___________ 。
(5)所得纯碱中可能含有少量 杂质,可以通过如下方法测定纯碱中碳酸钠的质量分数:
杂质,可以通过如下方法测定纯碱中碳酸钠的质量分数:
ⅰ.称取ag样品,溶于水中;
ⅱ.加入足量氯化钙溶液;
ⅲ.过滤、洗涤、干燥、称量,所得沉淀质量为bg。
①证明所加氯化钙溶液已经足量的方法是___________ 。
②该样品中碳酸钠的质量分数为___________ %(用含a、b的代数式表示)。

回答下列问题:
(1)向精制盐水中通入
 、
、 的顺序及理由为
的顺序及理由为(2)写出
 煅烧时发生反应的化学方程式:
煅烧时发生反应的化学方程式:(3)该流程中循环利用的物质为
(4)侯氏制碱法除了制取得到纯碱,还生成了一种副产品
(5)所得纯碱中可能含有少量
 杂质,可以通过如下方法测定纯碱中碳酸钠的质量分数:
杂质,可以通过如下方法测定纯碱中碳酸钠的质量分数:ⅰ.称取ag样品,溶于水中;
ⅱ.加入足量氯化钙溶液;
ⅲ.过滤、洗涤、干燥、称量,所得沉淀质量为bg。
①证明所加氯化钙溶液已经足量的方法是
②该样品中碳酸钠的质量分数为
您最近一年使用:0次
10 . 硫酸和硝酸是常用的工业产品和原料,根据下列流程,回答相关问题。
(1)某研究小组同学对硫酸的工业制备和性质进行探究。查阅资料,工业制硫酸的过程如下图所示:

“燃烧”前,黄铁矿需要粉碎处理,目的是___________ ;过程Ⅲ中,试剂X是___________ (填“水”或“98.3%的浓硫酸”)。
(2)为了提高硫酸工业的综合经济效益,可以用工业废碱渣(主要成分为Na2CO3)来吸收含SO2的烟气,同时得到亚硫酸钠(Na2SO3)粗品。其流程如图所示:
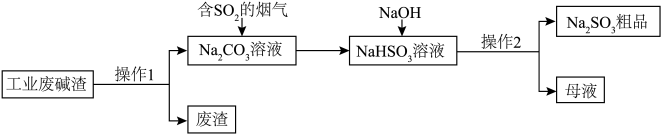
①操作1中包含溶解、___________ ;SO2被Na2CO3溶液吸收时,会释放出一种无色无味气体,写出该反应的离子方程式:___________ 。
②为证明亚硫酸钠粗品含有少量Na2SO4,设计如下方案:
在一支试管中加入少量亚硫酸钠粗品,用适量蒸馏水溶解,___________ ,出现白色沉淀,则证明含有Na2SO4。
③已知有标准状况下VL含SO2的烟气,通入足H2O2溶液吸收,再加足量BaCl2溶液充分反应后(不考虑废气中其他成分的反应),最终得到a g沉淀。H2O2吸收SO2的化学方程式为___________ ;烟气中SO2的体积分数的计算式是___________ (用含a、V的算式表示,不用化简)。
(3)目前,NaClO溶液广泛应用于脱硫脱硝,可对硫酸厂、硝酸厂产生的尾气进行处理,下图是当温度为50℃,溶液的pH=10,足气中c(SO2)=c(NO)=300mg·m-3,且流速固定的条件下,NaClO的质量分数对NO,SO2脱除效率(η/%)的影响。
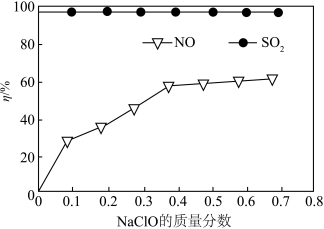
SO2的脱除效率一直维持在98%以上,而NO脱除效率相对较低,其原因可能是___________ 。
(1)某研究小组同学对硫酸的工业制备和性质进行探究。查阅资料,工业制硫酸的过程如下图所示:

“燃烧”前,黄铁矿需要粉碎处理,目的是
(2)为了提高硫酸工业的综合经济效益,可以用工业废碱渣(主要成分为Na2CO3)来吸收含SO2的烟气,同时得到亚硫酸钠(Na2SO3)粗品。其流程如图所示:

①操作1中包含溶解、
②为证明亚硫酸钠粗品含有少量Na2SO4,设计如下方案:
在一支试管中加入少量亚硫酸钠粗品,用适量蒸馏水溶解,
③已知有标准状况下VL含SO2的烟气,通入足H2O2溶液吸收,再加足量BaCl2溶液充分反应后(不考虑废气中其他成分的反应),最终得到a g沉淀。H2O2吸收SO2的化学方程式为
(3)目前,NaClO溶液广泛应用于脱硫脱硝,可对硫酸厂、硝酸厂产生的尾气进行处理,下图是当温度为50℃,溶液的pH=10,足气中c(SO2)=c(NO)=300mg·m-3,且流速固定的条件下,NaClO的质量分数对NO,SO2脱除效率(η/%)的影响。

SO2的脱除效率一直维持在98%以上,而NO脱除效率相对较低,其原因可能是
您最近一年使用:0次


 溶液中加入少量
溶液中加入少量 的HX和HY两种酸分别与足量的铁反应,排水法收集气体,HX放出的氢气多且反应速率快
的HX和HY两种酸分别与足量的铁反应,排水法收集气体,HX放出的氢气多且反应速率快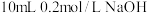 溶液中滴2滴
溶液中滴2滴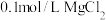 溶液,产生白色沉淀后再滴加2滴
溶液,产生白色沉淀后再滴加2滴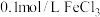 ,又生成红褐色沉淀
,又生成红褐色沉淀