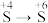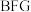1 . 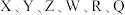 为原子序数依次增大的六种短周期主族元素。
为原子序数依次增大的六种短周期主族元素。 是原子半径最小的元素;
是原子半径最小的元素; 原子最外层电子数是核外电子层数的3倍;
原子最外层电子数是核外电子层数的3倍; 是短周期中金属性最强的元素;
是短周期中金属性最强的元素; 是地壳中含量最多的金属元素;
是地壳中含量最多的金属元素; 的最高正价与最低负价代数和为4。回答下列问题:
的最高正价与最低负价代数和为4。回答下列问题:
(1)用电子式表示
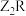 的形成过程:
的形成过程:(2)W在周期表中的位置是
(3)ZYX的电子式为
 中含有的化学键类型为
中含有的化学键类型为(4)
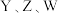 三种元素对应的简单离子半径由大到小的顺序是
三种元素对应的简单离子半径由大到小的顺序是(5)下列说法能证明非金属性
 强于
强于 的是
的是a.简单阴离子的还原性: b.简单氢化物热稳定性:
b.简单氢化物热稳定性:
c.氧化物对应的水化物的酸性: d.
d.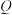 的单质能从
的单质能从 溶液中置换出
溶液中置换出 单质
单质
(6)
 的单质与
的单质与 的最高价氧化物对应的水化物反应的化学方程式为
的最高价氧化物对应的水化物反应的化学方程式为
您最近一年使用:0次
2024-03-29更新
|
167次组卷
|
2卷引用:山西省部分学校2023-2024学年高一上学期1月期末化学试题
名校
解题方法
2 . 某实验兴趣小组同学用如图所示装置制备氢氧化铁胶体(部分夹持装置已略去)。根据所学知识回答下列问题:
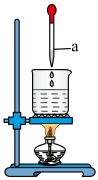
(1)仪器a的名称为___________ 。
(2)氢氧化铁胶体的制备:
①烧杯中发生反应的化学方程式为___________ 。
②证明有 胶体生成的方法是
胶体生成的方法是___________ 。
③下列关于氢氧化铁胶体的说法正确的是___________ (填序号)。
A.具有吸附性 B.单个氢氧化铁分子的直径大于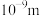
④向 胶体中逐滴加入过量稀硫酸,现象是
胶体中逐滴加入过量稀硫酸,现象是___________ 。

(1)仪器a的名称为
(2)氢氧化铁胶体的制备:
①烧杯中发生反应的化学方程式为
②证明有
 胶体生成的方法是
胶体生成的方法是③下列关于氢氧化铁胶体的说法正确的是
A.具有吸附性 B.单个氢氧化铁分子的直径大于
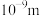
④向
 胶体中逐滴加入过量稀硫酸,现象是
胶体中逐滴加入过量稀硫酸,现象是
您最近一年使用:0次
名校
解题方法
3 . H2S是一种剧毒气体,直接排放会造成严重的环境污染。某种利用硫化氢气体生产硫黄的工艺流程为: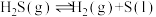 ,反应放热。回答下列问题:
,反应放热。回答下列问题:
(1)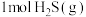 具有的能量
具有的能量___________ (填“ ”“
”“ ”或“
”或“ ”)
”) 和
和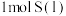 具有的总能量。
具有的总能量。
(2)在2L恒容密闭容器中充入 发生反应,20min时测得气体质量减少了8g。
发生反应,20min时测得气体质量减少了8g。
①前20min的平均反应速率
___________ 。20min时H2S的转化率为___________ 。
②下列说法可以证明反应已达平衡状态的是___________ (填字母,下同)。
A. B.
B.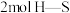 键断裂的同时生成
键断裂的同时生成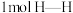 键
键
C.混合气体的密度不再变化 D.混合气体的平均摩尔质量不再变化
③下列措施中可以加快该反应的化学反应速率的是___________ 。
A.恒温充入He B.升高温度 C.恒温充入H2S D.恒温充入SO2
④下列曲线表示某物理量随时间的变化,其中正确的是___________ 。_________ 。
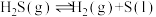 ,反应放热。回答下列问题:
,反应放热。回答下列问题:(1)
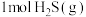 具有的能量
具有的能量 ”“
”“ ”或“
”或“ ”)
”) 和
和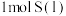 具有的总能量。
具有的总能量。(2)在2L恒容密闭容器中充入
 发生反应,20min时测得气体质量减少了8g。
发生反应,20min时测得气体质量减少了8g。①前20min的平均反应速率

②下列说法可以证明反应已达平衡状态的是
A.
 B.
B.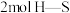 键断裂的同时生成
键断裂的同时生成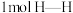 键
键C.混合气体的密度不再变化 D.混合气体的平均摩尔质量不再变化
③下列措施中可以加快该反应的化学反应速率的是
A.恒温充入He B.升高温度 C.恒温充入H2S D.恒温充入SO2
④下列曲线表示某物理量随时间的变化,其中正确的是
A.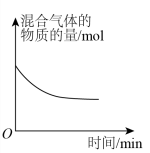 B.
B. 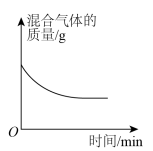 C.
C. 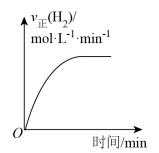 D.
D.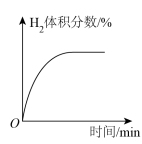
您最近一年使用:0次
解题方法
4 . 某小组为探究 溶解于
溶解于 溶液的反应机理,提出下列两种观点:
溶液的反应机理,提出下列两种观点:
观点一: 的水解导致
的水解导致 溶液呈酸性,
溶液呈酸性, 与
与 反应,从而促进了
反应,从而促进了 的沉淀溶解平衡
的沉淀溶解平衡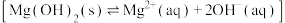 ]向溶解方向移动。
]向溶解方向移动。
观点二: 直接结合了
直接结合了 电离产生
电离产生 ,从而使得
,从而使得 的沉淀溶解平衡向溶解方向移动。
的沉淀溶解平衡向溶解方向移动。
资料:① 溶液呈中性;②
溶液呈中性;② 对该反应几乎无影响。
对该反应几乎无影响。
实验过程:各取 固体
固体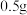 ,分别加入选取的实验试剂中。
,分别加入选取的实验试剂中。
(1)经检验,实验2中刺激性气味气体为 ,其具体方案为
,其具体方案为___________ 。
(2)甲同学对比实验1、2,认为实验2固体能溶解的原因是 溶液中
溶液中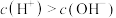 ,能与
,能与 反应。用化学用语解释
反应。用化学用语解释 溶液显酸性的原因
溶液显酸性的原因___________ 。
(3)乙同学通过实验3证明甲同学的说法不合理。
①X是___________ (填写溶质的化学式)。
②由实验3获取的证据为___________ 。
(4)为进一步探究实验2固体能溶解的原因,进行实验4.
乙依据上述实验,可以得出 能与
能与 直接反应。丙同学认为该方案不严谨,需要补充的实验方案是
直接反应。丙同学认为该方案不严谨,需要补充的实验方案是___________ 。
(5)由以上实验可以得出的结论是___________ 。
(6)为进一步分析 溶液浓度对沉淀溶解的实验效果,丁同学设计如下实验:
溶液浓度对沉淀溶解的实验效果,丁同学设计如下实验:
分析上述实验数据从平衡移动的角度解释上述现象___________ 。
 溶解于
溶解于 溶液的反应机理,提出下列两种观点:
溶液的反应机理,提出下列两种观点:观点一:
 的水解导致
的水解导致 溶液呈酸性,
溶液呈酸性, 与
与 反应,从而促进了
反应,从而促进了 的沉淀溶解平衡
的沉淀溶解平衡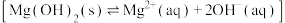 ]向溶解方向移动。
]向溶解方向移动。观点二:
 直接结合了
直接结合了 电离产生
电离产生 ,从而使得
,从而使得 的沉淀溶解平衡向溶解方向移动。
的沉淀溶解平衡向溶解方向移动。资料:①
 溶液呈中性;②
溶液呈中性;② 对该反应几乎无影响。
对该反应几乎无影响。实验过程:各取
 固体
固体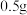 ,分别加入选取的实验试剂中。
,分别加入选取的实验试剂中。| 实验 | 实验试剂 | 实验现象 |
| 1 |  蒸馏水 蒸馏水 | 白色固体不溶解 |
| 2 | 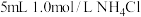 溶液 溶液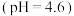 | 在微热下,产生刺激性气味气体且白色固体溶解 |
 ,其具体方案为
,其具体方案为(2)甲同学对比实验1、2,认为实验2固体能溶解的原因是
 溶液中
溶液中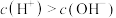 ,能与
,能与 反应。用化学用语解释
反应。用化学用语解释 溶液显酸性的原因
溶液显酸性的原因(3)乙同学通过实验3证明甲同学的说法不合理。
| 实验 | 实验试剂 | 实验现象 |
| 3 | 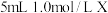 溶液 溶液 |
②由实验3获取的证据为
(4)为进一步探究实验2固体能溶解的原因,进行实验4.
| 实验 | 实验试剂 | 实验现象 |
| 4 | 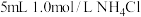 乙醇溶液 乙醇溶液 | 在微热下,白色固体溶解 |
 能与
能与 直接反应。丙同学认为该方案不严谨,需要补充的实验方案是
直接反应。丙同学认为该方案不严谨,需要补充的实验方案是(5)由以上实验可以得出的结论是
(6)为进一步分析
 溶液浓度对沉淀溶解的实验效果,丁同学设计如下实验:
溶液浓度对沉淀溶解的实验效果,丁同学设计如下实验: 溶液的浓度 溶液的浓度 | 现象 |
| 0.05 | 白色浑浊, 后仍有部分不溶解 后仍有部分不溶解 |
| 0.07 | 少量白色浑浊, 左右完全溶解 左右完全溶解 |
| 0.10 | 振荡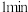 后完全溶解 后完全溶解 |
| 0.15 | 振荡 后完全溶解 后完全溶解 |
| 0.20 | 振荡后迅速溶解 |
| 0.30 | 振荡后迅速溶解 |
您最近一年使用:0次
解题方法
5 . 硫元素广泛存在于自然界中,是植物生长不可缺少的元素。回答下列问题:
(1)某小组同学设计实验实现不同价态含硫物质的转化。
可选用的实验试剂如下:
A. 溶液 B.浓硫酸 C.
溶液 B.浓硫酸 C. 溶液
溶液
D.稀硫酸 E.酸性 溶液 F.品红溶液 G.铜丝
溶液 F.品红溶液 G.铜丝
实验i选择的试剂是E和______ (填字母),证明实现转化的现象是______ 。
(2)该小组同学利用所选试剂,设计了如图所示装置研究实验ⅱ。
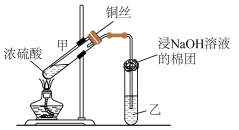
①试管甲中发生反应的化学方程式是__________ 。
②试管乙中的现象是_______ ;若实验结束后,将试管乙中的溶液加热,可以观察到的现象是______ 。
③下列关于 的说法,不正确的是
的说法,不正确的是__________ 。(填字母)
a.正常雨水的 等于7,酸雨因为溶解了
等于7,酸雨因为溶解了 ,其
,其 小于7
小于7
b.金属冶炼时产生的含 废气经回收后可用于制备硫酸
废气经回收后可用于制备硫酸
c. 在适当的温度并有催化剂存在的条件下,可以被氧气氧化,生成
在适当的温度并有催化剂存在的条件下,可以被氧气氧化,生成
(1)某小组同学设计实验实现不同价态含硫物质的转化。
可选用的实验试剂如下:
A.
 溶液 B.浓硫酸 C.
溶液 B.浓硫酸 C. 溶液
溶液D.稀硫酸 E.酸性
 溶液 F.品红溶液 G.铜丝
溶液 F.品红溶液 G.铜丝实验序号 | 预期转化 | 选择试剂 | 证明实现转化的现象 |
i |
| ||
ii |
|
|
(2)该小组同学利用所选试剂,设计了如图所示装置研究实验ⅱ。

①试管甲中发生反应的化学方程式是
②试管乙中的现象是
③下列关于
 的说法,不正确的是
的说法,不正确的是a.正常雨水的
 等于7,酸雨因为溶解了
等于7,酸雨因为溶解了 ,其
,其 小于7
小于7b.金属冶炼时产生的含
 废气经回收后可用于制备硫酸
废气经回收后可用于制备硫酸c.
 在适当的温度并有催化剂存在的条件下,可以被氧气氧化,生成
在适当的温度并有催化剂存在的条件下,可以被氧气氧化,生成
您最近一年使用:0次
名校
6 . 某食品合成香料(M)的一种制备流程如图(部分产物省略):
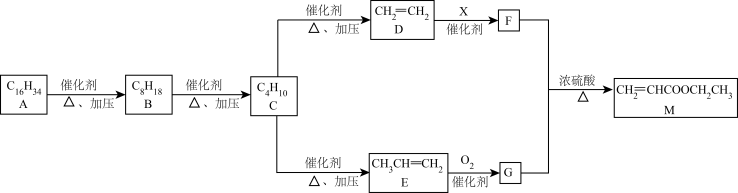
请回答下列问题:
(1)D→F的化学方程式为_______
(2)G的结构简式为_______ 。
(3)设计实验探究M的化学性质,实验结果如表:
能证明M含酯基的实验是_______ (填序号)。
(4)利用如图装置(加热装置省略)制备M。在三颈瓶中加入一定量F、浓硫酸和G,加热一段时间后,打开油水分离器,放出水层。待反应完全后,在混合物中加入饱和碳酸钠溶液,充分振荡,静置,分液得到较纯净的M。
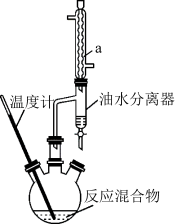
①仪器a的名称为_______ 。
②下列说法错误的是_______
A.冷凝管的主要作用是冷凝回流反应物,冷凝水从b出
B.酯化反应结束的标志是分水器内出现分层现象
C.利用分水器可分离出产生的水,提高酯的产率
D.生成乙酸乙酯反应的方程式为CH3CO18OH+C2H5OH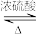 CH3COOC2H5+H218O
CH3COOC2H5+H218O
(5)设计一个方案:证明淀粉已经完全水解(方案格式例如:淀粉溶液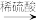 水解液→┈等等)加文字说明
水解液→┈等等)加文字说明_______
(6)写出乙醇催化氧化的反应方程式_______

请回答下列问题:
(1)D→F的化学方程式为
(2)G的结构简式为
(3)设计实验探究M的化学性质,实验结果如表:
| 序号 | 操作 | 现象 |
| ① | 向溴的四氯化碳溶液中加入过量M,振荡 | 溶液褪色,不分层 |
| ② | 向酸性 溶液中加入过量M,振荡 溶液中加入过量M,振荡 | 溶液褪色,分层 |
| ③ | 向NaOH溶液中加入适量M,加热 | 油层消失,不分层 |
(4)利用如图装置(加热装置省略)制备M。在三颈瓶中加入一定量F、浓硫酸和G,加热一段时间后,打开油水分离器,放出水层。待反应完全后,在混合物中加入饱和碳酸钠溶液,充分振荡,静置,分液得到较纯净的M。

①仪器a的名称为
②下列说法错误的是
A.冷凝管的主要作用是冷凝回流反应物,冷凝水从b出
B.酯化反应结束的标志是分水器内出现分层现象
C.利用分水器可分离出产生的水,提高酯的产率
D.生成乙酸乙酯反应的方程式为CH3CO18OH+C2H5OH
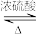 CH3COOC2H5+H218O
CH3COOC2H5+H218O(5)设计一个方案:证明淀粉已经完全水解(方案格式例如:淀粉溶液
 水解液→┈等等)加文字说明
水解液→┈等等)加文字说明(6)写出乙醇催化氧化的反应方程式
您最近一年使用:0次
2022-10-05更新
|
229次组卷
|
2卷引用:山西师范大学实验中学2021-2022学年高一下学期第二次月考化学试题
名校
解题方法
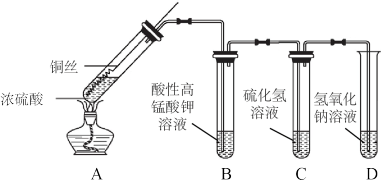
7 . 某化学实验小组的同学利用铜与浓硫酸反应制取二氧化硫并研究其性质,所用实验装置如下:
回答下列问题:
(1)将铜丝下端卷成螺旋状的理由是_______ 。
(2)向外拉铜丝,终止反应,冷却后,进一步证明A装置试管中反应所得产物含有铜离子的操作是_______ 。
(3)用化学方程式表示氢氧化钠溶液的作用是_______ 。
(4)装置A中反应的化学方程式是_______ 。
(5)装置B和装置C分别验证了二氧化硫的_______ 性质。
(6)化学实验小组的同学发现试管中有黑色物质产生,猜测黑色物质中可能含有CuO、Cu2S和CuS,针对产生的黑色物质,该小组同学利用装置A用不同浓度的浓硫酸与铜反应继续实验探究,并获得数据如下表。下列说法错误的是_______(填字母)。已知:Cu2S、CuS不溶于稀硫酸。

回答下列问题:
(1)将铜丝下端卷成螺旋状的理由是
(2)向外拉铜丝,终止反应,冷却后,进一步证明A装置试管中反应所得产物含有铜离子的操作是
(3)用化学方程式表示氢氧化钠溶液的作用是
(4)装置A中反应的化学方程式是
(5)装置B和装置C分别验证了二氧化硫的
(6)化学实验小组的同学发现试管中有黑色物质产生,猜测黑色物质中可能含有CuO、Cu2S和CuS,针对产生的黑色物质,该小组同学利用装置A用不同浓度的浓硫酸与铜反应继续实验探究,并获得数据如下表。下列说法错误的是_______(填字母)。已知:Cu2S、CuS不溶于稀硫酸。
| 硫酸浓度/(mol· L-1) | 黑色物质出现的温度/°C | 黑色物质消失的温度/°C |
| 15 | 约150 | 约236 |
| 16 | 约140 | 约250 |
| 18 | 约120 | 不消失 |
| A.取黑色物质洗涤、干燥后称量,加入足量稀硫酸充分混合,再取固体洗涤、干燥后称量,固体质量不变,说明黑色物质中不含CuO |
| B.黑色物质消失过程中有SO2、H2S生成 |
| C.相同条件下,硫酸浓度越大,反应速率越快,黑色物质越易出现、越易消失 |
| D.硫酸浓度为16mol/L时,先升温至250°C以上,再将铜丝与浓硫酸接触,可以避免产生黑色物质 |
您最近一年使用:0次
2022-04-27更新
|
230次组卷
|
2卷引用:山西省运城市高中联合体2021-2022学年高一下学期期中联考化学试题
名校
解题方法
8 . X、Y、Z、W、R、Q为原子序数依次增大的六种短周期主族元素。X是原子半径最小的元素;Y原子最外层电子数是核外电子层数的3倍;Z是短周期中金属性最强的元素;W是地壳中含量最多的金属元素;R的最高正价与最低负价代数和为4。请回答下列问题:
(1)Y的元素名称是______ 。
(2)W在周期表中的位置是______ 。
(3)写出化合物Z2R的电子式______ 。
(4)写出化合物X2Y2的结构式______ 。
(5)Y、Z、W三种元素对应的简单离子半径由大到小的顺序是______ (用元素的离子符号表示)。
(6)下列说法能证明非金属性Q强于R的是______ (填序号)。
a.简单阴离子的还原性:Q>R
b.简单氢化物热稳定性:Q>R
c.氧化物对应的水化物的酸性: Q>R
(7)W的单质与Z的最高价氧化物对应的水化物反应的化学方程式是______ 。
(1)Y的元素名称是
(2)W在周期表中的位置是
(3)写出化合物Z2R的电子式
(4)写出化合物X2Y2的结构式
(5)Y、Z、W三种元素对应的简单离子半径由大到小的顺序是
(6)下列说法能证明非金属性Q强于R的是
a.简单阴离子的还原性:Q>R
b.简单氢化物热稳定性:Q>R
c.氧化物对应的水化物的酸性: Q>R
(7)W的单质与Z的最高价氧化物对应的水化物反应的化学方程式是
您最近一年使用:0次
2021-01-19更新
|
592次组卷
|
5卷引用:山西省大同市第一中学校2022-2023学年高一上学期1月期末考试化学试题
名校
解题方法
9 . 如表是元素周期表的一部分,参照元素在表中的位置,回答下列问题:
(1)上述元素最高价氧化物对应水化物中,酸性最强的是__________ (填化学式),碱性最强的是__________ (填化学式),显两性的是__________ (填名称)。
(2)气态氢化物中,最稳定的是__________ (填化学式),④⑧形成的氢化物中沸点最高的是__________ (填化学式),原因是__________________ 。
(3)④分别和①、⑥两种元素的原子按1:1组成的常见化合物的电子式分别为__________ 和_______ 。用电子式表示②和④的三原子分子的形成过程____________ 。
(4)④⑥⑦⑨的简单离子半径由大到小的顺序为__________ (用离子符号和“>”表示)。
(5)⑥和⑦的最高价氧化物对应水化物之间发生反应的化学方程式___________ 。
(6)为了证明⑥和⑦两种元素的金属性强弱,下列说法或实验能提供证据的是______ 。
A.比较两种元素的单质的熔点、沸点高低
B.将两种元素的单质分别与冷水反应,观察反应的剧烈程度
C.比较两种元素的最高价氧化物对应的水化物的碱性强弱
主族 周期 | IA | IIA | IIA | IVA | VA | VIA | VIIA | 0族 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)气态氢化物中,最稳定的是
(3)④分别和①、⑥两种元素的原子按1:1组成的常见化合物的电子式分别为
(4)④⑥⑦⑨的简单离子半径由大到小的顺序为
(5)⑥和⑦的最高价氧化物对应水化物之间发生反应的化学方程式
(6)为了证明⑥和⑦两种元素的金属性强弱,下列说法或实验能提供证据的是
A.比较两种元素的单质的熔点、沸点高低
B.将两种元素的单质分别与冷水反应,观察反应的剧烈程度
C.比较两种元素的最高价氧化物对应的水化物的碱性强弱
您最近一年使用:0次
名校
解题方法
10 . 铁是日常生活中最常见的金属,某班同学在学习铁的知识时,有下列问题:
问题1:铁为何称为黑色金属?
问题2:CuO在高温下可分解为Cu2O和O2,Fe2O3在高温下可分解为FeO和O2吗?
(1)对于问题1,同学们上网查找,有两种解释:
A.因为在铁表面上有黑色的铁的氧化物,所以叫黑色金属
B.因为铁的粉末为黑色,铁的氧化物也均为黑色,所以叫黑色金属
①你认为正确的说法是__________ 。
②若有一黑色粉末,如何鉴别是铁粉,还是Fe3O4?______________________________________ 。
③若有一黑色粉末,为铁和四氧化三铁的混合物,如何证明其中有Fe3O4(只要求简述实验方法)?____________________________________ 。
(2)对于问题2,同学们准备实验探究,他们设想了两种方法:
A.将三氧化二铁高温灼烧,看灼烧前后颜色是否变化。
B.将三氧化二铁高温灼烧,看灼烧前后质量是否变化。
①实验中应将Fe2O3放在__________ (填仪器名称)中灼烧。
②方法A中,如果高温灼烧后颜色由__________ 变为__________ ,说明Fe2O3确实发生了变化。能说明生成的一定为FeO吗?__________ ,理由是________________________ 。
③方法B中,如果发生了预期的反应,固体高温灼烧前后质量比应为________ ,但是,实验结果固体灼烧前后质量比为30∶29,则高温灼烧后生成物是____________________ 。
④比较两种方法,你认为较好的方法是__________ 。
问题1:铁为何称为黑色金属?
问题2:CuO在高温下可分解为Cu2O和O2,Fe2O3在高温下可分解为FeO和O2吗?
(1)对于问题1,同学们上网查找,有两种解释:
A.因为在铁表面上有黑色的铁的氧化物,所以叫黑色金属
B.因为铁的粉末为黑色,铁的氧化物也均为黑色,所以叫黑色金属
①你认为正确的说法是
②若有一黑色粉末,如何鉴别是铁粉,还是Fe3O4?
③若有一黑色粉末,为铁和四氧化三铁的混合物,如何证明其中有Fe3O4(只要求简述实验方法)?
(2)对于问题2,同学们准备实验探究,他们设想了两种方法:
A.将三氧化二铁高温灼烧,看灼烧前后颜色是否变化。
B.将三氧化二铁高温灼烧,看灼烧前后质量是否变化。
①实验中应将Fe2O3放在
②方法A中,如果高温灼烧后颜色由
③方法B中,如果发生了预期的反应,固体高温灼烧前后质量比应为
④比较两种方法,你认为较好的方法是
您最近一年使用:0次