名校
1 . 盐碱地是土壤表层集聚过多盐碱成分,对农作物有害的土地。回答下列问题:
(1)盐碱地(含较多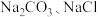 )不利于植物生长,盐碱地呈碱性的原因为
)不利于植物生长,盐碱地呈碱性的原因为___________ (用离子方程式说明);已知 时,
时, 的
的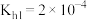 ,则当
,则当 溶液中
溶液中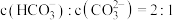 时,溶液的
时,溶液的
___________ 。
(2) 是农作物生长过程中不可缺少的微量元素。常用的铜肥是胆矾,在盐碱地施用胆矾时宜将其溶液
是农作物生长过程中不可缺少的微量元素。常用的铜肥是胆矾,在盐碱地施用胆矾时宜将其溶液___________ (填“喷在叶片上”或“随水灌入土壤中”),主要理由是___________ 。
(3)已知:常温下,碳酸的电离平衡常数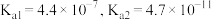 。常温下,向
。常温下,向 溶液中缓慢滴加
溶液中缓慢滴加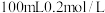 盐酸,溶液中各离子的物质的量随加入盐酸的物质的量的变化如图所示(
盐酸,溶液中各离子的物质的量随加入盐酸的物质的量的变化如图所示( 和
和 未画出)。根据图回答下列问题:
未画出)。根据图回答下列问题:
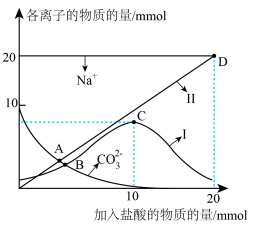
①曲线Ⅰ代表的离子是_______ 。
②A、B两点水的电离程度大小为A_______ B。
③根据上图,下列有关说法不正确的是_______ 。
a.滴加至 点时,
点时,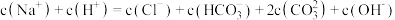
b.滴加至 点时,
点时,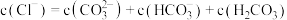
c.滴加至 点时,溶液
点时,溶液
④已知 电离平衡常数约为
电离平衡常数约为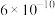 ,用一个离子方程式说明
,用一个离子方程式说明 和
和 结合
结合 能力的相对强弱
能力的相对强弱_______ 。
⑤证明 是弱电解质,你的设计方案是
是弱电解质,你的设计方案是_______ 。
(1)盐碱地(含较多
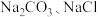 )不利于植物生长,盐碱地呈碱性的原因为
)不利于植物生长,盐碱地呈碱性的原因为 时,
时, 的
的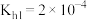 ,则当
,则当 溶液中
溶液中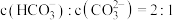 时,溶液的
时,溶液的
(2)
 是农作物生长过程中不可缺少的微量元素。常用的铜肥是胆矾,在盐碱地施用胆矾时宜将其溶液
是农作物生长过程中不可缺少的微量元素。常用的铜肥是胆矾,在盐碱地施用胆矾时宜将其溶液(3)已知:常温下,碳酸的电离平衡常数
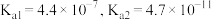 。常温下,向
。常温下,向 溶液中缓慢滴加
溶液中缓慢滴加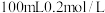 盐酸,溶液中各离子的物质的量随加入盐酸的物质的量的变化如图所示(
盐酸,溶液中各离子的物质的量随加入盐酸的物质的量的变化如图所示( 和
和 未画出)。根据图回答下列问题:
未画出)。根据图回答下列问题:
①曲线Ⅰ代表的离子是
②A、B两点水的电离程度大小为A
③根据上图,下列有关说法不正确的是
a.滴加至
 点时,
点时,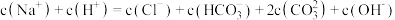
b.滴加至
 点时,
点时,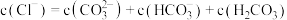
c.滴加至
 点时,溶液
点时,溶液
④已知
 电离平衡常数约为
电离平衡常数约为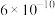 ,用一个离子方程式说明
,用一个离子方程式说明 和
和 结合
结合 能力的相对强弱
能力的相对强弱⑤证明
 是弱电解质,你的设计方案是
是弱电解质,你的设计方案是
您最近一年使用:0次
2023-12-13更新
|
65次组卷
|
2卷引用:广东省佛山市H7教育共同体2023-2024学年高二上学期联考化学试题
解题方法
2 . 氨的催化氧化过程是当下研究的重要课题。
(1) 与
与 在一定压强和800℃条件下发生催化氧化反应时,可发生不同反应:
在一定压强和800℃条件下发生催化氧化反应时,可发生不同反应:
反应i:

反应ii: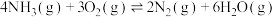
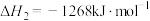
①该条件下 与
与 反应生成NO的热化学方程式为
反应生成NO的热化学方程式为___________ 。
②在恒温恒容密闭容器中,下列说法可以证明反应i已达到平衡状态的是___________ (填序号)。
A.
B.n个 键断裂的同时,有n个
键断裂的同时,有n个 键形成
键形成
C.混合气体的密度不变
D.容器内压强不变
③反应i与反应ii有关物质产率与温度的关系如图。下列说法正确 的是___________ 。
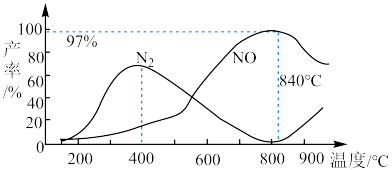
A.氨催化氧化生成 时,温度应控制在400℃左右
时,温度应控制在400℃左右
B.对反应升温可提高反应物转化率
C.提高物料比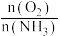 的值,主要目的的是提高反应速率
的值,主要目的的是提高反应速率
D.840℃后,NO产率下降的主要原因是以反应(ii)为主
(2)在两个恒压密闭容器中分别充入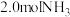 、
、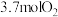 ,仅发生反应ii,测得
,仅发生反应ii,测得 的平衡转化率随温度的变化如图所示。
的平衡转化率随温度的变化如图所示。
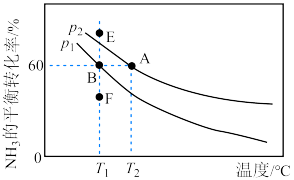
①
___________  (填“>”或“<”),理由是
(填“>”或“<”),理由是___________ 。
②若容器的初始体积为2.0L,则在A点状态下平衡时容器中
___________  。
。
③B点的平衡常数
___________ 。(用分压表示,气体分压=气体总压 气体的物质的量分数。写出代数式,无需计算具体结果)
气体的物质的量分数。写出代数式,无需计算具体结果)
④若温度为 ,压强为
,压强为 ,容器的初始体积为2.0L时,分别充入
,容器的初始体积为2.0L时,分别充入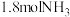 、
、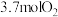 、0.2molAr发生反应ii,此时
、0.2molAr发生反应ii,此时 的平衡转化率为图中的点
的平衡转化率为图中的点___________ (选填“E”、“B”或“F”)。
(1)
 与
与 在一定压强和800℃条件下发生催化氧化反应时,可发生不同反应:
在一定压强和800℃条件下发生催化氧化反应时,可发生不同反应:反应i:


反应ii:
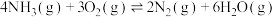
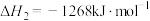
①该条件下
 与
与 反应生成NO的热化学方程式为
反应生成NO的热化学方程式为②在恒温恒容密闭容器中,下列说法可以证明反应i已达到平衡状态的是
A.

B.n个
 键断裂的同时,有n个
键断裂的同时,有n个 键形成
键形成C.混合气体的密度不变
D.容器内压强不变
③反应i与反应ii有关物质产率与温度的关系如图。下列说法

A.氨催化氧化生成
 时,温度应控制在400℃左右
时,温度应控制在400℃左右B.对反应升温可提高反应物转化率
C.提高物料比
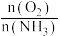 的值,主要目的的是提高反应速率
的值,主要目的的是提高反应速率D.840℃后,NO产率下降的主要原因是以反应(ii)为主
(2)在两个恒压密闭容器中分别充入
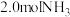 、
、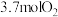 ,仅发生反应ii,测得
,仅发生反应ii,测得 的平衡转化率随温度的变化如图所示。
的平衡转化率随温度的变化如图所示。
①

 (填“>”或“<”),理由是
(填“>”或“<”),理由是②若容器的初始体积为2.0L,则在A点状态下平衡时容器中

 。
。③B点的平衡常数

 气体的物质的量分数。写出代数式,无需计算具体结果)
气体的物质的量分数。写出代数式,无需计算具体结果)④若温度为
 ,压强为
,压强为 ,容器的初始体积为2.0L时,分别充入
,容器的初始体积为2.0L时,分别充入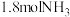 、
、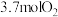 、0.2molAr发生反应ii,此时
、0.2molAr发生反应ii,此时 的平衡转化率为图中的点
的平衡转化率为图中的点
您最近一年使用:0次
名校
3 .  遇水极易发生水解。某化学兴趣小组设计实验制备
遇水极易发生水解。某化学兴趣小组设计实验制备 并探究其性质。
并探究其性质。
Ⅰ.氯化铁的制备:
(1)图1为湿法制备的装置,仪器A的名称为___________ ,烧杯中发生反应的离子方程式为___________ 。

(2)图2为干法制备的装置。反应前后都要鼓入氮气,目的是___________ 。
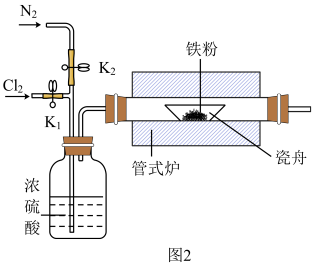
Ⅱ.氯化铁的性质探究:
(3)查阅资料:氯化铁在水溶液中分多步水解,生成净水性能更好的聚合氯化铁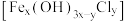 。写出氯化铁水解生成聚合氯化铁的总化学方程式
。写出氯化铁水解生成聚合氯化铁的总化学方程式___________ 。
(4)为了探究外界条件对氯化铁水解平衡的影响,该兴趣小组设计实验方案(忽略溶液体积的变化, 的浓度为1mol/L),获得以下数据:
的浓度为1mol/L),获得以下数据:
①实验1和实验2说明 的水解是
的水解是___________ (填“吸热”或“放热”)反应。
②由实验1和3可知,稀释 溶液,
溶液, 水解平衡
水解平衡___________ (填“正”或“逆”)向移动;结合表中数据,给出判断理由:___________ 。
③查阅资料,加入强电解质后,由于溶液中离子总浓度增大,离子间的相互牵制作用增强,水解离子的活性会改变。该兴趣小组同学求助老师,利用计算机手持技术得到实验4和实验5的结果分别如图3和图4所示。
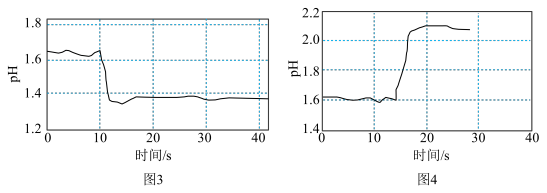
ⅰ.根据上述实验数据和结果,下列说法不正确的是___________ (填标号)。
A.实验过程中量取 溶液时应选用酸式滴定管
溶液时应选用酸式滴定管
B.实验4和实验5中a与b的关系式为
C.根据图3与图4结果可知,离子的水解活性强弱还受离子种类的影响
ⅱ.有同学猜想图3结果是因为氯离子促进了 的水解,请你设计其他简单实验证明该猜想成立:
的水解,请你设计其他简单实验证明该猜想成立:___________ (写出实验操作、现象或结果)。
 遇水极易发生水解。某化学兴趣小组设计实验制备
遇水极易发生水解。某化学兴趣小组设计实验制备 并探究其性质。
并探究其性质。Ⅰ.氯化铁的制备:
(1)图1为湿法制备的装置,仪器A的名称为

(2)图2为干法制备的装置。反应前后都要鼓入氮气,目的是

Ⅱ.氯化铁的性质探究:
(3)查阅资料:氯化铁在水溶液中分多步水解,生成净水性能更好的聚合氯化铁
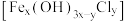 。写出氯化铁水解生成聚合氯化铁的总化学方程式
。写出氯化铁水解生成聚合氯化铁的总化学方程式(4)为了探究外界条件对氯化铁水解平衡的影响,该兴趣小组设计实验方案(忽略溶液体积的变化,
 的浓度为1mol/L),获得以下数据:
的浓度为1mol/L),获得以下数据:| 实验 | 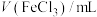 | 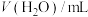 | n(NaCl)/mol | 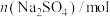 | 温度/℃ | pH |
| 1 | 10.00 | 90.00 | 0 | 0 | 25 | 1.62 |
| 2 | 10.00 | 90.00 | 0 | 0 | 35 | 1.47 |
| 3 | 10.00 | 0 | 0 | 0 | 25 | 0.74 |
| 4 | 10.00 | 90.00 | a | 0 | 25 | x |
| 5 | 10.00 | 90.00 | 0 | b | 25 | y |
 的水解是
的水解是②由实验1和3可知,稀释
 溶液,
溶液, 水解平衡
水解平衡③查阅资料,加入强电解质后,由于溶液中离子总浓度增大,离子间的相互牵制作用增强,水解离子的活性会改变。该兴趣小组同学求助老师,利用计算机手持技术得到实验4和实验5的结果分别如图3和图4所示。

ⅰ.根据上述实验数据和结果,下列说法不正确的是
A.实验过程中量取
 溶液时应选用酸式滴定管
溶液时应选用酸式滴定管B.实验4和实验5中a与b的关系式为

C.根据图3与图4结果可知,离子的水解活性强弱还受离子种类的影响
ⅱ.有同学猜想图3结果是因为氯离子促进了
 的水解,请你设计其他简单实验证明该猜想成立:
的水解,请你设计其他简单实验证明该猜想成立:
您最近一年使用:0次
2024-01-22更新
|
94次组卷
|
2卷引用:广东省深圳市南山区2023-2024学年高二上学期期末考试化学试题
名校
解题方法
4 . 某学习小组为证实Ba(OH)2溶液和H2SO4溶液的反应是离子反应,设计了如下实验。请补充完成该实验报告。当从滴定管中逐渐加入A溶液时,溶液的导电性的变化趋势如图所示。

(1)[实验原理] 溶液的导电性由溶液中_______ 及_______ 决定。观察_______ ,据此判断溶液中自由移动的离子浓度的变化,从而证明反应是离子反应。
[实验装置]如图所示。

(2)[实验过程与记录]
(3)关于图(2)下列说法中错误的是_______(填字母)。
(4)书写下列两种情况的离子方程式。
①向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至SO 恰好完全沉淀:
恰好完全沉淀:_______ 。
②向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液显中性:_______ 。
(5)请回答下列问题:
①NaHSO4属于_______ (填“酸”、“碱”或“盐”)。
②将NaHSO4溶液中逐滴加入Ba(OH)2溶液能否出现如图(2)的导电性曲线_______ 。
A.能 B.否

(1)[实验原理] 溶液的导电性由溶液中
[实验装置]如图所示。

(2)[实验过程与记录]
| 实验步骤 | 实验现象 | 实验结论 |
| 连接好装置,向烧杯中加入25mL一定浓度的Ba(OH)2溶液和2滴酚酞溶液,逐滴滴加一定浓度的H2SO4溶液直至过量,边滴边振荡 | Ba(OH)2溶液和H2SO4溶液的反应是离子反应 |
| A.反应前一段导电能力不断减弱,说明生成的BaSO4是非电解质 |
| B.图(2)中最低点导电能力约为零说明溶液中几乎没有自由移动的离子 |
| C.图(2)中最低点导电能力约为零时,Ba(OH)2溶液与稀硫酸恰好完全中和 |
| D.Ba(OH)2、H2SO4和BaSO4都是电解质 |
①向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至SO
 恰好完全沉淀:
恰好完全沉淀:②向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液显中性:
(5)请回答下列问题:
①NaHSO4属于
②将NaHSO4溶液中逐滴加入Ba(OH)2溶液能否出现如图(2)的导电性曲线
A.能 B.否
您最近一年使用:0次
名校
5 . 下表是元素周期表的短周期部分

(1)④、⑥和⑧的简单离子的半径从大到小为___________ (用离子符号表示)
(2)②、⑦和⑨的最高价氧化物对应水化物的酸性从强到弱为___________ (用化学式表示)。
(3)实验室制备③的简单氢化物化学方程式为___________ 。⑨所形成的单质与水反应的离子方程式为___________ 。
(4)主族元素砷(As)的部分信息如图所示
①砷(As)在周期表中的位置是___________ 。
②下列说法不正确的是___________ (填序号)。
A.砷元素的最高化合价为+4
B.推测砷有多种氧化物
C.③的气态氢化物的稳定性大于砷的气态氢化物的稳定性
D.As的最高价氧化物对应水化物是一种强酸
(5)设计一个简单的实验证明⑨的非金属性强于⑧___________ 。

(1)④、⑥和⑧的简单离子的半径从大到小为
(2)②、⑦和⑨的最高价氧化物对应水化物的酸性从强到弱为
(3)实验室制备③的简单氢化物化学方程式为
(4)主族元素砷(As)的部分信息如图所示

①砷(As)在周期表中的位置是
②下列说法不正确的是
A.砷元素的最高化合价为+4
B.推测砷有多种氧化物
C.③的气态氢化物的稳定性大于砷的气态氢化物的稳定性
D.As的最高价氧化物对应水化物是一种强酸
(5)设计一个简单的实验证明⑨的非金属性强于⑧
您最近一年使用:0次
名校
6 . I.如图是乙酸乙酯的绿色合成路线之一:
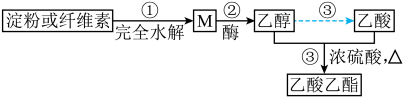
(1)M的分子式为___________ ,作为营养剂供给人体能量,在体内发生的主要反应类型是___________ ;
(2)下列说法不正确的是___________(填字母序号)。
Ⅱ.实验室制取乙酸乙酯的主要步骤如下:
①在甲试管(如图)中加入 浓硫酸、
浓硫酸、 乙醇和
乙醇和 乙酸的混合溶液。
乙酸的混合溶液。
②按如图连接好装置(装置气密性良好)并加入混合液,小火均匀地加热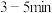 。
。
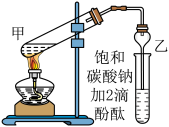
③待试管乙收集到一定量产物后停止加热,撤出试管并用力振荡,然后静置待分层。
④分离出乙酸乙酯层、洗涤、干燥。
(3)若实验中用乙酸和含 的乙醇作用,该反应的化学方程式是:
的乙醇作用,该反应的化学方程式是:___________ ;
(4)上述实验中饱和碳酸钠溶液的作用是___________ (填字母代号);
A.反应掉乙酸并吸收乙醇
B.加速酯的生成,提高其产率
C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出
(5)欲将乙试管中的物质分离以得到乙酸乙酯,必须使用的仪器是___________ ,分液时,乙酸乙酯应该从仪器___________ (填:“下口放”或“上口倒”)出;
(6)生成乙酸乙酯的反应是可逆反应,反应一段时间后,下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有___________ (填序号);
①混合物中各物质的浓度不再变化;
②单位时间里,生成 乙醇,同时生成
乙醇,同时生成 乙酸;
乙酸;
③单位时间里,生成 乙酸乙酯,同时生成
乙酸乙酯,同时生成 乙酸。
乙酸。
④单位时间里,生成 乙酸乙酯,同时生成
乙酸乙酯,同时生成 水
水
(7)为了证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用上图所示装置进行了以下4个实验。实验开始先用酒精灯微热 ,再加热使之微微沸腾
,再加热使之微微沸腾 。实验结束后充分振荡小试管Ⅱ再测有机层的厚度,实验记录如下:
。实验结束后充分振荡小试管Ⅱ再测有机层的厚度,实验记录如下:
①实验D的目的是与实验C相对照,证明 对酯化反应具有催化作用。实验D中应加入盐酸的体积和浓度分别是
对酯化反应具有催化作用。实验D中应加入盐酸的体积和浓度分别是___________ mL和___________  。
。
②分析实验___________ (填实验编号)的数据,可以推测出浓 的吸水性提高了乙酸乙酯的产率;
的吸水性提高了乙酸乙酯的产率;
(8)若现有乙酸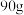 ,乙醇
,乙醇 发生酯化反应得到
发生酯化反应得到 乙酸乙酯,试计算该反应的产品产率为
乙酸乙酯,试计算该反应的产品产率为___________ (产率%= ×100%)。
×100%)。

(1)M的分子式为
(2)下列说法不正确的是___________(填字母序号)。
| A.淀粉和纤维素都属于天然高分子化合物 |
| B.M可与银氨溶液发生银镜反应 |
| C.所有的糖类都有甜味,都可以发生水解反应 |
| D.用KI溶液可以检验淀粉 |
Ⅱ.实验室制取乙酸乙酯的主要步骤如下:
①在甲试管(如图)中加入
 浓硫酸、
浓硫酸、 乙醇和
乙醇和 乙酸的混合溶液。
乙酸的混合溶液。②按如图连接好装置(装置气密性良好)并加入混合液,小火均匀地加热
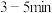 。
。
③待试管乙收集到一定量产物后停止加热,撤出试管并用力振荡,然后静置待分层。
④分离出乙酸乙酯层、洗涤、干燥。
(3)若实验中用乙酸和含
 的乙醇作用,该反应的化学方程式是:
的乙醇作用,该反应的化学方程式是:(4)上述实验中饱和碳酸钠溶液的作用是
A.反应掉乙酸并吸收乙醇
B.加速酯的生成,提高其产率
C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出
(5)欲将乙试管中的物质分离以得到乙酸乙酯,必须使用的仪器是
(6)生成乙酸乙酯的反应是可逆反应,反应一段时间后,下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有
①混合物中各物质的浓度不再变化;
②单位时间里,生成
 乙醇,同时生成
乙醇,同时生成 乙酸;
乙酸;③单位时间里,生成
 乙酸乙酯,同时生成
乙酸乙酯,同时生成 乙酸。
乙酸。④单位时间里,生成
 乙酸乙酯,同时生成
乙酸乙酯,同时生成 水
水(7)为了证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用上图所示装置进行了以下4个实验。实验开始先用酒精灯微热
 ,再加热使之微微沸腾
,再加热使之微微沸腾 。实验结束后充分振荡小试管Ⅱ再测有机层的厚度,实验记录如下:
。实验结束后充分振荡小试管Ⅱ再测有机层的厚度,实验记录如下:| 实验编号 | 试管I中试剂 | 试管II中试剂 | 有机层的厚度/cm |
| A |  乙醇、 乙醇、 乙酸、 乙酸、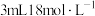 浓硫酸 浓硫酸 | 饱和 溶液 溶液 | 3.0 |
| B |  乙醇、 乙醇、 乙酸、 乙酸、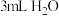 | 0.1 | |
| C |  乙醇、 乙醇、 乙酸、 乙酸、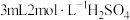 | 0.6 | |
| D |  乙醇、 乙醇、 乙酸、盐酸 乙酸、盐酸 | 0.6 |
 对酯化反应具有催化作用。实验D中应加入盐酸的体积和浓度分别是
对酯化反应具有催化作用。实验D中应加入盐酸的体积和浓度分别是 。
。②分析实验
 的吸水性提高了乙酸乙酯的产率;
的吸水性提高了乙酸乙酯的产率;(8)若现有乙酸
 ,乙醇
,乙醇 发生酯化反应得到
发生酯化反应得到 乙酸乙酯,试计算该反应的产品产率为
乙酸乙酯,试计算该反应的产品产率为 ×100%)。
×100%)。
您最近一年使用:0次
解题方法
7 . T℃时,在体积为2L的密闭容器内,与同一个化学反应有关的A、B、C、D四种物质(D为固体,其余均为气体)的物质的量随反应时间变化的曲线如图所示,回答下列问题。
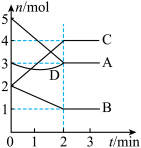
(1)该反应的化学方程式为_______ 。
(2)物质D在反应中的作用是______ 。
(3)若在上述反应中A是SO2、B是O2、C是SO3。下列说法能表示反应达到平衡状态的是______ (填字母);在0~2min内用O2表示的反应速率v(O2)=______ 。
A.容器内的气体压强保持不变 B.物质的量浓度:c(SO2)=2c(O2)
C.混合气的平均相对分子质量保持不变 D.化学反应速率:v(SO2)=v(SO3)
(4)某兴趣小组同学拟在实验室中制取SO2,并探究SO2使品红溶液褪色的原因。
①用Cu和浓硫酸反应制取SO2,化学反应方程式是_______ 。
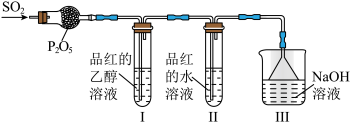
②兴趣小组同学利用如图装置探究SO2的漂白性,观察到I中品红溶液不褪色,II中品红溶液褪色。
查阅资料:SO2通入水中存在如下反应:SO2+xH2O SO2•xH2O
SO2•xH2O H++HSO
H++HSO +(x-1)H2O;HSO
+(x-1)H2O;HSO
 SO
SO +H+。
+H+。
通过分析上述现象,猜测使品红水溶液褪色的微粒可能是i.H2SO3;ii.______ ;iii.______ 。
③为了证明上述猜测ii和iii,进行表中实验1和2,记录现象。
该实验说明,两种粒子中,______ 使品红水溶液褪色程度更大。
④取实验1所得溶液直接加热接近沸腾,溶液不恢复红色,在热溶液中滴加稀硫酸则恢复红色;说明______ ;取实验2所得溶液直接加热,则慢慢恢复浅红色,说明NaHSO3与品红生成的物质不稳定。

(1)该反应的化学方程式为
(2)物质D在反应中的作用是
(3)若在上述反应中A是SO2、B是O2、C是SO3。下列说法能表示反应达到平衡状态的是
A.容器内的气体压强保持不变 B.物质的量浓度:c(SO2)=2c(O2)
C.混合气的平均相对分子质量保持不变 D.化学反应速率:v(SO2)=v(SO3)
(4)某兴趣小组同学拟在实验室中制取SO2,并探究SO2使品红溶液褪色的原因。
①用Cu和浓硫酸反应制取SO2,化学反应方程式是
②兴趣小组同学利用如图装置探究SO2的漂白性,观察到I中品红溶液不褪色,II中品红溶液褪色。

查阅资料:SO2通入水中存在如下反应:SO2+xH2O
 SO2•xH2O
SO2•xH2O H++HSO
H++HSO +(x-1)H2O;HSO
+(x-1)H2O;HSO
 SO
SO +H+。
+H+。通过分析上述现象,猜测使品红水溶液褪色的微粒可能是i.H2SO3;ii.
③为了证明上述猜测ii和iii,进行表中实验1和2,记录现象。
| 实验序号 | 实验1 | 实验2 |
| 实验操作 |  2mL0.20mol•L-1Na2SO3溶液 |  2mL0.20mol•L-1NaHSO3溶液 |
| 实验现象 | 迅速褪色 | 褪色较慢 |
④取实验1所得溶液直接加热接近沸腾,溶液不恢复红色,在热溶液中滴加稀硫酸则恢复红色;说明
您最近一年使用:0次
2023-04-28更新
|
407次组卷
|
3卷引用:广东省广州市、韶关市、深圳市、惠州市、梅州市重点校2022-2023学年高一下学期5月统一调研化学试题
8 . 某课外学习小组在一些化学实验中都用了碳酸盐。
(1)利用图装置进行Cu与 制取氮氧化物的反应。
制取氮氧化物的反应。
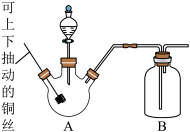
①若利用铜与浓硝酸反应制取并收集 ,为驱赶装置内的空气,可先在三颈烧瓶A中放入少量
,为驱赶装置内的空气,可先在三颈烧瓶A中放入少量___________ 粉末,再滴加浓硝酸。
②若利用该装置制取并收集NO时,则需对集气装置广口瓶B作必要的改动,改动措施是_______ 。
③针对上述实验,以下说法不正确的是___________ 。(填字母)
a.还缺少尾气吸收装置
b.不管是①还是②,每个实验,实验过程中整套装置都至少要组装两次
c.盖上滴液漏斗的玻璃塞,用水封住广口瓶B的长导管口,加热三颈烧瓶A,可以检查装置的气密性
d.在铜丝与橡皮塞之间涂抹少许凡士林,以润滑铜丝和封闭缝隙
(2) 难溶与水。难溶电解质遇到具有不同离子的可溶性强电解质溶液,会使难溶电解质溶解度增大,这种现象叫做“盐效应”。“盐效应”与离子浓度、离子所带电量有关。某小组设计实验探究
难溶与水。难溶电解质遇到具有不同离子的可溶性强电解质溶液,会使难溶电解质溶解度增大,这种现象叫做“盐效应”。“盐效应”与离子浓度、离子所带电量有关。某小组设计实验探究 是否能与
是否能与 形成络离子,分别取等量的
形成络离子,分别取等量的 进行实验,实验结果如图所示:
进行实验,实验结果如图所示:
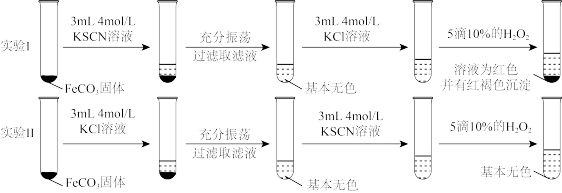
①不考虑 是否能与
是否能与 形成络离子,单就盐效应来讲,相同浓度下,KSCN溶液盐效应
形成络离子,单就盐效应来讲,相同浓度下,KSCN溶液盐效应___________ KCl溶液(填“>”、“=”、“<”)。
②滤液中+2价Fe总浓度:实验I___________ 实验II(填“>”、“=”、“<”)。
③设计实验II,对实验I的帮助作用是___________ 。
(3)常温下苯酚微溶于水,在水中形成乳浊液。苯酚是一种弱酸,常温下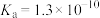 ,相同温度下碳酸
,相同温度下碳酸 ,
,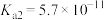 。限用两种药品或试剂(不包括蒸馏水),仪器不限,设计实验证明酸性:
。限用两种药品或试剂(不包括蒸馏水),仪器不限,设计实验证明酸性:
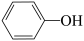 >
> 。
。
(1)利用图装置进行Cu与
 制取氮氧化物的反应。
制取氮氧化物的反应。
①若利用铜与浓硝酸反应制取并收集
 ,为驱赶装置内的空气,可先在三颈烧瓶A中放入少量
,为驱赶装置内的空气,可先在三颈烧瓶A中放入少量②若利用该装置制取并收集NO时,则需对集气装置广口瓶B作必要的改动,改动措施是
③针对上述实验,以下说法不正确的是
a.还缺少尾气吸收装置
b.不管是①还是②,每个实验,实验过程中整套装置都至少要组装两次
c.盖上滴液漏斗的玻璃塞,用水封住广口瓶B的长导管口,加热三颈烧瓶A,可以检查装置的气密性
d.在铜丝与橡皮塞之间涂抹少许凡士林,以润滑铜丝和封闭缝隙
(2)
 难溶与水。难溶电解质遇到具有不同离子的可溶性强电解质溶液,会使难溶电解质溶解度增大,这种现象叫做“盐效应”。“盐效应”与离子浓度、离子所带电量有关。某小组设计实验探究
难溶与水。难溶电解质遇到具有不同离子的可溶性强电解质溶液,会使难溶电解质溶解度增大,这种现象叫做“盐效应”。“盐效应”与离子浓度、离子所带电量有关。某小组设计实验探究 是否能与
是否能与 形成络离子,分别取等量的
形成络离子,分别取等量的 进行实验,实验结果如图所示:
进行实验,实验结果如图所示:
①不考虑
 是否能与
是否能与 形成络离子,单就盐效应来讲,相同浓度下,KSCN溶液盐效应
形成络离子,单就盐效应来讲,相同浓度下,KSCN溶液盐效应②滤液中+2价Fe总浓度:实验I
③设计实验II,对实验I的帮助作用是
(3)常温下苯酚微溶于水,在水中形成乳浊液。苯酚是一种弱酸,常温下
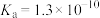 ,相同温度下碳酸
,相同温度下碳酸 ,
,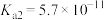 。限用两种药品或试剂(不包括蒸馏水),仪器不限,设计实验证明酸性:
。限用两种药品或试剂(不包括蒸馏水),仪器不限,设计实验证明酸性:
 >
> 。
。| 简要的实验操作 | 实验现象 | 实验结论 |
酸性:  | ||
酸性: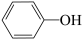 > > |
您最近一年使用:0次
名校
解题方法
9 . HNO3是重要的化工原料,浓HNO3与Cu反应的装置如图1所示:
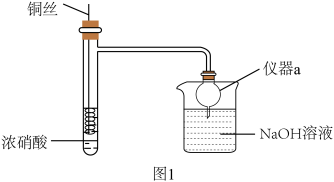
回答下列问题:
(1)仪器a的名称是_______ ,在该实验中的作用为_______ 。
(2)关于该实验下列说法错误的是_______。
(3)某小组同学发现Cu与浓HNO3反应所得混合溶液为绿色,Cu与稀HNO3反应所得混合溶液为蓝色,针对绿色产生的原因展开探究。
【提出猜想】
猜想a:Cu(NO3)2浓度大
猜想b:NO2溶解在Cu(NO3)2溶液中
【实验验证】
实验i:配制饱和Cu(NO3)2溶液,溶液呈_______ 色,证明猜想a不成立。
实验ii:取适量Cu与浓HNO3反应后的溶液,置于图2所示装置中,鼓入空气后,溶液上方可观察到_______ ,5min后,溶液完全变为蓝色,证明猜想b成立。
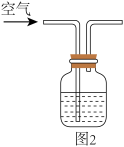
(4)另一组同学查阅资料发现:NO2能与水反应生成HNO2,进而发生下述反应:
①由此该组同学认为通过实验说明猜想b成立不严谨,理由是_______ 。
②写出NO2与水反应生成HNO2的化学方程式_______ 。
③该组同学改进后设计了新的实验:
实验iii:取适量Cu与浓HNO3反应后的溶液,置于图2所示装置中,鼓入氮气后,溶液上方现象与实验ii相同,但5min后,溶液仍为绿色。对比实验ii与实验iii,可推测Cu(NO3)2溶液为绿色的原因主要是_______ 。

回答下列问题:
(1)仪器a的名称是
(2)关于该实验下列说法错误的是_______。
| A.该反应需要加热才能进行 | B.可通过抽动铜丝控制反应开始和停止 |
| C.反应后迅速生成大量红棕色气体 | D.烧杯中仅发生中和反应 |
【提出猜想】
猜想a:Cu(NO3)2浓度大
猜想b:NO2溶解在Cu(NO3)2溶液中
【实验验证】
实验i:配制饱和Cu(NO3)2溶液,溶液呈
实验ii:取适量Cu与浓HNO3反应后的溶液,置于图2所示装置中,鼓入空气后,溶液上方可观察到

(4)另一组同学查阅资料发现:NO2能与水反应生成HNO2,进而发生下述反应:

①由此该组同学认为通过实验说明猜想b成立不严谨,理由是
②写出NO2与水反应生成HNO2的化学方程式
③该组同学改进后设计了新的实验:
实验iii:取适量Cu与浓HNO3反应后的溶液,置于图2所示装置中,鼓入氮气后,溶液上方现象与实验ii相同,但5min后,溶液仍为绿色。对比实验ii与实验iii,可推测Cu(NO3)2溶液为绿色的原因主要是
您最近一年使用:0次
2023-02-09更新
|
1338次组卷
|
3卷引用:广东省佛山市2023届普通高中教学质量检测(一)化学试题
10 . I.大气的成分在工业上有重要的应用。
(1)在恒容密闭容器中,发生反应N2(g)+3H2(g) 2NH3(g),下列说法可以证明反应已达到平衡状态的是
2NH3(g),下列说法可以证明反应已达到平衡状态的是_______ (填序号)。
①单位时间内生成nmolN2的同时生成2nmolNH3
②1个N≡N键断裂的同时,有6个N-H键形成
③混合气体的密度不再改变的状态
④混合气体的压强不再改变的状态
⑤混合气体的平均相对分子质量不再改变的状态
(2)为提高H2的转化率,实际生产中宜采取的措施是_______ (填字母)。
II.中国科学家首次实现了以二氧化碳为原料,不依赖植物光合作用,直接人工合成淀粉。已知CO2经催化加氢可以生成多种低碳有机物。
已知:
①CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H1=-49.5kJ•mol-1
CH3OH(g)+H2O(g) △H1=-49.5kJ•mol-1
②CO2(g)+H2(g) CO(g)+H2O(g) △H2=+40.9kJ•mol-1
CO(g)+H2O(g) △H2=+40.9kJ•mol-1
③CO(g)+2H2(g) CH3OH(g) △H3
CH3OH(g) △H3
回答下列问题:
(3)反应③的△H3为_______ 。
(4)一定温度下,在一体积固定的密闭容器中进行反应①,测得CO2的物质的量浓度随反应时间的变化如图所示,则反应进行的前5分钟内,v(H2)=_______ ;10min时,改变的外界条件可能是_______ 。

(5)已知一定温度下按照起始比 =2,在一密闭容器中进行反应③,保持总压为4MPa不变,达平衡时CO的平衡转化率为50%,则该条件下用平衡体系中各气体分压表示的平衡常数Kp=
=2,在一密闭容器中进行反应③,保持总压为4MPa不变,达平衡时CO的平衡转化率为50%,则该条件下用平衡体系中各气体分压表示的平衡常数Kp=_______ (各气体分压=平衡体系中各气体的体积分数×总压)。
(1)在恒容密闭容器中,发生反应N2(g)+3H2(g)
 2NH3(g),下列说法可以证明反应已达到平衡状态的是
2NH3(g),下列说法可以证明反应已达到平衡状态的是①单位时间内生成nmolN2的同时生成2nmolNH3
②1个N≡N键断裂的同时,有6个N-H键形成
③混合气体的密度不再改变的状态
④混合气体的压强不再改变的状态
⑤混合气体的平均相对分子质量不再改变的状态
(2)为提高H2的转化率,实际生产中宜采取的措施是
| A.及时移出氨 | B.适当增大压强 | C.减小压强 | D.降低温度 |
II.中国科学家首次实现了以二氧化碳为原料,不依赖植物光合作用,直接人工合成淀粉。已知CO2经催化加氢可以生成多种低碳有机物。
已知:
①CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H1=-49.5kJ•mol-1
CH3OH(g)+H2O(g) △H1=-49.5kJ•mol-1②CO2(g)+H2(g)
 CO(g)+H2O(g) △H2=+40.9kJ•mol-1
CO(g)+H2O(g) △H2=+40.9kJ•mol-1③CO(g)+2H2(g)
 CH3OH(g) △H3
CH3OH(g) △H3回答下列问题:
(3)反应③的△H3为
(4)一定温度下,在一体积固定的密闭容器中进行反应①,测得CO2的物质的量浓度随反应时间的变化如图所示,则反应进行的前5分钟内,v(H2)=

(5)已知一定温度下按照起始比
 =2,在一密闭容器中进行反应③,保持总压为4MPa不变,达平衡时CO的平衡转化率为50%,则该条件下用平衡体系中各气体分压表示的平衡常数Kp=
=2,在一密闭容器中进行反应③,保持总压为4MPa不变,达平衡时CO的平衡转化率为50%,则该条件下用平衡体系中各气体分压表示的平衡常数Kp=
您最近一年使用:0次



