名校
解题方法
1 . 有一瓶澄清的无色溶液,其中可能含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 。取该溶液进行以下实验:
。取该溶液进行以下实验:
(1)由题干可知溶液中一定不存在___________ (填离子符号,下同);用pH试纸检验,溶液呈强酸性,可以排除___________ 的存在。
(2)取出部分溶液滴加过量的NaOH溶液,只产生白色沉淀,则可证明___________ (填离子符号)的存在,生成白色沉淀的离子方程式为___________ 。
(3)取出部分上述碱性溶液滴加Na2SO4溶液,有白色沉淀生成,证明___________ (填离子符号,下同)的存在,同时可排除原溶液中___________ 的存在,产生白色沉淀的离子方程式为___________ 。
(4)根据上述实验事实可知原溶液中一定存在的离子有___________ ,不确定是否存在的离子有___________ 。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 。取该溶液进行以下实验:
。取该溶液进行以下实验:(1)由题干可知溶液中一定不存在
(2)取出部分溶液滴加过量的NaOH溶液,只产生白色沉淀,则可证明
(3)取出部分上述碱性溶液滴加Na2SO4溶液,有白色沉淀生成,证明
(4)根据上述实验事实可知原溶液中一定存在的离子有
您最近一年使用:0次
2023-11-02更新
|
356次组卷
|
3卷引用:吉林省四平市普通高中2023-2024学年高一上学期期中教学质量检测化学试题
2019高三·全国·专题练习
名校
解题方法
2 . 下列实验操作正确的是
| 选项 | 实验 | 操作 |
| A | 观察钠与水反应的现象 | 用镊子从煤油中取出金属钠,切下绿豆大小的钠,小心放入装满水的烧杯中 |
| B | 检验 与 与 溶液 溶液 | 用小试管分别取少量溶液,然后滴加澄清石灰水 |
| C | 证明 与 与 是放热反应 是放热反应 |  用棉花包裹,放入充满 用棉花包裹,放入充满 的集气瓶中,棉花燃烧说明是放热反应 的集气瓶中,棉花燃烧说明是放热反应 |
| D | 检验 与 与 溶液 溶液 | 用铂丝分别蘸取溶液,在酒精灯外焰上灼烧,直接观察火焰的颜色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-07-02更新
|
2563次组卷
|
61卷引用:吉林省四平市双辽市第二中学2019-2020学年高一上学期期末考试化学试题
吉林省四平市双辽市第二中学2019-2020学年高一上学期期末考试化学试题(已下线)2019高考备考一轮复习精品资料 第三章 金属及其化合物 第1讲 钠及其氧化物【押题专练】【全国百强校】宁夏回族自治区银川一中2018-2019学年高一上学期12月阶段性测试化学试题(已下线)2019高考热点题型和提分秘籍 第三章 金属及其化合物 第1讲 钠及化合物 (题型专练)河南省新乡市延津县高级中学2018-2019学年高一元月月考化学试题陕西省吴起高级中学2019届高三上学期期中考试化学试题【校级联考】福建省莆田四中、莆田六中2018-2019学年高一上学期期末联考化学试题黑龙江省大庆实验中学2019-2020学年高一11月月考化学试题黑龙江省宾县一中2019-2020学年高一上学期第三次月考化学试题吉林省长春市田家炳实验中学2019-2020学年高一上学期期末考试化学试题山西省怀仁市重点中学2019-2020学年高一上学期期末考试化学试题(已下线)2020年高考化学押题预测卷02(新课标Ⅲ卷)--《2020年高考押题预测卷》(已下线)第10讲 钠及其重要化合物(精练)——2021年高考化学一轮复习讲练测河南省郑州外国语中学2019-2020学年高一上学期12月月考化学试题(已下线)第02章 海水中的重要元素——钠和氯(A卷基础强化篇)——2020-2021学年高一化学必修第一册同步单元AB卷(新教材人教版)(已下线)第三章 能力提升检测卷(测)——2021年高考化学一轮复习讲练测苏教版(2020)高一必修第一册专题3第二单元课时2 钠的化合物人教版(2019)高一必修第一册 第二章 第一节课时2 钠的几种化合物辽宁省东北育才学校科学高中部2020-2021学年高一上学期第一学段检测化学试题内蒙古自治区乌兰察布市集宁一中(西校区)2021届高三上学期期中考试化学试题黑龙江省大庆市让胡路区大庆中学2020-2021学年高一上学期期中考试化学试题重庆市第二十九中学2020-2021学年高一上学期半期测试化学试题河北省唐县第一中学2020-2021学年高一上学期第三次(12月)月考化学试题河北省安平中学2020-2021学年高一上学期12月月考化学试题广东省台山市华侨中学2020-2021学年高一上学期期中考试化学试题(已下线)专题08 常见无机物及其应用——备战2021年高考化学纠错笔记新疆巴音郭楞蒙古自治州第二中学2021届高三上学期第一次摸底考试化学试题河北省石家庄市第二十四中学2020-2021学年高二第二学期期中考试化学试题(已下线)专题06 钠及其化合物(热点讲义)-2022届高考化学一轮复习热点题型归纳与变式训练(已下线)专题三 能力提升检测卷 (测) — 2022年高考化学一轮复习讲练测(新教材新高考)第2章第一节第3课时碳酸钠和碳酸氢钠(课后)——课前、课中、课后同步专题精编(人教版2019必修第一册)广东省普宁二中实验学校2021-2022学年高三上学期第一次月考化学试题山西省太原市第五中学2021-2022学年高一上学期10月月考化学试题安徽省滁州市定远县民族中学2021-2022学年高一上学期第一次月考化学试题重庆市育才中学校2021-2022学年高一上学期期中考试化学试题 广东省肇庆市实验中学2021-2022学年高一上学期期中考试化学试题重庆复旦中学2021-2022学年高一上学期期中考试化学试题(已下线)专题05 化学基础实验—2022年高考化学二轮复习讲练测(全国版)-测试浙江省当湖高级中学2021-2022学年高一上学期12月阶段性测试化学试题山西省太原师院附属中学、师苑中学2020-2021学年高一下学期期末考试化学试题(已下线)第07讲 钠及其氧化物-【帮课堂】2022-2023学年高一化学同步精品讲义(人教2019必修第一册 )广东省揭阳华侨高级中学2021-2022学年高一上学期期中考试化学试题黑龙江省牡丹江市第三高级中学2022-2023学年高三上学期第一次月考化学试题河北省邯郸市魏县旭日中学2021-2022学年高一上学期期中考试化学试题山西省稷山县稷山中学2020-201学年高一上学期期末考试化学试题陕西省黄陵中学2021-2022学年高三上学期期中考试化学试题(已下线)易错点05 钠及其化合物-备战2023年高考化学考试易错题天津市五十五中学2022-2023学年高一上学期期中学期调研化学试题广东省广州市第五中学2022-2023学年高一上学期段考试化学试题广东省广州市第五中学2022-2023学年高一上学期期中考试化学试题安徽省亳州市第二完全中学2022-2023学年高一上学期期中教学质量检测化学试题河南省鹤壁市浚县第一中学2022-2023学年高一上学期10月考试化学试题重庆市江津第五中学校2022-2023学年高一上学期半期考试化学试题重庆市育才中学2021-2022学年高一上学期期中考试化学试题广东省广州市西关外国语中学2022-2023学年高一上学期期中考试化学试题河北省张家口市2023-2024学年高一上学期期中考试化学试题安徽省肥东县综合高中2022-2023学年高一上学期11月期中化学试题新疆吐鲁番市2023-2024学年高一上学期期中考试化学试题河北省石家庄市第二十四中学2023-2024学年高一上学期期中考试化学试题河北省衡水市安平中学2023-2024学年高一下学期开学考试化学试题内蒙古呼伦贝尔市满洲里远方中学2023-2024学年高一上学期期末考试化学试题
9-10高一下·山东滨州·期末
名校
解题方法
3 . 下列事实中能证明甲烷分子是以碳原子为中心的正四面体结构而不是平面四边形结构的是
| A.CH3Cl只代表一种物质 | B.CH2Cl2只代表一种物质 |
| C.CHCl3只代表一种物质 | D.CCl4只代表一种物质 |
您最近一年使用:0次
2021-09-05更新
|
1432次组卷
|
20卷引用:吉林省公主岭市范家屯镇第一中学2019-2020学年高二上学期第二次月考化学试题
吉林省公主岭市范家屯镇第一中学2019-2020学年高二上学期第二次月考化学试题(已下线)2010年山东省阳信一中高一第二学期期末考试化学试题2015-2016学年黑龙江省大兴安岭实验中学高二上学期期末化学试卷2015-2016学年河北省邯郸市临漳一中高二下第一次月考化学试卷2015-2016学年吉林省汪清六中高一下学期期末化学试卷【全国百强校】西藏日喀则市第一高级中学2017-2018学年高二下学期期中考试化学试题上海第二工业大学附属龚路中学2018-2019学年高二下学期期中考试化学试题天津市南开中学人教版高中化学选修5预习练习:第一章 第二节 有机化合物的结构特点 第2课时西藏自治区山南市第二高级中学2019-2020学年高二下学期月考化学试题陕西省澄城县城关中学2019-2020学年高一下学期第三次月考化学试题(人教版2019)必修第二册 第七章 有机化合物 第一节 认识有机化合物上海市第二工业大学附属龚路中学2020-2021学年高二下学期期中考试化学试题广东省揭阳市华侨高级中学2020-2021学年高二下学期第一次段考化学试题(已下线)课时46 甲烷、乙烯和苯-2022年高考化学一轮复习小题多维练(全国通用)(已下线)第15讲 认识有机化合物(上)(word讲义)-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)上海市复兴高级中学2022-2023学年高二上学期有机测试化学试题上海市高桥中学2022-2023 学年高二上学期期末等级考试化学试题天津市第七中学2022-2023学年高一下学期期中考试化学试题天津市和平区第五十五中学2022-2023学年高一下学期期中化学试试题上海市洋泾中学2023学年高二上学期10月质量检测化学试题
4 . 下列实验能证明某溶液中不含有铵根离子的是
| A.向溶液中加入石蕊溶液后,溶液呈红色 |
| B.向溶液中加入酚酞溶液后,溶液呈红色 |
| C.将溶液在试管中加热至沸腾,试管口放置的红色石蕊试纸不变色 |
| D.将溶液中加入过量烧碱溶液加热至沸腾,试管口放置的红色石蕊试纸不变色 |
您最近一年使用:0次
2021-05-07更新
|
52次组卷
|
2卷引用:吉林省公主岭市第三中学校2021-2022学年高一下学期第一次月考化学试题
10-11高一上·吉林长春·期末
名校
5 . 能证明硅酸的酸性弱于碳酸酸性的实验事实是( )
| A.CO2溶于水形成碳酸,SiO2难溶于水 |
| B.CO2通入可溶性硅酸盐中析出硅酸沉淀 |
| C.高温下SiO2与碳酸盐反应生成CO2 |
| D.氯化氢通入可溶性碳酸盐溶液中放出气体,通入可溶性硅酸盐溶液中生成沉淀 |
您最近一年使用:0次
2020-10-19更新
|
447次组卷
|
29卷引用:2016-2017学年吉林省四平实验中学高一上月考二化学卷
2016-2017学年吉林省四平实验中学高一上月考二化学卷(已下线)2010年长春外国语学校高一第一学期期末考试化学试卷(已下线)2011-2012学年安徽省六安三中高一下学期期末考试化学A卷(已下线)2013-2014学年江苏省南京市高淳区高一上学期期末考试化学试卷(已下线)2013-2014江苏省教育学院附属高中高一期末模拟化学试卷2014-2015黑龙江省绥化市三校高一上学期期末联考化学试卷2016-2017学年宁夏吴忠中学高二上学期开学考试化学试卷2016-2017学年黑龙江省鸡西市第十九中学高一上学期期末考试化学试卷浙江省磐安县第二中学2017-2018学年高一12月月考化学试题甘肃省武威第二中学2017-2018学年高一上学期期末考试化学试题广西陆川县中学2017-2018学年高一下学期开学考试化学试题内蒙古北京八中乌兰察布分校2017-2018学年高一上学期期末考试化学试题2017-2018学年人教新版高一化学必修一第四章第一节基础题【全国校级联考】辽宁省葫芦岛市普通高中2017-2018学年高一教学质量监测(期末)化学试题广西壮族自治区贺州市平桂区平桂高级中学2019届高三摸底考试化学试题甘肃省武威市第五中学2018-2019学年高一上学期期末考试化学试题云南省玉溪一中2018-2019学年高一上学期期末考试化学试题(已下线)2019年8月8日《每日一题》2020年高考一轮复习—— 碳的化合物的性质河南省周口市扶沟县包屯高级中学2019---2020学年高一上期期末考试化学试题新疆阿克苏市实验中学2019-2020学年高一上学期期末考试化学试题陕西省西安市第一中学2018-2019学年高一上学期期末考试化学试题河北省石家庄市辛集市第一中学2020-2021学年高二上学期第一次考试化学试题宁夏海原第一中学2021届高三上学期第二次月考化学试题重庆市云阳江口中学校2021届高三上学期第三次月考化学试题福建省莆田第二中学2019~2020学年高一下学期4月线上月考化学试题(已下线)第09讲 无机非金属材料 (练) — 2022年高考化学一轮复习讲练测(新教材新高考)湖南省浏阳市第一中学2016-2017学年高一下学期入学考试化学试卷陕西省西安市建筑科技大学附属中学2021-2022学年高一上学期期末考试化学试题海南省琼海市嘉积中学2023-2024学年高一下学期第一次月考化学试题A卷
名校
解题方法
6 . 可以证明可逆反应N2+3H2 2NH3已达到平衡状态的是
2NH3已达到平衡状态的是
①一个N≡N断裂的同时,有3个H—H键断裂
②一个N≡N键断裂的同时,有6个N—H键断裂
③其它条件不变时,混合气体平均相对分子质量不再改变
④恒温恒容时,体系压强不再改变
⑤NH3、N2、H2的体积分数都不再改变
⑥恒温恒容时,混合气体的密度保持不变
⑦正反应速率v(H2)=0.6mol/(L·min),逆反应速率v(NH3)=0.4mol/(L·min)
 2NH3已达到平衡状态的是
2NH3已达到平衡状态的是①一个N≡N断裂的同时,有3个H—H键断裂
②一个N≡N键断裂的同时,有6个N—H键断裂
③其它条件不变时,混合气体平均相对分子质量不再改变
④恒温恒容时,体系压强不再改变
⑤NH3、N2、H2的体积分数都不再改变
⑥恒温恒容时,混合气体的密度保持不变
⑦正反应速率v(H2)=0.6mol/(L·min),逆反应速率v(NH3)=0.4mol/(L·min)
| A.全部 | B.①③④⑤ | C.②③④⑤⑦ | D.③⑤⑥⑦ |
您最近一年使用:0次
2020-04-27更新
|
300次组卷
|
15卷引用:吉林公主岭范家屯一中2020-2021学年高二上学期期中考试化学试题
吉林公主岭范家屯一中2020-2021学年高二上学期期中考试化学试题2016届陕西省西安铁一中高三上12月模拟化学试卷2017届湖南师大附中高三上月考四化学试卷江西省景德镇市第一中学2016-2017学年高一(16班)下学期期中考试化学试题湖南省长沙市长郡中学2017-2018学年度高二第一学期期末考试化学试题四川成都外国语学校2017-2018学年高二下学期入学考化学试题【全国市级联考】广西贵港市2017-2018学年高二下学期期中教学质量监测化学试题【全国百强校】吉林省实验中学2018-2019学年高二上学期期中考试化学试题河南省安阳市第二中学2018-2019学年高二上学期期中考试化学试题湖南省雅礼中学2019-2020学年高二上学期第一次月考化学试题湖北省荆州市2018-2019学年高二下学期质量检查化学试题山西省运城市景胜中学2020-2021学年高二9月月考化学试题江西省丰城市第九中学2020届高三上学期期中考试化学试题宁夏回族自治区青铜峡市高级中学2020-2021学年高二上学期第一次月考化学试题四川省内江市威远中学校2021-2022学年高二下学期第一次月考化学试题
7 . FeBr2是一种黄绿色固体,某学习小组制备并探究它的还原性
Ⅰ.实验室制备FeBr2
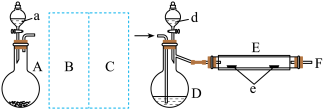
实验室用下图所示装置制取溴化亚铁.其中A为CO2发生装置,D和d中均盛有液溴,E为外套电炉丝的不锈钢管,e是两个耐高温的瓷皿,其中盛有细铁粉。
实验开始时先将铁粉加热至600℃~700℃,然后将干燥、纯净的CO2气流通入D中,E管中反应开始,不断将d中液溴滴入100℃~120℃的D中,经过几小时的连续反应,在铁管的一端沉积有黄绿色鳞片状溴化亚铁。
请回答:
(1)若在A中盛固体CaCO3,a中盛6mol/L盐酸,B处是装有饱和NaHCO3溶液的洗气瓶为使导入D中的CO2为干燥纯净的气体,则图中C处的装置和其中的试剂应是:________ ,为防止污染空气,实验时应在F处连接盛________ 的尾气吸收装置。
(2)反应过程中要不断通入CO2,其主要作用有两个:①是利用CO2把反应器中空气赶尽;②是________ .
Ⅱ.探究FeBr2的还原性
(1)实验需要90 mL 0.1 mol·L-1FeBr2溶液,配制FeBr2溶液除烧杯、量筒、胶头滴管、玻璃棒外还需的玻璃仪器是________ 。
(2)取10mL上述FeBr2溶液,向其中滴加少量新制的氯水,振荡后溶液呈黄色。某同学对产生黄色的原因提出了假设:
假设1:Br- 被Cl2氧化成Br2溶解在溶液中;
假设2:Fe2+ 被Cl2氧化成Fe3+。
设计实验证明假设2是正确的_______________________________
(3)实验证明:还原性Fe2+ > Br-请用一个离子方程式来证明:_____________ ;
(4)若在40mL上述FeBr2溶液中通入3×10-3molCl2,则反应的离子方程式为:____________ 。
Ⅰ.实验室制备FeBr2
实验室用下图所示装置制取溴化亚铁.其中A为CO2发生装置,D和d中均盛有液溴,E为外套电炉丝的不锈钢管,e是两个耐高温的瓷皿,其中盛有细铁粉。
实验开始时先将铁粉加热至600℃~700℃,然后将干燥、纯净的CO2气流通入D中,E管中反应开始,不断将d中液溴滴入100℃~120℃的D中,经过几小时的连续反应,在铁管的一端沉积有黄绿色鳞片状溴化亚铁。

请回答:
(1)若在A中盛固体CaCO3,a中盛6mol/L盐酸,B处是装有饱和NaHCO3溶液的洗气瓶为使导入D中的CO2为干燥纯净的气体,则图中C处的装置和其中的试剂应是:
(2)反应过程中要不断通入CO2,其主要作用有两个:①是利用CO2把反应器中空气赶尽;②是
Ⅱ.探究FeBr2的还原性
(1)实验需要90 mL 0.1 mol·L-1FeBr2溶液,配制FeBr2溶液除烧杯、量筒、胶头滴管、玻璃棒外还需的玻璃仪器是
(2)取10mL上述FeBr2溶液,向其中滴加少量新制的氯水,振荡后溶液呈黄色。某同学对产生黄色的原因提出了假设:
假设1:Br- 被Cl2氧化成Br2溶解在溶液中;
假设2:Fe2+ 被Cl2氧化成Fe3+。
设计实验证明假设2是正确的
(3)实验证明:还原性Fe2+ > Br-请用一个离子方程式来证明:
(4)若在40mL上述FeBr2溶液中通入3×10-3molCl2,则反应的离子方程式为:
您最近一年使用:0次
2019-10-08更新
|
147次组卷
|
3卷引用:吉林省公主岭市范家屯镇第一中学2020届高三上学期第二次月考化学试题
名校
8 . 下列设计的实验方案能达到相应实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 证明反应速率会随反应物浓度的增大而加快 | 用3mL稀硫酸与足量纯锌反应,产生气泡速率较慢,然后加入1mL 1mol·L−1CuSO4溶液,迅速产生较多气泡 |
| B | 检验Fe(NO3)2晶体是否已氧化变质 | 将Fe(NO3)2样品溶于稀硝酸后,滴加KSCN溶液,观察溶液是否变红 |
| C | 证明“84”消毒液的氧化能力随溶液pH的减小而增强 | 将“84”消毒液(含NaClO)滴入品红溶液中,褪色缓慢,若同时加入食醋,红色很快褪为无色 |
| D | 证明氯化银的溶解度大于硫化银的溶解度 | 向2mL 0.1mol·L−1硝酸银溶液中加入1mL 0.1 mol·L−1 NaCl溶液,出现白色沉淀,再加入几滴0.1mol·L−1的Na2S溶液,有黑色沉淀生成 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2019-03-18更新
|
1322次组卷
|
6卷引用:吉林省四平四中2019届高三下学期第二次模拟考试化学试题
9 . 某同学欲探究Na2O2与水的反应,可供使用的试剂有:Na2O2、蒸馏水、KMnO4酸性溶液、MnO2。该同学取4 g Na2O2样品与过量水反应,待完全反应后,得100 mL溶液X和448 mL O2(已折算为标准状况)。该同学推测反应中可能生成了H2O2,并进行实验探究。
⑴试设计实验证明溶液X中含过氧化氢_________________ 。
⑵通过上述实验证明溶液中确实存在H2O2。取少量X于试管中,滴加几滴酚酞试液,实验现象为___________ 。
⑶取少量X于试管中,滴加FeCl2溶液,立即生成红褐色沉淀,则该反应的离子方程式为___________ 。
⑷已知溶液X可使酸性KMnO4溶液褪色,同时放出氧气,完成并配平该反应的离子方程式:____
 ________MnO4-+ ________H2O2 + ________H+ — ________Mn2+ + ________O2↑ + __________。
________MnO4-+ ________H2O2 + ________H+ — ________Mn2+ + ________O2↑ + __________。
取100 mL 溶液X,使其与过量酸性KMnO4溶液反应,最终生成224 mL O2(已折算为标准状况),则此样品中Na2O2的质量分数是___________ 。
⑴试设计实验证明溶液X中含过氧化氢
⑵通过上述实验证明溶液中确实存在H2O2。取少量X于试管中,滴加几滴酚酞试液,实验现象为
⑶取少量X于试管中,滴加FeCl2溶液,立即生成红褐色沉淀,则该反应的离子方程式为
⑷已知溶液X可使酸性KMnO4溶液褪色,同时放出氧气,完成并配平该反应的离子方程式:
 ________MnO4-+ ________H2O2 + ________H+ — ________Mn2+ + ________O2↑ + __________。
________MnO4-+ ________H2O2 + ________H+ — ________Mn2+ + ________O2↑ + __________。取100 mL 溶液X,使其与过量酸性KMnO4溶液反应,最终生成224 mL O2(已折算为标准状况),则此样品中Na2O2的质量分数是
您最近一年使用:0次
名校
解题方法
10 . 下列有关说法不正确的是
| A.硫酸钡在医疗上可被用作消化系统X射线检查的内服药剂 |
| B.浓硫酸具有吸水性,故能使蔗糖炭化 |
| C.二氧化硫可用于杀菌消毒,还是一种食品添加剂 |
| D.液氨汽化时要吸收大量的热,因此液氨可用作制冷剂 |
您最近一年使用:0次
2024-05-07更新
|
67次组卷
|
2卷引用:吉林省四平市第一高级中学2023-2024学年高一下学期第一次月考化学试题



