名校
1 . 下列符号表征或说法正确的是
A.HClO的电子式: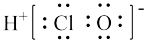 |
B. 的VSEPR模型: 的VSEPR模型: |
C. 的离子结构示意图: 的离子结构示意图: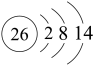 |
D.基态S原子的价电子排布图: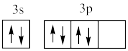 |
您最近一年使用:0次
2024-06-08更新
|
298次组卷
|
3卷引用:江西省赣州市2023-2024学年高三下学期5月二模考试化学试题
江西省赣州市2023-2024学年高三下学期5月二模考试化学试题(已下线)江苏省苏州市2023-2024学年高三下学期第三次模拟考试化学试题辽宁省沈阳市第二中学2023-2024学年高三下学期第五次模拟考试化学试卷
2 . 为了降低能耗,选择硝酸根作为电催法合成氨的原料,离子方程式为: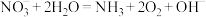 。下列说法正确的是
。下列说法正确的是
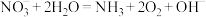 。下列说法正确的是
。下列说法正确的是A. 的VSEPR模型和空间结构一致 的VSEPR模型和空间结构一致 |
B. 分子之间氢键 分子之间氢键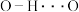 的键角约为109° 的键角约为109° |
C. 和 和 分子均含有非极性共价键 分子均含有非极性共价键 |
D. 的电子式为 的电子式为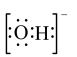 |
您最近一年使用:0次
3 . 研究低碳铬钢分别在不同温度下、不同硫酸浓度下的腐蚀情况,如下图所示,有关说法正确的是
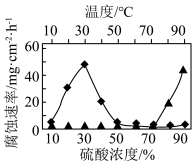
| A.约30℃时,低碳铬钢腐蚀严重 | B.30%硫酸,大量发生吸氧腐蚀 |
C.硫酸浓度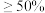 ,低碳铬钢钝化 ,低碳铬钢钝化 | D.超过70℃后,实验中有 生成 生成 |
您最近一年使用:0次
名校
解题方法
4 . 利用可再生能源驱动耦合电催化HCHO氧化与CO2还原,同步实现CO2与HCHO高效转化为高附加值的化学产品,可有效消除酸性工业废水中的甲醛,减少碳排放,实现碳中和。耦合电催化反应系统原理如图所示。

A.电源a极为正极, 通过质子交换膜从右侧移向左侧 通过质子交换膜从右侧移向左侧 |
B.阳极的电极反应式为: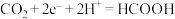 |
C.外电路转移 时,理论上可消除废水中0.5molHCHO 时,理论上可消除废水中0.5molHCHO |
D.电解生成1molHCOOH,理论上可消耗标准状况下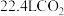 |
您最近一年使用:0次
2024-06-04更新
|
186次组卷
|
2卷引用:江西省赣州市2023-2024学年高三下学期5月二模考试化学试题
5 . 纳米 是新型能源材料,高温时合成反应为:
是新型能源材料,高温时合成反应为: 。阿伏加德罗常数的值为
。阿伏加德罗常数的值为 ,下列说法正确的是
,下列说法正确的是
 是新型能源材料,高温时合成反应为:
是新型能源材料,高温时合成反应为: 。阿伏加德罗常数的值为
。阿伏加德罗常数的值为 ,下列说法正确的是
,下列说法正确的是A. 氮气完全反应,该反应中转移的电子数为 氮气完全反应,该反应中转移的电子数为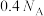 |
B.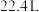  含有的共价键数为 含有的共价键数为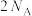 |
C.  含有的中子数为 含有的中子数为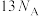 |
D.  中含有的离子数为 中含有的离子数为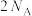 |
您最近一年使用:0次
6 . 下列离子方程式正确的是
| 选项 | 尾气处理 | 离子方程式 |
| A | 用 溶液吸收 溶液吸收 |  |
| B | 用 溶液吸收 溶液吸收 |  |
| C | 用 溶液吸收 溶液吸收 |  |
| D | 用 悬浊液吸收 悬浊液吸收 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . HfNbTaTiZr系的难熔高熵合金涂层,赋予材料更出色的弹性、塑性、断裂韧性等,下列有关说法正确的是
| A.该涂层为无机非金属材料 | B.该涂层为有机高分子材料 |
| C.该涂层为功能复合材料 | D.该涂层为金属材料 |
您最近一年使用:0次
解题方法
8 . 二甘氨酸合锌是常用的补锌药品,化学式为 ,针状白色晶体,可溶于水。制备过程如下:
,针状白色晶体,可溶于水。制备过程如下:
I.称取3.00 g 固体溶于25 mL水,滴加氨水产生大量白色沉淀,过滤,洗涤。
固体溶于25 mL水,滴加氨水产生大量白色沉淀,过滤,洗涤。
II.称取1.50 g甘氨酸,溶于40 mL水形成甘氨酸溶液,搅拌下用甘氨酸溶液溶解I中的白色沉淀。
III.过滤,转移液体于烧杯中。经一系列操作后,过滤、洗涤、干燥,得到针状白色晶体1.92 g。
请回答下列问题:
(1)①步骤I中所使用的玻璃仪器除烧杯、量筒外,还有___________ 。
②步骤I中若氨水过量较多、浓度较大,产率会明显降低,原因是___________ 。
③步骤I中洗涤除去的离子是___________ 。
(2)步骤II中发生的化学方程式为___________ 。
(3)步骤III中“一系列操作”是指___________ 、___________ 。
(4)产率为___________ 。
(5)直接法制备二甘氨酸合锌的方法是:用硫酸锌与甘氨酸直接反应,经实验步骤III得到晶体。本实验方法与直接法相比较,优点与缺点分别为___________ 、___________ 。
 ,针状白色晶体,可溶于水。制备过程如下:
,针状白色晶体,可溶于水。制备过程如下:I.称取3.00 g
 固体溶于25 mL水,滴加氨水产生大量白色沉淀,过滤,洗涤。
固体溶于25 mL水,滴加氨水产生大量白色沉淀,过滤,洗涤。II.称取1.50 g甘氨酸,溶于40 mL水形成甘氨酸溶液,搅拌下用甘氨酸溶液溶解I中的白色沉淀。
III.过滤,转移液体于烧杯中。经一系列操作后,过滤、洗涤、干燥,得到针状白色晶体1.92 g。
请回答下列问题:
(1)①步骤I中所使用的玻璃仪器除烧杯、量筒外,还有
②步骤I中若氨水过量较多、浓度较大,产率会明显降低,原因是
③步骤I中洗涤除去的离子是
(2)步骤II中发生的化学方程式为
(3)步骤III中“一系列操作”是指
(4)产率为
(5)直接法制备二甘氨酸合锌的方法是:用硫酸锌与甘氨酸直接反应,经实验步骤III得到晶体。本实验方法与直接法相比较,优点与缺点分别为
您最近一年使用:0次
解题方法
9 . 江西富含稀有金属铝,钼具有优异的物理化学性能,在冶金、农业、环保和航天等领域有着广泛应用。工业上以钼精矿(主要成分为 ,杂质有
,杂质有 、
、 、
、 和
和 等元素)制备四钼酸铵的流程如下:
等元素)制备四钼酸铵的流程如下:
(1)气体A化学式为___________ ,气体B的分子空间构型是___________ ,基态氧原子的最外层轨道表示式为___________ 。
(2)碱浸时把 转化成
转化成 ,其离子方程式为
,其离子方程式为___________ 。
(3)工业上探究了碱浸中钼浸出率与蒸发温度的关系,如下图所示:___________ 。
②80℃以后,蒸发温度上升,钼浸出率迅速下降,主要原因为___________ 。
(4)碱浸后的滤液中仍然有部分铜、锌和低价钼金属存在,净化时依次加入适量 、
、 溶液,其作用分别是
溶液,其作用分别是___________ 、___________ 。
(5)酸沉时主要发生的离子方程式为___________ 。
 ,杂质有
,杂质有 、
、 、
、 和
和 等元素)制备四钼酸铵的流程如下:
等元素)制备四钼酸铵的流程如下:
(1)气体A化学式为
(2)碱浸时把
 转化成
转化成 ,其离子方程式为
,其离子方程式为(3)工业上探究了碱浸中钼浸出率与蒸发温度的关系,如下图所示:

②80℃以后,蒸发温度上升,钼浸出率迅速下降,主要原因为
(4)碱浸后的滤液中仍然有部分铜、锌和低价钼金属存在,净化时依次加入适量
 、
、 溶液,其作用分别是
溶液,其作用分别是(5)酸沉时主要发生的离子方程式为
您最近一年使用:0次
10 . 水系锌离子可充电电池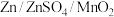 ,电解质中含有少量
,电解质中含有少量 。放电时总反应为:
。放电时总反应为: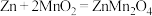 。下列说法正确的是
。下列说法正确的是
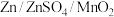 ,电解质中含有少量
,电解质中含有少量 。放电时总反应为:
。放电时总反应为: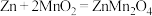 。下列说法正确的是
。下列说法正确的是| A.充、放电时锌离子浓度减小或增大 |
B. 可以抑制正极材料溶解 可以抑制正极材料溶解 |
C.放电时,正极反应: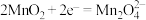 |
| D.充电时,锌离子移向电池的正极 |
您最近一年使用:0次



