解题方法
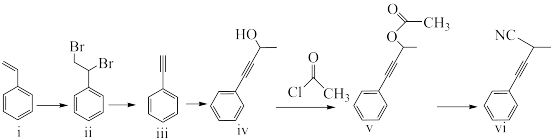
1 . 不对称合成在有机合成中有重要意义,某科研小组利用该技术制备得到化合物vi,其合成路线如下:
(1)化合物i的名称为______ 。化合物iv→v的反应类型为______ 。
(2)①化合物iii与 发生加成反应生成iv,
发生加成反应生成iv, 的结构简式为
的结构简式为______ 。iv中所含官能团有______ (写名称)。
②化合物 是iv的同分异构体,且满足以下条件:a.与
是iv的同分异构体,且满足以下条件:a.与 溶液作用显色,b.只有苯环一种环状结构且苯环上只有2个取代基。符合题意的
溶液作用显色,b.只有苯环一种环状结构且苯环上只有2个取代基。符合题意的 的稳定结构有
的稳定结构有______ 种(不考虑立体异构),其中核磁共振氢谱有5组峰的结构简式为______ (写一种)。
(3)下列说法错误的是______(填字母)。
(4)以 和
和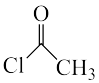 为起始原料,参考上述合成路线,其他无机试剂任选,合成
为起始原料,参考上述合成路线,其他无机试剂任选,合成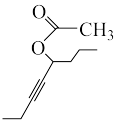
①写出最后一步的反应方程式:______ 。
②合成过程中,相关步骤涉及卤代烃制炔烃的反应,其化学方程式为______ (注明反应条件)。
(1)化合物i的名称为
(2)①化合物iii与
 发生加成反应生成iv,
发生加成反应生成iv, 的结构简式为
的结构简式为②化合物
 是iv的同分异构体,且满足以下条件:a.与
是iv的同分异构体,且满足以下条件:a.与 溶液作用显色,b.只有苯环一种环状结构且苯环上只有2个取代基。符合题意的
溶液作用显色,b.只有苯环一种环状结构且苯环上只有2个取代基。符合题意的 的稳定结构有
的稳定结构有(3)下列说法错误的是______(填字母)。
| A.化合物iv能与水形成氢键 |
B.化合物v→vi的反应有 键的断裂 键的断裂 |
C.化合物iii中,碳原子均采用 杂化 杂化 |
| D.化合物vi中不存在手性碳原子 |
(4)以
 和
和 为起始原料,参考上述合成路线,其他无机试剂任选,合成
为起始原料,参考上述合成路线,其他无机试剂任选,合成
①写出最后一步的反应方程式:
②合成过程中,相关步骤涉及卤代烃制炔烃的反应,其化学方程式为
您最近一年使用:0次
2 . 连二亚硫酸钠( )易溶于水,难溶于甲醇,在空气中极易被氧化,用于纺织业的还原性染色。甲酸钠法制备
)易溶于水,难溶于甲醇,在空气中极易被氧化,用于纺织业的还原性染色。甲酸钠法制备 的原理为
的原理为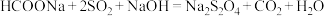 ,装置如图1.回答下列问题:
,装置如图1.回答下列问题:______ (填“ ”或“
”或“ ”),原因为
”),原因为______ 。
(2)装置丙的作用除了防倒吸还有______ 。
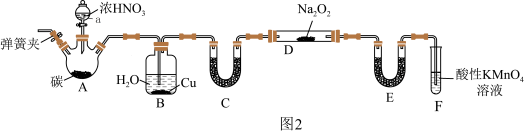
Ⅱ.亚硝酸钠( )是一种肉制品生产中常见的食品添加剂,使用时必须严格控制其用量:某兴趣小组设计了如图2所示的装置制备
)是一种肉制品生产中常见的食品添加剂,使用时必须严格控制其用量:某兴趣小组设计了如图2所示的装置制备 (A中加热装置已略去,
(A中加热装置已略去, 可与过氧化钠粉末发生化合反应,也能被酸性
可与过氧化钠粉末发生化合反应,也能被酸性 溶液氧化成
溶液氧化成 )。
)。
(3)为保证制得的亚硝酸钠的纯度,C装置中盛放的试剂可能是______(填字母)。
(4)F中发生反应的离子方程式为______ 。
(5)从提高氮原子利用率的角度出发,B装置设计存在一定缺陷,如何改进?______ 。
(6)已知: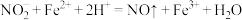 ;为测定得到产品中
;为测定得到产品中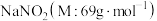 的纯度,采取如下实验步骤:准确称取质量为2.0g样品配成500mL溶液,取其中25mL于锥形瓶中,加入过量的
的纯度,采取如下实验步骤:准确称取质量为2.0g样品配成500mL溶液,取其中25mL于锥形瓶中,加入过量的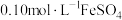 溶液20mL;然后滴加稀硫酸充分反应后,用
溶液20mL;然后滴加稀硫酸充分反应后,用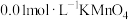 溶液滴定至终点,读数,重复以上操作4次,所消耗
溶液滴定至终点,读数,重复以上操作4次,所消耗 溶液的体积分别为20.02mL、20.00mL、19.98mL,21.25mL。
溶液的体积分别为20.02mL、20.00mL、19.98mL,21.25mL。
①所得样品中亚硝酸钠的质量分数为______ (填百分式,保留三位有效数字)。
②下列操作可能会导致测定结果偏高的是______ (填字母)
a.整个滴定操作过慢,用时过长
b.滴定前滴定管尖嘴部分有气泡,滴定后无气泡
c.读数时,滴定前俯视,滴定后仰视
d.滴定终点时未等30秒立即读数
 )易溶于水,难溶于甲醇,在空气中极易被氧化,用于纺织业的还原性染色。甲酸钠法制备
)易溶于水,难溶于甲醇,在空气中极易被氧化,用于纺织业的还原性染色。甲酸钠法制备 的原理为
的原理为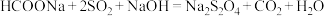 ,装置如图1.回答下列问题:
,装置如图1.回答下列问题: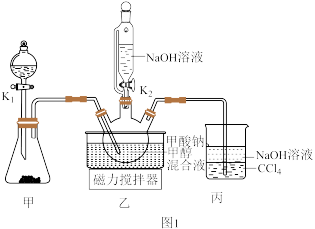
 ”或“
”或“ ”),原因为
”),原因为(2)装置丙的作用除了防倒吸还有
Ⅱ.亚硝酸钠(
 )是一种肉制品生产中常见的食品添加剂,使用时必须严格控制其用量:某兴趣小组设计了如图2所示的装置制备
)是一种肉制品生产中常见的食品添加剂,使用时必须严格控制其用量:某兴趣小组设计了如图2所示的装置制备 (A中加热装置已略去,
(A中加热装置已略去, 可与过氧化钠粉末发生化合反应,也能被酸性
可与过氧化钠粉末发生化合反应,也能被酸性 溶液氧化成
溶液氧化成 )。
)。(3)为保证制得的亚硝酸钠的纯度,C装置中盛放的试剂可能是______(填字母)。
| A.浓硫酸 | B. | C.无水 | D.碱石灰 |
(4)F中发生反应的离子方程式为
(5)从提高氮原子利用率的角度出发,B装置设计存在一定缺陷,如何改进?
(6)已知:
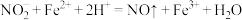 ;为测定得到产品中
;为测定得到产品中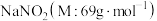 的纯度,采取如下实验步骤:准确称取质量为2.0g样品配成500mL溶液,取其中25mL于锥形瓶中,加入过量的
的纯度,采取如下实验步骤:准确称取质量为2.0g样品配成500mL溶液,取其中25mL于锥形瓶中,加入过量的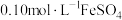 溶液20mL;然后滴加稀硫酸充分反应后,用
溶液20mL;然后滴加稀硫酸充分反应后,用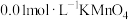 溶液滴定至终点,读数,重复以上操作4次,所消耗
溶液滴定至终点,读数,重复以上操作4次,所消耗 溶液的体积分别为20.02mL、20.00mL、19.98mL,21.25mL。
溶液的体积分别为20.02mL、20.00mL、19.98mL,21.25mL。①所得样品中亚硝酸钠的质量分数为
②下列操作可能会导致测定结果偏高的是
a.整个滴定操作过慢,用时过长
b.滴定前滴定管尖嘴部分有气泡,滴定后无气泡
c.读数时,滴定前俯视,滴定后仰视
d.滴定终点时未等30秒立即读数
您最近一年使用:0次
3 . 稀有重金属钽( )是新兴战略金属,广泛应用于航空航天、核工业及微电子技术领域。富钽矿(主要成分为
)是新兴战略金属,广泛应用于航空航天、核工业及微电子技术领域。富钽矿(主要成分为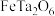 、含
、含 、
、 等氧化物)可用碱熔法制备
等氧化物)可用碱熔法制备 ,其工艺流程见下图:
,其工艺流程见下图: 难溶于水。
难溶于水。
(1)为加快“钠碱熔融”速率,可采取的措施是______ (任写一条)。
(2)已知“钠碱熔融”步骤中发生非氧化还原反应,产物为氧化物和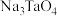 ,写出
,写出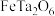 与
与 反应的化学方程式:
反应的化学方程式:______ 。
(3)“操作I”为______ ,富钽矿的杂质以______ (写化学式)形式存在于“残液”中。
(4)“盐酸洗”的目的是______ 。
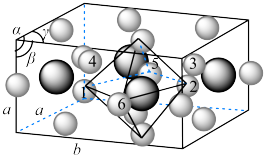
(5)已知 的晶胞结构如下图所示,晶胞参数分别为a nm、a nm、b nm;
的晶胞结构如下图所示,晶胞参数分别为a nm、a nm、b nm;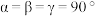 。
。
①电负性:
______  (填“<”或“>”),与
(填“<”或“>”),与 配位的氧原子有
配位的氧原子有______ 个。
②已知 的式量为
的式量为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,该晶胞的密度为
,该晶胞的密度为______  (列出算式)。
(列出算式)。
 )是新兴战略金属,广泛应用于航空航天、核工业及微电子技术领域。富钽矿(主要成分为
)是新兴战略金属,广泛应用于航空航天、核工业及微电子技术领域。富钽矿(主要成分为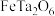 、含
、含 、
、 等氧化物)可用碱熔法制备
等氧化物)可用碱熔法制备 ,其工艺流程见下图:
,其工艺流程见下图: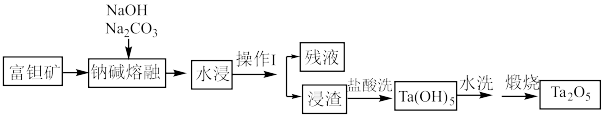
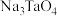 难溶于水。
难溶于水。(1)为加快“钠碱熔融”速率,可采取的措施是
(2)已知“钠碱熔融”步骤中发生非氧化还原反应,产物为氧化物和
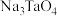 ,写出
,写出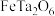 与
与 反应的化学方程式:
反应的化学方程式:(3)“操作I”为
(4)“盐酸洗”的目的是
(5)已知
 的晶胞结构如下图所示,晶胞参数分别为a nm、a nm、b nm;
的晶胞结构如下图所示,晶胞参数分别为a nm、a nm、b nm;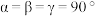 。
。
①电负性:

 (填“<”或“>”),与
(填“<”或“>”),与 配位的氧原子有
配位的氧原子有②已知
 的式量为
的式量为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,该晶胞的密度为
,该晶胞的密度为 (列出算式)。
(列出算式)。
您最近一年使用:0次
名校
解题方法
4 . 苯甲醛( )是有机制备中的一种重要原料。实验室常用苯甲醛与NaOH反应制备苯甲醇和苯甲酸钠:2
)是有机制备中的一种重要原料。实验室常用苯甲醛与NaOH反应制备苯甲醇和苯甲酸钠:2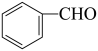 +NaOH→
+NaOH→ +
+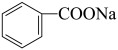 ,再将苯甲酸钠酸化得到苯甲酸。
,再将苯甲酸钠酸化得到苯甲酸。
| 名称 | 性质 | 熔点/℃ | 沸点/℃ | 溶解性 | ||
| 水 | 乙醇 | 乙醚 | ||||
| 苯甲醛 | 无色液体,具有苦杏仁味 | -26 | 178.1 | 微溶 | 混溶 | 混溶 |
| 苯甲酸 | 白色片状或针状晶体 | 122.4 | 248 | 微溶 | 易溶 | 易溶 |
| 苯甲醇 | 无色液体,具有芳香味 | -15.3 | 205.35 | 微溶 | 易溶 | 易溶 |
| 乙醚 | 无色透明液体,具有特殊刺激性气味 | -116.2 | 34.6 | 微溶 | 易溶 | — |
已知:a.RCHO+ ⇌
⇌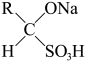 ;
;
实验步骤:

步骤②:搅拌、加热三颈烧瓶c,充分反应后,将c中液体冷却后倒入分液漏斗中,用乙醚萃取、分液,将乙醚层依次用25%亚硫酸氢钠溶液、水洗涤,水层保留待用。
步骤③:将乙醚层倒入盛少量无水MgSO4的锥形瓶中进行干燥,混匀、静置、过滤后采用一定的方法分离,收集苯甲醇。
步骤④:将步骤②中得到的水层和适量浓盐酸混合均匀,析出白色固体。冷却、抽滤得粗产品,将粗产品提纯得n g的苯甲酸。回答下列问题:
(1)步骤①中,冷凝管的作用是
(2)步骤②中,乙醚层用25%亚硫酸氢钠溶液洗涤的作用是
(3)步骤③中,分离出苯甲醇的方法是
(4)步骤④中,水层和浓盐酸混合后产生苯甲酸的离子方程式为
(5)苯甲酸的产率为
您最近一年使用:0次
昨日更新
|
90次组卷
|
3卷引用:江西省上饶市第二中学2024-2025学年高三上学期9月化学测试卷
名校
5 . “化学——我们的生活,我们的未来”,学习化学应该明白“从生活中来,到生活中去”的道理。请回答下列问题:
(1)在呼吸面具和潜水艇中可用过氧化钠作为供氧剂,请写出与水反应的化学方程式:_______ 。
(2)氯水和漂白粉都有漂白作用,也都可用于水体的杀菌消毒。
①工业上利用氯气和石灰乳(氢氧化钙)反应可制得漂白粉,其化学方程式为_______ 。
②下列收集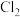 的正确装置是
的正确装置是_______ (填字母)。_______ 。与研究目的直接相关的实验现象是_______ 。该实验设计存在事故隐患,应在D处增加一装置,该装置中应加入 溶液以除去多余的氯气,该反应的化学方程式为
溶液以除去多余的氯气,该反应的化学方程式为_______ 。
④将2.3 g Na投入足量水中完全反应,生成气体的体积为_______ L(标准状况下)。若把Na投入盛有CuSO4 溶液的烧杯中,烧杯中会出现_______ (填沉淀颜色)沉淀。反应的化学方程式为_______ 。
(1)在呼吸面具和潜水艇中可用过氧化钠作为供氧剂,请写出与水反应的化学方程式:
(2)氯水和漂白粉都有漂白作用,也都可用于水体的杀菌消毒。
①工业上利用氯气和石灰乳(氢氧化钙)反应可制得漂白粉,其化学方程式为
②下列收集
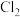 的正确装置是
的正确装置是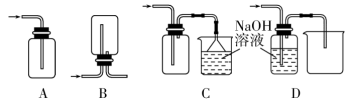
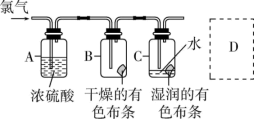
 溶液以除去多余的氯气,该反应的化学方程式为
溶液以除去多余的氯气,该反应的化学方程式为④将2.3 g Na投入足量水中完全反应,生成气体的体积为
您最近一年使用:0次
昨日更新
|
81次组卷
|
3卷引用:江西省上饶市私立世龙中学2024-2025学年高三上学期9月测试 化学试题
解题方法
6 . 如图为制备甲醇的微观过程。下列说法正确的是
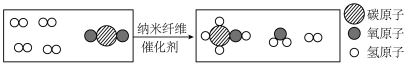
| A.该反应有利于减缓温室效应 |
| B.催化剂在化学反应前后质量和所有性质都保持不变 |
| C.该化学反应过程中,分子和原子的种类都发生了改变 |
D.参加反应的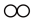 和 和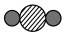 分子个数比为4:1 分子个数比为4:1 |
您最近一年使用:0次
昨日更新
|
40次组卷
|
2卷引用:江西省上饶市广丰五都中学2024-2025学年高三上学期9月第一次月考化学试题
解题方法
7 . 下列化学用语表示正确的是
A.中子数为8的碳原子: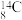 |
B.过氧化氢的电子式: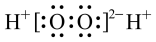 |
C. 的 的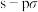 键电子云图: 键电子云图: |
D.基态 原子的价层电子轨道表示式: 原子的价层电子轨道表示式: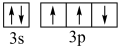 |
您最近一年使用:0次
8 . 电解硫酸钠溶液制取电池正极材料 的前驱体
的前驱体 ,其工作原理如图所示:
,其工作原理如图所示:
 的前驱体
的前驱体 ,其工作原理如图所示:
,其工作原理如图所示: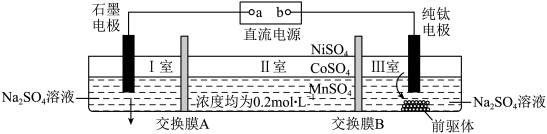
| A.a是直流电源的负极,石墨电极发生还原反应 |
B.交换膜A是阴离子交换膜,通电一段时间,I室 上升 上升 |
C.当产生 的 的 时,理论上纯钛电极上产生标准状况下 时,理论上纯钛电极上产生标准状况下 气体 气体 |
| D.若将纯钛电极直接放入Ⅱ室,则前驱体产率升高 |
您最近一年使用:0次
9 . LiBr易溶于水,溶解度随着温度降低明显减小,能溶于乙醇、丙酮等有机溶剂,可作为替代氟利昂的绿色制冷剂。一种用含溴蒸气的溴化氢气体合成LiBr的工艺流程如下(已知:Li2CO3微溶于水):
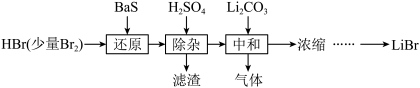
| A.结晶时,向溶液中加入丙酮不能促使产品析出 |
| B.“除杂”得到的滤渣中加CS2可以进行组分分离 |
| C.“中和”工序中的离子方程式为Li2CO3+2H+=2Li++CO2↑+H2O |
| D.“还原”工序逸出的Br2可用LiOH溶液吸收,吸收液直接返回浓缩工序 |
您最近一年使用:0次
10 .  是白色难溶于水的化合物,溶于较浓盐酸时生成
是白色难溶于水的化合物,溶于较浓盐酸时生成 。
。 可以定量吸收
可以定量吸收 ,也能吸收
,也能吸收 、
、 、
、 等气体,其吸收
等气体,其吸收 形成
形成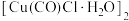 ,其结构为
,其结构为 ,下列说法正确的是
,下列说法正确的是
A.可用 的较浓盐酸溶液测定混合气体 的较浓盐酸溶液测定混合气体 、 、 和 和 中 中 的含量 的含量 |
B.由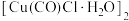 结构可知, 结构可知, 原子满足8电子稳定结构 原子满足8电子稳定结构 |
C.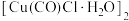 中 中 的化合价为+1价,配位数为3 的化合价为+1价,配位数为3 |
D.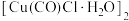 中只有 中只有 、 、 作配体 作配体 |
您最近一年使用:0次



