1 . 常温下向 饱和溶液(始终有
饱和溶液(始终有 固体存在)中滴加HCl溶液或者NaOH溶液调节pH,测得溶液中
固体存在)中滴加HCl溶液或者NaOH溶液调节pH,测得溶液中 浓度的对数lg(Ca)与溶液的pH之间的关系如下图。已知
浓度的对数lg(Ca)与溶液的pH之间的关系如下图。已知 的电离常数的负对数:
的电离常数的负对数: ,
, ;下列说法正确的是
;下列说法正确的是
 饱和溶液(始终有
饱和溶液(始终有 固体存在)中滴加HCl溶液或者NaOH溶液调节pH,测得溶液中
固体存在)中滴加HCl溶液或者NaOH溶液调节pH,测得溶液中 浓度的对数lg(Ca)与溶液的pH之间的关系如下图。已知
浓度的对数lg(Ca)与溶液的pH之间的关系如下图。已知 的电离常数的负对数:
的电离常数的负对数: ,
, ;下列说法正确的是
;下列说法正确的是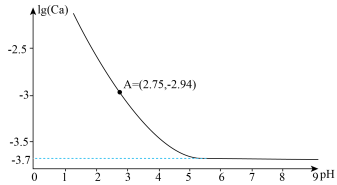
A.溶液中始终存在: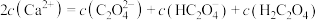 |
B.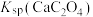 的数量级为 的数量级为 |
C.pH=7时,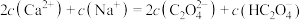 |
D.A点时,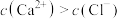 |
您最近一年使用:0次
2 . 根据实验事实能得出相应结论的是
A.在25℃和40℃测得0.1mol/L  溶液的pH分别为9.37和9.66。 溶液的pH分别为9.37和9.66。 的水解常数: 的水解常数: (40℃)> (40℃)> (25℃) (25℃) |
B. 在苯中的溶解度大于在水中。溶剂的极性:苯>水 在苯中的溶解度大于在水中。溶剂的极性:苯>水 |
C.将有机物X: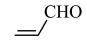 滴入溴水中,溶液褪色。可以检验X中的碳碳双键 滴入溴水中,溶液褪色。可以检验X中的碳碳双键 |
D.向溶液Y中滴加盐酸酸化的氯化钡溶液有白色沉淀生成。Y中一定含有 |
您最近一年使用:0次
3 . 丙醛是一种重要的有机原料,在许多领域都有广泛的应用。在铑催化剂作用下,乙烯羰基合成丙醛涉及的反应如下:
主反应Ⅰ.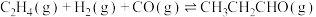

副反应Ⅱ.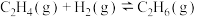

(1)
_____ 0 (填:“>”或“<)。
(2)保持温度不变,在恒容反应器中,按照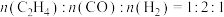 投料,发生反应Ⅰ和Ⅱ,初始压强为4p kPa,反应t min达到平衡,平衡时
投料,发生反应Ⅰ和Ⅱ,初始压强为4p kPa,反应t min达到平衡,平衡时 的转化率为80%,
的转化率为80%, 的选择性为25%,则
的选择性为25%,则 的转化率为
的转化率为______ %,
_____ kPa/min,反应Ⅰ的
_____  。(用含p的代数式表示,
。(用含p的代数式表示, 的选择性=
的选择性= )。
)。
(3)在装有相同催化剂的。相同恒压容器中,按照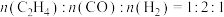 投料,发生反应Ⅰ和Ⅱ,相同时间内,测得不同温度下
投料,发生反应Ⅰ和Ⅱ,相同时间内,测得不同温度下 的转化率(
的转化率( )如图所示。则B、D两点的平均反应速率v(B)
)如图所示。则B、D两点的平均反应速率v(B)_____ v(D)(填“>”、“=”、“<”),产生这一结果的原因可能是______ 。
(4)T℃时,向恒温恒容的甲容器中,通入1mol 、1mol CO和2mol
、1mol CO和2mol  ;向绝热恒容的乙容器中通入1mol
;向绝热恒容的乙容器中通入1mol  、1mol CO、2mol
、1mol CO、2mol  ,若只发生上述反应Ⅰ。则甲乙容器中
,若只发生上述反应Ⅰ。则甲乙容器中 的平衡转化率
的平衡转化率
____  (填“>”、“<”或“=”),理由是
(填“>”、“<”或“=”),理由是_____ 。
主反应Ⅰ.
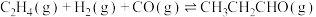

副反应Ⅱ.
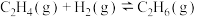


(1)

(2)保持温度不变,在恒容反应器中,按照
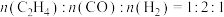 投料,发生反应Ⅰ和Ⅱ,初始压强为4p kPa,反应t min达到平衡,平衡时
投料,发生反应Ⅰ和Ⅱ,初始压强为4p kPa,反应t min达到平衡,平衡时 的转化率为80%,
的转化率为80%, 的选择性为25%,则
的选择性为25%,则 的转化率为
的转化率为

 。(用含p的代数式表示,
。(用含p的代数式表示, 的选择性=
的选择性= )。
)。(3)在装有相同催化剂的。相同恒压容器中,按照
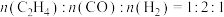 投料,发生反应Ⅰ和Ⅱ,相同时间内,测得不同温度下
投料,发生反应Ⅰ和Ⅱ,相同时间内,测得不同温度下 的转化率(
的转化率( )如图所示。则B、D两点的平均反应速率v(B)
)如图所示。则B、D两点的平均反应速率v(B)(4)T℃时,向恒温恒容的甲容器中,通入1mol
 、1mol CO和2mol
、1mol CO和2mol  ;向绝热恒容的乙容器中通入1mol
;向绝热恒容的乙容器中通入1mol  、1mol CO、2mol
、1mol CO、2mol  ,若只发生上述反应Ⅰ。则甲乙容器中
,若只发生上述反应Ⅰ。则甲乙容器中 的平衡转化率
的平衡转化率
 (填“>”、“<”或“=”),理由是
(填“>”、“<”或“=”),理由是
您最近一年使用:0次
解题方法
4 . 三氯化六氨合钴( )是一种重要的化工产品。实验室以
)是一种重要的化工产品。实验室以 为原料制备三氯六氨合钴的方法如下,回答下列问题:
为原料制备三氯六氨合钴的方法如下,回答下列问题:
Ⅰ.制备氯化钴:已知 易潮解,可用高熔点金属钴与氯气反应制取。实验室可用下图装置进行制备
易潮解,可用高熔点金属钴与氯气反应制取。实验室可用下图装置进行制备_____ 。
(2)A中固体为高锰酸钾,则反应的离子方程式为______ 。装置B中试剂X为____ 。
(3)球形干燥管中试剂的作用为______ 。
Ⅱ.制备三氯化六氨合钴:将制备的 按下图流程操作:
按下图流程操作:____ 。
(5)利用 、
、 、浓氨水、
、浓氨水、 制备
制备 的总反应化学方程式
的总反应化学方程式___ 。
(6)操作X中,加入浓盐酸的作用是____ 。
Ⅲ.测定钴含量:准确称量3.0000g样品 ,加入硫酸酸化的KI溶液至样品恰好完全溶解,配成250mL溶液。量取25.00mL溶液,加入适量缓冲溶液,几滴淀粉溶液,用0.1000mol/L
,加入硫酸酸化的KI溶液至样品恰好完全溶解,配成250mL溶液。量取25.00mL溶液,加入适量缓冲溶液,几滴淀粉溶液,用0.1000mol/L  溶液滴定生成的
溶液滴定生成的 ,消耗
,消耗 溶液的体积为10.00mL。
溶液的体积为10.00mL。
(已知:① 将
将 氧化成
氧化成 ,自身被还原成
,自身被还原成 ;②
;② )。
)。
(7)计算样品中钴元素的质量分数为_______ %(保留至小数点后两位)。
 )是一种重要的化工产品。实验室以
)是一种重要的化工产品。实验室以 为原料制备三氯六氨合钴的方法如下,回答下列问题:
为原料制备三氯六氨合钴的方法如下,回答下列问题:Ⅰ.制备氯化钴:已知
 易潮解,可用高熔点金属钴与氯气反应制取。实验室可用下图装置进行制备
易潮解,可用高熔点金属钴与氯气反应制取。实验室可用下图装置进行制备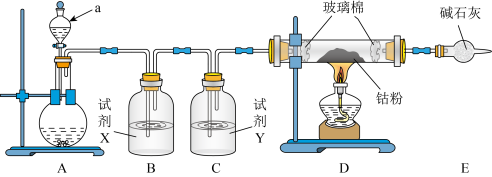
(2)A中固体为高锰酸钾,则反应的离子方程式为
(3)球形干燥管中试剂的作用为
Ⅱ.制备三氯化六氨合钴:将制备的
 按下图流程操作:
按下图流程操作:
(5)利用
 、
、 、浓氨水、
、浓氨水、 制备
制备 的总反应化学方程式
的总反应化学方程式(6)操作X中,加入浓盐酸的作用是
Ⅲ.测定钴含量:准确称量3.0000g样品
 ,加入硫酸酸化的KI溶液至样品恰好完全溶解,配成250mL溶液。量取25.00mL溶液,加入适量缓冲溶液,几滴淀粉溶液,用0.1000mol/L
,加入硫酸酸化的KI溶液至样品恰好完全溶解,配成250mL溶液。量取25.00mL溶液,加入适量缓冲溶液,几滴淀粉溶液,用0.1000mol/L  溶液滴定生成的
溶液滴定生成的 ,消耗
,消耗 溶液的体积为10.00mL。
溶液的体积为10.00mL。(已知:①
 将
将 氧化成
氧化成 ,自身被还原成
,自身被还原成 ;②
;② )。
)。(7)计算样品中钴元素的质量分数为
您最近一年使用:0次
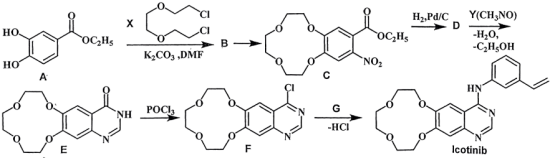
5 . 埃克替尼(Icotinib),商品名凯美纳,是我国首个具有完全自主知识产权的小分子靶向抗癌创新药。它由浙江贝达药业股份有限公司生产,于2011年在我国上市。埃克替尼的问世,标志着我国在抗癌药物研究领域取得了重大突破。Icotinib的合成路线如图所示,回答相关问题。_______ 。C生成D的反应类型为_______ 。
(2)解释A生成B的反应中 的作用
的作用______ (DMF作溶剂,不参与反应)。
(3)B生成C所需的试剂为________ 。
(4)写出A与足量的NaOH反应的化学方程式________ 。
(5)写出Y的化学名称________ 。
(6)写出G的结构简式________ 。
(7)A的同分异构体中满足下列条件的有______ 种。
①含有1个苯环;②既能发生银镜反应又能发生水解反应;③核磁共振氢谱显示有4组峰,峰面积比为1∶1∶2∶6;④不含过氧键(O—O)。
(2)解释A生成B的反应中
 的作用
的作用(3)B生成C所需的试剂为
(4)写出A与足量的NaOH反应的化学方程式
(5)写出Y的化学名称
(6)写出G的结构简式
(7)A的同分异构体中满足下列条件的有
①含有1个苯环;②既能发生银镜反应又能发生水解反应;③核磁共振氢谱显示有4组峰,峰面积比为1∶1∶2∶6;④不含过氧键(O—O)。
您最近一年使用:0次
6 . 由于钠资源储量丰富,便于开采,价格便宜,钠离子电池有望成为下一代大规模储能电池。我国化学家最近研制的一种钠离子电池如图所示。下列说法正确的是
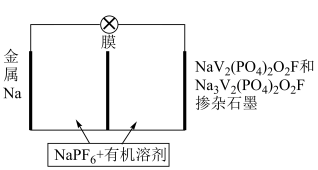
| A.膜是阴离子交换膜 |
B.充电时 向石墨电极移动 向石墨电极移动 |
C.放电时正极的电极反应: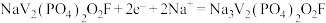 |
| D.有机溶剂可选择乙醇 |
您最近一年使用:0次
7 . 由大脑分泌的化合物X名为甲硫氨酸-脑啡肽,其结构如下图。下列叙述正确的是

| A.X是一种五肽 | B.组成X的氨基酸有5种 |
| C.X含有4个手性碳原子 | D.X不能使溴水褪色 |
您最近一年使用:0次
解题方法
8 . “结构决定性质”,下列有关物质结构与性质的说法中正确的是
A.温度相同时,水溶液中电离常数: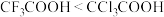 |
B.熔点: |
C.分子的极性: |
D. 、 、 、 、 三种分子中的键能:F-F<Cl-Cl<Br-Br 三种分子中的键能:F-F<Cl-Cl<Br-Br |
您最近一年使用:0次
9 . 下列有关阿伏伽德罗常数( )的叙述中正确的是
)的叙述中正确的是
 )的叙述中正确的是
)的叙述中正确的是A.18g液态水中含有氢键的数目为2 |
B.10g质量分数为46%的乙醇溶液中含有O-H键的数目为0.1 |
C.常温下2.7g Al加至足量的浓硝酸中,转移的电子数为0.3 |
D.25℃时,1L pH=2的 溶液中, 溶液中, 的数目为0.01 的数目为0.01 |
您最近一年使用:0次
解题方法
10 . 以红土镍镉矿(NiS、CdO,含 、CuO、PbO、
、CuO、PbO、 等杂质)为原料回收贵重金属Ni、Cd和Cu,其工艺流程如图所示:
等杂质)为原料回收贵重金属Ni、Cd和Cu,其工艺流程如图所示:
(1)“浆化”的目的是_____ 。
(2)滤渣Ⅰ中含有硫单质,写出“酸浸”时NiS反应的离子方程式_____ ;滤渣Ⅰ中还含有_____ 。(填化学式)
(3)溶液中金属离子开始沉淀和完全沉淀时(浓度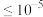 mol/L)的pH如下表,则物质X不可能是
mol/L)的pH如下表,则物质X不可能是_____ ;所调pH范围_____ 。
a. b.CuO c.
b.CuO c.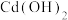 d.NaOH
d.NaOH
(4)电解时阴极的电极反应为_____ 。
(5)整个流程中可以循环使用的物质有______ 。(填化学式)
 、CuO、PbO、
、CuO、PbO、 等杂质)为原料回收贵重金属Ni、Cd和Cu,其工艺流程如图所示:
等杂质)为原料回收贵重金属Ni、Cd和Cu,其工艺流程如图所示: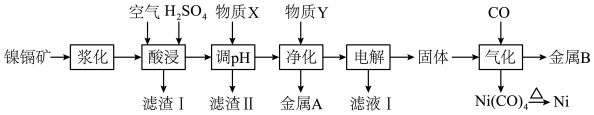
| 物质 | 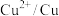 | 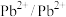 | 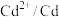 | 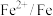 | 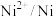 |
| E/V | +0.34 | -0.13 | -0.40 | -0.44 | -0.26 |
(1)“浆化”的目的是
(2)滤渣Ⅰ中含有硫单质,写出“酸浸”时NiS反应的离子方程式
(3)溶液中金属离子开始沉淀和完全沉淀时(浓度
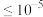 mol/L)的pH如下表,则物质X不可能是
mol/L)的pH如下表,则物质X不可能是| 离子 |  |  |  |  |  |
| 开始沉淀的pH | 1.5 | 6.5 | 7.2 | 4.7 | 6.8 |
| 沉淀完全的pH | 3.3 | 9.9 | 9.5 | 6.7 | 9.2 |
 b.CuO c.
b.CuO c.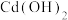 d.NaOH
d.NaOH(4)电解时阴极的电极反应为
(5)整个流程中可以循环使用的物质有
您最近一年使用:0次



