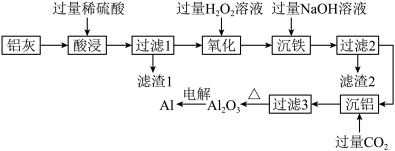
1 . 某回收站利用炼铝厂的废料—铝灰(含Al、Al2O3及少量SiO2、FeO和Fe2O3)回收少量铝。设计有关工艺流程如图:
回答下列问题:
(1)滤渣1的主要成分是______ (填化学式)。
(2)过滤用到的玻璃仪器有______ 、玻璃棒、烧杯.
(3)“氧化”时加入过量H2O2溶液发生反应的离子方程式是______ 。
(4)“沉铝”时通入过量CO2,有同学提出加入过量稀盐酸替换CO2,你认为行不行______ (填“行”或者“不行”),原因是______ 。
(5)电解Al2O3时发生的化学方程式是______ 。
(6)在电解Al2O3生产过程中Al的损失率为15%,若回收1tAl,则消耗的Al2O3的质量为______ t(结果保留2位有效数字)。
回答下列问题:
(1)滤渣1的主要成分是
(2)过滤用到的玻璃仪器有
(3)“氧化”时加入过量H2O2溶液发生反应的离子方程式是
(4)“沉铝”时通入过量CO2,有同学提出加入过量稀盐酸替换CO2,你认为行不行
(5)电解Al2O3时发生的化学方程式是
(6)在电解Al2O3生产过程中Al的损失率为15%,若回收1tAl,则消耗的Al2O3的质量为
您最近一年使用:0次
2 . ①、②、③、④、⑤、⑥、⑦是短周期主族元素,请根据下列相关信息,回答有关问题.
(1)元素②在元素周期表中的位置是_______ 与③同族的下一周期元素的原子结构示意图为_______ 。
(2)③与⑤两种元素的简单离子半径由大到小的顺序是_______ (用离子符号表示)。
(3)③在空气中加热燃烧后产物,既含离子键又含非极性共价键的离子化合物,写出该产物的电子式为_______ 。元素②与⑤按原子个数比1:2形成的化合物所含的化学键有______ 。(填化学键类型)
(4)④元素的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式是______ 。
(5)①与⑤两种元素组成含18个电子的分子的化学式为______ 。
(6)实验室制取⑥单质的离子方程式为______ 。
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | |
| 原子半径nm | 0.186 | 0.143 | 0.074 | 0.099 | 0.102 | ||
| 主要化合价 | -4,+4 | -2 | -1,+7 | -2,+6 | |||
| 其他 | 阳离子的核外无电子 | ②的一种核素可用于测定文物的年代 | 焰色试验呈现黄色 | 地壳中含量最多的金属元素 |
(2)③与⑤两种元素的简单离子半径由大到小的顺序是
(3)③在空气中加热燃烧后产物,既含离子键又含非极性共价键的离子化合物,写出该产物的电子式为
(4)④元素的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式是
(5)①与⑤两种元素组成含18个电子的分子的化学式为
(6)实验室制取⑥单质的离子方程式为
您最近一年使用:0次
3 . 某同学设计了如图所示装置(气密性良好,夹持装置已省略)来制备Fe(OH)2白色沉淀.可选择的试剂有:浓硫酸、稀硫酸、铝粉、铁粉、氢氧化钠溶液.______ ,试管Ⅱ中加入的试剂是______ 。
(2)配制溶液的蒸馏水常加热煮沸的原因是_______ 。
(3)按照图示装置,用两种不同的操作分别进行实验,并观察现象(试管Ⅱ中试剂过量)。
①操作1:夹紧止水夹,等试管I中的反应进行一段时间后,写出试管Ⅱ可能发生的两个化学反应方程式是_______ 、_______ 。
②操作2:打开止水夹,等试管I中的反应进行一段时间后再夹紧止水夹,继续反应一段时间后,试管Ⅱ中观察到的现象为_______ 。
(4)有如图4个装置,其中能较长时间看到Fe(OH)2白色絮状沉淀的有_______ 。
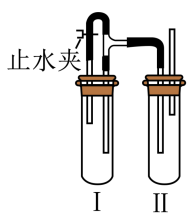
(2)配制溶液的蒸馏水常加热煮沸的原因是
(3)按照图示装置,用两种不同的操作分别进行实验,并观察现象(试管Ⅱ中试剂过量)。
①操作1:夹紧止水夹,等试管I中的反应进行一段时间后,写出试管Ⅱ可能发生的两个化学反应方程式是
②操作2:打开止水夹,等试管I中的反应进行一段时间后再夹紧止水夹,继续反应一段时间后,试管Ⅱ中观察到的现象为
(4)有如图4个装置,其中能较长时间看到Fe(OH)2白色絮状沉淀的有
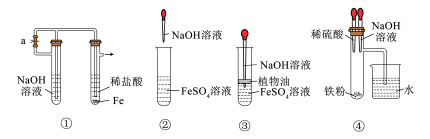
| A.①② | B.③④ | C.①③ | D.②④ |
您最近一年使用:0次
4 . 请回答下列问题:
(1)有下列微粒或物质:
① O、
O、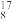 O、
O、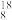 O ②H2O、D2O ③白磷、红磷 ④
O ②H2O、D2O ③白磷、红磷 ④ K、
K、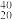 Ca、
Ca、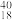 Ar
Ar
互为同素异形体的是_______ (填序号),其中互为同位素的是_______ (填序号)。
(2)同温同压下,同体积的 和
和 分子数之比为
分子数之比为_______ ,质量之比为______ 。
(3)实验室为监测空气中录蒸气的含量,往往悬挂涂有CuI的滤纸,根据滤纸是否变色或颜色发生变化所用去的时间来判断空气中的含汞量,其反应为(末配平)
 CuI+
CuI+ Hg——
Hg—— Cu2HgI4+
Cu2HgI4+ Cu。
Cu。
①反应产物Cu2HgI4中,Cu元素显______ 价。
②写出配平后的上述反应的化学方程式: CuI+
CuI+ Hg——
Hg—— Cu2HgI4+
Cu2HgI4+ Cu。
Cu。_______
(4)现欲配制480mL0.2mol/L的NaOH溶液,回答下列问题:
①配制该溶液时所需玻璃仪器除烧杯、玻璃棒、胶头滴管、量筒外,还需______ 。
②定容时,若俯视容量瓶刻度线会使配制的NaOH溶液浓度_______ (填“偏大”、“偏小”或“不变”)。
(1)有下列微粒或物质:
①
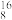 O、
O、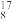 O、
O、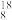 O ②H2O、D2O ③白磷、红磷 ④
O ②H2O、D2O ③白磷、红磷 ④ K、
K、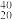 Ca、
Ca、 Ar
Ar互为同素异形体的是
(2)同温同压下,同体积的
 和
和 分子数之比为
分子数之比为(3)实验室为监测空气中录蒸气的含量,往往悬挂涂有CuI的滤纸,根据滤纸是否变色或颜色发生变化所用去的时间来判断空气中的含汞量,其反应为(末配平)
 CuI+
CuI+ Hg——
Hg—— Cu2HgI4+
Cu2HgI4+ Cu。
Cu。①反应产物Cu2HgI4中,Cu元素显
②写出配平后的上述反应的化学方程式:
 CuI+
CuI+ Hg——
Hg—— Cu2HgI4+
Cu2HgI4+ Cu。
Cu。(4)现欲配制480mL0.2mol/L的NaOH溶液,回答下列问题:
①配制该溶液时所需玻璃仪器除烧杯、玻璃棒、胶头滴管、量筒外,还需
②定容时,若俯视容量瓶刻度线会使配制的NaOH溶液浓度
您最近一年使用:0次
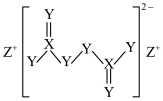
5 . “鱼浮灵”可作水产养鱼的增氧剂,其主要成分的结构如图所示。元素X、Y、Z均为短周期主族元素,原子序数依次增大,其中Z位于元素周期表第三周期。下列说法正确的是
| A.单质的沸点:X>Y | B.Z2Y2、Z2Y所含化学键类型完全相同 |
| C.原子半径:Z>Y>X | D.简单氢化物的稳定性:X>Y |
您最近一年使用:0次
解题方法
6 . 下列离子方程式书写正确的是
| A.金属钠溶于水:2Na+2H2O=2Na++2OH-+O2↑ |
B.小苏打溶液中加入醋酸:HCO +H+=CO2↑+H2O +H+=CO2↑+H2O |
| C.利用覆铜板制作印刷电路板:Fe3++Cu=Fe2++Cu2+ |
D.向氢氧化钠溶液中通入过量二氧化碳:CO2+OH-=HCO |
您最近一年使用:0次
7 . 在湿润的土壤中,氮元素有如图所示的转化过程,下列说法正确的是
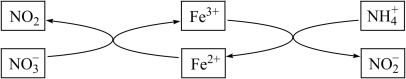
A.NO 是还原剂 是还原剂 | B.NO2是还原产物 |
C.NH 是氧化产物 是氧化产物 | D.NO 是氧化剂 是氧化剂 |
您最近一年使用:0次
8 . 以元素化合价为纵坐标,物质类别为横坐标的图像称为价类二维图,如图是氯元素的价类二维图,a、b、c、d、e、f均为含氯元素的物质。下列叙述不正确的是
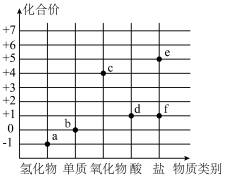
| A.从氧化还原角度分析可知:a和f混合可以制得b |
| B.c的化学式为ClO2,可作自来水消毒剂 |
| C.标准状况下,22.4Lb与水反应,转移2NA个电子 |
| D.84消毒液可由b与烧碱溶液制得 |
您最近一年使用:0次
9 . 下列实验能达到目的的是
| 选项 | 实验目的 | 实验方法或操作 |
| A | 测定新制氯水的pH | 用玻璃棒蘸取新制氯水点在pH试纸上 |
| B | 鉴别Na2CO3与NaHCO3 | 各取少量固体加水溶解,分别滴加石灰水,振荡,观察是否产生白色沉淀 |
| C | 检验铁锈中是否含有二价铁 | 将铁锈溶于稀盐酸,滴入KSCN溶液,观察溶液是否变成红色 |
| D | 检验Na2CO3溶液中是否含有Cl- | 取少量溶液于一支洁净试管中,加入过量稀硝酸使其酸化,再滴入AgNO3溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 . 下列关于物质的性质比较,不正确的是
| A.碱性强弱:NaOH>Mg(OH)2>Al(OH)3 |
| B.氢化物的稳定性强弱:HCl>H2S>H2O |
| C.酸性强弱:HClO4>H2SO4>H3PO4 |
| D.氧化性强弱:Cl2>Br2>I2 |
您最近一年使用:0次



