名校
1 . 2020年9月22日,中国政府在第75届联合国大会上提出:“中国将提高国家自主贡献力度,采取更有力的政策和措施。二氧化碳排放力争于2030年前达到峰值,努力争取2060年前实现碳中和。” 碳中和也叫碳补偿(Carbon Offset),是现代人为减缓全球变暖所作的努力之一。碳中和的实现方式包括两种:一是通过植树造林等方式增加CO2的吸收量,二是通过技术手段减少CO2的排放量。
Ⅰ.二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。二氧化碳加氢制甲醇的总反应可表示为:CO2(g)+3H2(g) ⇌ CH3OH(g)+H2O(g),该反应一般认为通过如下步骤来实现:
①CO2(g)+H2(g)⇌ CO(g)+H2O(g) △H1=+41kJ·mol-1
②CO(g)+2H2(g) ⇌ CH3OH(g) △H2= —99kJ·mol-1
(1)总反应的
_______ kJ·mol-1;
(2)氢氧燃料电池具有启动快,效率高等优点,若电解质为酸性,氢氧燃料电池的正极反应为_______
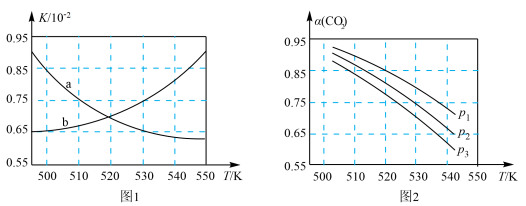
(3)图1中能正确反映平衡常数K随温度变化关系的曲线为_______ (填曲线标记字母),体系中的CO2平衡转化率(a)与温度和压强的关系如图2所示,则图2中的压强由大到小为_______ 。_______ (用含a的式子表示)。
Ⅱ. 和
和 的催化重整对温室气体的减排具有重要意义,其反应为:
的催化重整对温室气体的减排具有重要意义,其反应为: 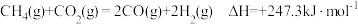 。回答下列问题:
。回答下列问题:
(5)该反应体系的熵值变化为_______ (填“增加”或“减小”);根据公式△G=△H—T△S判断:此反应在_______ (填“低温”或“高温”)条件下可以自发进行。
(6)其它条件相同,在不同催化剂(A、B)作用下,反应 进行相同时间后,
进行相同时间后, 的产率随反应温度的变化如图3所示。
的产率随反应温度的变化如图3所示。_______ ,在催化剂A、B作用下,它们反应活化能分别用 、
、 表示,则
表示,则
_______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(7)将原料 和
和 按等物质的量充入密闭容器中,保持体系压强为
按等物质的量充入密闭容器中,保持体系压强为 发生反应:
发生反应: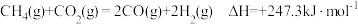 。达到平衡时,
。达到平衡时, 体积分数与温度的关系如图4所示,则在
体积分数与温度的关系如图4所示,则在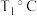 、
、 下,达平衡时
下,达平衡时 转化率=
转化率=_______ 。
Ⅰ.二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。二氧化碳加氢制甲醇的总反应可表示为:CO2(g)+3H2(g) ⇌ CH3OH(g)+H2O(g),该反应一般认为通过如下步骤来实现:
①CO2(g)+H2(g)⇌ CO(g)+H2O(g) △H1=+41kJ·mol-1
②CO(g)+2H2(g) ⇌ CH3OH(g) △H2= —99kJ·mol-1
(1)总反应的

(2)氢氧燃料电池具有启动快,效率高等优点,若电解质为酸性,氢氧燃料电池的正极反应为
(3)图1中能正确反映平衡常数K随温度变化关系的曲线为
Ⅱ.
 和
和 的催化重整对温室气体的减排具有重要意义,其反应为:
的催化重整对温室气体的减排具有重要意义,其反应为: 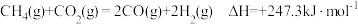 。回答下列问题:
。回答下列问题:(5)该反应体系的熵值变化为
(6)其它条件相同,在不同催化剂(A、B)作用下,反应
 进行相同时间后,
进行相同时间后, 的产率随反应温度的变化如图3所示。
的产率随反应温度的变化如图3所示。 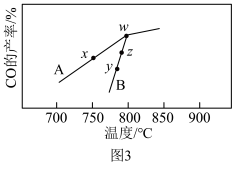
 、
、 表示,则
表示,则
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(7)将原料
 和
和 按等物质的量充入密闭容器中,保持体系压强为
按等物质的量充入密闭容器中,保持体系压强为 发生反应:
发生反应: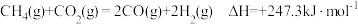 。达到平衡时,
。达到平衡时, 体积分数与温度的关系如图4所示,则在
体积分数与温度的关系如图4所示,则在 、
、 下,达平衡时
下,达平衡时 转化率=
转化率=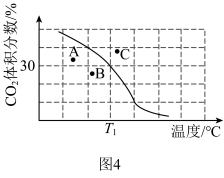
您最近一年使用:0次
名校
2 . ClO-结合H+ 弱于CO ,下列反应的离子方程式
,下列反应的离子方程式正确 的是
 ,下列反应的离子方程式
,下列反应的离子方程式A.向次氯酸钠溶液中通入少量二氧化碳气体: |
B.K2CO3水解:CO + 2H2O ⇌ H2CO3 + 2OH- + 2H2O ⇌ H2CO3 + 2OH- |
C.用惰性电极电解饱和 溶液:2Cl- + 2H2O = H2↑ + Cl2↑ + 2OH- 溶液:2Cl- + 2H2O = H2↑ + Cl2↑ + 2OH- |
D. 溶液中加入过量浓氨水: 溶液中加入过量浓氨水: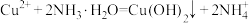 |
您最近一年使用:0次
名校
解题方法
3 . X、Y、Z、M、Q五种短周期主族元素,原子序数依次增大。X的核外电子数等于其周期数,YX3分子呈三角锥形,Z的核外电子数等于X、Y核外电子数之和。M与X同主族,Q是同周期中非金属性最强的元素。下列说法正确 的是
| A.Y与Z电负性:Y > Z |
| B.Y与Z第一电离能:Y > Z |
| C.M2Z与MQ的晶体类型不同 |
| D.由X、Y、Z三种元素组成的化合物的水溶液均显酸性 |
您最近一年使用:0次
名校
4 . 多巴胺是一种神经传导物质,会传递兴奋及开心的信息,其部分合成路线如下图,下列说法正确 的是
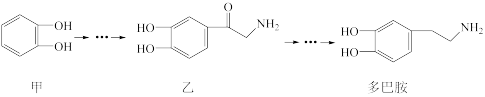
A.多巴胺的分子式为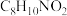 |
| B.甲分子的核磁共振氢谱有4组峰 |
C.甲能与 发生加成反应,且1mol甲最多能消耗2molH2 发生加成反应,且1mol甲最多能消耗2molH2 |
| D.多巴胺分子中含两种官能团,分别是酚羟基和氨基 |
您最近一年使用:0次
名校
解题方法
5 . 有关下列2种有机物的说法不正确 的是
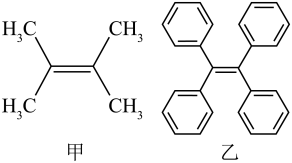
| A.甲、乙分子中官能团相同,两者互为同系物 |
| B.乙分子中所有碳原子可能处于同一平面上 |
C.甲使溴的四氯化碳溶液褪色和使酸性 溶液褪色的原理不同 溶液褪色的原理不同 |
| D.乙的一氯代物有3种(不考虑立体异构) |
您最近一年使用:0次
名校
解题方法
6 . 化学与生产生活科技密切相关,下列说法正确 的是
| A.中国空间站太阳翼使用氮化镓(GaN)半导体材料,GaN属于新型无机非金属材料 |
| B.目前我国加碘食盐中主要添加的是碘化钾 |
| C.“酒曲”的酿酒工艺,是利用了催化剂使平衡正向移动的原理 |
| D.医用外科口罩使用的,聚丙烯材料能使酸性高锰酸钾溶液褪色 |
您最近一年使用:0次
名校
7 .  溶液与
溶液与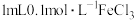 溶液发生反应:
溶液发生反应: 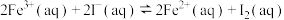 , 达到平衡,下列说法
, 达到平衡,下列说法不正确 的是
 溶液与
溶液与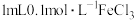 溶液发生反应:
溶液发生反应: 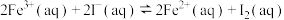 , 达到平衡,下列说法
, 达到平衡,下列说法| A.加入苯、振荡,平衡正向移动 |
B.经苯3次萃取分离后,在水溶液中加入 ,溶液呈红色,表明该化学反应存在限度 ,溶液呈红色,表明该化学反应存在限度 |
C.加入 固体,平衡逆向移动 固体,平衡逆向移动 |
D.该反应的平衡常数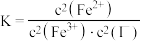 |
您最近一年使用:0次
名校
解题方法
8 . 我国科学家研制了一种铬(24号元素)基催化剂,实现了甲烷向甲醇的高效转化,微观示意图如下,下列说法正确 的是
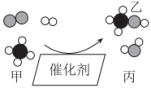
| A.基态铬原子的电子排布式为[Ar]3d44s2 |
| B.甲、乙、丙中的C和O原子都是sp3杂化 |
| C.甲是由极性键形成的极性分子 |
| D.该催化过程有极性键和非极性键的断裂,也有极性键和非极性键的形成 |
您最近一年使用:0次
名校
9 . W、X、Y、Z是元素周期表中的四种短周期元素,其相关信息及原子半径与原子序数的关系如表所示。请回答下列问题:
(1)W与X形成的含有共价键的常见化合物的电子式为_______ 。
(2)Y的价层电子排布式_______ 。
(3)Z的简单氢化物沸点比同主族上一周期元素简单氢化物沸点要_______ (填“高”或“低”)
(4)CuS晶胞中 的位置如图1所示,
的位置如图1所示, 位于顶点和面心,
位于顶点和面心, 位于
位于 所构成的四面体中心,晶胞侧视图如图2所示。
所构成的四面体中心,晶胞侧视图如图2所示。 距离最近的
距离最近的 数目为
数目为_______ 。
② CuS的晶胞参数为apm,阿伏加德罗常数的值为 ,则CuS晶体的密度为
,则CuS晶体的密度为_______  。
。
| 元素 | 相关信息 | 原子半径与原子序数的关系 |
| W | 其一种核素的质量数为18,中子数为10 |
|
| X | 其原子与电子排布式为1s22s22p6的原子的核外电子数相差1 | |
| Y | 其单质是一种常见的半导体材料 | |
| Z | 电负性在同周期元素中最大 |
(1)W与X形成的含有共价键的常见化合物的电子式为
(2)Y的价层电子排布式
(3)Z的简单氢化物沸点比同主族上一周期元素简单氢化物沸点要
(4)CuS晶胞中
 的位置如图1所示,
的位置如图1所示, 位于顶点和面心,
位于顶点和面心, 位于
位于 所构成的四面体中心,晶胞侧视图如图2所示。
所构成的四面体中心,晶胞侧视图如图2所示。
 距离最近的
距离最近的 数目为
数目为② CuS的晶胞参数为apm,阿伏加德罗常数的值为
 ,则CuS晶体的密度为
,则CuS晶体的密度为 。
。
您最近一年使用:0次
名校
解题方法
10 . 设NA阿伏加德罗常数的值下列说法正确 的是
A.常温下,1mol硝酸铵溶于稀氨水使溶液呈中性,则NH 数目为NA 数目为NA |
| B.在过氧化钠与水的反应中,每生成0.1mol O2,转移电子的数目为0.4NA |
| C.1mol乙二酸(H2C2O4)分子中π键的数目为3NA |
| D.室温下,pH=12的Na2CO3溶液中,由水电离出的OH-数目为0.01NA |
您最近一年使用:0次