名校
解题方法
1 . 有机物的种类多,在日常生活中有重要的用途。请回答下列问题:_____ 。
(2)请用系统命名法命名有机物②_____ 。
(3)⑤与⑦发生共聚反应的化学方程式_____ 。
(4)属于非极性分子的是_____ (填序号)。
(5)⑥中基态氧原子的核外电子的空间运动状态有_____ 种。
(6)硼在成键时能将一个2s电子激发进入2p能级参与形成化学键,请写出该激发态原子价电子轨道表示式:_____ ,该过程形成的原子光谱为_____ (填“吸收”或“发射”)光谱。
①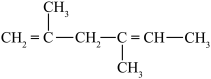 ;②
;②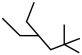 ;③
;③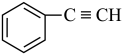 ;④
;④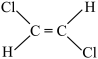 ;⑤
;⑤ ;⑥
;⑥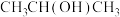 ;⑦
;⑦
(2)请用系统命名法命名有机物②
(3)⑤与⑦发生共聚反应的化学方程式
(4)属于非极性分子的是
(5)⑥中基态氧原子的核外电子的空间运动状态有
(6)硼在成键时能将一个2s电子激发进入2p能级参与形成化学键,请写出该激发态原子价电子轨道表示式:
您最近一年使用:0次
名校
解题方法
2 . 回答下列问题:
(1)下列状态的钙中,电离最外层一个电子所需能量最大的是_____(填标号);
(2)写出基态 离子的M层电子排布式
离子的M层电子排布式_____ 。
(3)实验室常用 检验
检验 ,
, 中
中 的配位数为
的配位数为_____ , 中碳原子的杂化轨道类型为
中碳原子的杂化轨道类型为_____ 杂化。
(4)已知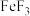 的熔点(1000℃)显著高于
的熔点(1000℃)显著高于 的熔点(306C),原因是
的熔点(306C),原因是_____ 。
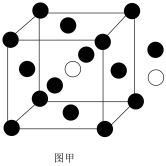
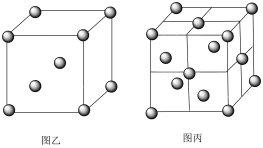
(5)铁和氨在640℃可发生置换反应,产物之一的立方晶胞结构如图甲所示,写出该反应的化学方程式:_____ 。 _____ ,图乙中铁原子沿着晶胞体对角线相切,图丙中铁原子沿着晶胞面对角线相切。若两种晶体中铁原子半径相同,则两种铁晶体中密度较高的是_____ 。(填“图乙”或“图丙”)
(1)下列状态的钙中,电离最外层一个电子所需能量最大的是_____(填标号);
A. 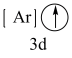 | B. 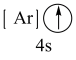 | C. 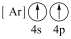 | D. 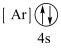 |
(2)写出基态
 离子的M层电子排布式
离子的M层电子排布式(3)实验室常用
 检验
检验 ,
, 中
中 的配位数为
的配位数为 中碳原子的杂化轨道类型为
中碳原子的杂化轨道类型为(4)已知
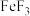 的熔点(1000℃)显著高于
的熔点(1000℃)显著高于 的熔点(306C),原因是
的熔点(306C),原因是(5)铁和氨在640℃可发生置换反应,产物之一的立方晶胞结构如图甲所示,写出该反应的化学方程式:
您最近一年使用:0次
名校
解题方法
3 . 设 为阿伏加德罗常数的值,下列说法不正确的是
为阿伏加德罗常数的值,下列说法不正确的是
 为阿伏加德罗常数的值,下列说法不正确的是
为阿伏加德罗常数的值,下列说法不正确的是A.1 配合物 配合物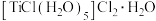 完全电离出的 完全电离出的 数目为2 数目为2 |
B.12g金刚石中含有的晶胞数目为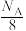 |
C.标准状况下,22.4L 中 中 键的数目为2 键的数目为2 |
D.28g乙烯和环己烷(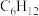 )的混合物中含有碳原子数为2 )的混合物中含有碳原子数为2 |
您最近一年使用:0次
名校
解题方法
4 . 下列各项比较中前者高于(或大于或强于)后者的是
| A.1-丁烯和1-戊烯的沸点 |
B.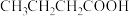 的酸性和 的酸性和 的酸性 的酸性 |
C. 分子中的 分子中的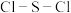 键角和 键角和 分子中的 分子中的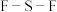 键角 键角 |
D.羟基苯甲醛(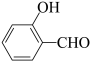 )沸点和对羟基米甲醛( )沸点和对羟基米甲醛(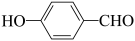 )沸点 )沸点 |
您最近一年使用:0次
5 . 下列化学用语或图示表达不正确的是
A.顺式聚异戊二烯的结构简式: |
B.基态铜原子的价层电子轨道表示式: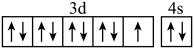 |
C. 的电子式: 的电子式: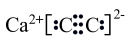 |
D. 的简化电子排布式: 的简化电子排布式: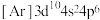 |
您最近一年使用:0次
名校
6 . Ⅰ.制备苯甲醇和苯甲酸的实验流程及涉及的主要实验装置(部分加热和固定装置已略)如图:_________________ ,仪器B的名称_____________________ 。
(2)第①步所用装置(如图),用搅拌器的目的是_____________ 。_____________ 。
(4)第⑥步的操作名称是_____________ 。
Ⅱ.铬的化合物氯化铬酰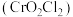 ,熔点
,熔点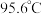 、沸点
、沸点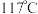 ,易溶于
,易溶于 ,可作为化工生产中的氧化剂。能通过反应
,可作为化工生产中的氧化剂。能通过反应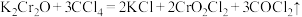 制备。
制备。
(5)固态 属于
属于_____________ 晶体。
(6)基态氯原子核外电子运动状态有_________ 种。
(7)基态钾原子核外电子排布式为_____________________________________ 。
(8)化合物 中存在的共价键类型是
中存在的共价键类型是_________________ 。(填 键或
键或 键)
键)
(9)氧族元素氢化物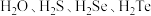 的熔沸点由高到低排列顺序为:
的熔沸点由高到低排列顺序为:_____________________ 。
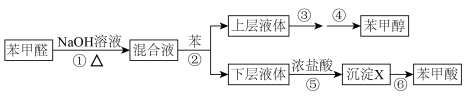
(2)第①步所用装置(如图),用搅拌器的目的是

(4)第⑥步的操作名称是
Ⅱ.铬的化合物氯化铬酰
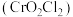 ,熔点
,熔点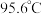 、沸点
、沸点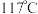 ,易溶于
,易溶于 ,可作为化工生产中的氧化剂。能通过反应
,可作为化工生产中的氧化剂。能通过反应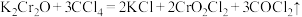 制备。
制备。(5)固态
 属于
属于(6)基态氯原子核外电子运动状态有
(7)基态钾原子核外电子排布式为
(8)化合物
 中存在的共价键类型是
中存在的共价键类型是 键或
键或 键)
键)(9)氧族元素氢化物
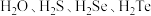 的熔沸点由高到低排列顺序为:
的熔沸点由高到低排列顺序为:
您最近一年使用:0次
名校
7 . 根据已学知识,请回答下列问题
(1)物质A的结构简式为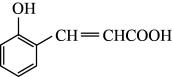 ,写出A中的含氧官能团名称
,写出A中的含氧官能团名称_____________________________ 。
(2)有机化合物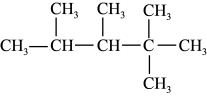 的名称是
的名称是_________________ ,其在核磁共振氢谱上有_________ 组峰。
(3)键线式 表示的有机物的分子式为
表示的有机物的分子式为 _________ ,其中等效氢个数比为_________________ 。
(4)写出1,3一丁二烯与 发生1,4-加成的反应方程式:
发生1,4-加成的反应方程式:_________________________________________________ 。
(5)与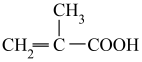 具有相同官能团的一种同分异构体的结构简式为
具有相同官能团的一种同分异构体的结构简式为_____________________ 。
(1)物质A的结构简式为
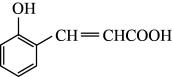 ,写出A中的含氧官能团名称
,写出A中的含氧官能团名称(2)有机化合物
 的名称是
的名称是(3)键线式
 表示的有机物的分子式为
表示的有机物的分子式为 (4)写出1,3一丁二烯与
 发生1,4-加成的反应方程式:
发生1,4-加成的反应方程式:(5)与
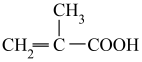 具有相同官能团的一种同分异构体的结构简式为
具有相同官能团的一种同分异构体的结构简式为
您最近一年使用:0次
名校
8 . 下列化学用语表达正确的是
A.乙烯的结构简式: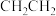 |
B.基态 原子价层电子的轨道表示式: 原子价层电子的轨道表示式: |
C. 的结构示意图: 的结构示意图: |
D. 原子最外层电子的电子云轮廓图: 原子最外层电子的电子云轮廓图: |
您最近一年使用:0次
名校
9 . 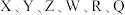 为前30号元素,且原子序数依次增大。
为前30号元素,且原子序数依次增大。 是元素周期表中原子半径最小的元素;
是元素周期表中原子半径最小的元素; 元素基态原子有三个能级上有电子,且每个能级上的电子数相等
元素基态原子有三个能级上有电子,且每个能级上的电子数相等 元素基态原子的单电子数在同周期元素基态原子中最多;
元素基态原子的单电子数在同周期元素基态原子中最多; 与
与 同周期,第一电离能比
同周期,第一电离能比 的低;
的低; 与
与 同主族;
同主族; 基态原子最外层电子排布为
基态原子最外层电子排布为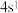 ,内层处于全充满状态。请回答下列问题:
,内层处于全充满状态。请回答下列问题:
(1)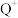 的核外电子排布式为
的核外电子排布式为 _________________ 。
(2)化合物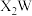 中
中 的杂化方式为
的杂化方式为_____________ ;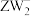 的空间结构为
的空间结构为_________________ 。
(3) 、
、 的最高价氧化物中沸点较高的是
的最高价氧化物中沸点较高的是_____________ (填化学式),原因是_____________________________ 。
(4) 有多种同素异形体,其中一种同素异形体的晶胞结构如图所示,该晶体的晶胞中所含
有多种同素异形体,其中一种同素异形体的晶胞结构如图所示,该晶体的晶胞中所含 原子的个数为
原子的个数为_____________ ;若晶胞的边长为 ,晶体的密度为
,晶体的密度为 ,相对分子质量为
,相对分子质量为 ,则阿伏加德罗常数的值
,则阿伏加德罗常数的值 为
为_____________ (用含 和
和 的代数式表示)。
的代数式表示)。
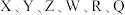 为前30号元素,且原子序数依次增大。
为前30号元素,且原子序数依次增大。 是元素周期表中原子半径最小的元素;
是元素周期表中原子半径最小的元素; 元素基态原子有三个能级上有电子,且每个能级上的电子数相等
元素基态原子有三个能级上有电子,且每个能级上的电子数相等 元素基态原子的单电子数在同周期元素基态原子中最多;
元素基态原子的单电子数在同周期元素基态原子中最多; 与
与 同周期,第一电离能比
同周期,第一电离能比 的低;
的低; 与
与 同主族;
同主族; 基态原子最外层电子排布为
基态原子最外层电子排布为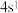 ,内层处于全充满状态。请回答下列问题:
,内层处于全充满状态。请回答下列问题:(1)
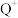 的核外电子排布式为
的核外电子排布式为 (2)化合物
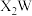 中
中 的杂化方式为
的杂化方式为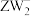 的空间结构为
的空间结构为(3)
 、
、 的最高价氧化物中沸点较高的是
的最高价氧化物中沸点较高的是(4)
 有多种同素异形体,其中一种同素异形体的晶胞结构如图所示,该晶体的晶胞中所含
有多种同素异形体,其中一种同素异形体的晶胞结构如图所示,该晶体的晶胞中所含 原子的个数为
原子的个数为 ,晶体的密度为
,晶体的密度为 ,相对分子质量为
,相对分子质量为 ,则阿伏加德罗常数的值
,则阿伏加德罗常数的值 为
为 和
和 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
名校
10 .  是制造芯片的新型半导体材料。回答下列问题:
是制造芯片的新型半导体材料。回答下列问题:
(1)镓为第四周期元素,基态 原子的价层电子轨道表示式为:
原子的价层电子轨道表示式为:_________________________ 。
(2) 的电负性由强到弱的顺序为
的电负性由强到弱的顺序为_________________________ (元素符号表示,下同);
 的第一电离能由大到小的顺序
的第一电离能由大到小的顺序_____________________________ 。
(3)芯片制造中用到光刻胶,可由甲基丙烯酸甲酯(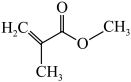 )、马来酸酐(
)、马来酸酐(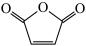 )等通过加聚反应制得。甲基丙烯酸甲酯中碳原子的轨道杂化类型为
)等通过加聚反应制得。甲基丙烯酸甲酯中碳原子的轨道杂化类型为_________________ ,马来酸酐分子中, 键和
键和 键个数比为
键个数比为_________________ 。
(4)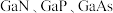 的结构类似于金刚石,熔点如表所示:
的结构类似于金刚石,熔点如表所示:
试分析三者熔点变化的原因:_________________________ 。
(5) 的晶胞结构如图所示(白球是
的晶胞结构如图所示(白球是 ,黑球是
,黑球是 )。
)。
图甲中,与 原子紧邻的
原子紧邻的 原子有
原子有_________ 个,若 晶体密度为
晶体密度为 ,相对分子质量为
,相对分子质量为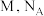 表示阿伏加德罗常数,则晶胞中距离最近的两个
表示阿伏加德罗常数,则晶胞中距离最近的两个 原子间距离为
原子间距离为_____________  。(用含
。(用含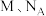 和
和 的代数式表示)
的代数式表示)
 是制造芯片的新型半导体材料。回答下列问题:
是制造芯片的新型半导体材料。回答下列问题:(1)镓为第四周期元素,基态
 原子的价层电子轨道表示式为:
原子的价层电子轨道表示式为:(2)
 的电负性由强到弱的顺序为
的电负性由强到弱的顺序为 的第一电离能由大到小的顺序
的第一电离能由大到小的顺序(3)芯片制造中用到光刻胶,可由甲基丙烯酸甲酯(
 )、马来酸酐(
)、马来酸酐( )等通过加聚反应制得。甲基丙烯酸甲酯中碳原子的轨道杂化类型为
)等通过加聚反应制得。甲基丙烯酸甲酯中碳原子的轨道杂化类型为 键和
键和 键个数比为
键个数比为(4)
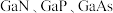 的结构类似于金刚石,熔点如表所示:
的结构类似于金刚石,熔点如表所示:| 物质 |  | 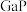 |  |
熔点/ | 1700 | 1480 | 1238 |
(5)
 的晶胞结构如图所示(白球是
的晶胞结构如图所示(白球是 ,黑球是
,黑球是 )。
)。图甲中,与
 原子紧邻的
原子紧邻的 原子有
原子有 晶体密度为
晶体密度为 ,相对分子质量为
,相对分子质量为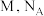 表示阿伏加德罗常数,则晶胞中距离最近的两个
表示阿伏加德罗常数,则晶胞中距离最近的两个 原子间距离为
原子间距离为 。(用含
。(用含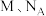 和
和 的代数式表示)
的代数式表示)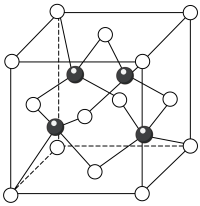
您最近一年使用:0次



