名校
解题方法
1 . 下列关于物质的结构和性质说法错误的是
A. 离子键成分的百分数大于MgO 离子键成分的百分数大于MgO |
B. 中H-O-H键角小于 中H-O-H键角小于 中键角 中键角 |
C. 分子结构中,因含有-N=N-,存在顺反异构,反式结构能量低更稳定 分子结构中,因含有-N=N-,存在顺反异构,反式结构能量低更稳定 |
D. 无色溶液接触空气会很快变成深蓝色 无色溶液接触空气会很快变成深蓝色 ,属于配离子被氧化过程 ,属于配离子被氧化过程 |
您最近一年使用:0次
2 . 新型材料的不断发展和应用,能够推动新质生产力的提升。下列新型材料主要成分属于有机物的是
| A.砷化镓太阳能电池 | B.Ti-Ni形状记忆合金 |
| C.可编程水泥 | D.超高分子量聚乙烯纤维 |
您最近一年使用:0次
3 .  是原子序数依次增大的短周期元素,
是原子序数依次增大的短周期元素, 分别位于不同周期,
分别位于不同周期, 是同周期中金属性最强的元素。四种元素可“组合”成一种具有高效催化性能的超分子,其结构如图(
是同周期中金属性最强的元素。四种元素可“组合”成一种具有高效催化性能的超分子,其结构如图( 与
与 之间都是
之间都是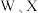 构成的相同结构)。下列说法错误的是
构成的相同结构)。下列说法错误的是
 是原子序数依次增大的短周期元素,
是原子序数依次增大的短周期元素, 分别位于不同周期,
分别位于不同周期, 是同周期中金属性最强的元素。四种元素可“组合”成一种具有高效催化性能的超分子,其结构如图(
是同周期中金属性最强的元素。四种元素可“组合”成一种具有高效催化性能的超分子,其结构如图( 与
与 之间都是
之间都是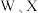 构成的相同结构)。下列说法错误的是
构成的相同结构)。下列说法错误的是
A. 位于第二周期第ⅥA族 位于第二周期第ⅥA族 | B. 单质不存在能导电的晶体 单质不存在能导电的晶体 |
C. 与 与 之间可能存在配位键 之间可能存在配位键 | D.利用该超分子可以分离简单 离子和钡离子 离子和钡离子 |
您最近一年使用:0次
4 . 舌尖中“海南美食”享誉世界。下列与海南美食有关的物质的主要成分不属于高分子的是
| A.临高烤乳猪——油脂 | B.海南粉——淀粉 |
| C.清蒸和乐蟹——蛋白质 | D.椰子饭外包装盒——塑料 |
您最近一年使用:0次
5 . 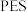 材料在生产、生活中有广泛应用。环氧乙烷合成
材料在生产、生活中有广泛应用。环氧乙烷合成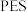 的原理如图所示:
的原理如图所示:
 材料在生产、生活中有广泛应用。环氧乙烷合成
材料在生产、生活中有广泛应用。环氧乙烷合成 的原理如图所示:
的原理如图所示: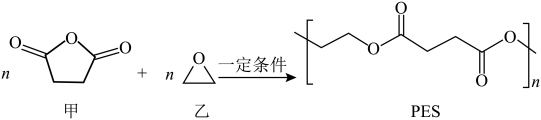
A.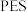 属于混合物 属于混合物 | B.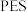 中含酯基,乙中含醚键 中含酯基,乙中含醚键 |
| C.乙醛是乙的同分异构体 | D.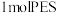 最多能消耗 最多能消耗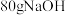 |
您最近一年使用:0次
名校
6 . 实验是化学的灵魂。下列有关实验的说法正确的是
A.用酸性 溶液鉴别苯酚和苯甲醇 溶液鉴别苯酚和苯甲醇 |
B.用 量筒准确量取 量筒准确量取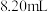 稀盐酸 稀盐酸 |
C.使用广泛 试纸测定氯水的 试纸测定氯水的 |
D.用浓氨水可以清洗试管内壁上的 |
您最近一年使用:0次
名校
7 . 由下列实验步骤得到的实验现象、结论或解释均正确的是
| 选项 | 实验步骤 | 实验现象 | 结论或解释 |
| A | 向 溶液中滴加酸性 溶液中滴加酸性 溶液 溶液 | 溶液紫色褪去 |  具有还原性 具有还原性 |
| B | 分别向置于不同温度下的 氢硫酸和 氢硫酸和 氢硫酸中通入等量氯气 氢硫酸中通入等量氯气 |  氢硫酸先出现浑浊 氢硫酸先出现浑浊 | 增大浓度可加快反应速率 |
| C | 向 溶液中同时通入 溶液中同时通入 和 和 | 出现白色沉淀 | 白色沉淀为 |
| D | 向 溶液中逐滴加入氨水至过量 溶液中逐滴加入氨水至过量 | 产生蓝色沉淀 |  难溶于水 难溶于水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
8 . 下列物质用途和解释匹配的是
| 选项 | 用途 | 解释 |
| A | 热纯碱溶液常作餐具洗涤剂 | 纯碱是强电解质 |
| B | 石膏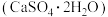 用于制作豆腐的凝固剂 用于制作豆腐的凝固剂 |  微溶于水 微溶于水 |
| C | 丁基羟基茴香醚 作油脂制品的抗氧化剂 作油脂制品的抗氧化剂 | 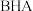 具有较强的还原性 具有较强的还原性 |
| D | 干冰、冰常用作制冷剂 | 断裂化学键吸收热量 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
9 . 某小组设计实验探究 的漂白原理,装置如图所示。
的漂白原理,装置如图所示。
下列叙述正确的是
 的漂白原理,装置如图所示。
的漂白原理,装置如图所示。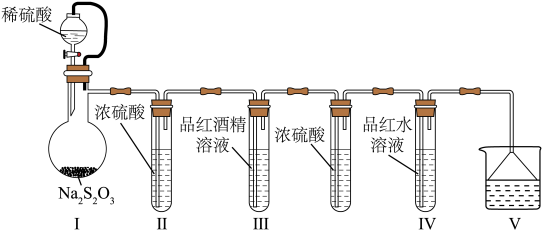
下列叙述正确的是
A.Ⅰ中 表现还原性, 表现还原性, 表现氧化性 表现氧化性 |
| B.撤去Ⅱ装置也能得出正确的实验结论 |
C.比较Ⅲ、Ⅳ中现象可知,在水存在下 表现漂白性 表现漂白性 |
D.若V中装酸性 溶液,可能观察到溶液褪色 溶液,可能观察到溶液褪色 |
您最近一年使用:0次
名校
解题方法
10 . 钠是一种活泼金属,其单质及化合物在科研、生产中有重要的作用。
(1)基态钠原子核外电子的空间运动状态有___________ 种。
(2)冰晶石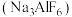 是铝电解的助熔剂,其晶胞与氯化钠的晶胞结构相似(如图所示),
是铝电解的助熔剂,其晶胞与氯化钠的晶胞结构相似(如图所示), 占据的位置相当于氯化钠晶胞中
占据的位置相当于氯化钠晶胞中 占据的位置。
占据的位置。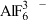 是正八面体结构,中心原子的杂化方式是
是正八面体结构,中心原子的杂化方式是___________ (填字母)。
A. B.
B. C.
C. D.
D.
② 晶体中存在的作用力有
晶体中存在的作用力有___________ (填字母)。
A.非极性共价键 B.配位键 C.范德华力 D.离子键
(3) 与
与 均为第三周期元素,
均为第三周期元素, 熔点明显高于
熔点明显高于 ,其原因是
,其原因是___________ 。
(4)硼氢化钠是一种常用的还原剂和催化剂。硼氢化钠的晶胞结构如图所示。 ,硼氢化钠溶于水的化学方程式为
,硼氢化钠溶于水的化学方程式为___________ ,硼氢化钠晶胞中与 紧邻的
紧邻的 个数是
个数是___________ 。
(5)有研究表明,在超高压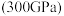 下,金属钠和氦之间可形成化合物电子盐(即电子是阴离子),在这一结构中,钠离子主要是按照简单立方排列的(如图1),并且形成
下,金属钠和氦之间可形成化合物电子盐(即电子是阴离子),在这一结构中,钠离子主要是按照简单立方排列的(如图1),并且形成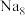 立方体空隙,电子对(2e-)和氦原子交替分布填充在立方体的中心。晶体结构俯视图如图2所示:
立方体空隙,电子对(2e-)和氦原子交替分布填充在立方体的中心。晶体结构俯视图如图2所示: 的最短距离为
的最短距离为___________  (用含a的代数式表示)。
(用含a的代数式表示)。
(1)基态钠原子核外电子的空间运动状态有
(2)冰晶石
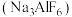 是铝电解的助熔剂,其晶胞与氯化钠的晶胞结构相似(如图所示),
是铝电解的助熔剂,其晶胞与氯化钠的晶胞结构相似(如图所示), 占据的位置相当于氯化钠晶胞中
占据的位置相当于氯化钠晶胞中 占据的位置。
占据的位置。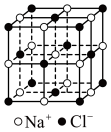
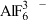 是正八面体结构,中心原子的杂化方式是
是正八面体结构,中心原子的杂化方式是A.
 B.
B. C.
C. D.
D.
②
 晶体中存在的作用力有
晶体中存在的作用力有A.非极性共价键 B.配位键 C.范德华力 D.离子键
(3)
 与
与 均为第三周期元素,
均为第三周期元素, 熔点明显高于
熔点明显高于 ,其原因是
,其原因是(4)硼氢化钠是一种常用的还原剂和催化剂。硼氢化钠的晶胞结构如图所示。
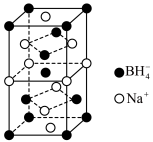
 ,硼氢化钠溶于水的化学方程式为
,硼氢化钠溶于水的化学方程式为 紧邻的
紧邻的 个数是
个数是(5)有研究表明,在超高压
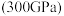 下,金属钠和氦之间可形成化合物电子盐(即电子是阴离子),在这一结构中,钠离子主要是按照简单立方排列的(如图1),并且形成
下,金属钠和氦之间可形成化合物电子盐(即电子是阴离子),在这一结构中,钠离子主要是按照简单立方排列的(如图1),并且形成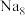 立方体空隙,电子对(2e-)和氦原子交替分布填充在立方体的中心。晶体结构俯视图如图2所示:
立方体空隙,电子对(2e-)和氦原子交替分布填充在立方体的中心。晶体结构俯视图如图2所示: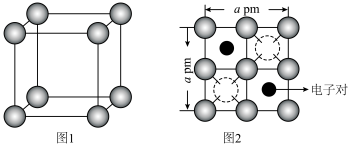
 的最短距离为
的最短距离为 (用含a的代数式表示)。
(用含a的代数式表示)。
您最近一年使用:0次



