解题方法
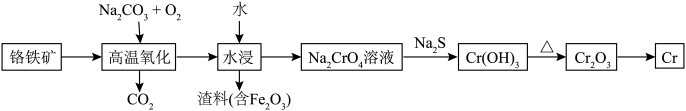
1 . 铬用于制不锈钢、汽车零件、工具、磁带和录像带等,铬铁矿炼铬过程中部分物质之间的转化关系如图。 原子的价电子排布式为
原子的价电子排布式为___________ ,最高能层上的电子占据的原子轨道轮廓图为___________ 形。
(2)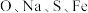 元素的电负性由小到大的顺序是
元素的电负性由小到大的顺序是___________ 。
(3) 的立体构型为
的立体构型为___________ 形,其中C的杂化轨道类型为___________ 。
(4)K和 位于同一周期,且核外最外层电子构型相同,但金属钾的熔点比金属铬低,原因为
位于同一周期,且核外最外层电子构型相同,但金属钾的熔点比金属铬低,原因为___________ 。
(5)将 糊状物用盐酸溶解,经过一系列操作可制得
糊状物用盐酸溶解,经过一系列操作可制得 晶体,已知
晶体,已知 晶体有3种不同颜色,其配位数均为6,实验测得
晶体有3种不同颜色,其配位数均为6,实验测得 不同颜色的晶体分别与足量的硝酸银溶液反应,生成沉淀的物质的量如表所示。
不同颜色的晶体分别与足量的硝酸银溶液反应,生成沉淀的物质的量如表所示。
写出浅绿色晶体配合物的化学式:___________ 。
(6) 晶体为六方晶系,结构如图所示。图中“
晶体为六方晶系,结构如图所示。图中“ ”代表
”代表___________ (填“ ”或“
”或“ ”)。已知:六棱柱底边边长为
”)。已知:六棱柱底边边长为 ,高为
,高为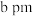 ,
, ,
,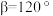 ,
, 为阿伏加德罗常数的值。
为阿伏加德罗常数的值。 晶体的密度为
晶体的密度为___________  (列出计算式即可)。
(列出计算式即可)。
 原子的价电子排布式为
原子的价电子排布式为(2)
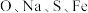 元素的电负性由小到大的顺序是
元素的电负性由小到大的顺序是(3)
 的立体构型为
的立体构型为(4)K和
 位于同一周期,且核外最外层电子构型相同,但金属钾的熔点比金属铬低,原因为
位于同一周期,且核外最外层电子构型相同,但金属钾的熔点比金属铬低,原因为(5)将
 糊状物用盐酸溶解,经过一系列操作可制得
糊状物用盐酸溶解,经过一系列操作可制得 晶体,已知
晶体,已知 晶体有3种不同颜色,其配位数均为6,实验测得
晶体有3种不同颜色,其配位数均为6,实验测得 不同颜色的晶体分别与足量的硝酸银溶液反应,生成沉淀的物质的量如表所示。
不同颜色的晶体分别与足量的硝酸银溶液反应,生成沉淀的物质的量如表所示。| 晶体颜色 | 深绿色 | 浅绿色 | 紫色 |
 沉淀的物质的量/ 沉淀的物质的量/ | 1 | 2 | 3 |
(6)
 晶体为六方晶系,结构如图所示。图中“
晶体为六方晶系,结构如图所示。图中“ ”代表
”代表 ”或“
”或“ ”)。已知:六棱柱底边边长为
”)。已知:六棱柱底边边长为 ,高为
,高为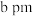 ,
, ,
,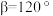 ,
, 为阿伏加德罗常数的值。
为阿伏加德罗常数的值。 晶体的密度为
晶体的密度为 (列出计算式即可)。
(列出计算式即可)。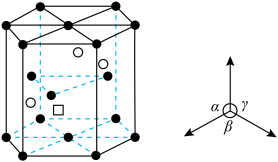
您最近一年使用:0次
解题方法
2 . 高砷烟尘(主要成分有 、PbO、
、PbO、 、ZnO、
、ZnO、 等)属于危险固体废弃物,对高砷烟尘进行综合处理回收
等)属于危险固体废弃物,对高砷烟尘进行综合处理回收 和金属铟的工业流程如下:
和金属铟的工业流程如下: 或
或 形式存在,氧化性环境中主要存在
形式存在,氧化性环境中主要存在 ;
;
② 在90℃~95℃易分解为
在90℃~95℃易分解为 ,
, 难溶于水;
难溶于水;
③ 。
。
回答下列问题:
(1)“高压酸浸”时,As的浸出率随硫酸浓度的增大而变化的曲线如图所示,硫酸浓度超过 时,As的浸出率随硫酸浓度增大而略微减小的原因可能为
时,As的浸出率随硫酸浓度增大而略微减小的原因可能为________ ,滤渣的主要成分为________ (填化学式)。 ,发生反应的离子方程式为
,发生反应的离子方程式为________ 。已知 在水溶液中电离的总反应式为
在水溶液中电离的总反应式为
 ,
, 。当“硫化”操作后溶液中
。当“硫化”操作后溶液中 ,则此时溶液的
,则此时溶液的
________ 。
(3)“还原”后溶液酸性增强,主要原因是________ (用离子方程式表示)。
(4)“结晶”操作为________ 、过滤、洗涤、干燥。
(5)“萃余液”中含有的金属阳离子为________ (填离子符号),将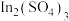 溶液电解得到金属钢,阴极的电极反应式为
溶液电解得到金属钢,阴极的电极反应式为________ 。
 、PbO、
、PbO、 、ZnO、
、ZnO、 等)属于危险固体废弃物,对高砷烟尘进行综合处理回收
等)属于危险固体废弃物,对高砷烟尘进行综合处理回收 和金属铟的工业流程如下:
和金属铟的工业流程如下:
 或
或 形式存在,氧化性环境中主要存在
形式存在,氧化性环境中主要存在 ;
;②
 在90℃~95℃易分解为
在90℃~95℃易分解为 ,
, 难溶于水;
难溶于水;③
 。
。回答下列问题:
(1)“高压酸浸”时,As的浸出率随硫酸浓度的增大而变化的曲线如图所示,硫酸浓度超过
 时,As的浸出率随硫酸浓度增大而略微减小的原因可能为
时,As的浸出率随硫酸浓度增大而略微减小的原因可能为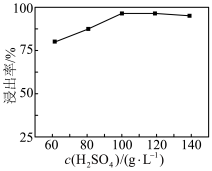
 ,发生反应的离子方程式为
,发生反应的离子方程式为 在水溶液中电离的总反应式为
在水溶液中电离的总反应式为
 ,
, 。当“硫化”操作后溶液中
。当“硫化”操作后溶液中 ,则此时溶液的
,则此时溶液的
(3)“还原”后溶液酸性增强,主要原因是
(4)“结晶”操作为
(5)“萃余液”中含有的金属阳离子为
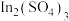 溶液电解得到金属钢,阴极的电极反应式为
溶液电解得到金属钢,阴极的电极反应式为
您最近一年使用:0次
2024-06-01更新
|
72次组卷
|
2卷引用:2024届青海省西宁市大通县高三下学期三模理科综合试题-高中化学
名校
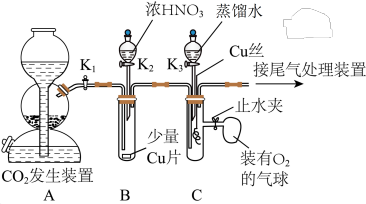
3 . 某兴趣小组设计实验验证铜与浓硝酸、稀硝酸的反应,装置如图所示(夹持装置未画出):
按图示连接好装置,_______后,装入药品,关闭 、
、 ,打开
,打开 ,一段时间后,再关闭
,一段时间后,再关闭 ,打开
,打开 ,加入足量的浓
,加入足量的浓 。
。
实验二:验证铜与稀硝酸的反应
待装置B中反应完全后……
回答下列有关问题:
(1)实验一中的横线上应填入的内容是_______ ;装置B中装浓硝酸的仪器名称是_______ 。
(2)实验一中“关闭 、
、 ,打开
,打开 ”的目的是
”的目的是_______
(3)装置B中发生反应的离子方程式为_______
(4)实验二的后续操作顺序为_______ (填标号),打开止水夹后装置C的具支试管中的现象为_______ 。
a.打开止水夹 b.打开 c.打开
c.打开 ,加入蒸馏水 d.关闭
,加入蒸馏水 d.关闭 e.插入铜丝。
e.插入铜丝。
(5)实验结束后,有同学观察到装置B中溶液呈绿色,装置C中溶液呈蓝色。小组同学认为颜色不同的原因可能如下:
猜想1:硝酸铜溶液的物质的量浓度不同,溶液颜色不同,浓度小时呈蓝色,浓度大时呈绿色。
猜想2: 溶解在硝酸铜溶液中,导致溶液颜色不同。
溶解在硝酸铜溶液中,导致溶液颜色不同。
继续实验,打开 ,一段时间后,装置B中溶液变为蓝色,说明
,一段时间后,装置B中溶液变为蓝色,说明_______ 可能成立,请设计实验验证另一猜想的可能性:_______ 。
按图示连接好装置,_______后,装入药品,关闭
 、
、 ,打开
,打开 ,一段时间后,再关闭
,一段时间后,再关闭 ,打开
,打开 ,加入足量的浓
,加入足量的浓 。
。实验二:验证铜与稀硝酸的反应
待装置B中反应完全后……
回答下列有关问题:
(1)实验一中的横线上应填入的内容是
(2)实验一中“关闭
 、
、 ,打开
,打开 ”的目的是
”的目的是(3)装置B中发生反应的离子方程式为
(4)实验二的后续操作顺序为
a.打开止水夹 b.打开
 c.打开
c.打开 ,加入蒸馏水 d.关闭
,加入蒸馏水 d.关闭 e.插入铜丝。
e.插入铜丝。(5)实验结束后,有同学观察到装置B中溶液呈绿色,装置C中溶液呈蓝色。小组同学认为颜色不同的原因可能如下:
猜想1:硝酸铜溶液的物质的量浓度不同,溶液颜色不同,浓度小时呈蓝色,浓度大时呈绿色。
猜想2:
 溶解在硝酸铜溶液中,导致溶液颜色不同。
溶解在硝酸铜溶液中,导致溶液颜色不同。继续实验,打开
 ,一段时间后,装置B中溶液变为蓝色,说明
,一段时间后,装置B中溶液变为蓝色,说明
您最近一年使用:0次
2024-06-01更新
|
353次组卷
|
4卷引用:2024届青海省海南藏族自治州高三下学期二模理综试题-高中化学
解题方法
4 . 羰基钻催化剂可在温和条件下催化氢甲酰化反应,其结构为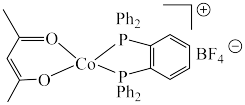 (Ph代表苯基)。回答下列问题:
(Ph代表苯基)。回答下列问题:
(2)羰基钴催化剂中位于第二周期的元素中,电负性由小到大的顺序为
 的晶体类型相同,
的晶体类型相同, 的熔点高于羰基钴催化剂的原因是
的熔点高于羰基钴催化剂的原因是(3)羰基钴催化剂阳离子中Co处于平面四边形中心,羰基钴催化剂中采取
 杂化的元素种数为
杂化的元素种数为 形成羰基钴催化剂过程中,
形成羰基钴催化剂过程中,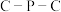 键角
键角(4)一种掺Co催化剂的晶胞结构及晶胞沿面对角线投影如下图所示。晶胞中与Co最近的氧原子所构成的几何形状为
 ,晶体的密度为
,晶体的密度为 ,则距离最近的两个氧原子间的距离为
,则距离最近的两个氧原子间的距离为 、
、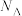 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
2024-06-01更新
|
75次组卷
|
2卷引用:2024届青海省西宁市大通县高三下学期三模理科综合试题-高中化学
名校
解题方法
5 . 为实现“碳中和”“碳达峰”,碳的循环利用是重要措施。利用氢气和CO反应生成甲烷,涉及的反应如下:
i.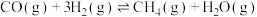

ii.

iii.

回答下列问题:
(1)在25℃和101kPa下, 转变为
转变为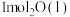 时放出44.0kJ热量,
时放出44.0kJ热量, 的燃烧热为
的燃烧热为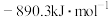 ,CO的燃烧热为
,CO的燃烧热为 ,
, 的燃烧热为
的燃烧热为 ,则
,则
________  。
。
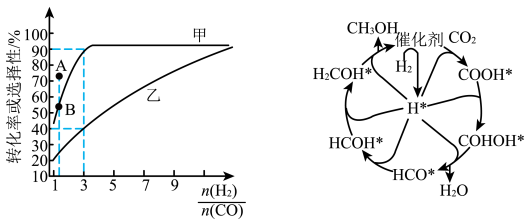
(2)一定温度下,在恒容的密闭容器中进行上述反应,平衡时CO的转化率及 的选择性随
的选择性随 变化的情况如图所示[已知
变化的情况如图所示[已知 的选择性
的选择性 ]。
]。 选择性变化的曲线是
选择性变化的曲线是________ (填“甲”或“乙”),保持 不变,曲线甲由B点达到A点需要的条件为
不变,曲线甲由B点达到A点需要的条件为________ 。
②相同温度下,向恒容容器内加入 和1molCO,初始压强为10MPa,平衡时
和1molCO,初始压强为10MPa,平衡时 的物质的量为
的物质的量为________ mol,反应ii的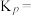
________ (保留小数点后一位)。
(3) 催化加氢制甲醇也是碳循环的重要途径。
催化加氢制甲醇也是碳循环的重要途径。 在某催化剂表面与氢气作用制备甲醇的反应机理如图所示。催化循环中产生的中间体微粒共
在某催化剂表面与氢气作用制备甲醇的反应机理如图所示。催化循环中产生的中间体微粒共________ 种, 催化加氢制甲醇总反应的化学方程式为
催化加氢制甲醇总反应的化学方程式为________ 。
i.
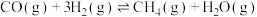

ii.


iii.


回答下列问题:
(1)在25℃和101kPa下,
 转变为
转变为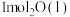 时放出44.0kJ热量,
时放出44.0kJ热量, 的燃烧热为
的燃烧热为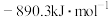 ,CO的燃烧热为
,CO的燃烧热为 ,
, 的燃烧热为
的燃烧热为 ,则
,则
 。
。(2)一定温度下,在恒容的密闭容器中进行上述反应,平衡时CO的转化率及
 的选择性随
的选择性随 变化的情况如图所示[已知
变化的情况如图所示[已知 的选择性
的选择性 ]。
]。
 选择性变化的曲线是
选择性变化的曲线是 不变,曲线甲由B点达到A点需要的条件为
不变,曲线甲由B点达到A点需要的条件为②相同温度下,向恒容容器内加入
 和1molCO,初始压强为10MPa,平衡时
和1molCO,初始压强为10MPa,平衡时 的物质的量为
的物质的量为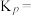
(3)
 催化加氢制甲醇也是碳循环的重要途径。
催化加氢制甲醇也是碳循环的重要途径。 在某催化剂表面与氢气作用制备甲醇的反应机理如图所示。催化循环中产生的中间体微粒共
在某催化剂表面与氢气作用制备甲醇的反应机理如图所示。催化循环中产生的中间体微粒共 催化加氢制甲醇总反应的化学方程式为
催化加氢制甲醇总反应的化学方程式为
您最近一年使用:0次
2024-06-01更新
|
209次组卷
|
7卷引用:2024届青海省西宁市大通县高三下学期三模理科综合试题-高中化学
名校
解题方法
6 . 亚硝酸钙 可用作化学合成反应中的催化剂、氧化剂、中间体等。实验室根据反应
可用作化学合成反应中的催化剂、氧化剂、中间体等。实验室根据反应 利用如下装置制备亚硝酸钙(加热及夹持装置略)。
利用如下装置制备亚硝酸钙(加热及夹持装置略)。 溶液能将NO氧化为
溶液能将NO氧化为 。
。
回答下列问题:
(1)检查装置气密性,加入相应的试剂。先通 ,其目的是
,其目的是________ 。通 后进行的操作为(i)打开管式炉,对瓷舟进行加热;(ii)……;(iii)打开
后进行的操作为(i)打开管式炉,对瓷舟进行加热;(ii)……;(iii)打开 ,使稀硝酸滴入三颈烧瓶中;(iv)关闭
,使稀硝酸滴入三颈烧瓶中;(iv)关闭 ,打开
,打开 ,通入
,通入 。操作(ii)是
。操作(ii)是________ 。
(2)仪器a的名称为________ ,装置D中盛装的试剂是________ (填名称),装置E的作用是________ 。
(3)制备的产品 样品中含有杂质
样品中含有杂质 ,通过下列方法可测定产品的纯度:称量mg样品溶于水,加
,通过下列方法可测定产品的纯度:称量mg样品溶于水,加 固体,充分振荡,过滤后将溶液转移到250mL容量瓶,配制溶液,取25mL溶液进行以下操作:
固体,充分振荡,过滤后将溶液转移到250mL容量瓶,配制溶液,取25mL溶液进行以下操作: ;“还原
;“还原 ”时加入
”时加入 的
的 标准液,“滴定剩余
标准液,“滴定剩余 ”时消耗
”时消耗 的
的 标准溶液VmL。“滴定剩余
标准溶液VmL。“滴定剩余 ”过程中发生反应的离子方程式为
”过程中发生反应的离子方程式为________ ,样品中 的纯度为
的纯度为________ (用含m、V的式子表示)。
 可用作化学合成反应中的催化剂、氧化剂、中间体等。实验室根据反应
可用作化学合成反应中的催化剂、氧化剂、中间体等。实验室根据反应 利用如下装置制备亚硝酸钙(加热及夹持装置略)。
利用如下装置制备亚硝酸钙(加热及夹持装置略)。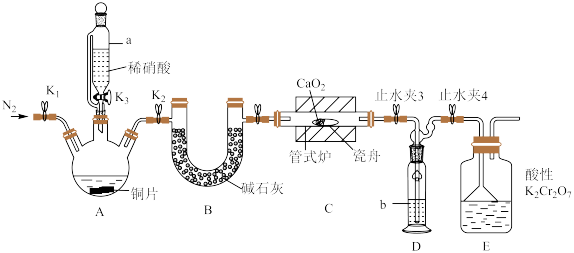
 溶液能将NO氧化为
溶液能将NO氧化为 。
。回答下列问题:
(1)检查装置气密性,加入相应的试剂。先通
 ,其目的是
,其目的是 后进行的操作为(i)打开管式炉,对瓷舟进行加热;(ii)……;(iii)打开
后进行的操作为(i)打开管式炉,对瓷舟进行加热;(ii)……;(iii)打开 ,使稀硝酸滴入三颈烧瓶中;(iv)关闭
,使稀硝酸滴入三颈烧瓶中;(iv)关闭 ,打开
,打开 ,通入
,通入 。操作(ii)是
。操作(ii)是(2)仪器a的名称为
(3)制备的产品
 样品中含有杂质
样品中含有杂质 ,通过下列方法可测定产品的纯度:称量mg样品溶于水,加
,通过下列方法可测定产品的纯度:称量mg样品溶于水,加 固体,充分振荡,过滤后将溶液转移到250mL容量瓶,配制溶液,取25mL溶液进行以下操作:
固体,充分振荡,过滤后将溶液转移到250mL容量瓶,配制溶液,取25mL溶液进行以下操作: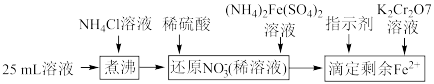
 ;“还原
;“还原 ”时加入
”时加入 的
的 标准液,“滴定剩余
标准液,“滴定剩余 ”时消耗
”时消耗 的
的 标准溶液VmL。“滴定剩余
标准溶液VmL。“滴定剩余 ”过程中发生反应的离子方程式为
”过程中发生反应的离子方程式为 的纯度为
的纯度为
您最近一年使用:0次
2024-06-01更新
|
282次组卷
|
7卷引用:2024届青海省西宁市大通县高三下学期三模理科综合试题-高中化学
解题方法
7 . 下列仪器在相应实验中选用合理的是

| A.蒸馏海水:①②③⑤ |
| B.实验室分离碘单质和氯化钠的混合物:③⑦ |
C.用碳酸钠和稀硫酸制备 :⑥ :⑥ |
D.用酸性高锰酸钾标准溶液测定溶液中 含量:④⑤ 含量:④⑤ |
您最近一年使用:0次
2024-06-01更新
|
34次组卷
|
2卷引用:2024届青海省西宁市大通县高三下学期三模理科综合试题-高中化学
8 . 科教兴国,我国科技发展在多个领域获得突破。下列说法错误的是
| A.新能源甲醇燃料电池汽车在行驶时其能量的转化形式:电能→化学能 |
| B.新一代航空发动机陶瓷基复合材料:具有耐高温、耐腐蚀特性 |
| C.利用高纯硅可以制成通信设备的芯片:高纯硅是广泛的半导体材料 |
| D.火焰喷雾技术制备纳米材料:在高温火焰喷雾中形成的胶体属于气溶胶 |
您最近一年使用:0次
2024-06-01更新
|
154次组卷
|
2卷引用:2024届青海省西宁市大通县高三下学期三模理科综合试题-高中化学
名校
9 . 一种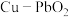 双极膜电池可长时间工作,其工作原理如图所示。已知双极膜中间层中的
双极膜电池可长时间工作,其工作原理如图所示。已知双极膜中间层中的 解离为
解离为 和
和 。下列说法错误的是
。下列说法错误的是
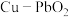 双极膜电池可长时间工作,其工作原理如图所示。已知双极膜中间层中的
双极膜电池可长时间工作,其工作原理如图所示。已知双极膜中间层中的 解离为
解离为 和
和 。下列说法错误的是
。下列说法错误的是
A.电极电势: 电极 电极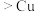 电极 电极 |
B.双极膜中 解离出的 解离出的 透过膜q向Cu电极移动 透过膜q向Cu电极移动 |
C.Cu电极的电极反应式为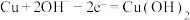 |
| D.双极膜中质量每减少18g,左侧溶液中硫酸质量减少98g |
您最近一年使用:0次
2024-06-01更新
|
187次组卷
|
7卷引用:2024届青海省西宁市大通县高三下学期三模理科综合试题-高中化学
名校
10 . 实验室制备纳米ZnO的步骤如下:
①称量10.0000g 固体于100mL小烧杯中,加50mL水溶解,配制成
固体于100mL小烧杯中,加50mL水溶解,配制成 溶液。再称量9.0000g
溶液。再称量9.0000g  固体于50mL小烧杯中,加入40mL水溶解,配制成草酸溶液。
固体于50mL小烧杯中,加入40mL水溶解,配制成草酸溶液。
②将上述两种溶液加入250mL烧杯中,搅拌2h,生成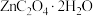 沉淀。
沉淀。
③过滤反应后的混合物,沉淀用蒸馏水洗涤干净后,在真空干燥箱中于110℃下干燥。
④干燥后的沉淀样品在氧气气氛中于350~450℃下焙烧2h,得到白色纳米ZnO。
上述实验中,下列仪器用不到的是
①称量10.0000g
 固体于100mL小烧杯中,加50mL水溶解,配制成
固体于100mL小烧杯中,加50mL水溶解,配制成 溶液。再称量9.0000g
溶液。再称量9.0000g  固体于50mL小烧杯中,加入40mL水溶解,配制成草酸溶液。
固体于50mL小烧杯中,加入40mL水溶解,配制成草酸溶液。②将上述两种溶液加入250mL烧杯中,搅拌2h,生成
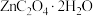 沉淀。
沉淀。③过滤反应后的混合物,沉淀用蒸馏水洗涤干净后,在真空干燥箱中于110℃下干燥。
④干燥后的沉淀样品在氧气气氛中于350~450℃下焙烧2h,得到白色纳米ZnO。
上述实验中,下列仪器用不到的是
A.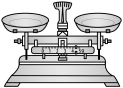 | B. | C. | D. |
您最近一年使用:0次
2024-05-30更新
|
89次组卷
|
2卷引用:2024届青海省海南藏族自治州高三下学期二模理综试题-高中化学



