1 . 异苯丙醛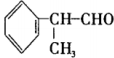 在工业上有重要用途,其合成流程如下:
在工业上有重要用途,其合成流程如下:
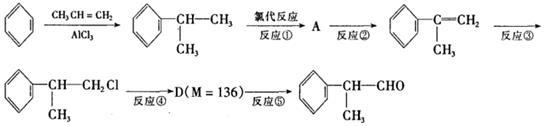
(1)异苯丙醛被酸性高锰酸钾氧化后所得有机物的结构简式是____________ 。
(2)在合成流程上②的反应类型是____________ ,反应④发生的条件是____________ ,
(3)反应⑤的化学方程式为____________ 。
(4)异苯丙醛发生银镜反应的化学方程式为__________ 。
(5)D物质与有机物X在一定条件下可生成一种相对分子质量为178的酯类物质,则X的名称是____________ 。D物质有多种同分异构体,其中满足苯环上有两个取代基,且能使FeCl3溶液显紫色的同分异构体有____________ 种。
 在工业上有重要用途,其合成流程如下:
在工业上有重要用途,其合成流程如下:
(1)异苯丙醛被酸性高锰酸钾氧化后所得有机物的结构简式是
(2)在合成流程上②的反应类型是
(3)反应⑤的化学方程式为
(4)异苯丙醛发生银镜反应的化学方程式为
(5)D物质与有机物X在一定条件下可生成一种相对分子质量为178的酯类物质,则X的名称是
您最近一年使用:0次
2 . 某化学小组为探究草酸的性质并制备草酸钠及其用途,查阅到如下信息:

探究草酸部分性质并制备草酸钠的生产流程如下:

请回答下列问题:
(1)写出反应①的化学方程式__________ 。表明草酸具有__________ 性。
(2)向溶液A中加入NaOH溶液,开始滴加速度要尽量快些.其目的是__________ 。该反应达到终点时的化学方程式为__________ 。
(3)操作②的名称是__________ 。用乙醇淋洗晶体B的目的是__________
(4)用0.01000mol/L的高锰酸钾溶液滴定25.00mL某浓度的草酸钠溶液时.需要加入适量的稀硫酸,所发生反应为:5C2O42-+2MnO4-+16H+=2Mn2++10CO2↑+8H2O,若硫酸加入太多,结果会__________ :操作中需用__________ 滴定管(填“酸式”或“碱式”),当达到反应终点时的现象是__________ ;测得此时消耗上述高锰酸钾溶液20.00mL,则该草酸钠溶液浓度为__________ mol/L。

探究草酸部分性质并制备草酸钠的生产流程如下:

请回答下列问题:
(1)写出反应①的化学方程式
(2)向溶液A中加入NaOH溶液,开始滴加速度要尽量快些.其目的是
(3)操作②的名称是
(4)用0.01000mol/L的高锰酸钾溶液滴定25.00mL某浓度的草酸钠溶液时.需要加入适量的稀硫酸,所发生反应为:5C2O42-+2MnO4-+16H+=2Mn2++10CO2↑+8H2O,若硫酸加入太多,结果会
您最近一年使用:0次
3 . 氮、磷、砷是原子序数依次增大的第VA族元素,它们的化合物有着独特的性质和重要用途。
(1)基态砷原子的核外电子排布式为________。氮、磷、砷的第一电离能顺序为__________>__________>__________(填元素符号)。
(2)已知N2O为直线形结构,结构式为N=N=O。则N2O是__________(填“极性”或“非极性”)分子。中间的氮原子的杂化轨道类型为__________杂化。
(3)已知下列数据:
NH3的熔、沸点均高于PH3的原因是__________;PH3的分解温度高于其沸点,其原因是__________。
(4)根据价层电子对互斥理论,氨分子中的键角__________(填“>”、“<”或“=”)109°28′;PO43-离子的空间构型为__________。
(5)磷化铝的结构与金刚石相似,其结构单元如图所示:

①经过计算,该晶体的化学式是__________。
②该晶体中__________(填“是”或“否”)存在配位键。
(1)基态砷原子的核外电子排布式为________。氮、磷、砷的第一电离能顺序为__________>__________>__________(填元素符号)。
(2)已知N2O为直线形结构,结构式为N=N=O。则N2O是__________(填“极性”或“非极性”)分子。中间的氮原子的杂化轨道类型为__________杂化。
(3)已知下列数据:
| 物质 | 熔点/K | 沸点/K | 分解温度/K |
| NH3 | 195.3 | 239.7 | 1073 |
| PH3 | 139.2 | 185.4 | 713.2 |
NH3的熔、沸点均高于PH3的原因是__________;PH3的分解温度高于其沸点,其原因是__________。
(4)根据价层电子对互斥理论,氨分子中的键角__________(填“>”、“<”或“=”)109°28′;PO43-离子的空间构型为__________。
(5)磷化铝的结构与金刚石相似,其结构单元如图所示:

①经过计算,该晶体的化学式是__________。
②该晶体中__________(填“是”或“否”)存在配位键。
您最近一年使用:0次
4 . 三氯化碘(ICl3)在药物合成中用途非常广泛,其熔点:33 ℃,沸点:73 ℃。实验室可用如图装置制取 ICl3。
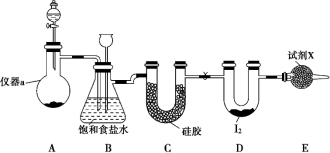
(1)仪器 a 的名称是_____ 。
(2)制备氯气选用的药品为漂白精固体[ 主要成分为 Ca(ClO)2] 和浓盐酸, 相关反应的化学方程式为______ 。
(3)装置 B 可用于除杂,也是安全瓶,能监测实验进行时装置 C 中是否发生堵塞,请写出发生堵塞时 B 中的现象是____ 。
(4)试剂 X 为_____ 。
(5)氯气与单质碘反应温度稍低于 70 ℃,则装置 D 适宜的加热方式为__ 。

(1)仪器 a 的名称是
(2)制备氯气选用的药品为漂白精固体[ 主要成分为 Ca(ClO)2] 和浓盐酸, 相关反应的化学方程式为
(3)装置 B 可用于除杂,也是安全瓶,能监测实验进行时装置 C 中是否发生堵塞,请写出发生堵塞时 B 中的现象是
(4)试剂 X 为
(5)氯气与单质碘反应温度稍低于 70 ℃,则装置 D 适宜的加热方式为
您最近一年使用:0次
2016-12-09更新
|
318次组卷
|
5卷引用:2016届海南省海南中学等七校联盟高三第一次联考化学卷
11-12高二上·四川雅安·阶段练习
5 . 铜是重要金属,Cu的化合物在科学研究和工业生产中具有许多用途,如CuSO4溶液常用作电解液、电镀液等。请回答以下问题:
(1)CuSO4可由金属铜与浓硫酸反应制备,该反应的化学方程式为_______ ;
(2)CuSO4粉末常用来检验一些有机物中的微量水分,其原因是_______ ;
(3) 的立体构型是
的立体构型是_______ ,其中S原子的杂化轨道类型是_______ ;
(4)元素金(Au)处于周期表中的第六周期,与Cu同族,Au原子最外层电子排布式为_______ ;一种铜合金晶体具有立方最密堆积的结构,在晶胞中Cu原子处于面心,Au原子处于顶点位置,则该合金中Cu原子与Au原子数量之比为_______ ;该晶体中,原子之间的作用力是_______ ;
(5)上述晶体具有储氢功能,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中。若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构为CaF2的结构相似,该晶体储氢后的化学式应为___ 。
(1)CuSO4可由金属铜与浓硫酸反应制备,该反应的化学方程式为
(2)CuSO4粉末常用来检验一些有机物中的微量水分,其原因是
(3)
 的立体构型是
的立体构型是(4)元素金(Au)处于周期表中的第六周期,与Cu同族,Au原子最外层电子排布式为
(5)上述晶体具有储氢功能,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中。若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构为CaF2的结构相似,该晶体储氢后的化学式应为
您最近一年使用:0次
2016-12-09更新
|
758次组卷
|
3卷引用:2011年普通高等学校招生全国统一考试化学(海南卷)
2011年普通高等学校招生全国统一考试化学(海南卷)(已下线)2011-2012学年四川省雅安中学高二12月月考化学试卷河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:3.3 金属晶体
2011高三上·江苏·专题练习
名校
6 . 镁及其合金是一种用途很广的金属材料,海水中镁的含量为1.10 mg·L-1,目前世界上60%的镁是从海水中提取的。主要步骤如下:

(1)为了使MgSO4完全转化为Mg(OH)2,可以加入过量试剂①,试剂①最好选用__________ 。
(2)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是
________________________________________________________________ 。
(3)试剂②可以选用________ ,其反应的离子方程式为______________________ 。
(4)无水MgCl2在熔融状态下,通电后会产生Cl2和Mg,写出该反应的化学方程式______________________________________________ 。
(5)若假设海水中镁元素全部存在于MgSO4中,则海水中MgSO4的含量为____ mg·L-1,若某工厂每天生产1.00 t镁,则每天需要海水的体积为________ L。

(1)为了使MgSO4完全转化为Mg(OH)2,可以加入过量试剂①,试剂①最好选用
(2)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是
(3)试剂②可以选用
(4)无水MgCl2在熔融状态下,通电后会产生Cl2和Mg,写出该反应的化学方程式
(5)若假设海水中镁元素全部存在于MgSO4中,则海水中MgSO4的含量为
您最近一年使用:0次
7 . 下列关于物质的用途或变化的说法正确的是
| A.耐火陶瓷可以选用熔点很高的 Al2O3等材料制作 |
| B.含量为 99.9999%的高纯硅用于制作光导纤维 |
| C.高炉炼铁可用铝热反应来迚行冶炼 |
| D.“雷雨肥田”是因为 N2与O2在放电条件下生成氮的化合物 |
您最近一年使用:0次
11-12高二上·山西晋中·期中
8 . 下列属于油脂的用途的是
①人类的营养物质②制取肥皂③制取甘油④制备汽油
①人类的营养物质②制取肥皂③制取甘油④制备汽油
| A.①②④ | B.①③⑤ | C.②③④⑤ | D.①②③ |
您最近一年使用:0次
2016-10-17更新
|
92次组卷
|
4卷引用:海南省临高县新盈中学2021-2022学年高二上学期(5-8班)期中考试化学试题
海南省临高县新盈中学2021-2022学年高二上学期(5-8班)期中考试化学试题(已下线)2011-2012年山西省平遥中学高二上学期期中考试化学(文)试卷(已下线)2014秋贵州省遵义市第四中学高二上学期期中化学(文)试卷2016-2017学年甘肃省天水一中高二上第一次月考化学卷
9 . 下列用品的主要成分及用途对应不正确的是
| A | B | C | D | |
| 用品 |  |  |  |  |
| 成分 | (NH4)2SO4 | Na2CO3 | 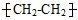 | Fe2O3 |
| 用途 | 化肥 | 制玻璃 | 盛放食品 | 涂料 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 . 材料是科学进步的关键,不同的化学物质有不同的用途。现有①氯气、②氨气、③单质硅、④水玻璃四种物质。其中可以用作制冷剂的是______________ ;常用作木材防火剂材料的是__________ ;可以用来消毒杀菌的是______________ 。(填序号)
您最近一年使用:0次



