1 . 下列方案设计、现象和结论均正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 鉴定某涂改液中是否存在含氯化合物 | 涂改液与KOH溶液混合加热,充分反应,取上层清液,加入足量稀硝酸,最后滴加硝酸银溶液 | 出现白色沉淀,说明涂改液中存在含氯化合物 |
| B | 证明非金属性 | 向装有FeS固体的试管中滴加稀盐酸 | 固体溶解,生成臭鸡蛋气味气体,证明非金属性 |
| C | 检验乙醇中是否混有乙醛 | 取待测液,滴加酸性高锰酸钾溶液 | 高锰酸钾溶液褪色,证明乙醇中混有乙醛 |
| D | 检验 样品是否变质 样品是否变质 | 将 样品溶于稀 样品溶于稀 ,滴加KSCN溶液 ,滴加KSCN溶液 | 观察到溶液变红,证明样品已氧化变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
2 . 下列实验方案能达到实验目的的是
选项 | 实验目的 | 实验方案 |
| A | 证明 沉淀可以转化为 沉淀可以转化为 | 向 溶液中先加入2滴 溶液中先加入2滴 溶液,再加入2滴 溶液,再加入2滴 溶液 溶液 |
| B | 证明 溶液中存在水解平衡 溶液中存在水解平衡 | 向滴有酚酞的 溶液中加入少量 溶液中加入少量 固体,溶液红色稍微变浅 固体,溶液红色稍微变浅 |
| C | 检验 晶体是否已氧化变质 晶体是否已氧化变质 | 将 样品溶于稀盐酸后,滴加 样品溶于稀盐酸后,滴加 溶液,观察溶液是否变红 溶液,观察溶液是否变红 |
| D | 比较 和 和 的酸性强弱 的酸性强弱 | 常温下,用pH试纸分别测定浓度均为 的 的 溶液和 溶液和 溶液的pH 溶液的pH |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
3 . 现有某KOH样品因部分变质含K2CO3。某化学课外小组的同学用滴定法测定该样品中KOH的质量分数。
【实验步骤】
Ⅰ.迅速地称取样品1.000g,溶解后准确配制成250mL溶液,备用;
Ⅱ.将0.1000mol/L标准溶液装入酸式滴定管,调零,记录起始读数V0;用碱式滴定管取25.00mL样品溶液于锥形瓶中,滴加2滴酚酞;以HCl标准溶液滴定至第一终点(此时溶质为KCl和KHCO3),记录酸式滴定管的读数V1;然后再向锥形瓶内滴加2滴甲基橙,继续用HCl标准溶液滴定至第二终点,记录酸式滴定管的读数V2。重复上述操作两次,记录数据如表:
(1)步骤Ⅰ中所需的玻璃仪器有烧杯、玻璃棒、胶头滴管、量筒和____ 。
(2)下列有关步骤Ⅰ中样品溶液的说法正确的是____ (填字母序号)。
a.样品溶液中水的电离程度比相同pH的KOH溶液中的小
b.向该溶液中滴加盐酸至第一终点时,n(Cl-)+n(CO )+n(HCO
)+n(HCO )+n(H2CO3)=n(K+)
)+n(H2CO3)=n(K+)
c.c(H+)+c(K+)=2c(CO )+c(HCO
)+c(HCO )+c(OH-)
)+c(OH-)
d.c(K+)>c(CO )>c(HCO
)>c(HCO )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
(3)滴定至第一终点的过程中,发生的离子方程式是____ 。判断滴定至第一终点的现象是:当最后半滴HCl标准溶液滴下后,____ 。
(4)样品中KOH的质量分数ω(KOH)=____ %。
(5)下列操作会导致测得的KOH质量分数偏高的是_____ (填字母序号)。
a.溶液由浅红色变为无色后继续滴加HCl至产生气泡,然后记录第一终点的读数
b.记录酸式滴定管读数V1时,仰视标准液液面
c.第一终点后继续滴定时,锥形瓶中有少许液体溅出
d.记录酸式滴定管读数V2时,仰视标准液液面
【实验步骤】
Ⅰ.迅速地称取样品1.000g,溶解后准确配制成250mL溶液,备用;
Ⅱ.将0.1000mol/L标准溶液装入酸式滴定管,调零,记录起始读数V0;用碱式滴定管取25.00mL样品溶液于锥形瓶中,滴加2滴酚酞;以HCl标准溶液滴定至第一终点(此时溶质为KCl和KHCO3),记录酸式滴定管的读数V1;然后再向锥形瓶内滴加2滴甲基橙,继续用HCl标准溶液滴定至第二终点,记录酸式滴定管的读数V2。重复上述操作两次,记录数据如表:
| 实验序号 | 1 | 2 | 3 |
| V0/mL | 0.00 | 0.00 | 0.00 |
| V1/mL | 16.73 | 16.77 | 16.75 |
| V2/mL | 17.48 | 17.52 | 17.50 |
(2)下列有关步骤Ⅰ中样品溶液的说法正确的是
a.样品溶液中水的电离程度比相同pH的KOH溶液中的小
b.向该溶液中滴加盐酸至第一终点时,n(Cl-)+n(CO
 )+n(HCO
)+n(HCO )+n(H2CO3)=n(K+)
)+n(H2CO3)=n(K+)c.c(H+)+c(K+)=2c(CO
 )+c(HCO
)+c(HCO )+c(OH-)
)+c(OH-)d.c(K+)>c(CO
 )>c(HCO
)>c(HCO )>c(OH-)>c(H+)
)>c(OH-)>c(H+)(3)滴定至第一终点的过程中,发生的离子方程式是
(4)样品中KOH的质量分数ω(KOH)=
(5)下列操作会导致测得的KOH质量分数偏高的是
a.溶液由浅红色变为无色后继续滴加HCl至产生气泡,然后记录第一终点的读数
b.记录酸式滴定管读数V1时,仰视标准液液面
c.第一终点后继续滴定时,锥形瓶中有少许液体溅出
d.记录酸式滴定管读数V2时,仰视标准液液面
您最近一年使用:0次
名校
解题方法
4 . 根据下列实验操作和实验现象,得出的实验结论正确的是
| 实验操作 | 实验现象 | 实验结论 | |
| A | 常温下,分别测定0.01mol/L的NaHSO3溶液和0.01mol/L的NaHCO3溶液的pH值 | NaHCO3的pH值大 | 非金属性:S>C |
| B | 向某钠盐中滴加稀盐酸,将产生的无色气体通入品红溶液 | 品红溶液褪色 | 该钠盐可能为Na2S2O3 |
| C | 将 样品溶于稀硫酸,滴加KSCN溶液 样品溶于稀硫酸,滴加KSCN溶液 | 溶液变红 |  样品已变质 样品已变质 |
| D | 向盛有过量AgNO3溶液的试管中滴加少量NaCl溶液,再向其中滴加Na2CrO4溶液 | 先观察到白色沉淀,后产生砖红色沉淀 | AgCl沉淀可转化为更难溶的沉淀Ag2CrO4 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-11-26更新
|
268次组卷
|
2卷引用:重庆南开中学2022-2023学年高二上学期线上教学质量诊断考试化学试题
名校
解题方法
5 . 比亚迪推出了基于磷酸亚铁锂技术的“刀片电池”,该电池能量密度大,安全性高。生产“刀片电池”需要用到FeSO4,某工业废料中主要含Fe2O3、Al2O3、SiO2 (其他成分与酸碱都不反应),某同学设计如下工艺流程从工业废料中回收绿矾

请回答:
(1)“碱浸”过程中,将工业废料粉碎的目的是___________ (写出一种)。
(2)“碱浸”时发生的离子方程式为___________ 。
(3)“提纯操作1”制取绿矾晶体需先加入少量稀硫酸,再经过___________ 、冷却结晶、过滤、洗涤、干燥。
(4)某同学为了验证某久置的FeSO4溶液是否变质,取少量待测液于试管中,加入2滴___________ 溶液,若观察到___________ ,则证明该溶液已经变质。
(5)称取1.390 0 g新制绿矾样品,以稀硫酸酸化,用0.040 0 mol·L-1的KMnO4标准液滴定至终点,消耗KMnO4标准液24.00 mL。该滴定反应的离子方程式为___________ ,取样样品的纯度为___________ (已知FeSO4·7H2O的摩尔质量为278 g·mol-1)。

请回答:
(1)“碱浸”过程中,将工业废料粉碎的目的是
(2)“碱浸”时发生的离子方程式为
(3)“提纯操作1”制取绿矾晶体需先加入少量稀硫酸,再经过
(4)某同学为了验证某久置的FeSO4溶液是否变质,取少量待测液于试管中,加入2滴
(5)称取1.390 0 g新制绿矾样品,以稀硫酸酸化,用0.040 0 mol·L-1的KMnO4标准液滴定至终点,消耗KMnO4标准液24.00 mL。该滴定反应的离子方程式为
您最近一年使用:0次
2022-03-08更新
|
233次组卷
|
4卷引用:重庆市缙云教育联盟2021-2022学年高二下学期4月质量检测化学试题
名校
解题方法
6 . 为了测定某氯化钙样品中钙元素的含量,进行如下实验(实验步骤已打乱):
①将沉淀全部放入锥形瓶中,加入足量的10% H2SO4和适量的蒸馏水,使沉淀完全溶解,溶液呈酸性,加热至75℃,趁热用0.0500mol/L KMnO4溶液进行滴定,记录所用KMnO4溶液的体积。
②过滤并洗涤沉淀。
③准确称取氯化钙样品0.2400g,放入烧杯中,加入适量6mol/L的盐酸和适量蒸馏水使样品完全溶解,再滴加35.00mL 0.2500mol/L (NH4)2C2O4溶液,水浴加热,逐渐生成CaC2O4沉淀。经检验,Ca2+已沉淀完全。
④再重复以上操作3次并进行数据处理,得出平均所用KMnO4溶液的体积为16.00mL
完成下列各题:
(1)上面的实验步骤合理的顺序是_______ 。(填序号)
(2)写出步骤①中加入KMnO4溶液后发生反应的离子方程式_______ 。
(3)滴定终点判断的依据是_______ 。
(4)某次实验滴定结束时滴定管内的液面见图,则此时液面读数为_______ mL。

(5)根据数据计算,样品中钙元素的质量分数为_______ %。(保留两位小数)
(6)同学乙重复实验,计算出的钙元素质量分数偏大,可能有的原因有_______。
①将沉淀全部放入锥形瓶中,加入足量的10% H2SO4和适量的蒸馏水,使沉淀完全溶解,溶液呈酸性,加热至75℃,趁热用0.0500mol/L KMnO4溶液进行滴定,记录所用KMnO4溶液的体积。
②过滤并洗涤沉淀。
③准确称取氯化钙样品0.2400g,放入烧杯中,加入适量6mol/L的盐酸和适量蒸馏水使样品完全溶解,再滴加35.00mL 0.2500mol/L (NH4)2C2O4溶液,水浴加热,逐渐生成CaC2O4沉淀。经检验,Ca2+已沉淀完全。
④再重复以上操作3次并进行数据处理,得出平均所用KMnO4溶液的体积为16.00mL
完成下列各题:
(1)上面的实验步骤合理的顺序是
(2)写出步骤①中加入KMnO4溶液后发生反应的离子方程式
(3)滴定终点判断的依据是
(4)某次实验滴定结束时滴定管内的液面见图,则此时液面读数为

(5)根据数据计算,样品中钙元素的质量分数为
(6)同学乙重复实验,计算出的钙元素质量分数偏大,可能有的原因有_______。
| A.酸性高锰酸钾溶液已部分变质 |
| B.滴定过程中,用蒸馏水冲洗锥形瓶内壁上的KMnO4溶液 |
| C.滴定时有部分高锰酸钾溶液滴在了实验台上 |
| D.酸式滴定管用蒸馏水洗过后又用所要盛装的溶液润洗 |
您最近一年使用:0次
2022-04-11更新
|
332次组卷
|
3卷引用:重庆市万州第二高级中学2021-2022学高二下学期入学考试化学试题
7 . 氨基甲酸铵(NH2COONH4)是一种受热易分解、易水解的白色固体,难溶于CCl4。实验室将干燥的二氧化碳和干燥的氨气通入CCl4中进行制备,化学方程式为:2NH3(g)+CO2(g)=NH2COONH4(s) △H<0。某同学从如图装置(不能重复使用)中选用一部分连接后进行实验。
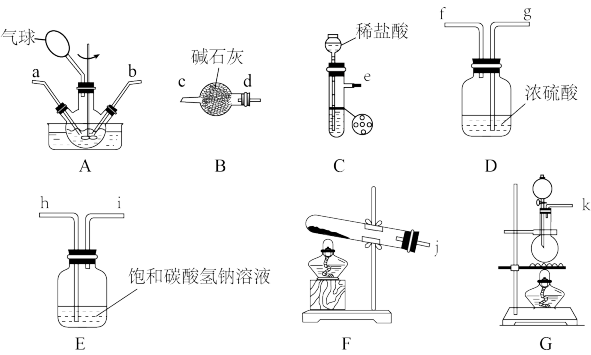
回答下列问题:
(1)氨气的发生装置可以选择图中的___ (填序号,用大写字母表示),反应的化学方程式为___ 。
(2)装置C用来制备二氧化碳气体,块状石灰石放置在试管中的带孔塑料板上。制备时,不能用稀硫酸代替稀盐酸,其原因是___ 。
(3)选择上图中的部分装置制备NH2COONH4,其连接顺序为:氨气的发生装置→__ →ab←___ ←e(按气流方向,用小写字母表示)。
(4)反应时三颈瓶需用冷水浴冷却,其目的是___ 。
(5)从装置A的混合物中分离出产品的方法是___ (填操作名称)。
(6)氨基甲酸铵因吸潮会变质为碳酸氢铵,现取部分变质后的样品11.730g,用足量石灰水充分处理后,碳元素会完全转化为碳酸钙,再过滤、洗涤、干燥、称量,质量为15.000g。则样品中氨基甲酸铵的物质的量分数 为___ %。[已知:M(NH2COONH4)=78g/mol、M(NH4HCO3)=79g/mol、M(CaCO3)=100g/mol]

回答下列问题:
(1)氨气的发生装置可以选择图中的
(2)装置C用来制备二氧化碳气体,块状石灰石放置在试管中的带孔塑料板上。制备时,不能用稀硫酸代替稀盐酸,其原因是
(3)选择上图中的部分装置制备NH2COONH4,其连接顺序为:氨气的发生装置→
(4)反应时三颈瓶需用冷水浴冷却,其目的是
(5)从装置A的混合物中分离出产品的方法是
(6)氨基甲酸铵因吸潮会变质为碳酸氢铵,现取部分变质后的样品11.730g,用足量石灰水充分处理后,碳元素会完全转化为碳酸钙,再过滤、洗涤、干燥、称量,质量为15.000g。则样品中氨基甲酸铵的
您最近一年使用:0次
8 . 无水AlCl3可用作有机合成的催化剂、食品膨松剂等。
已知:①AlCl3、FeCl3分别在183 ℃、315 ℃时升华;②无水AlCl3遇潮湿空气变质。
Ⅰ. 实验室可用下列装置制备无水AlCl3。

(1)组装好仪器后,首先应_____________ ,具体操作为_____________________
(2)装置 B中盛放饱和NaCl溶液,该装置的主要作用是__________________ 。装置C中盛放的试剂是________________ 。装置F中试剂的作用是__________ 。若用一件仪器装填适当试剂后也可起到F和G的作用,所装填的试剂为_______
(3)将所制得的无水AlCl3配制溶液时需加入盐酸的目的是_________
Ⅱ. 工业上可由铝土矿(主要成分是Al2O3和Fe2O3)和焦炭制备,流程如下:

(1)氯化炉中Al2O3、Cl2和焦炭在高温下发生反应的化学方程式为___________________
(2)700 ℃时,升华器中物质充分反应后降温实现FeCl3和AlCl3的分离。温度范围应为_______
a.低于183 ℃ b.介于183 ℃和315 ℃之间 c.高于315 ℃
(3)样品(含少量FeCl3)中AlCl3含量可通过下列操作测得(部分物质略去)。

计算该样品中AlCl3的质量分数________ (结果用m、n表示,不必化简)。
已知:①AlCl3、FeCl3分别在183 ℃、315 ℃时升华;②无水AlCl3遇潮湿空气变质。
Ⅰ. 实验室可用下列装置制备无水AlCl3。

(1)组装好仪器后,首先应
(2)装置 B中盛放饱和NaCl溶液,该装置的主要作用是
(3)将所制得的无水AlCl3配制溶液时需加入盐酸的目的是
Ⅱ. 工业上可由铝土矿(主要成分是Al2O3和Fe2O3)和焦炭制备,流程如下:

(1)氯化炉中Al2O3、Cl2和焦炭在高温下发生反应的化学方程式为
(2)700 ℃时,升华器中物质充分反应后降温实现FeCl3和AlCl3的分离。温度范围应为
a.低于183 ℃ b.介于183 ℃和315 ℃之间 c.高于315 ℃
(3)样品(含少量FeCl3)中AlCl3含量可通过下列操作测得(部分物质略去)。

计算该样品中AlCl3的质量分数
您最近一年使用:0次
名校
解题方法
9 . 活性氧化锌能对太阳光线和其他大气物质形成防护,常用于敏感皮肤的面霜和化妆品。工业上用菱锌矿(主要成分为ZnCO3,还含有Ni、Cd、Fe、Cu等元素及少量不溶于水的杂质)制备ZnO,工艺流程图所示:

(1)为了提高“溶浸”效果,可采取的措施有___________ (任写两条)。
(2)常温下Fe2+比Fe3+更容易被氧化变质,请从结构角度加以解释___________ 。
(3)“除铁”时,先加入H2O2溶液发生反应的离子方程式为___________ ;“调pH”时除ZnO外还可以选用的物质是___________ 。
a.氨水 b.氢氧化钠 c.氢氧化锌
(4)常温下pH=5时,Fe3+的浓度降到了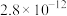 mo1/L,此时Fe(OH)3的溶度积常数的数值为
mo1/L,此时Fe(OH)3的溶度积常数的数值为___________ ,证明Fe3+已除尽的化学方法是___________ 。
(5)已知沉锌时固体产物是Zn2(OH)2CO3,写出该过程的离子方程式:___________ 。
(6)粗锌中含有少量Al、Fe、Cu等杂质,可用电解法制备高纯度锌,下列叙述正确的是___________。

(1)为了提高“溶浸”效果,可采取的措施有
(2)常温下Fe2+比Fe3+更容易被氧化变质,请从结构角度加以解释
(3)“除铁”时,先加入H2O2溶液发生反应的离子方程式为
a.氨水 b.氢氧化钠 c.氢氧化锌
(4)常温下pH=5时,Fe3+的浓度降到了
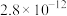 mo1/L,此时Fe(OH)3的溶度积常数的数值为
mo1/L,此时Fe(OH)3的溶度积常数的数值为(5)已知沉锌时固体产物是Zn2(OH)2CO3,写出该过程的离子方程式:
(6)粗锌中含有少量Al、Fe、Cu等杂质,可用电解法制备高纯度锌,下列叙述正确的是___________。
| A.电解过程中,阳极质量的减少与阴极质量的增加相等 |
| B.电解后,溶液中存在的金属阳离子只有Al3+、Fe2+和Zn2+ |
| C.粗锌作阳极,纯锌作阴极,电解质溶液是硫酸锌溶液 |
| D.电解后,电解槽底部的阳极泥中只有Cu |
您最近一年使用:0次
名校
解题方法
10 . 下列方案设计、现象和结论都正确的是
| 编号 | 目的 | 方案设计 | 现象和结论 |
| A | 判断淀粉是否完全水解 | 在试管中加入0.5g淀粉和 溶液,加热,冷却后,取少量水解后的溶液于试管中,加入碘水 溶液,加热,冷却后,取少量水解后的溶液于试管中,加入碘水 | 溶液显蓝色,则说明淀粉未水解 |
| B | 探究苯酚的性质 | 向苯酚浓溶液中加入少量稀溴水 | 若产生白色沉淀,则证明苯酚和稀溴水发生了反应 |
| C | 探究1-溴丙烷的消去产物具有还原性 | 向试管中注入5mL1-溴丙烷和10mL饱和氢氧化钾乙醇溶液,均匀加热,把产生的气体直接通入酸性高锰酸钾溶液中 | 若高锰酸钾溶液褪色,则证明生成了丙烯 |
| D | 检验乙醚中是否含有乙醇,向该乙醚样品中加入一小粒金属钠 | 产生无色气体 | 乙醚中含有乙醇 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-06-30更新
|
242次组卷
|
2卷引用:重庆西南大学附属中学校2022-2023学年高二下学期6月期末考试化学试题



