名校
1 . 下列说法能证明一元酸(HA)是弱电解质的是
| A.HA溶液的导电性比醋酸溶液弱。 |
| B.常温下测得0.01mol/LHA溶液的pH=2 |
| C.常温下测得NaA溶液呈碱性 |
| D.往HA溶液中滴加甲基橙,溶液显红色 |
您最近一年使用:0次
2 . 下列实验操作或现象可以达到实验目的的是
选项 | 实验目的 | 实验操作 |
A | 探究次氯酸钠溶液的酸碱性 | 用pH试纸测溶液的pH值 |
B | 证明 和 和 之间是可逆反应 之间是可逆反应 | 向   溶液中滴加 溶液中滴加  的 的 溶液,充分反应后,滴加几滴 溶液,充分反应后,滴加几滴 溶液后变为红色 溶液后变为红色 |
C | 证明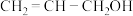 中含有碳碳双键 中含有碳碳双键 | 向酸性 溶液中加入 溶液中加入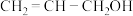 |
D | 除去 溶液中混有的 溶液中混有的 | 加入过量铁粉,充分反应后,过滤 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
3 . Ⅰ.实验室欲用NaOH固体配制490mL 0.25mol·L−1的NaOH溶液。
回答下列问题:
(1)称取NaOH质量为___________ g。
(2)在配制的过程中一定不需要使用到的仪器是___________  填字母
填字母 ,还缺少的仪器有
,还缺少的仪器有___________ (填仪器名称)
A.烧杯 B.药匙 C.玻璃棒 D.托盘天平 E.锥形瓶 F.胶头滴管
(3)下列的实验操作可能导致配制的溶液浓度偏低的是___________  填字母
填字母 。
。
A.容量瓶内原来存有少量的水未进行干燥
B. 称量固体时,所用砝码已生锈
C. NaOH固体溶解后,未冷却至室温就开始进行转移
D. 定容时仰视视刻度线
E.定容时液面超过刻度线,用胶头滴管吸出
Ⅱ.某学习小组为探究CO2与过氧化钠反应时是否需要与水接触,设计了如下实验装置
步骤1:先打开K2,关闭K1,然后打开分液漏斗活塞加入盐酸,一段时间后,将带火星的木条放在a处。
步骤2:先打开K1,关闭K2,然后打开分液漏斗活塞加入盐酸,一段时间后,将带火星的木条放在a处。
(4)装置②是为了除去CO2中的HCl气体,所选试剂是___________ (填字母)。
A.浓H2SO4 B.饱和Na2CO3溶液 C.饱和NaHCO3溶液
(5)从上述试剂中选择,装置③中的试剂是___________ (填字母),其作用为___________ 。
(6)甲同学根据实验现象认为:CO2与过氧化钠反应时需要与水接触。据此推断他观察到的步骤1和步骤2的a处的实验现象分别是___________ 。
(7)乙同学对此结论提出质疑,他认为:上述实验不足以证明“有水存在时,过氧化钠与CO2发生了化学反应”。用化学方程式表示乙同学的理由___________ 。
回答下列问题:
(1)称取NaOH质量为
(2)在配制的过程中一定不需要使用到的仪器是
 填字母
填字母 ,还缺少的仪器有
,还缺少的仪器有A.烧杯 B.药匙 C.玻璃棒 D.托盘天平 E.锥形瓶 F.胶头滴管
(3)下列的实验操作可能导致配制的溶液浓度偏低的是
 填字母
填字母 。
。A.容量瓶内原来存有少量的水未进行干燥
B. 称量固体时,所用砝码已生锈
C. NaOH固体溶解后,未冷却至室温就开始进行转移
D. 定容时仰视视刻度线
E.定容时液面超过刻度线,用胶头滴管吸出
Ⅱ.某学习小组为探究CO2与过氧化钠反应时是否需要与水接触,设计了如下实验装置

步骤1:先打开K2,关闭K1,然后打开分液漏斗活塞加入盐酸,一段时间后,将带火星的木条放在a处。
步骤2:先打开K1,关闭K2,然后打开分液漏斗活塞加入盐酸,一段时间后,将带火星的木条放在a处。
(4)装置②是为了除去CO2中的HCl气体,所选试剂是
A.浓H2SO4 B.饱和Na2CO3溶液 C.饱和NaHCO3溶液
(5)从上述试剂中选择,装置③中的试剂是
(6)甲同学根据实验现象认为:CO2与过氧化钠反应时需要与水接触。据此推断他观察到的步骤1和步骤2的a处的实验现象分别是
(7)乙同学对此结论提出质疑,他认为:上述实验不足以证明“有水存在时,过氧化钠与CO2发生了化学反应”。用化学方程式表示乙同学的理由
您最近一年使用:0次
4 . 针对表中10种元素及由这些元素形成的单质和化合物,完成以下问题。
(1)最活泼的金属元素是___________ (填元素符号),最高价氧化物对应水化物酸性最强的是___________ (填氧化物对应水化物的化学式)。
(2)用电子式表示⑤和⑨两种元素组成的化合物的形成过程___________ 。
(3)①②⑦的原子半径由大到小的顺序为___________ (填元素符号)。
(4)①和⑧非金属性比较①___________ ⑧(填>、<或=),请设计实验证明___________ (用一个化学方程式表示)。
(5)写出元素⑥的单质与元素④最高价氧化物对应水化物反应的化学方程式___________ 。
(6)为证明某溶液中不含Fe3+而可能含有Fe2+,选用下列试剂进行实验,可行的操作顺序___________。
①加入少量的氯水 ②加入少量酸性KMnO4溶液 ③加入KSCN溶液
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |
| 2 | ① | ② | ③ | ||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ |
(2)用电子式表示⑤和⑨两种元素组成的化合物的形成过程
(3)①②⑦的原子半径由大到小的顺序为
(4)①和⑧非金属性比较①
(5)写出元素⑥的单质与元素④最高价氧化物对应水化物反应的化学方程式
(6)为证明某溶液中不含Fe3+而可能含有Fe2+,选用下列试剂进行实验,可行的操作顺序___________。
①加入少量的氯水 ②加入少量酸性KMnO4溶液 ③加入KSCN溶液
| A.①③ | B.③② | C.③① | D.①② |
您最近一年使用:0次
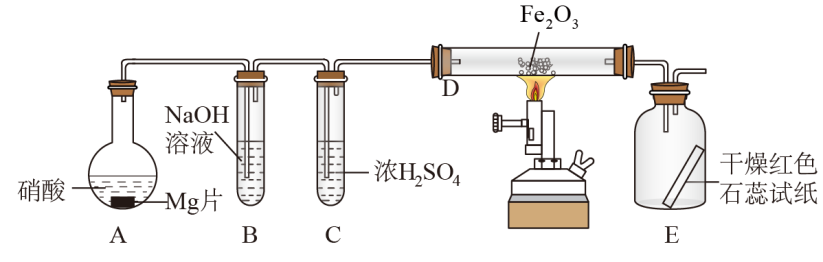
5 . 硝酸与金属反应时,浓度不同生成的还原产物也可能不同,某兴趣小组进行了如下图所示的实验探究,实验现象及相关数据如下:
②从C进入D中的气体有两种,且体积比为1∶1;
③将D加热一段时间后,E中干燥的红色石蕊试纸逐渐变蓝。(设实验前,装置中的空气已排尽;气体的体积均在同温同压下测定)
已知:2NO2+2NaOH=NaNO3+NaNO2+H2O,NO2+NO+2NaOH=2NaNO2+H2O,且水蒸气的体积忽略不计,实验中的液体药品均过量。请回答:
(1)装置中仪器A的名称___________ ;硝酸与Mg片反应生成的气体成分是___________ (用化学式表示)。
(2)硝酸在装置A的反应中所表现的性质有___________ 。
(3)利用所提供的试剂(NaNO2溶液、KMnO4溶液、KI溶液、稀硫酸、淀粉溶液)设计实验,证明B中生成的这种盐在酸性条件下具有氧化性___________ 。
(4)写出D中发生反应的化学方程式___________ 。
(5)若向反应后的A中加入足量的NaOH固体,使产生的气体全部逸出,其体积为硝酸与Mg片反应生成的气体体积的 (同温同压),写出符合上述实验事实的硝酸与Mg片反应的离子方程式
(同温同压),写出符合上述实验事实的硝酸与Mg片反应的离子方程式___________ 。
②从C进入D中的气体有两种,且体积比为1∶1;
③将D加热一段时间后,E中干燥的红色石蕊试纸逐渐变蓝。(设实验前,装置中的空气已排尽;气体的体积均在同温同压下测定)
已知:2NO2+2NaOH=NaNO3+NaNO2+H2O,NO2+NO+2NaOH=2NaNO2+H2O,且水蒸气的体积忽略不计,实验中的液体药品均过量。请回答:
(1)装置中仪器A的名称
(2)硝酸在装置A的反应中所表现的性质有
(3)利用所提供的试剂(NaNO2溶液、KMnO4溶液、KI溶液、稀硫酸、淀粉溶液)设计实验,证明B中生成的这种盐在酸性条件下具有氧化性
(4)写出D中发生反应的化学方程式
(5)若向反应后的A中加入足量的NaOH固体,使产生的气体全部逸出,其体积为硝酸与Mg片反应生成的气体体积的
 (同温同压),写出符合上述实验事实的硝酸与Mg片反应的离子方程式
(同温同压),写出符合上述实验事实的硝酸与Mg片反应的离子方程式
您最近一年使用:0次
6 . 下列对实验设计的评价错误的是
| 选项 | 实验设计 | 实验评价 |
| A. | 将含有二氧化硫的气体通入酸性高锰酸钾中,然后加入足量氯化钡溶液。通过测定白色沉淀的质量,可推算二氧化硫的物质的量 | 不合理,酸性高锰酸钾中的稀硫酸会与氯化钡产生沉淀 |
| B. | 实验室用浓硫酸和乙醇制取乙烯时,若要检验所得气体含有CH2=CH2,可将混合气体干燥后,通入溴的四氯化碳溶液中。若溶液褪色,则证明有乙烯 | 合理,混合气体中,只有乙烯可使溴的四氯化碳溶液褪色 |
| C. | 常温下,用pH计分别测定等体积 CH3COONH4溶液和 CH3COONH4溶液和 CH3COONH4溶液的pH.通过比较pH值,探究浓度对水的电离程度的影响 CH3COONH4溶液的pH.通过比较pH值,探究浓度对水的电离程度的影响 | 合理 |
| D. | 探究浓度对反应速率的影响,向2支盛有5mL不同浓度NaHSO3溶液的试管中同时加入2mL5%H2O2溶液。通过观察现象,探究浓度对反应速率的影响 | 不合理,该实验无明显现象 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-16更新
|
425次组卷
|
3卷引用:2024届四川省雅安市天全中学高三下学期模拟预测化学试题
名校
7 . 硫脲 是一种杀菌剂。某小组设计实验制备硫脲并探究其性质。
是一种杀菌剂。某小组设计实验制备硫脲并探究其性质。
实验(一):制备硫脲。装置如图所示(加热装置已省略)。

已知:① ;
;
②25℃时硫脲溶解度为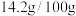 水;
水;
③实验室常用FeS与稀 在常温下制
在常温下制 。
。
(1)盛放石灰乳的仪器的名称是_______ ,B的加热方式宜选择_______ (填标号)。
a.直接用酒精灯加热 b.油浴加热(100~250℃) c.热水浴加热
(2)当C装置中出现_______ (填实验现象)时表明B中生成了 。
。
(3)实验发现,硫脲产率与投料比 的关系如图所示。
的关系如图所示。
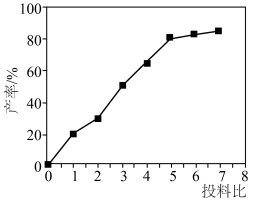
最佳投料比为_______ 。
实验(二):探究硫脲的性质。
资料显示:①150℃时 转化成
转化成 。
。
②酸性 溶液和硫脲反应,还原产物为
溶液和硫脲反应,还原产物为 ,氧化产物为
,氧化产物为 和
和 。
。
(4)取少量 溶于水,加热至150℃,一段时间后再冷却至室温时,滴加
溶于水,加热至150℃,一段时间后再冷却至室温时,滴加_______ ,可检验是否有 生成。
生成。
(5)取少量 溶于NaOH溶液,加入
溶于NaOH溶液,加入 溶液,过滤、洗涤,得到黑色固体,由此推知,
溶液,过滤、洗涤,得到黑色固体,由此推知, 在碱性条件下会生成
在碱性条件下会生成_______ (填离子符号)。
(6)甲同学取少量 溶于水,滴加几滴酸性
溶于水,滴加几滴酸性 溶液,振荡,溶液褪色;再滴加
溶液,振荡,溶液褪色;再滴加 和盐酸溶液,产生白色沉淀。
和盐酸溶液,产生白色沉淀。
①乙同学认为甲同学的实验不能证明生成了 ,理由是
,理由是_______ 。
②乙同学设计如图装置验证氧化产物中含有 。
。
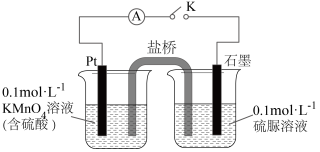
关闭K,发现电流计指针偏转。一段时间后,左烧杯中酸性高锰酸钾溶液褪色。铂电极上的反应式为_______ ,经检验石墨电极附近还有 和
和 生成,总反应的离子方程式为
生成,总反应的离子方程式为_______ 。
 是一种杀菌剂。某小组设计实验制备硫脲并探究其性质。
是一种杀菌剂。某小组设计实验制备硫脲并探究其性质。实验(一):制备硫脲。装置如图所示(加热装置已省略)。

已知:①
 ;
;②25℃时硫脲溶解度为
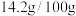 水;
水;③实验室常用FeS与稀
 在常温下制
在常温下制 。
。(1)盛放石灰乳的仪器的名称是
a.直接用酒精灯加热 b.油浴加热(100~250℃) c.热水浴加热
(2)当C装置中出现
 。
。(3)实验发现,硫脲产率与投料比
 的关系如图所示。
的关系如图所示。
最佳投料比为
实验(二):探究硫脲的性质。
资料显示:①150℃时
 转化成
转化成 。
。②酸性
 溶液和硫脲反应,还原产物为
溶液和硫脲反应,还原产物为 ,氧化产物为
,氧化产物为 和
和 。
。(4)取少量
 溶于水,加热至150℃,一段时间后再冷却至室温时,滴加
溶于水,加热至150℃,一段时间后再冷却至室温时,滴加 生成。
生成。(5)取少量
 溶于NaOH溶液,加入
溶于NaOH溶液,加入 溶液,过滤、洗涤,得到黑色固体,由此推知,
溶液,过滤、洗涤,得到黑色固体,由此推知, 在碱性条件下会生成
在碱性条件下会生成(6)甲同学取少量
 溶于水,滴加几滴酸性
溶于水,滴加几滴酸性 溶液,振荡,溶液褪色;再滴加
溶液,振荡,溶液褪色;再滴加 和盐酸溶液,产生白色沉淀。
和盐酸溶液,产生白色沉淀。①乙同学认为甲同学的实验不能证明生成了
 ,理由是
,理由是②乙同学设计如图装置验证氧化产物中含有
 。
。
关闭K,发现电流计指针偏转。一段时间后,左烧杯中酸性高锰酸钾溶液褪色。铂电极上的反应式为
 和
和 生成,总反应的离子方程式为
生成,总反应的离子方程式为
您最近一年使用:0次
2024-04-01更新
|
240次组卷
|
2卷引用:四川省雅安市雅安中学等校联考2023-2024学年高三下学期开学考试理综试题-高中化学
名校
解题方法
8 . 某化学课外兴趣小组用如图所示装置进行实验,制备某气体并验证其性质。请回答下列问题:
①装置A中发生反应的化学方程式为___________ 。
②实验中,取一定质量的铜片和一定体积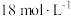 的浓硫酸在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
的浓硫酸在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
A.有一定量的余酸但未能使铜片完全溶解,你认为原因是___________ 。
B.下列药品中能用来证明反应结束后的烧瓶中确有余酸的是___________ (填标号)。
a.铁粉 b. 溶液 c.银粉 d.
溶液 c.银粉 d. 溶液
溶液
(2)若装置A中分液漏斗盛装浓硫酸,圆底烧瓶盛装木炭。
①装置A中发生反应的化学方程式为___________ 。
②设计实验证明装置C中含有 时,所需的试剂有
时,所需的试剂有___________ (填标号)。
a. 溶液 b.澄清石灰水 c.品红溶液 d.酸性
溶液 b.澄清石灰水 c.品红溶液 d.酸性 溶液
溶液
(3)若装置A中分液漏斗盛装浓盐酸,圆底烧瓶盛装 粉末。
粉末。
①装置B的作用是贮存多余的气体。当D处有明显的现象后,关闭止水夹K并移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B中现象是___________ 。
②D中品红溶液褪色,加热试管里已褪色溶液时的现象为___________ 。
(4)装置D中试管口放置的棉花中浸了一种液体,可适用于(1)(2)(3)小题中实验,该液体是___________ 。
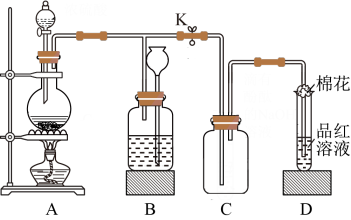
①装置A中发生反应的化学方程式为
②实验中,取一定质量的铜片和一定体积
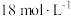 的浓硫酸在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
的浓硫酸在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。A.有一定量的余酸但未能使铜片完全溶解,你认为原因是
B.下列药品中能用来证明反应结束后的烧瓶中确有余酸的是
a.铁粉 b.
 溶液 c.银粉 d.
溶液 c.银粉 d. 溶液
溶液(2)若装置A中分液漏斗盛装浓硫酸,圆底烧瓶盛装木炭。
①装置A中发生反应的化学方程式为
②设计实验证明装置C中含有
 时,所需的试剂有
时,所需的试剂有a.
 溶液 b.澄清石灰水 c.品红溶液 d.酸性
溶液 b.澄清石灰水 c.品红溶液 d.酸性 溶液
溶液(3)若装置A中分液漏斗盛装浓盐酸,圆底烧瓶盛装
 粉末。
粉末。①装置B的作用是贮存多余的气体。当D处有明显的现象后,关闭止水夹K并移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B中现象是
②D中品红溶液褪色,加热试管里已褪色溶液时的现象为
(4)装置D中试管口放置的棉花中浸了一种液体,可适用于(1)(2)(3)小题中实验,该液体是
您最近一年使用:0次
2024-03-13更新
|
410次组卷
|
4卷引用:四川省雅安市天全中学2024届高三下学期模拟预测化学试题4
9 . 人类对氯的认识经历了漫长的过程。回答下列问题:
(1)18世纪70年代,瑞典化学家舍勒将软锰矿(主要成分是MnO2)与浓盐酸混合加热,首次制得Cl2,该反应的离子方程式是___________ 。
(2)1785年,贝托雷最早利用氯气的水溶液做漂白剂,可以永久性地漂白纸张和鲜花,且在阳光下能够分解产生氧气。某实验小组利用如下实验装置探究氯气是否具有漂白性。___________ ,装置接口的连接顺序是a→______→______→______→______→f。___________
②装置乙中的试剂Y是___________ 。
③实验开始后,关闭装置乙中的开关K,观察到干燥有色布条___________ (填“褪色”或“不褪色”);打开开关K,观察到干燥有色布条___________ (填“褪色”或“不褪色”),证明氯气没有漂白性,但氯气与水反应的产物___________ 具有漂白性。
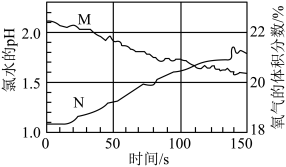
④实验小组利用数字传感器测定广口瓶中的氯水在光照条件下的pH和瓶中氧气的体积分数变化曲线如下图所示,其中表示氯水的pH变化的曲线是___________ (填“M”或“N”),据此分析,此时广口瓶中发生反应的化学方程式是___________ 。___________ 。
(1)18世纪70年代,瑞典化学家舍勒将软锰矿(主要成分是MnO2)与浓盐酸混合加热,首次制得Cl2,该反应的离子方程式是
(2)1785年,贝托雷最早利用氯气的水溶液做漂白剂,可以永久性地漂白纸张和鲜花,且在阳光下能够分解产生氧气。某实验小组利用如下实验装置探究氯气是否具有漂白性。

②装置乙中的试剂Y是
③实验开始后,关闭装置乙中的开关K,观察到干燥有色布条
④实验小组利用数字传感器测定广口瓶中的氯水在光照条件下的pH和瓶中氧气的体积分数变化曲线如下图所示,其中表示氯水的pH变化的曲线是
您最近一年使用:0次
2024-01-24更新
|
46次组卷
|
2卷引用:四川省雅安市天立学校2023-2024学年高一上学期第三次教学质量检测化学试题
名校
10 . 根据下列实验操作与现象所得出的结论正确的是
| 选项 | 实验操作与现象 | 结论 |
| A | 向Fe(NO3)2溶液中滴入硫酸酸化的H2O2溶液,溶液由浅绿色变为黄色 | 氧化性:H2O2>>Fe2+ |
| B | 向4mL0.1mol/LK2CrO4溶液中缓慢滴加1molL稀硫酸,溶液由黄色变为橙色 | 增大c(H+)有利于 转化为 转化为 |
| C | 等体积pH=2的HX和HY两种酸溶液分别与足量的锌粒反应,用排水法收集气体,HX溶液放出的氢气多且反应速率快 | 证明HX的酸性比HY强 |
| D | 室温下,向浓度均为0.05mol/L的NaI和NaCl的混合溶液中滴加少量AgNO3溶液,有黄色沉淀生成 | Ksp(AgI)>Ksp(AgCI) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



