名校
解题方法
1 . 甘氨酸亚铁[ (H2NCH2COO)2Fe]是一种补血剂,工业上用赤铁矿(含少量铝、铜、硅、锰的氧化物)制备甘氨酸亚铁的流程图如下:
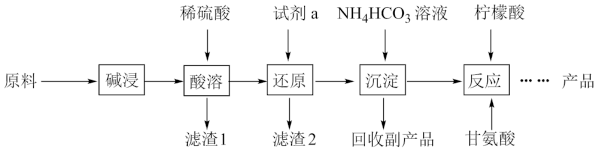
已知:甘氨酸(H2NCH2COOH),易溶于水,微溶于乙醇,具有两性。
回答下列问题:
(1)“碱浸”去除的元素是_________ , “滤渣1”是_________ (填化学式)
(2)“'还原”时的还原产物是_________ 。
(3)“沉淀”的离子方程式_________ ,“副产品”是_________ (写名称)
(4)柠檬酸的作用防止Fe2+氧化,“反应”的化学方程式为_________ 。
(5)FeSO4·7H2O也是一种常用的补血剂, 在空气中易变质,检验其是否变质的试剂是_________ ,某同学通过如下实验测定该补血剂中Fe2+的含量:
①配制:用分析天平称取1. 4000gFeSO4·7H2O样品,再用煮沸并冷却的蒸馏水配制100mL溶液。配制时还需要的定量仪器是_________ 。
②滴定:用酸化的KMnO4溶液滴定
用移液管移取25. 00mLFeSO4溶液于锥形瓶中,用0. 0100mol·L-1的KMnO4,溶液滴定,平行滴定3次,KMnO4溶液的平均用量为24. 00mL,则样品Fe2+的含量为________ % (保留2位小数) 。

已知:甘氨酸(H2NCH2COOH),易溶于水,微溶于乙醇,具有两性。
回答下列问题:
(1)“碱浸”去除的元素是
(2)“'还原”时的还原产物是
(3)“沉淀”的离子方程式
(4)柠檬酸的作用防止Fe2+氧化,“反应”的化学方程式为
(5)FeSO4·7H2O也是一种常用的补血剂, 在空气中易变质,检验其是否变质的试剂是
①配制:用分析天平称取1. 4000gFeSO4·7H2O样品,再用煮沸并冷却的蒸馏水配制100mL溶液。配制时还需要的定量仪器是
②滴定:用酸化的KMnO4溶液滴定
用移液管移取25. 00mLFeSO4溶液于锥形瓶中,用0. 0100mol·L-1的KMnO4,溶液滴定,平行滴定3次,KMnO4溶液的平均用量为24. 00mL,则样品Fe2+的含量为
您最近一年使用:0次
2022-08-08更新
|
996次组卷
|
7卷引用:宁夏回族自治区中卫市中宁县第一中学2022-2023学年高三上学期10月月考化学试题
宁夏回族自治区中卫市中宁县第一中学2022-2023学年高三上学期10月月考化学试题四川省达州市2021-2022学年高三上学期第一次诊断考试理科综合化学试题四川省达州市普通高中2022届高三第一次诊断性测试理综化学试题(已下线)专题讲座(八) 无机化工流程题的解题策略(讲)-2023年高考化学一轮复习讲练测(全国通用)内蒙古自治区霍林郭勒市第一中学2022-203学年高三上学期9月月考化学试题四川省资中县球溪高级中学2022-2023学年高三上学期10月月考化学试题(已下线)易错点06 铁及其化合物-备战2023年高考化学考试易错题
2 . 由实验操作和现象,可得出相应正确结论的是
| 实验操作 | 现象 | 结论 | |
| A | 蘸取待测液在火焰上灼烧 | 观察到黄色火焰 | 有Na+无K+ |
| B | 向NaBr溶液中滴加过量氯水,再加入淀粉KI溶液 | 先变橙色,后变蓝色 | 氧化性:Cl2>Br2>I2 |
| C | 将铁锈溶于浓盐酸,滴入KMnO4溶液 | 溶液紫色褪去 | 铁锈中含有二价铁 |
| D | 取少量Na2SO3待测样品溶于蒸馏水,加入足量稀盐酸,再加入足量BaCl2溶液 | 有白色沉淀产生 | 样品已经变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-11-22更新
|
105次组卷
|
2卷引用:宁夏银川市第二中学2022-2023学年高三上学期统练三化学试题
名校
3 . 锶(Sr)和镁位于同主族,锶比镁更活泼,锶与氮气在加热条件下反应产生氮化锶,已知氮化锶遇水剧烈反应。某同学设计如下装置制备氮化锶。

方案Ⅰ:制备氮气来制取氮化锶
(1)仪器A的名称是___________ 。
(2)实验时先点燃___________ 处酒精灯(填“B”或“C”),一段时间后,再点燃另一只酒精灯。
(3)方案Ⅰ中用饱和氯化铵溶液和亚硝酸钠溶液共热制备氮气,其化学方程式为:___________ 。
方案II:利用工业氮气样品来制取氮化锶
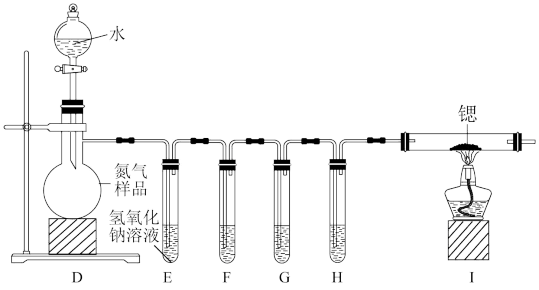
已知:①所使用的氮气样品可能含有少量CO、CO2、O2等气体杂质。
②醋酸二氨合亚铜CH3COO[Cu(NH3)2]溶液能定量吸收CO,但易被O2氧化,失去吸收CO能力;连苯三酚碱性溶液能定量吸收O2。
(4)打开分液漏斗的旋塞,装置D能持续提供N2,这是利用了N2___________ 的物理性质。
(5)装置F、G、H盛装的试剂分别是___________ (填代号)。
甲:浓硫酸 乙:连苯三酚碱性溶液 丙:醋酸二氨合亚铜溶液
(6)所有的安全问题都要“小题大做”,锶一旦失火,下列可用于的灭火的是__________
A.泡沫灭火器 B.碳酸氢钠干粉灭火器(利用CO2或N2作推动力) C.干冰灭火器 D.干燥的沙土 E.自来水 F.潮湿的抹布
(7)方案Ⅰ和方案II存在相同的缺陷,可能会导致产品变质,改进方案为:____________ 。

方案Ⅰ:制备氮气来制取氮化锶
(1)仪器A的名称是
(2)实验时先点燃
(3)方案Ⅰ中用饱和氯化铵溶液和亚硝酸钠溶液共热制备氮气,其化学方程式为:
方案II:利用工业氮气样品来制取氮化锶

已知:①所使用的氮气样品可能含有少量CO、CO2、O2等气体杂质。
②醋酸二氨合亚铜CH3COO[Cu(NH3)2]溶液能定量吸收CO,但易被O2氧化,失去吸收CO能力;连苯三酚碱性溶液能定量吸收O2。
(4)打开分液漏斗的旋塞,装置D能持续提供N2,这是利用了N2
(5)装置F、G、H盛装的试剂分别是
甲:浓硫酸 乙:连苯三酚碱性溶液 丙:醋酸二氨合亚铜溶液
(6)所有的安全问题都要“小题大做”,锶一旦失火,下列可用于的灭火的是
A.泡沫灭火器 B.碳酸氢钠干粉灭火器(利用CO2或N2作推动力) C.干冰灭火器 D.干燥的沙土 E.自来水 F.潮湿的抹布
(7)方案Ⅰ和方案II存在相同的缺陷,可能会导致产品变质,改进方案为:
您最近一年使用:0次
2022-01-01更新
|
247次组卷
|
2卷引用:宁夏银川一中2021-2022学年高三上学期第五次月考理综化学试题
名校
解题方法
4 . 锶(Sr)和镁位于同主族,锶比镁更活泼,锶与氮气在加热条件下反应产生氮化锶,已知氮化锶遇水剧烈反应。某同学设计如下装置制备氮化锶(Sr3N2相对分子质量:290.8)。
方案Ⅰ:制备氮气来制取氮化锶
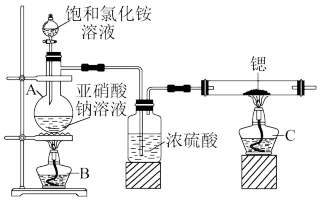
(1)仪器 A 的名称是_____ 。
(2)实验时先点燃_____ 处酒精灯(填“B”或“C”),一段时间后,再点燃另一只酒精灯。
(3)方案Ⅰ中用饱和氯化铵溶液和亚硝酸钠溶液共热制备氮气,其化学方程式为:_____ 。
方案 II:利用氮气样品来制取氮化锶
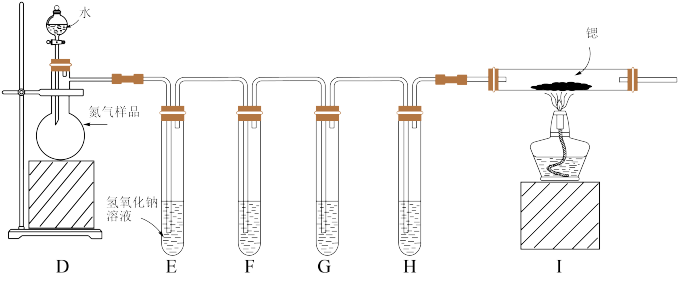
已知:① 所使用的氮气样品可能含有少量 CO、CO2、O2等气体杂质。
② 醋酸二氨合亚铜 CH3COO[Cu(NH3)2]溶液能定量吸收 CO,但易被 O2氧化, 失去吸收 CO 能力;连苯三酚碱性溶液能定量吸收 O2。
(4)打开分液漏斗的旋塞,装置 D 能持续提供 N2,这是利用了 N2_____ 的物理性质。
(5)装置 F、G、H 盛装的试剂分别是_____ (填代号)。
甲 浓硫酸 乙 连苯三酚碱性溶液 丙 醋酸二氨合亚铜溶液
(6)方案Ⅰ和方案 II 设计存在相同的缺陷,可能会导致产品变质,提出改进方案为:_____ 。
(7)产品纯度的测定:称取 0.8000 g 方案Ⅰ中所得产品,加入干燥的三颈瓶中,加入蒸馏水,并通入足量水蒸气,将产生的氨全部蒸出,用 20.00 mL 1.00mol/L 的盐酸标准溶液完全吸收,再用 1.00 mol/LNaOH 标准溶液滴定过剩的 HCl,到终点时消耗 16.00mLNaOH 溶液。则产品纯度为_____ (计算结果保留 4 位有效数字)。
方案Ⅰ:制备氮气来制取氮化锶

(1)仪器 A 的名称是
(2)实验时先点燃
(3)方案Ⅰ中用饱和氯化铵溶液和亚硝酸钠溶液共热制备氮气,其化学方程式为:
方案 II:利用氮气样品来制取氮化锶

已知:① 所使用的氮气样品可能含有少量 CO、CO2、O2等气体杂质。
② 醋酸二氨合亚铜 CH3COO[Cu(NH3)2]溶液能定量吸收 CO,但易被 O2氧化, 失去吸收 CO 能力;连苯三酚碱性溶液能定量吸收 O2。
(4)打开分液漏斗的旋塞,装置 D 能持续提供 N2,这是利用了 N2
(5)装置 F、G、H 盛装的试剂分别是
甲 浓硫酸 乙 连苯三酚碱性溶液 丙 醋酸二氨合亚铜溶液
(6)方案Ⅰ和方案 II 设计存在相同的缺陷,可能会导致产品变质,提出改进方案为:
(7)产品纯度的测定:称取 0.8000 g 方案Ⅰ中所得产品,加入干燥的三颈瓶中,加入蒸馏水,并通入足量水蒸气,将产生的氨全部蒸出,用 20.00 mL 1.00mol/L 的盐酸标准溶液完全吸收,再用 1.00 mol/LNaOH 标准溶液滴定过剩的 HCl,到终点时消耗 16.00mLNaOH 溶液。则产品纯度为
您最近一年使用:0次
2020-09-04更新
|
687次组卷
|
8卷引用:宁夏银川一中2021届高三第三次月考理综化学试题
名校
解题方法
5 . 砂质土壤分析中常用 Karl Fischer法是测定其中微量水含量,该方法是利用I2和SO2反应定量消耗水作为原理(假设土壤中其他成分不参加反应),据此回答下列问题:
(1)写出该反应的化学反应方程式为_________________________________ 。
步骤Ⅰ:反应样品中的水
下图是某同学在实验室模拟Karl Fischer法的实验装置图:

(2)装置连接的顺序为a→____________ (填接口字母顺序);M仪器的名称为_____________ ,其在实验过程中的作用是________________________________ ;
(3)操作步骤为:①连接装置并检查装置气密性,②装入药品,____________________ ;③关闭弹簧夹,打开分液漏斗活塞;④反应结束后,关闭分液漏斗活塞,继续通入N2,⑤取下D装置。
步骤④中继续通入N2的目的是___________________________________________
步骤Ⅱ:测定剩余的碘
向反应后的D装置加入蒸馏水,过滤,充分洗涤,并合并洗涤液和滤液,将其配成250.00 mL溶液,取25.00mL 用0.20 mol·L-1 Na2S2O3标准液滴定剩余的I2单质,已知反应如下:2 +I2=
+I2= +2I-。
+2I-。
(4)将Na2S2O3标准液装在______ (填“酸式”“碱式”)滴定管中,调整液面后开始滴定;
(5)滴定实验重复四次得到数据如下:
①若实验开始时,向D 装置中加入10.00 g土壤样品和10.16g I2(已知I2过量),则样品土壤中水的含量为_________ %。
②若Na2S2O3标准液已部分氧化变质,则水含量测定结果将________ (填“偏高”“偏低”或“不变”)。
(1)写出该反应的化学反应方程式为
步骤Ⅰ:反应样品中的水
下图是某同学在实验室模拟Karl Fischer法的实验装置图:

(2)装置连接的顺序为a→
(3)操作步骤为:①连接装置并检查装置气密性,②装入药品,
步骤④中继续通入N2的目的是
步骤Ⅱ:测定剩余的碘
向反应后的D装置加入蒸馏水,过滤,充分洗涤,并合并洗涤液和滤液,将其配成250.00 mL溶液,取25.00mL 用0.20 mol·L-1 Na2S2O3标准液滴定剩余的I2单质,已知反应如下:2
 +I2=
+I2= +2I-。
+2I-。(4)将Na2S2O3标准液装在
(5)滴定实验重复四次得到数据如下:
| 实验 | ① | ② | ③ | ④ |
| 消耗的标准液的体积/mL | 18.37 | 20.05 | 19.95 | 20.00 |
②若Na2S2O3标准液已部分氧化变质,则水含量测定结果将
您最近一年使用:0次
名校
6 . 下列有关实验说法,正确的是
| A.某溶液加强碱并加热,产生使湿润的红色石蕊试纸变蓝的气体,则该溶液溶质为铵盐 |
| B.将硝酸亚铁样品溶于稀硫酸,滴加硫氰化钾溶液,溶液变为血红色,可推知该样品已经氧化变质 |
| C.往含有FeBr2和FeI2的混合溶液中通入足量的氯气,然后把溶液蒸干,得到FeCl3固体 |
| D.向含有酚酞的Na2CO3溶液中加入少量BaCl2固体,溶液红色变浅,证明Na2CO3溶液中存在水解平衡 |
您最近一年使用:0次
2020-07-12更新
|
160次组卷
|
2卷引用:宁夏固原市隆德县中学2021届高三上学期第二次月考化学试题
名校
解题方法
7 . 三氯化铬(CrCl3)为紫色单斜晶体,熔点为83 ℃,易潮解,易升华,能溶于水但不易水解,高温下能被氧气氧化,工业上主要用作媒染剂和催化剂。在实验室中利用Cr2O3与CCl4反应制备无水CrCl3,并收集该反应产生的光气(COCl2),实验装置如图所示(夹持、加热及部分冷却装置已省略)。
实验步骤如下:

Ⅰ.检查完装置气密性后,按照图示装入药品,打开K1、K2、K3,通入氮气。
Ⅱ.一段时间后,关闭K3,将装置B加热到预定温度,再将装置A在85 ℃下进行水浴加热。
Ⅲ.待装置B中反应结束后,装置A、B停止加热;一段时间后,停止通入氮气。
Ⅳ.将装置C在30 ℃下进行加热,得到产物和光气。
已知:ⅰ.光气能溶于CCl4,易与水发生反应生成CO2和HCl。
ⅱ.有关物质的熔、沸点如下表:
回答下列问题:
(1)仪器d中盛有无水CaCl2固体,其作用为___________ ;若无仪器d和后续装置,仪器b的上管口可能出现的现象为___________ 。
(2)通入N2除起到将装置内空气排出的作用外,还具有的作用为___________ (写一条即可)。
(3)步骤Ⅳ中,将光气分离出的操作名称为___________ ;
(4)B中得到产品的化学方程式为___________ 。
(5)光气剧毒,该实验中用NaOH溶液吸收逸出的少量光气。也可以用乙醇处理COCl2,生成一种含氧酸酯(C2H5OCOOC2H5),用乙醇处理光气的化学方程式为___________ 。
(6)样品中三氯化铬质量分数的测定
称取样品0.3300g,加水溶解并定容于250mL容量瓶中。移取25.00mL于碘量瓶(一种带塞的锥形瓶)中,加热至沸后加入1gNa2O2,充分加热煮沸,适当稀释,然后加入过量的2mol/LH2SO4至溶液呈强酸性,此时铬以Cr2O 存在,再加入1.1gKI,密塞,摇匀,于暗处静置5分钟后,加入1mL指示剂,用0.0250mol/L硫代硫酸钠溶液滴定至终点,平行测定三次,平均消耗标准硫代硫酸钠溶液24.00mL。
存在,再加入1.1gKI,密塞,摇匀,于暗处静置5分钟后,加入1mL指示剂,用0.0250mol/L硫代硫酸钠溶液滴定至终点,平行测定三次,平均消耗标准硫代硫酸钠溶液24.00mL。
已知:Cr2O +6I-+14H+=2Cr3++3I2+7H2O,2Na2S2O3+I2=Na2S4O6+2NaI。
+6I-+14H+=2Cr3++3I2+7H2O,2Na2S2O3+I2=Na2S4O6+2NaI。
①该实验可选用的指示剂名称为___________ 。
②样品中无水三氯化铬的质量分数为___________ 。
实验步骤如下:

Ⅰ.检查完装置气密性后,按照图示装入药品,打开K1、K2、K3,通入氮气。
Ⅱ.一段时间后,关闭K3,将装置B加热到预定温度,再将装置A在85 ℃下进行水浴加热。
Ⅲ.待装置B中反应结束后,装置A、B停止加热;一段时间后,停止通入氮气。
Ⅳ.将装置C在30 ℃下进行加热,得到产物和光气。
已知:ⅰ.光气能溶于CCl4,易与水发生反应生成CO2和HCl。
ⅱ.有关物质的熔、沸点如下表:
| 化学式 | Cr2O3 | CrCl3 | CCl4 | COCl2 |
| 熔点/℃ | 1435 | 1 152 | -23 | -118 |
| 沸点/℃ | 4000 | 1 300 | 76 | 8.2 |
(1)仪器d中盛有无水CaCl2固体,其作用为
(2)通入N2除起到将装置内空气排出的作用外,还具有的作用为
(3)步骤Ⅳ中,将光气分离出的操作名称为
(4)B中得到产品的化学方程式为
(5)光气剧毒,该实验中用NaOH溶液吸收逸出的少量光气。也可以用乙醇处理COCl2,生成一种含氧酸酯(C2H5OCOOC2H5),用乙醇处理光气的化学方程式为
(6)样品中三氯化铬质量分数的测定
称取样品0.3300g,加水溶解并定容于250mL容量瓶中。移取25.00mL于碘量瓶(一种带塞的锥形瓶)中,加热至沸后加入1gNa2O2,充分加热煮沸,适当稀释,然后加入过量的2mol/LH2SO4至溶液呈强酸性,此时铬以Cr2O
 存在,再加入1.1gKI,密塞,摇匀,于暗处静置5分钟后,加入1mL指示剂,用0.0250mol/L硫代硫酸钠溶液滴定至终点,平行测定三次,平均消耗标准硫代硫酸钠溶液24.00mL。
存在,再加入1.1gKI,密塞,摇匀,于暗处静置5分钟后,加入1mL指示剂,用0.0250mol/L硫代硫酸钠溶液滴定至终点,平行测定三次,平均消耗标准硫代硫酸钠溶液24.00mL。已知:Cr2O
 +6I-+14H+=2Cr3++3I2+7H2O,2Na2S2O3+I2=Na2S4O6+2NaI。
+6I-+14H+=2Cr3++3I2+7H2O,2Na2S2O3+I2=Na2S4O6+2NaI。①该实验可选用的指示剂名称为
②样品中无水三氯化铬的质量分数为
您最近一年使用:0次
名校
解题方法
8 . I.亚氯酸钠(NaClO2)是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。马蒂逊(Mathieson)法制备亚氯酸钠的流程如下:

(1)反应①阶段,参加反应的NaClO3和SO2的物质的量之比为___________
(2)若反应①通过原电池来实现,则ClO2是___________ 极产物
(3)反应②中的H2O2___________ 用NaClO4代替(填能或不能)
(4)写出反应②的离子方程式___________
II.聚合硫酸铁[Fe2(OH)6-2n(SO4)n]m广泛用于水的净化。以FeSO4·7H2O为原料,经溶解、氧化、水解聚合等步骤,可制备聚合硫酸铁。
(5)将一定量的FeSO4·7H2O溶于稀硫酸,在约70℃下边搅拌边缓慢加入一定量的H2O2溶液,继续反应一段时间,得到红棕色黏稠液体。H2O2氧化Fe2+的离子方程式为___________ ;水解聚合反应会导致溶液的pH___________ 。
(6)测定聚合硫酸铁样品中铁的质量分数:准确称取液态样品3.000g,置于250mL锥形瓶中,加入适量稀盐酸,加热,滴加稍过量的SnCl2溶液(Sn2+将Fe3+还原为Fe2+),充分反应后,除去过量的Sn2+。用5.000×10-2mol·L-1K2Cr2O7溶液滴定至终点(滴定过程中 与Fe2+反应生成Cr3+和Fe3+),消耗K2Cr2O7溶液22.00mL。
与Fe2+反应生成Cr3+和Fe3+),消耗K2Cr2O7溶液22.00mL。
①上述实验中若不除去过量的Sn2+,样品中铁的质量分数的测定结果将__ (填“偏大”“偏小”或“无影响”)。
②计算该样品中铁的质量分数_____ (写出计算过程)。

(1)反应①阶段,参加反应的NaClO3和SO2的物质的量之比为
(2)若反应①通过原电池来实现,则ClO2是
(3)反应②中的H2O2
(4)写出反应②的离子方程式
II.聚合硫酸铁[Fe2(OH)6-2n(SO4)n]m广泛用于水的净化。以FeSO4·7H2O为原料,经溶解、氧化、水解聚合等步骤,可制备聚合硫酸铁。
(5)将一定量的FeSO4·7H2O溶于稀硫酸,在约70℃下边搅拌边缓慢加入一定量的H2O2溶液,继续反应一段时间,得到红棕色黏稠液体。H2O2氧化Fe2+的离子方程式为
(6)测定聚合硫酸铁样品中铁的质量分数:准确称取液态样品3.000g,置于250mL锥形瓶中,加入适量稀盐酸,加热,滴加稍过量的SnCl2溶液(Sn2+将Fe3+还原为Fe2+),充分反应后,除去过量的Sn2+。用5.000×10-2mol·L-1K2Cr2O7溶液滴定至终点(滴定过程中
 与Fe2+反应生成Cr3+和Fe3+),消耗K2Cr2O7溶液22.00mL。
与Fe2+反应生成Cr3+和Fe3+),消耗K2Cr2O7溶液22.00mL。①上述实验中若不除去过量的Sn2+,样品中铁的质量分数的测定结果将
②计算该样品中铁的质量分数
您最近一年使用:0次
名校
解题方法
9 . 三草酸合铁酸钾晶体{K3[Fe(C2O4)3]·3H2O}易溶于水,难溶于乙醇,可用于摄影和蓝色印刷。三草酸合铁酸钾晶体在110 ℃可完全失去结晶水,继续升高温度可发生分解反应。
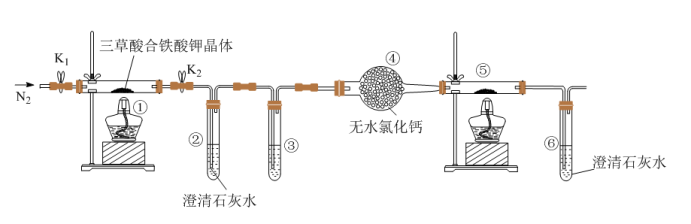
(1)分解得到的气体产物用如下装置进行实验:检查装置气密性后先通一段时间的N2,其目的是_____________ ;为了实验安全,应先点燃___________________ (①或⑤)处的酒精灯;
(2)若③和⑤中分别盛放_____________ 、_______________ 就可检验生成的CO;
(3)分解得到的固体产物含有K2CO3、FeO、Fe,加水溶解、过滤、洗涤、干燥,得到含铁样品。现设计下列两种实验方案对该样品进行铁元素含量测定:
【甲】a g样品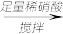 溶液
溶液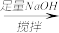
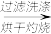 得固体b g
得固体b g
【乙】a g样品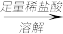 配制250 mL溶液
配制250 mL溶液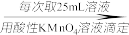 ,三次平均消耗0.1 mol·L-1酸性KMnO4溶液V mL.
,三次平均消耗0.1 mol·L-1酸性KMnO4溶液V mL.
你认为以上________ (填“甲”或“乙”)方案可确定样品的组成,测得铁元素的含量是__________ ,不可确定样品组成的方案的理由是_____________________________________ 。

(1)分解得到的气体产物用如下装置进行实验:检查装置气密性后先通一段时间的N2,其目的是
(2)若③和⑤中分别盛放
(3)分解得到的固体产物含有K2CO3、FeO、Fe,加水溶解、过滤、洗涤、干燥,得到含铁样品。现设计下列两种实验方案对该样品进行铁元素含量测定:
【甲】a g样品
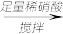 溶液
溶液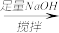
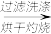 得固体b g
得固体b g【乙】a g样品
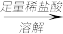 配制250 mL溶液
配制250 mL溶液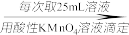 ,三次平均消耗0.1 mol·L-1酸性KMnO4溶液V mL.
,三次平均消耗0.1 mol·L-1酸性KMnO4溶液V mL.你认为以上
您最近一年使用:0次



