解题方法
1 . 化学工业为疫情防控提供了强有力的物质支撑。氯的许多化合物既是重要化工原料,又是高效、广谱的灭菌消毒剂。回答下列问题:
(1)实验室制Cl2的反应中,浓盐酸所起的作用有_______ (填序号)。
①氧化性 ②还原性 ③碱性 ④酸性
(2)“84消毒液”的有效成分是NaClO,可由Cl2与NaOH溶液反应得到,其离子方程式为_______ (用离子方程式表示,)。
(3)在实验室中用二氧化锰与浓盐酸反应制备干燥纯净的氯气。进行此实验,所用仪器如图:
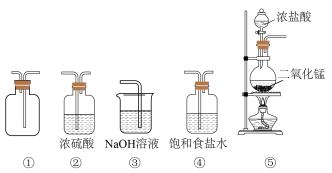
A.上述仪器的正确顺序(用序号表示):_______ ;
B.②装置中,浓硫酸的作用是_______ ;
C.⑤装置中发生反应的离子方程式为:_______ 。
(1)实验室制Cl2的反应中,浓盐酸所起的作用有
①氧化性 ②还原性 ③碱性 ④酸性
(2)“84消毒液”的有效成分是NaClO,可由Cl2与NaOH溶液反应得到,其离子方程式为
(3)在实验室中用二氧化锰与浓盐酸反应制备干燥纯净的氯气。进行此实验,所用仪器如图:

A.上述仪器的正确顺序(用序号表示):
B.②装置中,浓硫酸的作用是
C.⑤装置中发生反应的离子方程式为:
您最近一年使用:0次
2023-02-10更新
|
62次组卷
|
2卷引用:宁夏银川市贺兰县景博中学2022-2023学年高一下学期第一次质量检测化学试题
名校
解题方法
2 . 下列关于元素周期表和元素周期律的说法不正确的是
| A.从钠到氯,最高价氧化物的水化物碱性逐渐减弱,酸性逐渐增强 |
| B.因为钠原子比铝原子容易失去电子,所以钠比铝的还原性强 |
| C.从氯到碘,生成的氢化物熔、沸点逐渐升高,稳定性逐渐增强 |
| D.氧与硫为同主族元素,氧比硫的原子半径小,氧比硫的氧化性强 |
您最近一年使用:0次
名校
解题方法
3 . 铜质电路板可采用酸性蚀刻与碱性蚀刻两种方法。将二者的废液混合可实现回收再利用。其主要流程如图:
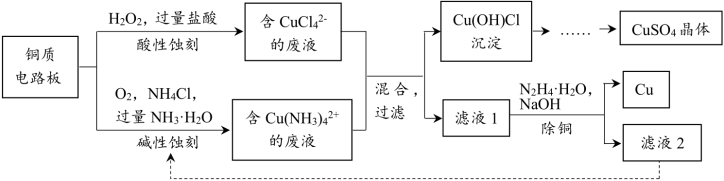
已知:①水合肼N2H4·H2O具有强还原性,易被氧化为N2
②Cu2++4NH3 Cu(NH3)
Cu(NH3)
(1)蚀刻
①酸性蚀刻铜的离子方程式:___________
②关于蚀刻的下列说法正确的是___________ 。
A.碱性蚀刻和酸性蚀刻分别利用了O2、H2O2的氧化性
B.酸性蚀刻时盐酸的主要作用是增强溶液的酸性
C.用H2O2、H2SO4、NaCl也可以使Cu溶解
(2)滤液1的pH约为5,其中除少量Cu2+外,还大量存在的离子是___________ 。
(3)除铜
①利用水合肼N2H4·H2O还原Cu2+的离子方程式是___________ 。
②已知该反应瞬间完成。滤渣成分只有Cu。测得铜去除率、水合肼还原能力随溶液pH的变化情况如图所示。由图可知。随溶液pH增大,铜去除率先增加后减小,结合图给值息和已知信息分析其原因:___________ 。
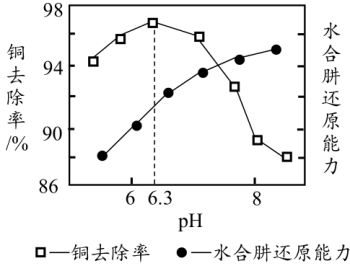

已知:①水合肼N2H4·H2O具有强还原性,易被氧化为N2
②Cu2++4NH3
 Cu(NH3)
Cu(NH3)
(1)蚀刻
①酸性蚀刻铜的离子方程式:
②关于蚀刻的下列说法正确的是
A.碱性蚀刻和酸性蚀刻分别利用了O2、H2O2的氧化性
B.酸性蚀刻时盐酸的主要作用是增强溶液的酸性
C.用H2O2、H2SO4、NaCl也可以使Cu溶解
(2)滤液1的pH约为5,其中除少量Cu2+外,还大量存在的离子是
(3)除铜
①利用水合肼N2H4·H2O还原Cu2+的离子方程式是
②已知该反应瞬间完成。滤渣成分只有Cu。测得铜去除率、水合肼还原能力随溶液pH的变化情况如图所示。由图可知。随溶液pH增大,铜去除率先增加后减小,结合图给值息和已知信息分析其原因:

您最近一年使用:0次
2021-11-27更新
|
480次组卷
|
3卷引用:宁夏石嘴山市平罗中学2022-2023学年高三上学期期中考试(重点班)化学试题
宁夏石嘴山市平罗中学2022-2023学年高三上学期期中考试(重点班)化学试题黑龙江省牡丹江市第一高级中学2021-2022学年高三上学期期中考试化学试题(已下线)解密06 金属及其化合物(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)
4 . 下列递变规律正确的是
A.稳定性: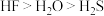 还原性: 还原性: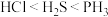 |
B.原子半径: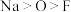 离子半径: 离子半径: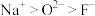 |
C.酸性: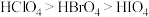 碱性: 碱性: |
D.还原性: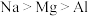 氧化性: 氧化性: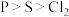 |
您最近一年使用:0次
12-13高一上·黑龙江大庆·期末
名校
5 . 物质在反应中可表现氧化性、还原性、酸性、碱性等,下面方程式中划线的物质,能在同一反应中同时表现上述两种或两种以上性质的有( )
①3FeO + 10HNO3 = 3Fe(NO3)3 + NO + 5H2O
②C + 2H2SO4(浓) = CO2 + 2SO2 + 2H2O
③8NH3 + 3Cl2 =6NH4Cl + N2
④2Na2O2 + 2H2O =4NaOH + O2
①3FeO + 10HNO3 = 3Fe(NO3)3 + NO + 5H2O
②C + 2H2SO4(浓) = CO2 + 2SO2 + 2H2O
③8NH3 + 3Cl2 =6NH4Cl + N2
④2Na2O2 + 2H2O =4NaOH + O2
| A.①② | B.①④ | C.③④ | D.全部 |
您最近一年使用:0次
2020-10-24更新
|
125次组卷
|
15卷引用:宁夏回族自治区中卫市海原县第一中学2020-2021学年高一上学期第二次月考化学试题
宁夏回族自治区中卫市海原县第一中学2020-2021学年高一上学期第二次月考化学试题(已下线)2011—2012学年度黑龙江大庆实验中学高一上学期期末考试化学试卷(已下线)2011-2012学年河北省邯郸市高一下学期期末教学质量检测化学试卷(已下线)2012-2013学年黑龙江省集贤县第一中学高一上学期期末考试化学试卷(已下线)2015届福建省三明一中高三学年度上学期第一次月考化学试卷(已下线)2015届福建省三明一中高三上学期第一次月考化学试卷2016届湖南省衡阳市第八中学高三上学期第二次月考化学试卷2017届湖南省衡阳八中高三上学期9月月考化学试卷湖南省邵东县第一中学2017届高三上学期第三次月考化学试题福建省龙海市第二中学2016-2017学年高二下学期期末考试化学试题(已下线)二轮复习 专题6 非金属及其化合物 押题专练(已下线)2019高考备考二轮复习精品资料-专题6 非金属及其化合物(押题专练)浙江省余姚中学2020-2021学年高二上学期10月质量检测化学试题浙江省宁波市余姚中学2020-2021学年高一上学期10月质量检测化学试题(已下线)【浙江新东方】62
2010·全国·一模
名校
解题方法
6 . 人体血红蛋白中含有Fe2+,如果误食亚硝酸盐会使人中毒,因为亚硝酸盐会使Fe2+变Fe3+,生成高铁血红蛋白而丧失与O2结合的能力。服用维生素C可缓解亚硝酸盐中毒。说明维生素C具有
| A.氧化性 | B.还原性 | C.酸性 | D.碱性 |
您最近一年使用:0次
2020-11-09更新
|
1006次组卷
|
70卷引用:2015-2016学年宁夏吴忠中学高一上学期期末考试化学试卷
2015-2016学年宁夏吴忠中学高一上学期期末考试化学试卷(已下线)高考第一轮复习化学反应与能量变化单元测试(已下线)2010—2011学年云南省元阳一中高一上学期期末考试化学试卷(已下线)2011-2012学年上海理工大学附属中学高一上学期期末考试化学试卷(已下线)2011-2012学年广东省汕头金山中学高一第一学期期末考试化学(文)试卷(已下线)2011-2012学年浙江省余姚中学高一下学期期中考试文科化学试卷(已下线)2011-2012学年福建省泉州一中高一下学期期中考试化学试卷(已下线)2012-2013学年河北省邢台一中高一上学期第三次月考化学试卷(已下线)2012-2013学年浙江省杭州十四中高一上学期期末考试化学试卷(已下线)2012-2013学年上海市上海理工大学附属中学高一上期末考试化学试卷(已下线)2012-2013学年浙江省杭州地区七校高一下学期期中联考文科化学试卷(已下线)2013-2014学年山东省临沂市重点中学高一上学期期中考试化学试卷2014-2015山西省原平市一中高一上学期期末考试化学试卷2015-2016学年吉林省吉林五十五中高二上学期期中(文)化学试卷2015-2016学年广东广州执信中学高二上期中文化学试卷2015-2016学年湖南省常德一中高一上学期期末化学试卷2015-2016学年福建省莆田二十五中高一下学期第一次月考化学试卷2015-2016学年山西晋城市高平市特立高级中学高二下期中理科化学卷2016-2017学年广东佛山一中高一上第一次段考化学卷2016-2017学年遵义市第四中学高二上学期期中考试化学(文)试卷2016-2017学年广东省广州执信中学高二上期中化学卷2016-2017学年广东省汕头市金山中学高二上学业水平测试化学卷甘肃省武威市河西成功学校2017-2018学年高一上学期期中考试化学试题山东省临沂市蒙阴县实验中学2017-2018学年高一上学期期中考试化学试题山东省桓台第二中学2017-2018学年高一12月月考化学试题陕西省西安市长安区第一中学2017-2018学年高二上学期期末考试化学(文)试题广东省惠州市2017-2018学年高一上学期期末教学质量检测化学试题湖南省师范大学附属中学2017-2018学年高二上学期期末考试化学(文)试题云南省昆明市黄冈实验学校2017-2018学年高二上学期期末考试化学(理)试题云南民族大学附属中学2017-2018学年高一下学期期中考试化学试题2018-2019学年鲁科版必修1第2章元素与物质世界本章测试题广东省普通高中2018-2019学年高二学业水平测试预测试题福建省晋江市季延中学2018-2019学年高二(文)上学期期中考试化学试题山西省祁县第二中学校2018-2019学年高二下学期5月考试化学试题江苏省苏州陆慕高级中学2018-2019学年高一下学期5月月考化学试题江苏省苏州市第五中学2018-2019学年高二上学期期中考试(必修)化学试题甘肃省嘉峪关市一中2017-2018学年高一上学期期中考试化学试题云南省云天化中学2019-2020学年高一9月月考化学试题黑龙江省哈尔滨市第三中学2019-2020学年高二上学期期中考试化学(文)试题黑龙江省哈尔滨市阿城区龙涤中学2019-2020学年高一上学期第一次段考化学试题上海市嘉定区封浜高中2019-2020学年高二上学期期中考试化学试题湖南省常德市2018-2019学年高二下学期第一次月考化学试题江西省抚州市南城县第二中学2019-2020学年高一上学期第二次月考化学试题江苏省海头高级中学2019-2020学年高一上学期第三次月考化学试题福建省晋江市养正中学2019-2020学年高二上学期第二次月考化学试题山西省运城市盐湖五中2019-2020学年高一上学期期中考试化学试题安徽省六安市第一中学2019-2020学年高一下学期疫情防控延期开学期间辅导测试(三)化学试题安徽省芜湖市2019-2020学年高二上学期期末考试化学(文)试题辽宁省东北育才学校科学高中部2020-2021学年高一上学期第一学段检测化学试题(已下线)【浙江新东方】7广东省佛山市第一中学2020-2021学年高一上学期第一次段考化学试题江苏省常州市2020-2021学年高一上学期期中考试化学试题江西省九江市浔阳区九江市第七中学2020-2021学年高一上学期期中考试化学试题吉林省大安市第六中学2019-2020学年高二下学期期末考试化学(理)试题上海市奉城高级中学2018-20219学年高二上学期期中考试化学试题河北省石家庄市第二中学西校区2020-2021学年高一上学期12月月考化学试卷河南省南阳市第四中学2020-2021学年高一上学期第二次月考化学试题河南省南阳市油田第一中学2020-2021学年高二上学期期中考试化学试题福建省莆田第一中学2021-2022学年高一上学期期中考试化学试题山西省大同市2021-2022学年高一上学期期末调研化学试题上海理工大学附属中学中2021-2022学年高一下学期期中考试化学试题江苏省常州市金坛区2021-2022学年高一上学期期中教学质量调研化学试题广东省华南师范大学附属中学2020-2021学年高一上学期期中考试化学试题辽宁省锦州市黑山县黑山中学2021-2022学年高一上学期12月月考化学试题北京清华大学附属中学2022-2023学年高一上学期期末考试化学试卷海南省临高县新盈中学2021-2022学年高二上学期(5-8班)期中考试化学试题湖南省株洲市炎陵县第一中学等2校2022-2023学年高一下学期3月月考化学试题甘肃省武威市天祝藏族自治县第一中学2022-2023学年高一下学期开学考试化学试题广东省汕头市潮阳第一中学2023-2024学年高一上学期12月月考化学试题北京市顺义区杨镇第一中学2023-2024学年高一上学期期中考试化学试题
名校
7 . 硫酸铁铵晶体[Fe2(SO4)3·2(NH4)2SO4·3H2O]在工业上常用作分析试剂,它可用含SiO2、CeO2和Fe2O3的工业废料作原料来获得,同时可回收CeO2,工艺流程设计如下:
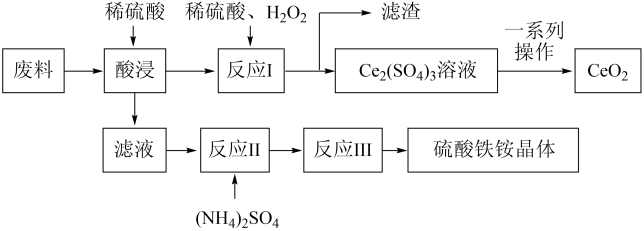
已知:①SiO2、CeO2不溶于稀硫酸;
②酸性条件下,CeO2可与H2O2反应;
③“反应I”所得溶液中含有Ce3+;
④碱性条件下, 与OH-结合生成NH3·H2O。
与OH-结合生成NH3·H2O。
请回答下列问题:
(1)“酸浸”时发生反应的离子方程式为______ 未发生反应的物质是_______ (填化学式)。
(2)“滤液”中含有的阳离子有______ (填离子符号)。
(3)写出“反应I”的化学方程式:____ ;“反应I”后进行固液分离时用到的玻璃仪器有______ 。
(4)在酸性条件下,H2O2、CeO2两种物质中,氧化性较弱的是_______ (填化学式)。
(5)若往硫酸铁铵溶液中加入过量的NaOH,写出该反应的离子方程式:______ 。

已知:①SiO2、CeO2不溶于稀硫酸;
②酸性条件下,CeO2可与H2O2反应;
③“反应I”所得溶液中含有Ce3+;
④碱性条件下,
 与OH-结合生成NH3·H2O。
与OH-结合生成NH3·H2O。请回答下列问题:
(1)“酸浸”时发生反应的离子方程式为
(2)“滤液”中含有的阳离子有
(3)写出“反应I”的化学方程式:
(4)在酸性条件下,H2O2、CeO2两种物质中,氧化性较弱的是
(5)若往硫酸铁铵溶液中加入过量的NaOH,写出该反应的离子方程式:
您最近一年使用:0次
名校
解题方法
8 . 比较下列性质(用“>”、“=”、“<”填空)
①半径 P________ F
②酸性 H3PO4________ H2SO4
③碱性Mg(OH)2________ Al(OH)3
④稳定性 H2S________ H2O
⑤还原性H2S________ HCl
⑥氧化性 Cl2________ Br2 .
①半径 P
②酸性 H3PO4
③碱性Mg(OH)2
④稳定性 H2S
⑤还原性H2S
⑥氧化性 Cl2
您最近一年使用:0次
2020-03-06更新
|
473次组卷
|
2卷引用:宁夏吴忠市吴忠中学高二化学下学期第一章《原子结构与性质》单元测试
名校
解题方法
9 . 为了探究元素周期律,设计实验验证卤素单质氧化性的相对强弱,实验如下:
资料:稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色。
(1)a中反应的离子方程式是___________ 。
(2)实验I中b可以得出的氧化性强弱是___________ 。
(3)①甲同学认为:实验Ⅱ观察到___________ 现象,得出氧化性Br2>I2。
②乙同学对上述实验进行反思,认为实验II不能充分证明氧化性Br2>I2,他补做了实验Ⅲ.
补做实验Ⅲ的目的是___________ 。
综合实验I和Ⅲ,得出氧化性Cl2>Br2>I2.由此实验得出的结论:同主族元素从上到下,原子的得电子能力逐渐减弱
资料:稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色。
| 实验I | 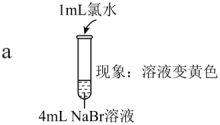 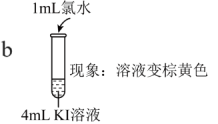 |
| 实验II | 取a中的黄色溶液少许,加入KI溶液,再加入淀粉溶液。 |
(1)a中反应的离子方程式是
(2)实验I中b可以得出的氧化性强弱是
(3)①甲同学认为:实验Ⅱ观察到
②乙同学对上述实验进行反思,认为实验II不能充分证明氧化性Br2>I2,他补做了实验Ⅲ.
| 实验III | 另取a中黄色溶液少许,加入足量NaBr固体,振荡,然后加入KI溶液和淀粉溶液。 |
综合实验I和Ⅲ,得出氧化性Cl2>Br2>I2.由此实验得出的结论:同主族元素从上到下,原子的得电子能力逐渐减弱
您最近一年使用:0次
2024-02-13更新
|
75次组卷
|
2卷引用:宁夏回族自治区石嘴山市第三中学2023-2024学年高一上学期1月期末化学试题
名校
解题方法
10 . 以下有关氨及铵盐的叙述中不正确的是( )
| A.铵态氮肥不能与碱性物质如草木灰混合施用 |
| B.氨的喷泉实验体现了氨的溶解性和氧化性 |
| C.实验室常用固体氯化铵与氢氧化钙反应制取氨气 |
| D.氨具有还原性,一定条件下可与氧化性物质如氧气发生反应 |
您最近一年使用:0次
2020-06-11更新
|
415次组卷
|
17卷引用:【全国百强校】宁夏回族自治区石嘴山市第三中学2019届高三上学期期中考试化学试题
【全国百强校】宁夏回族自治区石嘴山市第三中学2019届高三上学期期中考试化学试题2015-2016学年天津市平和区高一上学期期末考试化学试卷【全国市级联考】贵州省毕节市2017-2018学年高一毕业学业达标模拟考试化学试题(已下线)【走进新高考】(人教版必修一)4.4.1氨、硝酸、硫酸——氨 同步练习02云南省广南县第三中学2019-2020学年高二上学期开学考试化学试题步步为赢高一化学寒假作业:作业十五 氨 硝酸 硫酸贵州省岑巩县第二中学2019-2020学年高一上学期期末考试化学试题吉林省白山市第七中学2019-2020学年高一下学期第一次月考化学试题陕西省延安市第一中学2019-2020学年高一下学期线上摸底考试化学试题内蒙古呼和浩特市土默特左旗第一中学2019-2020学年高一下学期期中考试化学试题安徽省阜阳市第十一中学2019-2020学年高一下学期期中考试化学试题(已下线)7.3.1 铵盐的性质 练习 -2020-2021学年下学期高一化学同步精品课堂(苏教版2019必修第二册)江西省新建一中2020-2021学年高一下学期开学考试化学试题四川省绵阳南山中学双语学校2021-2022学年高一下学期入学考试化学试题四川省绵阳南山中学2021-2022学年高一下学期开学考试化学试题四川省绵阳南山中学2023-2024学年高一下学期3月月考试题 化学试题河南省新乡市原阳县第一高级中学2023-2024学年高一下学期4月月考化学试题



