名校
解题方法
1 . 用下图装置探究铜与硝酸的反应,实验记录如下:
下列说法不正确 的是
| 装置 | 步骤 | 操作 | 现象 |
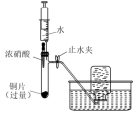 | ① | 打开止水夹,挤压胶头,使浓硝酸滴入试管 | 产生红棕色气体,溶液变为绿色 |
| ② | 一段时间后,关闭止水夹,推动注射器活塞使部分水进入试管 | 注射器内剩余的水被“吸入”试管;铜表面产生无色气泡,溶液变蓝,试管内气体逐渐变为无色 | |
| ③ | 一段时间后,打开止水夹,拉动注射器活塞吸取少量无色气体;拔下注射器,再拉动活塞吸入少量空气 | 注射器中无色气体变为红棕色 |
| A.①中反应的化学方程式是Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O |
| B.②中注射器内剩余的水被“吸入”试管的原因可能是NO2与H2O反应导致压强减小 |
| C.③中的实验现象能证明②中Cu与硝酸反应生成了NO |
| D.待②中反应停止后,向试管内滴加少量稀硫酸,有气体产生 |
您最近一年使用:0次
2021-04-10更新
|
695次组卷
|
9卷引用:新疆伊犁州“华-伊高中联盟校”2022-2023学年高一下学期期末考试化学试题
18-19高二下·新疆伊犁·阶段练习
2 . 下列说法不正确 的是( )
| A.已知冰的熔化热为6.0kJ﹒mol-1,冰中氢键键能为20 kJ﹒mol-1,假设每摩尔冰中有2mol氢键,且熔化热完全用于打破冰的氢键,则最多只能破坏冰中15%的氢键 |
| B.实验测得环己烷(1)、环己烯(1)和苯(1)的标准燃烧热分别为-3916kJ/mol-1、-3747kJ/mol-1和-3265kJ/mol-1,可以证明在苯分子中不存在独立的碳碳双键 |
| C.已知:Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g) △H=489.0kJ/mol CO(g)+  O2(g)=CO2(g) △H=-283.0kJ/mol O2(g)=CO2(g) △H=-283.0kJ/molC(石墨)+O2(g)=CO2(g) △H=-393.5kJ/mol 则4Fe(s)+3O2(g)=2Fe2O3(g) △H=-1641.0kJ·mol-1 |
| D.除干燥CH4中混有的少量C2H4,将混合气体依次通过盛有酸性KMnO4溶液,浓硫酸的洗气瓶 |
您最近一年使用:0次
名校
3 . 下列叙述正确的是
①A和B是元素周期表中同主族金属元素,且A在B的下方,则A肯定比B的金属性强
②1molA能从酸中置换出1.5mol ,1molB能从酸中置换出1mol
,1molB能从酸中置换出1mol ,可以证明A比B的金属性强
,可以证明A比B的金属性强
③ 比
比 碱性弱,则可以得到Fe比Mg的金属性弱
碱性弱,则可以得到Fe比Mg的金属性弱
④ 比HBr的酸性弱,证明Br比S的非金属性强
比HBr的酸性弱,证明Br比S的非金属性强
⑤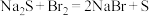 ,足以证明非金属性Br>S
,足以证明非金属性Br>S
①A和B是元素周期表中同主族金属元素,且A在B的下方,则A肯定比B的金属性强
②1molA能从酸中置换出1.5mol
 ,1molB能从酸中置换出1mol
,1molB能从酸中置换出1mol ,可以证明A比B的金属性强
,可以证明A比B的金属性强③
 比
比 碱性弱,则可以得到Fe比Mg的金属性弱
碱性弱,则可以得到Fe比Mg的金属性弱④
 比HBr的酸性弱,证明Br比S的非金属性强
比HBr的酸性弱,证明Br比S的非金属性强⑤
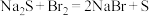 ,足以证明非金属性Br>S
,足以证明非金属性Br>S| A.①②④ | B.①⑤ | C.②③⑤ | D.②③④ |
您最近一年使用:0次
2024-02-06更新
|
105次组卷
|
2卷引用:新疆伊犁州霍城县江苏中学2023-2024学年高一上学期12月 化学试题
4 . 按要求回答下列问题:
(1)已知下列物质电离平衡常数
①次氯酸的电离方程式为___________ 。
②物质的量浓度相同的HF、CH3COOH、H2CO3、HClO中,酸性由小到大的顺序为___________ 。
③下列实验事实不能证明醋酸是弱酸的是___________ 。
A.相同pH的醋酸溶液和盐酸分别与同样颗粒大小的锌反应时,产生H2的起始速率相等
B.常温下,测得0.1mol·L-1醋酸溶液的pH=4
C.常温下,将pH=1的醋酸溶液稀释1000倍,测得pH<4
D.在相同条件下,同浓度醋酸溶液的导电性比盐酸的弱
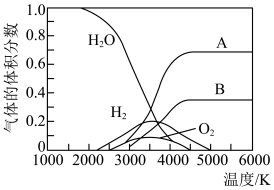
(2)高温下H2O可以分解成分子或原子。
①若在相同温度下,1molH2O按下列两种途径转化成氢原子与氧原子。则△H1、△H2、△H3三者之间的关系是___________ 。
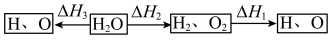
②高温下水分解体系中主要气体的体积分数与温度的关系如图所示。图中A表示的物质(或微粒)是___________ 。等物质的量的A、H2相比,化学能较低的物质是___________ 。
(1)已知下列物质电离平衡常数
| 化学式 | HF |  |  |  |
| 电离平衡常数 | 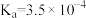 |  | 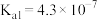  | 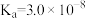 |
②物质的量浓度相同的HF、CH3COOH、H2CO3、HClO中,酸性由小到大的顺序为
③下列实验事实不能证明醋酸是弱酸的是
A.相同pH的醋酸溶液和盐酸分别与同样颗粒大小的锌反应时,产生H2的起始速率相等
B.常温下,测得0.1mol·L-1醋酸溶液的pH=4
C.常温下,将pH=1的醋酸溶液稀释1000倍,测得pH<4
D.在相同条件下,同浓度醋酸溶液的导电性比盐酸的弱
(2)高温下H2O可以分解成分子或原子。
①若在相同温度下,1molH2O按下列两种途径转化成氢原子与氧原子。则△H1、△H2、△H3三者之间的关系是
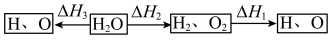
②高温下水分解体系中主要气体的体积分数与温度的关系如图所示。图中A表示的物质(或微粒)是

您最近一年使用:0次
名校
解题方法
5 . 下列实验操作、现象和结论都正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 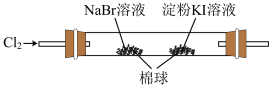 | 左边棉球变为橙色,右边棉球变为蓝色 | 氧化性: |
| B | 向 溶液中加入一小块钠 溶液中加入一小块钠 | 产生无色气泡,溶液底部有蓝色沉淀生成 | 水溶液中 不能置换铜 不能置换铜 |
| C | 向某溶液中加入盐酸产生无色气体,将该气体通入澄清石灰水 | 澄清石灰水变浑浊 | 该溶液中一定含有 或 或 |
| D | 干燥的氯气依次通过干燥有色布条、湿润有色布条 | 干燥有色布条不褪色、湿润有色布条褪色 | 证明 具有漂白性 具有漂白性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-12-04更新
|
193次组卷
|
3卷引用:新疆伊犁州霍城县江苏中学2023-2024学年高一上学期12月 化学试题
名校
解题方法
6 . 某化学兴趣小组为检验木炭和浓硫酸反应生成的产物,设计如图装置,请回答:
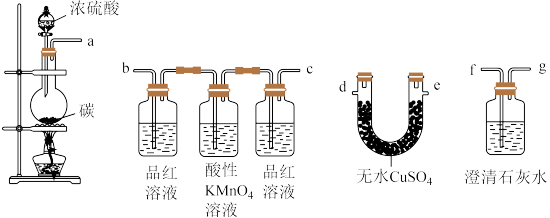
(1)盛装浓硫酸的仪器的名称是_______ ;盛装碳粉的仪器的名称是_______ 。
(2)上述装置接口的连接顺序为a→_______ 。
(3)写出木炭和浓硫酸发生反应的化学方程式_______ 。
(4)U形管中现象是_______ ,证明产物中有_______ (填化学式)。
(5)酸性KMnO4溶液的作用是_______ 。
(6)澄清石灰水的作用是_______ 。
(7)写出SO2与H2S反应的化学方程式_______ 。

(1)盛装浓硫酸的仪器的名称是
(2)上述装置接口的连接顺序为a→
(3)写出木炭和浓硫酸发生反应的化学方程式
(4)U形管中现象是
(5)酸性KMnO4溶液的作用是
(6)澄清石灰水的作用是
(7)写出SO2与H2S反应的化学方程式
您最近一年使用:0次
2023-08-28更新
|
183次组卷
|
2卷引用:新疆伊犁州“华-伊高中联盟校”2022-2023学年高一下学期期末考试化学试题
9-10高二下·山东潍坊·期末
名校
解题方法
7 . 要证明某溶液中不含Fe3+,而可能含有Fe2+,进行如下实验操作的最佳顺序为
①加入足量氯水②加入足量KMnO4(H+)溶液③加入少量KSCN溶液
①加入足量氯水②加入足量KMnO4(H+)溶液③加入少量KSCN溶液
| A.①③ | B.③① | C.①②③ | D.③②① |
您最近一年使用:0次
2023-01-09更新
|
375次组卷
|
113卷引用:新疆新源县第二中学2019-2020学年高一上学期期末考试化学试题
新疆新源县第二中学2019-2020学年高一上学期期末考试化学试题(已下线)2010年潍坊市高二下学期新课程期末测试化学(已下线)2010年江苏省泰兴市重点中学高三上学期第一次检测化学试题(已下线)2010年上海市吴淞中学高二上学期期中考试化学试卷(已下线)2010—2011年福建省厦门市杏南中学高一12月月考化学卷(已下线)2012届上海市松江二中高三上学期期中考试化学试卷(已下线)2011-2012学年上海市崇明中学高二上学期期中考试化学试卷(已下线)2011-2012学年江苏省泰州中学高三化学期中化学试卷(已下线)2011-2012学年内蒙古巴彦淖尔市中学高三期中考试化学试卷(已下线)2011-2012学年黑龙江省庆安三中高一上学期期末考试化学试卷(已下线)2011-2012学年云南省玉溪一中高一下学期期中考试化学试卷(已下线)2013届辽宁朝阳柳城高级中学高三上学期第二次月考化学试卷(已下线)2015河北保定某重点中学同步作业(必修1苏教版)3.2.2铜铁及其化合物(已下线)2014-2015学年福建省三明一中高一上学期期中化学试卷2015-2016学年黑龙江省哈尔滨六中高一上期末化学试卷2015-2016学年河北省冀州中学高一下开学考试化学试卷2015-2016学年广东省清远市高一上学期期末考试化学试卷2016届江西省宜春市铜鼓中学高三二模化学试卷2015-2016学年黑龙江省海林林业局一中高一上学期期末化学试卷2015-2016学年河南省安阳三十六中高二6月月考化学试卷2015-2016学年辽宁省庄河高中高一下期末化学试卷2015-2016学年山西晋城市高平市特立高级中学高二下期中理科化学卷2017届河北省故城县高级中学高三上学期期中化学试卷2016-2017学年福建省三明一中高一上期中化学卷2016-2017学年吉林省实验中学高一上学期期末化学试卷上海市金山中学2016-2017学年高二上学期期末等级考试化学试题宁夏银川市兴庆区2018届高三上学期第二次月考化学试题河南省鹤壁市淇滨高级中学2017-2018学年高一上学期第三次月考化学试题安徽省濉溪县临涣中学2017-2018学年高一上学期第二次月考化学试题河北省辛集中学2017-2018学年高一上学期第三次阶段考试化学试题湖北省长阳中学2017-2018学年高一化学上学期期末考试题山东省昌邑市第一中学2017-2018学年高一上学期第二次期末模拟考试化学试题湖南省石门县第一中学2016-2017学年高一下学期期末考试化学试题内蒙古阿拉善左旗高级中学2017-2018学年高二下学期期末考试化学试题黑龙江省伊春市第二中学2017-2018学年高二下学期期末考试化学试题人教版2017-2018学年高一化学必修1:3.2 几种重要的金属化合物 同步测试1(已下线)2019高考备考一轮复习精品资料 第三章 金属及其化合物 第3讲 铁及其化合物【教学案】【全国校级联考】新疆维吾尔自治区昌吉市教育共同体2019届高三上学期9月月考化学试题吉林省辽源市田家炳高级中学等五校2017-2018学年高一上学期期末联考(第64届)化学试题(已下线)2019高考热点题型和提分秘籍 第三章 金属及其化合物 第3讲 铁及其化合物 (教学案)【全国百强校】云南省玉溪市第一中学2018-2019学年高一上学期第一次月考化学试题山东省泰安市宁阳一中2018-2019学年高一上学期阶段性考试二(12月)化学试题【全国百强校】黑龙江省牡丹江市第一高级中学2018-2019学年高一上学期期末考试化学试题内蒙古开来中学2018-2019学年高二下学期期末考试化学试题新疆疏勒县八一中学2018-2019学年高一上学期期末考试化学试题黑龙江省牡丹江市第三高级中学2018-2019学年高二下学期期末考试化学试题云南省易门一中2019-2020学年高二开学考试化学试题(已下线)上海市华东师范大学第二附属中学2016-2017学年高二上学期期末考试化学试题上海市吴淞中学2017-2018学年高二上第一次月考化学试题上海市复旦中学2019-2020学年高二上学期第一次月考化学试题上海市上海交大附中2017-2018高二上期末化学题2019学年上海市奉贤区曙光中学高二化学上学期期中考试试卷福建省三明第一中学2019-2020学年高一上学期期中考试化学试题浙江省金华市东阳中学2019-2020学年高一上学期期中考试化学试题山东省德州市夏津县双语中学2019-2020学年高一12月月考化学试题宁夏青铜峡市高级中学2019-2020学年高一上学期期末考试化学试题甘肃省武威第八中学2019—2020学年高一上学期期末考试化学试题四川省三台县芦溪中学2017—2018学年高一上学期第三次月考化学试题四川省绵阳市三台县芦溪中学2017-2018学年高一上学期第三次月考化学试题上海市华东师大二附中2016-2017学年高二(上)期末化学试卷人教版高中化学必修一第三章《金属及其化合物》测试卷1山西省运城市盐湖五中2019-2020学年高一上学期期中考试化学试题上海市青浦二中2016届高三上学期8月摸底考试化学试题(已下线)上海市建平中学2013届高三第一次模拟化学试题(已下线)【南昌新东方】湾里一中2019-2020 高一(上)期末吉林省长春市九台区第四中学2019-2020高一上学期期末测试化学试题海南省海南枫叶国际学校2019-2020学年高一上学期期末考试化学试题甘肃省武威市第十八中学2019-2020学年高一上学期期末考试化学试题辽宁省阜新市第二高级中学2019-2020学年高一下学期期末考试化学试题上海南洋中学2019-2020学年高二上学期期中复习卷(沪科版)化学试题广东省中山市中山纪念中学2020届高三第二次质量检测化学试题(已下线)3.1.2 铁及其化合物之间的转化关系练习(1)——《高中新教材同步备课》(鲁科版 必修第一册)人教版(2019)高一必修第一册第三章 铁 金属材料 第一节 铁及其化合物 课时2 铁盐、亚铁盐鲁科版(2019)高一必修第一册第三章第1节 铁的多样性 课时1 亚铁盐和铁盐铁 铁的氧化物和铁的氢氧化物陕西省榆林市第十二中学2021届高三上学期第一次月考化学试题福建省莆田第二十五中学2021届高三上学期月考二化学试题(已下线)第三章 铁 金属材料(能力提升)-2020-2021学年高一化学单元测试定心卷(人教版2019必修第一册)(已下线)3.1.2 铁的重要化合物-2020-2021学年高一化学同步课堂帮帮帮(人教版2019必修第一册)(已下线)【浙江新东方】71.河北省石家庄市第二中学西校区2020-2021学年高一上学期12月月考化学试卷陕西省榆林市子洲中学2021届高三上学期第一次月考化学试题(已下线)专题05 金属及其重要化合物-备战2021届高考化学二轮复习题型专练辽宁省阜新市第二高级中学2020-2021学年高一上学期期末考试化学试题宁夏青铜峡市高级中学2020-2021学年高一上学期期末考试化学试题黑龙江省大庆市肇州县肇州中学2020-2021学年高一下学期第一次月考化学试题黑龙江省伊春市伊美区第二中学2020-2021学年高一上学期第三次月考化学试题福建省莆田第十五中学2018-2019学年高一下学期期中测试化学试题(苏教版2019)必修第二册专题9 金属与人类文明 第二单元 探究铁及其化合物的转化(已下线)微专题13 亚铁离子、三价铁离子的性质及检验-备战2022年高考化学考点微专题广东省普宁二中实验学校2021-2022学年高三上学期第一次月考化学试题黑龙江省双鸭山市第一中学2020-2021学年高一第二次月考化学试题上海市向明中学2021-2022学年高二上学期期中考试化学试题上海市向明中学2021-2022学年高三上学期期中考试化学试题浙江省乐清市知临中学2021-2022学年高一上学期期中考试化学(B)试题黑龙江省牡丹江市第三高级中学2021-2022学年高一上学期期末考试化学试题黑龙江省牡丹江市第三高级中学2021-2022学年高一下学期开学考试化学试题第三章 铁金属材料 本章复习提升(已下线)第07讲 铁及其化合物(练)-2023年高考化学一轮复习讲练测(新教材新高考)黑龙江省牡丹江市第三高级中学2022-2023学年高三上学期第一次月考化学试题黑龙江省嫩江市第一中学2021-2022学年高一下学期开学考试化学试题甘肃省武威市古浪县第二中学2021-2022学年高一上学期期末考试化学试题四川省凉山州宁南中学2022-2023学年高一上学期第二次月考化学试题辽宁省大石桥市第三高级中学2021-2022学年高一12月月考化学试题新疆阿克苏市实验中学2021-2022学年高一上学期期末考试化学(文)试题云南省大姚县第一中2021-2022学年高一下学期3月份考试化学试题新疆阿克苏市实验中学2021-2022学年高一上学期期末考试化学(理)试题吉林省永吉县第四中学2022-2023学年高一上学期期末考试化学试题新疆可克达拉市镇江高级中学2022-2023学年高一上学期期末考试化学试题黑龙江省富锦市第一中学2022-2023学年高一下学期第一次考试化学试题新疆昌吉州行知学校2022-2023学年高一下学期第一次月考化学试题第1课时 亚铁盐和铁盐新疆石河子第一中学2023-2024学年高一上学期11月月考化学试题四川省宜宾市兴文第二中学校2023-2024学年高一下学期开学化学试题
8 . “套管实验”的实验装置如图所示,请分析实验原理,并回答下列问题:
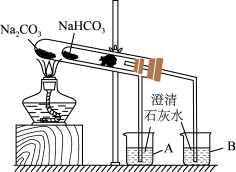
(1)整个实验过程中,能观察到烧杯A中的现象是_______ ;烧杯B中的现象是_______ 。
(2)写出实验过程中套管中发生反应的化学方程式:_______ 。
(3)该实验可证明NaHCO3的热稳定性_______ (填“强于”“弱于”或“等于”)Na2CO3;证明热稳定性的实验装置中,能否将NaHCO3、Na2CO3的位置互换?_______ (填“能”或“不能”)。

(1)整个实验过程中,能观察到烧杯A中的现象是
(2)写出实验过程中套管中发生反应的化学方程式:
(3)该实验可证明NaHCO3的热稳定性
您最近一年使用:0次
9 . 某课外活动小组的同学,在实验室做锌与浓硫酸反应的实验中,甲同学认为产生的气体是二氧化硫,而乙同学认为除产生二氧化硫气体外,还可能产生氢气。为了验证哪位同学的判断正确,丙同学设计了如图所示的实验装置(锌与浓硫酸共热时产生的气体为X,且该装置略去。已知C为CuO)。试回答:
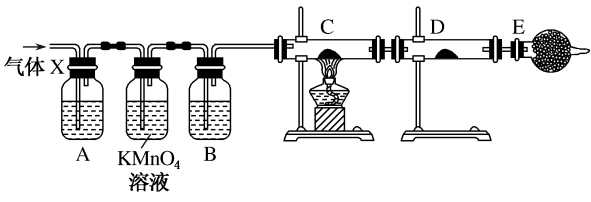
(1)上述反应中能生成二氧化硫的化学方程式为________ 。
(2)乙同学认为还可能产生氢气的理由是___________________________ 。
(3)A中加入的试剂可能是_______ ,作用是_______ ;B中加入的试剂可能是________ ,作用是___________ 。
(4)可以证明气体X中含有氢气的实验现象是:___________________ 。
(5)如果去掉装置B,还能否根据D中的现象判断气体X中有氢气?________ (填“能”或“不能”),原因是___________ 。
(6)下列有关硫及其化合物的叙述正确的是___________。
A.食品中添加适量二氧化硫可以起到防腐和抗氧化等作用
B.SO2与CO2均为酸性氧化物,化学性质相同
C.2molSO2与1molO2在一定条件下反应能生成2mol的SO3
D.浓硫酸与红热的炭反应体现了浓硫酸的酸性和强氧化性
E.除去SO2中含有的少量HCl气体,可以使气体通过饱和Na2SO3溶液

(1)上述反应中能生成二氧化硫的化学方程式为
(2)乙同学认为还可能产生氢气的理由是
(3)A中加入的试剂可能是
(4)可以证明气体X中含有氢气的实验现象是:
(5)如果去掉装置B,还能否根据D中的现象判断气体X中有氢气?
(6)下列有关硫及其化合物的叙述正确的是___________。
A.食品中添加适量二氧化硫可以起到防腐和抗氧化等作用
B.SO2与CO2均为酸性氧化物,化学性质相同
C.2molSO2与1molO2在一定条件下反应能生成2mol的SO3
D.浓硫酸与红热的炭反应体现了浓硫酸的酸性和强氧化性
E.除去SO2中含有的少量HCl气体,可以使气体通过饱和Na2SO3溶液
您最近一年使用:0次
10 . 氰化钠是一种重要的基本化工原料,同时也是一种剧毒物质,严重危害人类健康。一旦泄漏需要及时处理,一般可以通过喷洒双氧水或硫代硫酸钠溶液来处理,以减轻环境污染。
I.已知:氰化钠化学式为NaCN,氰化钠是一种白色结晶颗粒,剧毒,易溶于水,水溶液呈碱性,易水解生成氰化氢。
(1)写出NaCN的电子式_______ ,CN-中C元素显+2价,N元素显-3价,则非金属性N_______ C(填“<”“>”或“=”),请设计实验证明:_______ 。
(2)NaCN用双氧水处理后,产生一种酸式盐和一种能使湿润红色石蕊试纸变蓝的气体,该反应的离子方程式是_______ 。
Ⅱ.硫代硫酸钠的工业制备的反应原理为2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2。某化学兴趣小组用上述原理实验室制备硫代硫酸钠,并检测用硫代硫酸钠溶液处理后的氰化钠废水能否达标排放。
【查阅资料】ⅰ.Na2S2O3易溶于水,其稀溶液与BaCl2溶液混合物无沉淀生成。
ⅱ.Na2S2O3易被氧化;BaSO3难溶于水,可溶于稀盐酸。
实验室通过如图所示装置制备Na2S2O3。
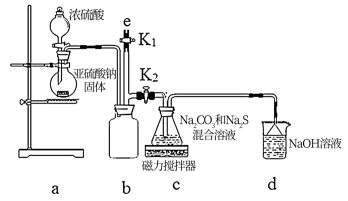
(1)实验中要控制SO2生成速率,可采取的措施有_______ (写出一条)。
(2)b装置的作用是_______ 。
(3)反应开始后,c中先有淡黄色浑浊产生后又变为澄清,此浑浊物_______ (填化学式)。
(4)实验结束后,在e处最好连接盛_______ (填“NaOH溶液”、“水”、“CCl4”中的一种) 的注射器,接下来的操作为_______ ,最后拆除装置。
I.已知:氰化钠化学式为NaCN,氰化钠是一种白色结晶颗粒,剧毒,易溶于水,水溶液呈碱性,易水解生成氰化氢。
(1)写出NaCN的电子式
(2)NaCN用双氧水处理后,产生一种酸式盐和一种能使湿润红色石蕊试纸变蓝的气体,该反应的离子方程式是
Ⅱ.硫代硫酸钠的工业制备的反应原理为2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2。某化学兴趣小组用上述原理实验室制备硫代硫酸钠,并检测用硫代硫酸钠溶液处理后的氰化钠废水能否达标排放。
【查阅资料】ⅰ.Na2S2O3易溶于水,其稀溶液与BaCl2溶液混合物无沉淀生成。
ⅱ.Na2S2O3易被氧化;BaSO3难溶于水,可溶于稀盐酸。
实验室通过如图所示装置制备Na2S2O3。

(1)实验中要控制SO2生成速率,可采取的措施有
(2)b装置的作用是
(3)反应开始后,c中先有淡黄色浑浊产生后又变为澄清,此浑浊物
(4)实验结束后,在e处最好连接盛
您最近一年使用:0次



